| Имена | |||
|---|---|---|---|
| Название ИЮПАК фторид сурьмы (V) | |||
| Другие имена пентафторид сурьмы пентафторид сурьмы | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.110 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1732 г. | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| SbF 5 | |||
| Молярная масса | 216,74 г / моль | ||
| Внешность | бесцветная маслянистая жидкость гигроскопична | ||
| Запах | острый | ||
| Плотность | 2,99 г / см 3 [1] | ||
| Температура плавления | 8,3 ° С (46,9 ° F, 281,4 К) | ||
| Точка кипения | 149,5 ° С (301,1 ° F, 422,6 К) | ||
| Реагирует | |||
| Растворимость | растворим в KF , жидком SO 2 | ||
| Опасности | |||
| Основные опасности | Высвобождает плавиковую кислоту при контакте с водой или биологическими тканями. | ||
| Паспорт безопасности | ICSC 0220 | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасность | ||
| H302 , H314 , H332 , H411 , H412 | |||
| Р260 , Р261 , Р264 , Р270 , Р271 , Р273 , Р280 , Р301 + 312 , P301 + 330 + 331 , P303 + 361 + 353 , Р304 + 312 , Р304 + 340 , P305 + 351 + 338 , P310 , P312 , P321 , P330 , P363 , P391 , P405 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 0,5 мг / м 3 (как Sb) [2] | ||
REL (рекомендуется) | TWA 0,5 мг / м 3 (как Sb) [2] | ||
| Родственные соединения | |||
Другие анионы | Пентахлорид сурьмы | ||
Другие катионы | Пентафторид фосфора Пентафторид мышьяка Пентафторид висмута | ||
Родственные соединения | Трифторид сурьмы | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
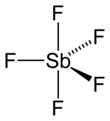
Пентафторид сурьмы представляет собой неорганическое соединение с формулой Sb F 5 . Эта бесцветная вязкая жидкость представляет собой ценную кислоту Льюиса и компонент суперкислоты фторантимоновой кислоты , самой сильной известной кислоты, образующейся при смешивании жидкого HF с жидким SbF 5 в соотношении 2: 1. Он примечателен своей кислотностью Льюиса и способностью реагировать практически со всеми известными соединениями. [4]
Подготовка [ править ]
Пентафторид сурьмы получают реакцией пентахлорида сурьмы с безводным фтористым водородом : [5]
- SbCl 5 + 5 HF → SbF 5 + 5 HCl
Его также можно приготовить из трифторида сурьмы и фтора. [6]
Строение и химические реакции [ править ]
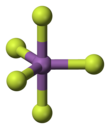
В газовой фазе SbF 5 принимает тригонально-бипирамидальную структуру симметрии точечной группы D 3h (см. Рисунок). Материал имеет более сложную структуру в жидком и твердом состояниях. Жидкость содержит полимеры, в которых каждый Sb является октаэдрическим, структура описывается формулой [SbF 4 (μ-F) 2 ] n ((μ-F) обозначает тот факт, что фторидные центры соединяют два центра Sb). Кристаллический материал представляет собой тетрамер, что означает, что он имеет формулу [SbF 4 (μ-F)] 4 . Связи Sb-F составляют 2,02 Å в восьмичленном Sb 4 F 4.звенеть; остальные фторидные лиганды, исходящие из четырех центров Sb, короче на 1,82 Å. [7] Соответствующие виды PF 5 и АФС 5 являются мономерный в твердом и жидком состояниях, вероятно , из - за небольших размеров центрального атома, что ограничивает их координационное число. BiF 5 - полимер. [8]
Точно так же, как SbF 5 увеличивает кислотность HF по Бренстеду , он увеличивает окислительную способность F 2 . Этот эффект иллюстрируется окислением кислорода : [9]
- 2 SbF 5 + F 2 + 2 O 2 → 2 [O 2 ] + [SbF 6 ] -
Пентафторид сурьмы также использовался в первой обнаруженной химической реакции, которая производит газообразный фтор из фторидных соединений:
- 4 SbF
5 + 2 К
2MnF
6 → 4 тыс.
6+ 2 MnF
3 + F
2
Движущей силой этой реакции является высокое сродство SbF 5 к F-
, что является тем же свойством, которое рекомендует использовать SbF 5 для создания суперкислот.
Гексафторантимонат [ править ]
SbF 5 является сильной кислотой Льюиса, особенно по отношению к источникам F - для получения очень стабильного аниона [SbF 6 ] - , называемого гексафторантимонатом. [SbF 6 ] - это слабо координационном анион сродни PF 6 - . Хотя он слабоосновен, [SbF 6 ] - действительно реагирует с дополнительным SbF 5, давая центросимметричный аддукт :
- SbF 5 + [SbF 6 ] - → [Sb 2 F 11 ] -
Безопасность [ править ]
SbF 5 бурно реагирует со многими соединениями, часто выделяя опасный фтороводород . Разъедает кожу и глаза. [10] [11]
Ссылки [ править ]
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 0-8493-0487-3.
- ^ a b Карманный справочник NIOSH по химической опасности. «# 0036» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ World of Chemicals SDS
- ^ Олах, Джорджия; Пракаш, ГКС; Wang, Q .; Ли, X.-y. «Фторид сурьмы (V)» в Энциклопедии реагентов для органического синтеза (Эд: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. DOI : 10.1002 / 047084289X .
- ↑ Сабина С. Грунд, Куниберт Хануш, Ханс Дж. Бройниг, Ханс Уве Вольф «Сурьма и соединения сурьмы» в Энциклопедии промышленной химии Ульманна 2006, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a03_055.pub2
- ^ Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, NY. Vol. 1. п. 200.
- ^ Эдвардс, AJ; Тейлор П. "Кристаллическая структура пентафторида сурьмы" Журнал Химического общества, Химические сообщения 1971, стр. 1376-7. DOI : 10.1039 / C29710001376
- ^ Holleman, AF; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5 .
- ^ Шамир, J .; Binenboym, J. "Dioxygenyl Salts" Inorganic Syntheses 1973, XIV, 109-122. ISSN 0073-8077
- ^ Международная программа по химической безопасности (2005). «Пентафторид сурьмы» . Комиссия Европейских сообществ (CEC) . Проверено 10 мая 2010 .
- ^ Barbalace, Кеннет (2006). «Химическая база данных - пентафторид сурьмы» . Химия окружающей среды . Проверено 10 мая 2010 .
Внешние ссылки [ править ]
- Страница веб-книги для SbF5
- Национальный реестр загрязнителей - информационный бюллетень по сурьме и соединениям
- Национальный реестр загрязнителей - информационный бюллетень по фторидным соединениям