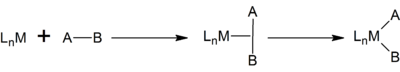Эта статья требует дополнительных ссылок для проверки . ( январь 2021 г. ) ( Узнайте, как и когда удалить это сообщение-шаблон ) |
Окислительное добавление и восстановительное отщепление - два важных и связанных класса реакций в металлоорганической химии . [1] [2] [3] [4] Окислительное добавление - это процесс, который увеличивает степень окисления и координационное число металлического центра. Окислительное добавление часто является стадией каталитических циклов в сочетании с его обратной реакцией, восстановительным отщеплением. [5]
Роль в химии переходных металлов [ править ]
Для переходных металлов, окислительные реакции приводят к уменьшению д п к конфигурации с меньшим количеством электронов, часто 2e меньше. Окислительная добавка предпочтительна для металлов, которые (i) являются основными и / или (ii) легко окисляются. Металлы с относительно низкой степенью окисления часто удовлетворяют одному из этих требований, но даже металлы с высокой степенью окисления подвергаются окислительному присоединению, как показано окислением Pt (II) хлором:
- [PtCl 4 ] 2− + Cl 2 → [PtCl 6 ] 2−
В классической металлоорганической химии формальная степень окисления металла и количество электронов в комплексе увеличиваются на два. [6] Одноэлектронные изменения также возможны, и на самом деле некоторые реакции окислительного присоединения протекают через серию изменений 1e. Хотя окислительные добавки могут происходить при внедрении металла во многие различные субстраты, окислительные добавки чаще всего наблюдаются со связями H – H, H – X и C – X, поскольку эти субстраты наиболее актуальны для коммерческого применения.
Окислительное добавление требует, чтобы комплекс металла имел свободный координационный центр. По этой причине окислительные добавки обычны для четырех- и пятикоординированных комплексов.
Восстановительное удаление является обратным окислительному добавлению. [7] Восстановительное устранение предпочтительнее, когда вновь образованная связь X – Y прочная. Для того, чтобы произошло восстановительное отщепление, две группы (X и Y) должны быть взаимно соседними на координационной сфере металла . Восстановительное отщепление является ключевым этапом высвобождения продукта в нескольких реакциях, которые образуют связи C – H и C – C. [5]
Механизмы окислительного присоединения [ править ]
Окислительные добавки происходят по многим путям, которые зависят от металлического центра и субстратов.
Согласованный путь [ править ]
Окислительные добавки неполярных субстратов, таких как водород и углеводороды, по-видимому, происходят согласованными путями. В таких субстратах отсутствуют π-связи , следовательно, активируется трехцентровый σ-комплекс с последующим разрывом внутримолекулярной лигандной связи лиганда (вероятно, путем передачи электронной пары на сигма-орбиталь межлигандной связи) с образованием окисленного комплекса. Полученные лиганды будут взаимно цис , [2] , хотя последующая изомеризация может произойти.
Этот механизм применяется к добавлению гомоядерных двухатомных молекул, таких как H 2 . Многие реакции активации C – H также следуют согласованному механизму через образование агостического комплекса M– (C – H) . [2]
Типичным примером является реакция водорода с комплексом Васьки , транс- IrCl (CO) [P (C 6 H 5 ) 3 ] 2 . В этом превращении иридий меняет свою формальную степень окисления с +1 на +3. Продукт формально связан с тремя анионами: одним хлоридным и двумя гидридными лигандами. Как показано ниже, исходный металлический комплекс имеет 16 валентных электронов и координационное число четыре, тогда как продукт представляет собой шестикоординированный 18-электронный комплекс.
Образование тригонально-бипирамидного дигидроген-интермедиата сопровождается разрывом связи H – H из-за обратного донорства электронов в H – H σ * -орбиталь. Эта система также находится в химическом равновесии с обратной реакцией, протекающей путем удаления газообразного водорода с одновременным восстановлением металлического центра. [8]
Обратное донорство электронов на H – H σ * -орбиталь для разрыва связи H – H заставляет богатые электронами металлы поддерживать эту реакцию. [8] Согласованный механизм производит цис- дигидрид, в то время как стереохимия других путей окислительного присоединения обычно не приводит к образованию цис- аддуктов.
S N 2-типа [ править ]
Некоторые окислительные добавки протекают аналогично хорошо известным реакциям бимолекулярного нуклеофильного замещения в органической химии . Нуклеофильная атака металлическим центром на менее электроотрицательный атом в субстрате приводит к разрыву связи R – X с образованием частиц [M – R] + . Эта стадия сопровождается быстрой координацией аниона с катионным металлическим центром. Например, реакция плоско-квадратного комплекса с йодистым метилом :
Этот механизм часто предполагается при добавлении полярных и электрофильных субстратов, таких как алкилгалогениды и галогены . [2]
Ионный [ править ]
Ионный механизм окислительного присоединения аналогичен типу S N 2 в том, что он включает ступенчатое добавление двух отдельных фрагментов лиганда. Ключевое отличие состоит в том, что ионные механизмы включают субстраты, которые диссоциируют в растворе до любых взаимодействий с металлическим центром. Примером ионного окислительного присоединения является добавление соляной кислоты. [2]
Радикальный [ править ]
Помимо прохождения реакций типа S N 2, алкилгалогениды и подобные субстраты могут присоединяться к металлическому центру посредством радикального механизма, хотя некоторые детали остаются спорными. [2] Однако известны реакции, которые, как принято считать, протекают по радикальному механизму. Один пример был предложен Леднором и сотрудниками. [9]
- Посвящение
- [(CH 3 ) 2 C (CN) N] 2 → 2 (CH 3 ) 2 (CN) C • + N 2
- (CH 3 ) 2 (CN) C • + PhBr → (CH 3 ) 2 (CN) CBr + Ph •
- Распространение
- Ph • + [Pt (PPh 3 ) 2 ] → [Pt (PPh 3 ) 2 Ph] •
- [Pt (PPh 3 ) 2 Ph] • + PhBr → [Pt (PPh 3 ) 2 PhBr] + Ph •
Приложения [ править ]
Окислительное добавление и восстановительное отщепление используются во многих каталитических процессах как при гомогенном катализе (т. Е. В растворе), таких как процесс Monsanto, так и гидрирование алкена с использованием катализатора Уилкинсона . Часто предполагается, что реакции, подобные окислительному присоединению, также участвуют в механизмах гетерогенного катализа , например, гидрирование, катализируемое металлической платиной. Однако металлы характеризуются полосовой структурой , поэтому степень окисления не имеет значения. Окислительное добавление также необходимо для нуклеофильного присоединения.алкильной группы. Окислительный вставки также является важным шагом во многих кросс-сочетания реакций , таких как реакции сочетания Сузуки , Негиши муфты , и муфты Соногашира .
Ссылки [ править ]
- ^ Джей А. Лабинджер "Учебник по окислительному добавлению" Металлоорганические соединения, 2015, том 34, стр 4784–4795. DOI : 10.1021 / acs.organomet.5b00565
- ^ Б с д е е Crabtree, Роберт (2005). Металлоорганическая химия переходных металлов . Wiley-Interscience. С. 159–180. ISBN 0-471-66256-9.
- ^ Мисслер, Гэри Л .; Тарр, Дональд А. Неорганическая химия (3-е изд.).[ ISBN отсутствует ]
- ^ Шрайвер, Д. Ф.; Аткинс, П.В. Неорганическая химия .[ ISBN отсутствует ]
- ^ а б Хартвиг, JF (2010). Органопереходная химия металлов, от связывания до катализа . Нью-Йорк: Университетские научные книги. ISBN 978-1-891389-53-5.
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) « Окислительная добавка ». DOI : 10,1351 / goldbook.O04367
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « редуктивное исключение ». DOI : 10,1351 / goldbook.R05223
- ^ a b Джонсон, Кертис; Айзенберг, Ричард (1985). «Стереоселективное окислительное присоединение водорода к комплексам иридия (I). Кинетический контроль на основе электронных эффектов лиганда». Журнал Американского химического общества . 107 (11): 3148–3160. DOI : 10.1021 / ja00297a021 .
- ^ Холл, Томас L .; Лапперт, Майкл Ф .; Леднор, Питер В. (1980). "Механистические исследования некоторых реакций окислительного присоединения: свободнорадикальные пути в реакциях Pt 0 -RX, Pt 0 -PhBr и Pt II -R'SO 2 X (R = алкил, R '= арил, X = галогенид) и в родственных родиевых (I) или иридиевых (I) системах ». J. Chem. Soc., Dalton Trans. (8): 1448–1456. DOI : 10.1039 / DT9800001448 .
Дальнейшее чтение [ править ]
- Анаников, Валентин П .; Мусаев, Джамаладдин Г .; Морокума, Кейджи (2005). "Теоретическое понимание реакций связывания C − C виниловых, фенильных, этинильных и метиловых комплексов палладия и платины". Металлоорганические соединения . 24 (4): 715. DOI : 10.1021 / om0490841 .
Внешние ссылки [ править ]
- Тореки, Р. «Окислительная добавка » . Металлоорганический гипертекст . Interactive Learning Paradigms Inc.
- Тореки, Р. "Редуктивное устранение" . Металлоорганический гипертекст . Interactive Learning Paradigms Inc.