| Имена | |||
|---|---|---|---|
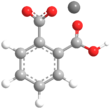
| Название ИЮПАК Гидрофталат калия | |||
| Другие имена фталат калия водорода; калиевая соль фталевой кислоты; бифталат калия; фталат калиевой кислоты; 1,2-бензолдикарбоновая кислота, монокалиевая соль; KHP; KHPh | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.011.718 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 8 Н 5 К О 4 | |||
| Молярная масса | 204,222 г · моль -1 | ||
| Внешность | Белое или бесцветное твердое вещество | ||
| Плотность | 1,636 г / см 3 | ||
| Температура плавления | ~ 295 ° C (разлагается) | ||
| 80 г / л (20 ° C) [1] | |||
| Растворимость | слабо растворим в спирте | ||
| Кислотность (p K a ) | 5,4 [2] | ||
| Структура | |||
| четырехгранный | |||
| Опасности | |||
| Основные опасности | Раздражает глаза, кожу и дыхательную систему | ||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| R-фразы (устаревшие) | R36 R37 R38 | ||
| точка возгорания | Негорючий | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Гидрофталат калия , часто называемый просто KHP , представляет собой кислотное солевое соединение. Он образует белый порошок, бесцветные кристаллы, бесцветный раствор и ионное твердое вещество, которое представляет собой монокалиевую соль фталевой кислоты . KHP является слабокислым , и его часто используют в качестве основного стандарта для кислотно-основного титрования, поскольку он твердый и устойчивый на воздухе, что упрощает точное взвешивание. Не гигроскопичен . [3] [4] [5] Он также используется в качестве основного стандарта для калибровки pH-метров, потому что, помимо только что упомянутых свойств, его pHв растворе очень стабильна. Он также служит термическим эталоном в термогравиметрическом анализе. [6]
KHP полностью диссоциирует в воде, давая катион калия (K + ) и анион гидрофталата (HP - или Hphthalate - ).
- KHP + H 2 O ⇌ K + + HP -
Затем в качестве слабокислой гидрофталат обратимо реагирует с водой с образованием ионов гидроксония (H 3 O + ) и фталата.
- HP - + H 2 O ⇌ P 2− + H 3 O +
KHP можно использовать в качестве буферного агента в сочетании с соляной кислотой (HCl) или гидроксидом натрия (NaOH) в зависимости от того, на какой стороне pH 4,0 должен быть буфер.
KHP также является полезным стандартом для тестирования общего органического углерода (TOC). Большинство анализаторов ТОС основаны на окислении органических веществ до диоксида углерода и воды с последующим количественным определением диоксида углерода. Многие аналитики TOC предлагают тестировать свои инструменты с двумя стандартами: один, как правило, легко окисляется для прибора (KHP), а другой - трудно окисляемый. Для последнего предлагается бензохинон .
Ссылки [ править ]
- ^ http://www.merckmillipore.com/INTL/en/product/pharmaceutical-ingredients/potassium-hydrogen-phthalate,MDA_CHEM-104874
- ^ http://archpdfs.lps.org/Chemicals/Potassium%20Hydrogen%20Phthalate.pdf
- ^ Хендриксон, WS (1920). «Дальнейшая работа над фталатом водорода калия как стандартом объемного анализа» . J Am Chem Soc . 42 (4): 724–727. DOI : 10.1021 / ja01449a008 .
- ^ «Фталат водорода калия» . Арлингтон, Техас: Ricca Chemical Company. Архивировано из оригинала на 2012-11-30 . Проверено 3 октября 2012 .
- ^ «Стандартизация NaOH и анализа KHP» (PDF) . Колледж Кларка. Архивировано из оригинального (PDF) 19 ноября 2012 года . Проверено 3 октября 2012 .
- ^ Смолли, И.Дж., Лилль, Г.О., Бентли, С.П., Вуд, Д.Р. 1977. Термогравиметрия гидрофталата калия и его использование в качестве теплового стандарта. Канадский минералог 15, 30-35