 | |
 | |
| Имена | |
|---|---|
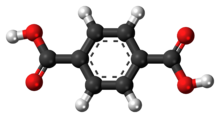
| Предпочтительное название IUPAC Бензол-1,4-дикарбоновая кислота | |
| Другие имена 1,4-Бензолдиовая кислота Бензол-1,4-диовая кислота Терефталевая кислота пара- Фталевая кислота TPA PTA BDC | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| 3DMet | |
| 1909333 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100,002,573 |
| Номер ЕС |
|
| 50561 | |
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| С 8 Н 6 О 4 | |
| Молярная масса | 166,132 г · моль -1 |
| Внешность | Белые кристаллы или порошок |
| Плотность | 1,522 г / см 3 |
| Температура плавления | 427 ° C (801 ° F; 700 K) в герметичной пробирке. Возгоняется при стандартном атмосферном давлении. |
| Точка кипения | Разлагается |
| 0,0015 г / 100 мл при 20 ° C | |
| Растворимость | полярные органические растворители водная основа |
| Кислотность (p K a ) | 3,51, 4,82 [1] |
| −83,51 × 10 −6 см 3 / моль | |
| Структура | |
| 0 | |
| Опасности | |
| Паспорт безопасности | См .: страницу данных лист MSDS |
| Пиктограммы GHS | |
| Сигнальное слово GHS | Предупреждение |
Положения об опасности GHS | H315 , H319 , H335 |
Меры предосторожности GHS | Р261 , Р264 , Р271 , Р280 , Р302 + 352 , Р304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , Р405 , Р501 |
| Родственные соединения | |
Родственные карбоновые кислоты | Фталевая кислота Изофталевая кислота Бензойная кислота п -Толуиловая кислота |
Родственные соединения | п-Ксилол Полиэтилентерефталат Диметилтерефталат |
| Страница дополнительных данных | |
Структура и свойства | Показатель преломления ( n ), диэлектрическая проницаемость (ε r ) и т. Д. |
Термодинамические данные | Фазовое поведение твердое тело – жидкость – газ |
Спектральные данные | УФ , ИК , ЯМР , МС |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Терефталевая кислота - это органическое соединение с формулой C 6 H 4 (CO 2 H) 2 . Это белое твердое вещество является товарным химическим веществом , используемым в основном как предшественник полиэфирного ПЭТ , используемого для изготовления одежды и пластиковых бутылок . Ежегодно производится несколько миллионов тонн. [2] Общее название происходит от производящего скипидар дерева Pistacia terebinthus и фталевой кислоты .
История [ править ]
Терефталевая кислота была впервые выделена (из скипидара) французским химиком Амеде Кайо (1805–1884) в 1846 году. [3] Терефталевая кислота стала промышленно важной после Второй мировой войны . Терефталевая кислота была получена окислением п- ксилола разбавленной азотной кислотой . Окисление п- ксилола воздухом дает п- толуиловую кислоту, которая сопротивляется дальнейшему окислению воздухом. Превращение п- толуиловой кислоты в п-толуат метилового ряда (CH 3 C 6 H 4 CO 2 CH 3) открывает путь для дальнейшего окисления до монометилтерефталата, который далее этерифицируется до диметилтерефталата . В 1955 году Mid-Century Corporation и ICI объявили об окислении п- толуиловой кислоты до терафталевой кислоты с помощью бромида. Это нововведение позволило превратить п- ксилол в терефталевую кислоту без необходимости выделения промежуточных продуктов. Amoco (как Standard Oil of Indiana) приобрела технологию Mid-Century / ICI. [4]
Синтез [ править ]
Amoco process [ править ]
В процессе Amoco, который широко принятой во всем мире, терефталевую кислоту получают путем каталитического окисления в п - ксилола : [4]
Процесс использует кобальт - марганец - бромид катализатора . Источник бромида может быть бромид натрия , бромид водорода или тетрабромэтана . Бром действует как регенерирующий источник свободных радикалов . Уксусная кислота является растворителем, а сжатый воздух - окислителем. Комбинация брома и уксусной кислоты вызывает сильную коррозию , поэтому требуются специальные реакторы, например, с титановой футеровкой . Смесь п- ксилола , уксусной кислоты , катализатор системы, а сжатый воздух подается в реактор.
Механизм [ править ]
Окисление п- ксилола протекает свободнорадикальным процессом. Радикалы брома разлагают гидропероксиды кобальта и марганца. Образующиеся радикалы на основе кислорода отводят водород от метильной группы, которая имеет более слабые связи C – H, чем ароматическое кольцо. Было выделено много промежуточных продуктов. п- ксилол превращается в п- толуиловую кислоту , которая менее реакционноспособна, чем п-ксилол, из-за влияния группы электроноакцепторной карбоновой кислоты . Неполное окисление дает 4-карбоксибензальдегид (4-CBA), который часто является проблемной примесью. [4] [5] [6]
Проблемы [ править ]
Приблизительно 5% растворителя уксусной кислоты теряется при разложении или «горении». Потеря продукта декарбоксилированием до бензойной кислоты является обычным явлением. Высокая температура снижает растворимость кислорода в системе, уже испытывающей недостаток кислорода. Чистый кислород нельзя использовать в традиционной системе из-за опасности горючих смесей органических соединений с O 2 . Вместо него можно использовать атмосферный воздух, но после прохождения реакции его необходимо очистить от токсинов и разрушителей озона, таких как метилбромид, перед выпуском . Кроме того, коррозионная природа бромидов при высоких температурах требует, чтобы реакция проводилась в дорогостоящих титановых реакторах. [7] [8]
Альтернативные СМИ реакции [ править ]
Использование углекислого газа решает многие проблемы исходного промышленного процесса. Поскольку CO 2 является лучшим ингибитором пламени, чем N 2 , среда CO 2 позволяет напрямую использовать чистый кислород вместо воздуха, что снижает опасность воспламенения. Растворимость молекулярного кислорода в растворе также повышается в среде CO 2 . Поскольку системе доступно больше кислорода, сверхкритический диоксид углерода ( T c = 31 ° C) имеет более полное окисление с меньшим количеством побочных продуктов, меньшее образование оксида углерода , меньшее декарбоксилирование и более высокую чистоту, чем коммерческий процесс. [7][8]
В сверхкритической водной среде окисление может эффективно катализироваться MnBr 2 с чистым O 2 при средне-высокой температуре. Использование сверхкритической воды вместо уксусной кислоты в качестве растворителя снижает воздействие на окружающую среду и дает экономическое преимущество. Однако возможности таких реакционных систем ограничены еще более суровыми условиями, чем промышленный процесс (300–400 ° C,> 200 бар). [9]
Промоторы и добавки [ править ]
Как и в случае любого крупномасштабного процесса, многие добавки были исследованы на предмет потенциальных положительных эффектов. Об обнадеживающих результатах сообщается следующее. [4]
- Кетоны действуют как промоторы для образования активного катализатора на основе кобальта (III). В частности, кетоны с α-метиленовыми группами окисляются до гидропероксидов, которые, как известно, окисляют кобальт (II). Часто используется бутанон .
- Соли циркония усиливают активность катализаторов Co-Mn-Br. Избирательность также улучшена. [4]
- N-гидроксифталимид является потенциальной заменой бромида, который очень агрессивен. Фталимид функционирует за счет образования оксильного радикала.
- Гуанидин ингибирует окисление первого метила, но усиливает обычно медленное окисление толуиловой кислоты.
Альтернативные маршруты [ править ]
Терефталевую кислоту можно получить в лаборатории путем окисления многих пара- дизамещенных производных бензола , включая тминное масло или смесь цимола и куминола с хромовой кислотой .
Так называемый « процесс Хенкеля » или «процесс Раеке», названный в честь компании и патентообладателя, не имеет коммерческого значения . Этот процесс включает перенос карбоксилатных групп. Например, бензоат калия диспропорционирует до терефталата калия, а фталат калия перестраивается в терефталат калия. [10] [11]
Lummus (в настоящее время дочерняя компания McDermott International ) сообщила о способе получения динитрила путем аммоксидирования п- ксилола.
Приложения [ править ]
Практически все мировые запасы терефталевой кислоты и диметилтерефталата потребляются в качестве прекурсоров полиэтилентерефталата (ПЭТ). Мировое производство в 1970 году составляло около 1,75 миллиона тонн. [2] К 2006 году мировой спрос на очищенную терефталевую кислоту (PTA) превысил 30 миллионов тонн. Меньшая, но, тем не менее, значительная потребность в терефталевой кислоте существует при производстве полибутилентерефталата и некоторых других технических полимеров . [12]
Другое использование [ править ]
- Полиэфирные волокна на основе ПТА обеспечивают легкий уход за тканью как сами по себе, так и в смеси с натуральными и другими синтетическими волокнами . Полиэфирные пленки широко используются в лентах для аудио- и видеозаписи, лентах для хранения данных, фотопленках, этикетках и других листовых материалах, требующих как стабильности размеров, так и прочности.
- Терефталевая кислота используется в красках как носитель.
- Терефталевая кислота используется в качестве сырья для изготовления терефталатных пластификаторов, таких как диоктилтерефталат и дибутилтерефталат.
- Он используется в фармацевтической промышленности как сырье для некоторых лекарств.
- Помимо этих конечных применений, полиэфиры и полиамиды на основе терефталевой кислоты также используются в клеях-расплавах.
- PTA является важным сырьем для получения насыщенных полиэфиров с более низким молекулярным весом для порошковых и водорастворимых покрытий .
- В исследовательской лаборатории терефталевая кислота была популяризирована как компонент для синтеза металлоорганических каркасов .
- Обезболивающее препарат оксикодон иногда приходит как ПЭТФ соли; однако более обычной солью оксикодона является гидрохлорид . Фармакологически один миллиграмм terephthalas oxycodonae эквивалентен 1,13 мг hydrochloridum oxycodonae .
- Терефталевая кислота используется в качестве наполнителя в некоторых военных дымовых гранатах , в первую очередь в американских дымовых гранатах M83 и дымовых гранатах M90, используемых в транспортных средствах, поскольку при горении образуется густой белый дым, который действует как затемняющее средство в видимом и ближнем инфракрасном спектрах.
Растворимость [ править ]
Терефталевая кислота плохо растворяется в воде и спиртах; следовательно, примерно до 1970 года терефталевая кислота очищалась как ее диметиловый эфир . Он возвышается при нагревании.
|
|
Токсичность [ править ]
Терефталевой кислоты и ее диметилового эфира имеют очень низкую токсичность , с LD 50 с более 1 г / кг (перорально, мышь). [2]
Ссылки [ править ]
- ^ Браун, H.C .; и другие. (1955). Baude, E. A .; Наход, Ф. К. (ред.). Определение органических структур физическими методами . Нью-Йорк, штат Нью-Йорк: Academic Press.
- ^ a b c Sheehan, Ричард Дж. «Терефталевая кислота, диметилтерефталат и изофталевая кислота». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a26_193 .
- ^ Cailliot, Amédée (1847). "Études sur l'essence de térébenthine" [Исследования сущности скипидара]. Annales de Chimie et de Physique . Серия 3. 21 : 27–40.Терефталевая кислота указана на стр. 29: «Je désignerai le premier de ces acides, celui qui est insoluble, sous le nom d ' acide téréphtalique ». (Я обозначу первую из этих кислот, которая нерастворима, названием терефталевая кислота .)
- ^ a b c d e Томас, Роджерио А.Ф .; Bordado, Joao CM; Гомеш, Жоао ФП (2013). «Окисление п-ксилола до терефталевой кислоты: обзор литературы, ориентированный на оптимизацию и развитие процесса». Химические обзоры . 113 (10): 7421–69. DOI : 10.1021 / cr300298j . PMID 23767849 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Ван, Циньбо; Ченг, Ювэй; Ван, Лицзюнь; Ли, Си (2007). "Полунепрерывные исследования механизма и кинетики реакции жидкофазного окисления п- ксилола до терефталевой кислоты". Промышленные и инженерные химические исследования . 46 (26): 8980–8992. DOI : 10.1021 / ie0615584 .
- ^ Сяо, Ю.; Luo, W.-P .; Zhang, X.-Y .; Guo, C.-C .; Liu, Q .; Jiang, G.-F .; Ли, К.-Х. (2010). «Аэробное окисление п- толуиловой кислоты до терефталевой кислоты над T ( p -Cl) PPMnCl / Co (OAc) 2 в умеренных условиях». Письма о катализе . 134 (1–2): 155–161. DOI : 10.1007 / s10562-009-0227-1 .
- ^ а б Цзо, Сяобинь; Субраманиам, Бала; Буш, Дэрил Х. (2008). «Жидкофазное окисление толуола и п- толуиловой кислоты в мягких условиях: синергетические эффекты кобальта, циркония, кетонов и диоксида углерода». Промышленные и инженерные химические исследования . 47 (3): 546–552. DOI : 10.1021 / ie070896h .
- ^ Перес, Эдуардо; Фрага Дюбрей, Жанна; Гарсиа Вердуго, Эдуардо; Hamley, Paul A .; Томас, В. Барри; Хаусли, Дункан; Партенхаймер, Подождите; Поляков, Мартын (2011). «Селективное аэробное окисление пара- ксилола в воде в суб- и сверхкритическом состоянии. Часть 1. Сравнение с ортоксилолом и роль катализатора». Зеленая химия . 13 (12): 2389–2396. DOI : 10.1039 / C1GC15137A .
- ^ Огата, Йоширо; Цучида, Масару; Мурамото, Акихико (1957). «Получение терефталевой кислоты из фталевой или бензойной кислоты». Журнал Американского химического общества . 79 (22): 6005–6008. DOI : 10.1021 / ja01579a043 .
- ^ Огата, Йоширо; Ходжо, Масару; Морикава, Масанобу (1960). «Дальнейшие исследования по получению терефталевой кислоты из фталевой или бензойной кислоты». Журнал органической химии . 25 (12): 2082–2087. DOI : 10.1021 / jo01082a003 .
- ^ Словарь промышленных химикатов Эшфорда (3-е изд.). 2011. с. 8805.
- Британская энциклопедия, одиннадцатое издание
Внешние ссылки и дальнейшее чтение [ править ]
- Tedder, J.M .; Нечватал, А .; Табб, А. Х., ред. (1975). Основы органической химии: Часть 5, Промышленные продукты . Чичестер, Великобритания: John Wiley & Sons.
- Международная карта химической безопасности 0330
См. Также [ править ]
- Полициклогексилендиметилентерефталат термопластичный полиэфир, образованный из терефталевой кислоты.