| HTR2C | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||||||||||||||||||
| Псевдонимы | HTR2C , 5-HT2C, 5-5HTR1C, 5-HT1C, рецептор 5-HT2C, рецептор 5-гидрокситриптамина 2C | ||||||||||||||||||||||||
| Внешние идентификаторы | OMIM : 312861 MGI : 96281 HomoloGene : 20242 GeneCards : HTR2C | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ортологи | |||||||||||||||||||||||||
| Разновидность | Человек | Мышь | |||||||||||||||||||||||
| Entrez |
|
| |||||||||||||||||||||||
| Ансамбль |
|
| |||||||||||||||||||||||
| UniProt |
|
| |||||||||||||||||||||||
| RefSeq (мРНК) |
|
| |||||||||||||||||||||||
| RefSeq (белок) |
|
| |||||||||||||||||||||||
| Расположение (UCSC) | Chr X: 114,58 - 114,91 Мб | Chr X: 146.96 - 147.2 Мб | |||||||||||||||||||||||
| PubMed поиск | [3] | [4] | |||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
5-НТ 2C рецептор является подтипом рецептора 5-HT , который связывает эндогенный нейромедиатор серотонин (5-гидрокситриптамин, 5-НТ). Это рецептор, связанный с G-белком (GPCR), который связан с G q / G 11 и опосредует возбуждающую нейротрансмиссию . HTR2C обозначает человеческий ген, кодирующий рецептор , [5] [6]что у человека находится в Х-хромосоме. Поскольку у мужчин есть одна копия гена, а у женщин одна из двух копий гена репрессирована, полиморфизм этого рецептора может влиять на оба пола в разной степени.
Структура [ править ]
На поверхности клетки рецептор существует в виде гомодимера . [7] Кристаллическая структура известна с 2018 года. [8]
Распространение [ править ]
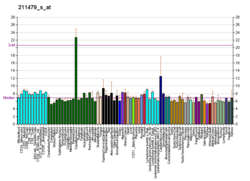
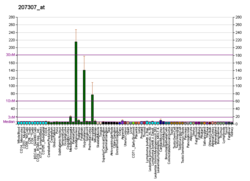
5-НТ 2C рецепторы расположены в основном в сосудистое сплетение , [9] , и у крыс также встречается во многих других областях мозга в высоких концентрациях, в том числе части гиппокампа , переднего обонятельного ядра , черной субстанции , несколько стволовых ядер, миндалине , субталамическое ядро и боковые габенулы . Рецепторы 5-HT 2C также обнаруживаются на эпителиальных клетках, выстилающих желудочки . [10]
Функция [ править ]
Рецептор 5-HT 2C является одним из многих сайтов связывания серотонина . Активация этого рецептора серотонином подавляет высвобождение дофамина и норадреналина в определенных областях мозга. [11]
Рецепторы 5-HT 2C, как утверждается, в значительной степени регулируют настроение, беспокойство, кормление и репродуктивное поведение. [12] Рецепторы 5-HT 2C регулируют высвобождение дофамина в полосатом теле , префронтальной коре , прилежащем ядре , гиппокампе , гипоталамусе и миндалевидном теле , среди прочего.
Исследования показывают, что у некоторых жертв самоубийства аномально высокое количество рецепторов 5-HT 2C в префронтальной коре головного мозга. [13] Существуют противоречивые данные о том, что агомелатин , антагонист 5-HT 2C , является эффективным антидепрессантом . [14] Антагонизм агомелатина к рецепторам 5-HT 2C приводит к увеличению активности дофамина и норадреналина в лобной коре головного мозга. И наоборот, многие СИОЗС (но не флуоксетин , который является антагонистом 5-HT2C [15] ) косвенно стимулируют активность 5-HT 2C за счет повышения уровня серотонина в синапсе.хотя замедленное повышение настроения, которое обычно типично для СИОЗС, обычно сопровождается подавлением рецепторов 5-HT2C. [16] Многие атипичные нейролептики блокируют рецепторы 5-HT 2C , но их клиническое применение ограничено множеством нежелательных воздействий на различные нейротрансмиттеры и рецепторы . Флуоксетин действует как прямой антагонист 5-HT 2C в дополнение к ингибированию обратного захвата серотонина , однако клиническое значение этого действия варьируется. [15]
Повышенная активность рецепторов 5-HT 2C может способствовать возникновению депрессивных и тревожных симптомов у определенной группы пациентов. Активация 5-HT 2C серотонином ответственна за многие негативные побочные эффекты препаратов СИОЗС и СИОЗСН , таких как сертралин , пароксетин , венлафаксин и другие. Некоторая первоначальная тревога, вызванная СИОЗС, связана с избыточной передачей сигналов 5-HT 2C . В течение 1-2 недель рецептор начинает снижать регуляцию , наряду с подавлением 5-HT 2A , 5-HT1 A.и другие рецепторы серотонина. Это подавление происходит параллельно с появлением клинических преимуществ СИОЗС. Рецепторы 5-HT 2C проявляют конститутивную активность in vivo и могут сохранять способность влиять на нейротрансмиссию в отсутствие занятости лиганда. Таким образом, рецепторы 5-HT 2C не требуют связывания лигандом (серотонином), чтобы оказывать влияние на нейротрансмиссию. Для полного подавления конститутивной активности 5-HT 2C могут потребоваться обратные агонисты , и они могут оказаться полезными при лечении состояний, опосредованных 5-HT 2C, в отсутствие типичной активности серотонина. [16] В дополнение к доказательствам роли 5-HT2C стимуляции рецептора в депрессивных симптомов существует также доказательства того, что активация 5-НТ 2С рецепторов может оказывать благотворное воздействие на определенные аспекты депрессии, одна группа исследователей было установлено , что прямой стимуляции 5-НТ 2С рецепторов с 5-HT 2C агониста снижается когнитивные нарушения у мышей с мутацией потери функции TPH2 . [17]
Рецепторы 5-HT 2C опосредуют высвобождение и увеличение внеклеточного дофамина в ответ на многие лекарства [18] [19], включая кофеин , никотин , амфетамин , морфин , кокаин и другие. Антагонизм 5-HT 2C увеличивает высвобождение дофамина в ответ на усиливающие препараты и многие дофаминергические стимулы. Кормление, социальное взаимодействие и сексуальная активность - все это высвобождает дофамин, который ингибируется 5-HT 2C . Повышенная экспрессия 5-HT 2C снижает высвобождение дофамина как в присутствии, так и в отсутствие стимулов.
Условия, при которых повышается уровень цитокинов в организме человека, могут потенциально повышать экспрессию гена 5-HT 2C в головном мозге. Возможно, это может быть связано между вирусными инфекциями и связанной с ними депрессией. Цитокина терапия была показана увеличение 5-НТ 2С экспрессии генов, что приводит к увеличению активности 5-НТ 2С рецепторов в головном мозге [ править ] .
Эндокринология [ править ]
Серотонин участвует в базальной и стресс-индуцированной регуляции гормонов гипоталамуса и гипофиза, таких как пролактин , адренокортикотропный гормон ( АКТГ ), вазопрессин и окситоцин , в основном за счет действия подтипов рецепторов 5-HT 2A и 5-HT 2C . [20] Таким образом, рецептор 5-HT 2C является важным модулятором оси гипоталамус-гипофиз-надпочечники ( ось HPA ). [21] Ось HPA является главным контроллером острой симпатической реакции на стресс, связанной с реакцией « бей или беги».. Длительная активация и нарушения оси HPA способствуют возникновению депрессивных и тревожных симптомов, наблюдаемых при многих психопатологических состояниях.
Стимуляция рецепторов 5-HT 2C приводит к увеличению уровня рилизинг-гормона кортикотропина ( CRH ) и мРНК вазопрессина в паравентрикулярном ядре и проопиомеланокортина в передней доле гипофиза. У крыс сдерживающий стресс (который может вызывать депрессивные симптомы, если он хронический) вызывает секрецию пролактина, АКТГ, вазопрессина и окситоцина, которая частично опосредуется рецептором 5-HT 2C . Ответы во время таких состояний, как обезвоживание или кровотечение, вызывают высвобождение окситоцина через серотонинергический ответ, который частично опосредуется 5-HT 2C . Кроме того, периферическое высвобождение вазопрессина включает серотонинергический ответ, который частично опосредуется 5-HT 2C .
Экспрессия рецептора 5-HT 2C в ЦНС регулируется женскими половыми гормонами эстрадиолом и прогестероном . Комбинация гормонов снижает концентрацию рецепторов в вентральном гиппокампе у крыс и, таким образом, может влиять на настроение. [22]
Генетика [ править ]
Было идентифицировано множество человеческих полиморфизмов, влияющих на экспрессию 5-HT 2C . Предлагаются значительные корреляции, особенно в отношении психических расстройств, таких как депрессия, ОКР и состояния, связанные с тревогой. Полиморфизм также коррелирует с восприимчивостью к ряду состояний, включая злоупотребление наркотиками и ожирение. Есть указания на то, что альтернативный сплайсинг 5-HT 2C рецептора регулируется snoRNA, называемой SNORD115 , делеция которой связана с синдромом Прадера-Вилли . [23] [24]Поскольку человеческий ген расположен в Х-хромосоме, у мужчин есть только одна копия гена, тогда как у женщин - две, а это означает, что мутации в гене влияют на фенотип мужчин, даже если аллель будет рецессивным по своей природе. Поскольку у женщин есть две копии гена, но в каждой клетке экспрессируется только один аллель, они представляют собой мозаику для полиморфизмов, что означает, что один генетический вариант может преобладать в одной ткани, а другой вариант будет преобладать в другой ткани (как в случае с все другие х-сцепленные генетические вариации).
Лиганды [ править ]
Первые аллостерические модуляторы были разработаны в 2018 году [25].
Агонисты [ править ]
- А-372 159
- AL-38022A
- CP-809,101
- CPD-1 [26]
- Фенфлурамин
- Лисурид
- Лорказерин
- Мезулергин
- МК-212
- Нафтилизопропиламин
- Норфенфлурамин
- Организация 12 962
- ORG-37 684
- Оксафлозан
- PF-04479745 [27]
- PNU-22394
- PNU-181731
- Психоделики
- Лизергамиды ( ЛСД и др.)
- Фенэтиламины ( 2C-B , DOI , DOM , мескалин и др.)
- Пиперазины ( mCPP , TFMPP и др.)
- Триптамины ( 5-MeO-DMT , буфотенин , DMT , псилоцин и др.)
- Ro60-0175
- Вабикасерин
- ПУТЬ-629
- ПУТЬ-161,503
- ПУТЬ-163,909
- YM-348
- CP-132,484 также агонист 5HT2a.
Частичные агонисты [ править ]
- Арипипразол
Антагонисты [ править ]
- Агомелатин
- CEPC [28]
- Элтопразин
- Этоперидон
- Флибансерин [29]
- Флуоксетин
- FR-260 010
- Тедатиоксетин
- Метизергид
- Миртазапин
- Нефазодон
- Норфлуоксетин
- О-десметилтрамадол
- Прометазин
- RS-102 221
- SB-200,646
- SB-221 284
- SB-228,357
- SB-242,084
- СДЗ SER-082
- Трамадол
- Тразодон
Обратные агонисты [ править ]
- Антидепрессанты [ необходима ссылка ]
- Трициклические препараты ( Амитриптилин , Кломипрамин , Имипрамин , Нортриптилин , Доксепин и др.)
- Тетрациклические препараты ( Миртазапин , Миансерин , Амоксапин и др.)
- Антигистаминные ( Ципрогептадин , гидроксизин , латрепирдин и т.д.)
- Нейролептики
- Typicals ( хлорпромазин , флуфеназин , Loxapine , тиоридазин , и т.д.)
- Атипичные препараты ( клозапин , оланзапин , кветиапин , рисперидон , зипразидон и др.)
- Цинансерин
- Дерамциклан
- Кетансерин
- LY-53,857
- Метерголин
- Метиотепин
- Пизотифен
- Ритансерин
- S-32212 [30]
- SB-206,553
- SB-228,357
- SB-243 213
- SB-242,084
Взаимодействия [ править ]
Было показано, что рецептор 5-HT 2C взаимодействует с MPDZ . [31] [32]
Редактирование РНК [ править ]
Пре-мРНК 5HT2CR может быть предметом редактирования РНК . [33] Это единственный рецептор серотонина, а также единственный член большого семейства из 7 трансмембранных рецепторов (7TMR), которые, как известно, редактируются. Различные уровни редактирования приводят к различным эффектам на функцию рецепторов.
Тип [ редактировать ]
Тип редактирования РНК, который происходит в пре-мРНК 5HT2CR, представляет собой редактирование аденозина в инозин (от A до I).
Редактирование РНК от A до I катализируется семейством аденозиндезаминаз, действующих на РНК (ADAR), которые специфически распознают аденозины в двухцепочечных областях пре-мРНК и дезаминируют их до инозина . Инозины распознаются как гуанозин механизмом трансляции клеток. Есть три члена семейства ADAR, ADAR 1-3, причем ADAR1 и ADAR2 являются единственными ферментативно активными членами. ADAR3считается, что он играет регулирующую роль в мозге. ADAR1 и ADAR2 широко экспрессируются в тканях, в то время как ADAR3 ограничивается мозгом. Двухцепочечные области РНК образуются спариванием оснований между остатками в области, близкой к области редактирующего сайта, с остатками обычно в соседнем интроне, но могут быть экзонной последовательностью. Область, которая образует пары оснований с областью редактирования, известна как редактируемая комплементарная последовательность (ECS).
ADARs bind взаимодействуют напрямую с субстратом дцРНК через свои двухцепочечные РНК-связывающие домены. Если сайт редактирования находится в кодирующей последовательности, это может привести к смене кодона. Это может привести к трансляции изоформы белка из-за изменения ее первичной белковой структуры. Следовательно, редактирование также может изменить функцию белка. Редактирование от A до I происходит в некодирующих последовательностях РНК, таких как интроны , нетранслируемые области (UTR), LINE , SINE (особенно Alu-повторы). Считается, что функция редактирования от A до I в этих областях включает создание сайтов сплайсинга и сохранение Среди прочего, РНК в ядре.
Местоположение [ править ]
Редактирование происходит в 5 различных близко расположенных сайтах экзона 5, что соответствует второй внутриклеточной петле конечного белка. Сайты известны как A, B, C '(ранее называвшиеся E), C и D, и предполагается, что они находятся в положениях аминокислот 156, 158 и 160. Некоторые изменения кодонов могут происходить из-за редактирования A-to-I в эти сайты. Могут встречаться 32 различных варианта мРНК, приводящие к 24 различным изоформам белка.
- Изолейцин в валин (I / V) в положении аминокислоты 157, 161.
- Изолейцин в метионин (I / M) в положении аминокислоты 157
- Аспартат к серину (N / S) на уровне 159
- Аспартат к аспарагину (N / D) на уровне 159
- От аспарагина к глицину (N / G) на 159.
Эти изменения кодонов, которые могут происходить из-за редактирования от A до I в этих сайтах, могут привести к максимуму 32 различным вариантам мРНК, приводящим к 24 различным изоформам белка. Количество изоформ белка меньше 32, поскольку некоторые аминокислоты кодируются более чем одним кодоном. [34] Другой сайт редактирования, сайт F, также был расположен в экзонной комплементарной последовательности (ECS) интрона 5. [35] ECS, необходимый для образования двухцепочечной структуры РНК, находится внутри интрона 5. [33]
Сохранение [ править ]
Редактирование РНК этого рецептора происходит в 4 местах у крысы. [33] Редактирование также происходит с помощью мыши. [36] Первая демонстрация редактирования РНК у крысы. [33] Преобладающей изоформой в головном мозге крыс является VNV, который отличается от наиболее распространенного типа, обнаруживаемого у людей. [33] [37] Редактирующая комплементарная последовательность, как известно, сохраняется у млекопитающих.
Регламент [ править ]
Рецептор 5-HT 2c является единственным редактируемым рецептором серотонина, несмотря на его близкое сходство последовательностей с другими членами семейства. [37] 5HT2CR отличается наличием несовершенного инвертированного повтора в конце экзона 5 и в начале интрона 5, что позволяет формировать дуплекс РНК, продуцирующий дцРНК, необходимую ADAR для редактирования. Было продемонстрировано, что нарушение этого перевернутого повтора прекращает всякое редактирование. [33]Различные изоформы мРНК 5HT2CR по-разному экспрессируются в головном мозге, но не все из 24 были обнаружены, возможно, из-за тканеспецифической экспрессии или низкочастотного редактирования определенного типа. Те изоформы, которые не выражаются совсем или с очень низкой частотой, связаны посредством редактирования только на сайте C 'и / или сайте B, но не на сайте A. Некоторые примеры различий в частоте редактирования и сайта, редактируемого в разных частях человеческий мозг 5HT2CR включает низкую частоту редактирования в мозжечке, и почти все редактирование происходит в сайте D, в то время как в гиппокампе частота редактирования выше, а сайт A является основным сайтом редактирования. Сайт C 'находится только в таламусе в редактированном виде. Наиболее распространенной изоформой в мозге человека является изоформа VSV. [34] [37] [38]
Нокаут мышей и другие исследования были использованы для определения того, какой фермент ADAR участвует в редактировании. Было продемонстрировано, что редактирование на сайтах A и B связано с редактированием ADAR1. [39] [40] [41] Кроме того, поскольку экспрессия ADAR1 увеличивается в ответ на присутствие интерферона α, также было замечено, что редактирование сайтов A и B также увеличивалось из-за этого. [39] Сайты C 'и D требуют ADAR2, и редактирование уменьшается за счет присутствия ADAR1, при этом редактирование сайта C' наблюдается только у мышей с двойным нокаутом ADAR1. [42]Было показано, что сайт C в основном редактируется ADAR2, но в присутствии усиленной экспрессии ADAR1 наблюдалось усиление редактирования этого сайта, и присутствие ферментов также может приводить к ограниченному редактированию у мышей, нокаутированных по ADAR 2. [39] [42] Это демонстрирует, что между двумя редактирующими ферментами от A до I должно быть какое-то взаимодействие формы. Также такие взаимодействия и тканеспецифическая экспрессия взаимодействия ADAR могут объяснить разнообразие паттернов редактирования в различных областях мозга.
Последствия [ править ]
Во-вторых, паттерн редактирования контролирует количество мРНК 5-HT2CR, которая приводит к экспрессии полноразмерного белка посредством модуляции выбора альтернативных сайтов сплайсинга 76,77. Среди трех альтернативных донорных сайтов сплайсинга (GU1 - GU3; рис. 4C), GU2 является единственным сайтом, который формирует зрелую мРНК для производства функционального полноразмерного белка 5-HT2CR. Неотредактированные пре-мРНК имеют тенденцию к сплайсингу на сайте GU1, что приводит к усеченному нефункциональному белку при трансляции 76,77. Однако большинство пре-мРНК, редактируемых более чем в одной позиции, сплайсируются в GU2 77. Таким образом, когда редактирование неэффективно, усиление сплайсинга в GU1 может действовать как контрольный механизм для снижения биосинтеза 5-HT2CR-INI и тем самым ограничения серотонинового ответа. . В третьих,Редактирование РНК контролирует конечный физиологический выход конститутивно активных рецепторов, влияя на экспрессию 5-HT2CR на клеточной поверхности. 5-HT2CR-VGV, который демонстрирует самый низкий уровень конститутивной активности, полностью экспрессируется на поверхности клетки в базовых условиях и быстро интернализуется в присутствии агониста 78. Напротив, 5-HT2CR-INI постоянно интернализуется и накапливается в эндосомах 78.
Состав
Как уже упоминалось, редактирование приводит к изменению нескольких кодонов. Сайты редактирования находятся во втором внутриклеточном домене белка, который также является доменом связывания G-белка рецепторов. Следовательно, редактирование этих сайтов может повлиять на сродство рецептора к связыванию G-белка. [33]
Функция
Редактирование приводит к снижению сродства к конкретным G-белкам, что, в свою очередь, влияет на внутреннюю передачу сигналов через вторичные мессенджеры (система передачи сигналов фосфолипазы C). Полностью отредактированная изоформа VGV значительно снижает активность 5-HT, связывание с G-белком и связывание с агонистом по сравнению с неотредактированной изоформой белка INI. 72-76. Большинство доказательств влияния редактирования на функцию поступает из последующих измерений активности рецепторов, связывания радиолиганда и функциональных исследований. Тормозящие эффекты связаны со степенью редактирования. Те изоформы с более высоким уровнем редактирования требуют более высоких уровней серотонина для активации пути фосфолипазы c. Неотредактированная форма INI имеет большую тенденцию к изомеризации в активную форму, которая может легче взаимодействовать с G-белками.Это указывает на то, что редактирование РНК здесь может быть механизмом регуляции возбудимости нейронов путем стабилизации передачи сигналов рецептора.[33] [37]
Также считается, что редактирование влияет на экспрессию подтипа рецептора на клеточной поверхности. Полностью отредактированный VGV, который имеет самый низкий уровень конститутивной активности, полностью экспрессируется на поверхности клетки, в то время как неотредактированный INI интернализуется и накапливается в эндосоме. [43]
Также считается, что редактирование влияет на сварку. Существуют три разные сплайсированные изоформы рецептора. Редактирование регулирует количество мРНК 5HT2CR, что приводит к трансляции полноразмерного белка выборки альтернативных сайтов сплайсинга. t76,77. Эти сайты сплайсинга обозначаются как Gu1, Gu2, GU3. Только сплайсинг сайта GU2 приводит к трансляции полноразмерного рецептора, тогда как редактирование на GU1, как известно, приводит к трансляции усеченного белка. Считается, что это регуляторный механизм для уменьшения количества неотредактированной изоформы INI для ограничения серотонинового ответа, когда редактирование неэффективно. Большинство редактируемых пре-мРНК сплайсируются на сайте GU2. [35] [38]
Нарушение регуляции
Семейство рецепторов серотонина часто связано с патологией нескольких психических состояний человека, таких как шизофрения, тревога, биполярное расстройство и большая депрессия. [44] Было проведено несколько экспериментальных исследований эффектов альтернативных паттернов редактирования 5HT2CR и этих условий с широким разбросом результатов, особенно тех, которые касаются шизофрении. [45] Некоторые исследования отметили, что у жертв суицида в депрессивном состоянии наблюдается усиление редактирования РНК на участке А. [13] [45] У людей, страдающих большой депрессией, наблюдалось усиление редактирования электронных сайтов. [46]В моделях на крысах это увеличение также наблюдается и может быть отменено флуоксетином с некоторым предположением, что редактирование E-сайта может быть связано с большой депрессией. [47] [48]
См. Также [ править ]
- 5-HT рецептор
- 5-HT 2 рецептор
- Беспокойство / депрессия, вызванная агрессией
- Ингибитор норэпинефрина-дофамина
Ссылки [ править ]
- ^ a b c GRCh38: Ensembl, выпуск 89: ENSG00000147246 - Ensembl , май 2017 г.
- ^ a b c GRCm38: выпуск Ensembl 89: ENSMUSG00000041380 - Ensembl , май 2017 г.
- ^ "Human PubMed Reference:" . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ "Entrez Gene: HTR2C 5-гидрокситриптамин (серотонин) рецептор 2C" .
- ^ Ст штат Нью - Джерси, Вандерхейден Р, ван Alebeek С, Кломп Дж, де Бур Т, ван Делфт А.М., Olijve Вт (ноябрь 1994 года). «Геномная организация и функциональная экспрессия гена, кодирующего рецептор серотонина 5-HT2C человека». Европейский журнал фармакологии . 269 (3): 339–48. DOI : 10.1016 / 0922-4106 (94) 90042-6 . PMID 7895773 .
- Перейти ↑ Herrick-Davis K, Grinde E, Lindsley T, Cowan A, Mazurkiewicz JE (июль 2012 г.). «Размер олигомера серотонинового 5-гидрокситриптамин 2C (5-HT2C) рецептора, выявленный с помощью флуоресцентной корреляционной спектроскопии с анализом гистограммы подсчета фотонов: доказательства гомодимеров без мономеров или тетрамеров» . Журнал биологической химии . 287 (28): 23604–14. DOI : 10.1074 / jbc.M112.350249 . PMC 3390635 . PMID 22593582 .
- ^ Пэн Y, McCorvy JD, Harpsøe К, Lansu К, Юань S, Попов Р, Ку л, Pu М, Че Т, Nikolajsen НЧ, Хуанг XP, Ву Y, Шен л, Бьорн-Есимото Мы, Дин К, Wacker Д , Han GW, Cheng J, Katritch V, Jensen AA, Hanson MA, Zhao S, Gloriam DE, Roth BL, Stevens RC, Liu ZJ (февраль 2018 г.). «Структуры рецепторов 5-HT2C раскрывают структурную основу полипармакологии GPCR» . Cell . 172 (4): 719–730.e14. DOI : 10.1016 / j.cell.2018.01.001 . PMC 6309861 . PMID 29398112 .
- ^ Abramowski Д, Риго М, дык D, D Хойер, Staufenbiel М (1995). «Локализация белка рецептора 5-Hydroxytryptamine2c в мозге человека и крысы с использованием специальных антисывороток». Нейрофармакология . 34 (12): 1635–1645. DOI : 10.1016 / 0028-3908 (95) 00138-7 . PMID 8788961 .
- ^ Hoffman BJ, Mezey E (1989). «Распределение мРНК рецептора серотонина 5-HT1C в мозге взрослых крыс». Письма FEBS . 247 (2): 453–62. DOI : 10.1016 / 0014-5793 (89) 81390-0 . PMID 2714444 .
- ^ Alex KD, Yavanian GJ, Макфарлейн HG, Плутон CP, Pehek EA (март 2005). «Модуляция высвобождения дофамина полосатыми рецепторами 5-HT2C». Синапс . 55 (4): 242–51. DOI : 10.1002 / syn.20109 . PMID 15668911 .
- ↑ Heisler LK, Zhou L, Bajwa P, Hsu J, Tecott LH (июль 2007 г.). «Рецепторы серотонина 5-HT (2C) регулируют тревожное поведение» . Гены, мозг и поведение . 6 (5): 491–6. DOI : 10.1111 / j.1601-183X.2007.00316.x . PMID 17451451 .
- ^ a b Нисвендер К.М., Херрик-Дэвис К., Дилли Г.Е., Мельцер Х.Ю., Оверхользер Дж. К., Стокмайер, Калифорния, Эмесон РБ, Сандерс-Буш Е. «Редактирование РНК человеческого рецептора серотонина 5-HT2C. Изменения в суициде и последствия для серотонинергической фармакотерапии» . Нейропсихофармакология . 24 (5): 478–91. DOI : 10.1016 / S0893-133X (00) 00223-2 . PMID 11282248 .
- ^ Десять D, Baghai TC, Möller HJ (2010). «Агомелатин: доказательства его места в лечении депрессии» . Основные доказательства . 4 : 171–9. DOI : 10,2147 / CE.S6005 . PMC 2899775 . PMID 20694073 .
- ^ a b Ni YG, Miledi R (март 1997 г.). «Блокировка рецепторов серотонина 5HT2C флуоксетином (прозак)» . Труды Национальной академии наук Соединенных Штатов Америки . 94 (5): 2036–40. Bibcode : 1997PNAS ... 94.2036N . DOI : 10.1073 / pnas.94.5.2036 . PMC 20038 . PMID 9050900 .
- ^ a b Берг К.А., Харви Дж. А., Spampinato U, Clarke WP (декабрь 2005 г.). «Физиологическое значение конститутивной активности рецепторов 5-HT2A и 5-HT2C». Направления фармакологических наук . 26 (12): 625–30. DOI : 10.1016 / j.tips.2005.10.008 . PMID 16269190 .
- ^ Del'Guidice Т, Р Lemay, Лемассон М, Левасёр-Моро J, S Манта, Etievant А, Эскофья G, Дора ФГ, Роман Ф., Болье JM (апрель 2014). «Стимуляция рецепторов 5-HT2C улучшает когнитивный дефицит, вызванный мутацией потери функции триптофангидроксилазы 2 человека» . Нейропсихофармакология . 39 (5): 1125–34. DOI : 10.1038 / npp.2013.313 . PMC 3957106 . PMID 24196946 .
- ^ Эспозито E (февраль 2006 г.). «Взаимодействие серотонина и дофамина как фокус новых антидепрессантов». Текущие цели в отношении лекарств . 7 (2): 177–85. DOI : 10,2174 / 138945006775515455 . PMID 16475959 .
- ^ Bubar MJ, Cunningham KA (2006). «Серотониновые рецепторы 5-HT2A и 5-HT2C как потенциальные мишени для модуляции использования психостимуляторов и зависимости». Актуальные темы медицинской химии . 6 (18): 1971–85. DOI : 10.2174 / 156802606778522131 . PMID 17017968 .
- ↑ Jørgensen HS (ноябрь 2007 г.). «Исследования нейроэндокринной роли серотонина». Датский медицинский бюллетень . 54 (4): 266–88. PMID 18208678 .
- ^ Хейлер ЛК, Pronchuk Н, Nonogaki К, Чжоу л, Raber Дж, Танг л, Ео Г.С., O'Rahilly S, Colmers WF, Elmquist Ю.К., Tecott ЛГ (июнь 2007 г.). «Серотонин активирует гипоталамо-гипофизарно-надпочечниковую систему посредством стимуляции рецептора серотонина 2С» . Журнал неврологии . 27 (26): 6956–64. DOI : 10.1523 / JNEUROSCI.2584-06.2007 . PMID 17596444 .
- ^ Бирзниеце V, Johansson IM, Ван MD, Бэкстрем T, T Олссон (февраль 2002). «Эффекты гормона яичников на экспрессию мРНК рецепторов 5-гидрокситриптамина (2A) и 5-гидрокситриптамина (2C) в вентральном гиппокампе и фронтальной коре головного мозга самок крыс». Письма неврологии . 319 (3): 157–61. DOI : 10.1016 / S0304-3940 (01) 02570-8 . PMID 11834317 .
- Перейти ↑ Kishore S, Stamm S (январь 2006 г.). «SnoRNA HBII-52 регулирует альтернативный сплайсинг серотонинового рецептора 2C». Наука . 311 (5758): 230–2. Bibcode : 2006Sci ... 311..230K . DOI : 10.1126 / science.1118265 . PMID 16357227 .
- ^ Sahoo T, D - дель Годио, немецкий JR, Shinawi M, Питерс SU, Person RE, Garnica A, Cheung SW, Beaudet AL (июнь 2008). «Фенотип Прадера-Вилли, вызванный отцовской недостаточностью для небольшого кластера ядрышковой РНК HBII-85 C / D box» . Генетика природы . 40 (6): 719–21. DOI : 10.1038 / ng.158 . PMC 2705197 . PMID 18500341 .
- ^ Wild CT, Miszkiel JM, Уолд Е.А., Soto CA, Дин C, Хартли RM, Белый MA, Anastasio NC, Cunningham KA, Чжоу J (апрель 2018). «Дизайн, синтез и характеристика 4-ундецилпиперидин-2-карбоксамидов как положительных аллостерических модуляторов рецептора серотонина (5-HT) 5-HT2C» . J. Med. Chem . 62 (1): 288–305. DOI : 10.1021 / acs.jmedchem.8b00401 . PMC 6533912 . PMID 29620897 .
- ^ Родригес MM, Overshiner C, Leander JD, Li X, Morrow D, Conway RG, Nelson DL, Briner K, Witkin JM (2017). «Поведенческие эффекты нового агониста рецепторов бензофуранил-пиперазин-серотонин-2С предполагают возможное терапевтическое применение при лечении обсессивно-компульсивного расстройства» . Фронтальная психиатрия . 8 : 89. DOI : 10,3389 / fpsyt.2017.00089 . PMC 5438973 . PMID 28588509 .
- ^ Стоер Р.И., Бреннан П.Е., Браун А.Д., Бунгей П.Дж., Конлон К.М., Корбетт М.С. и др. (Июнь 2014 г.). «Многопараметрическая оптимизация в открытии лекарств для ЦНС: дизайн пиримидо [4,5-d] азепинов как сильнодействующих агонистов 5-гидрокситриптаминовых рецепторов 2C (5-HT₂C) с высокой функциональной селективностью по отношению к рецепторам 5-HT₂A и 5-HT₂B». Журнал медицинской химии . 57 (12): 5258–69. DOI : 10.1021 / jm5003292 . PMID 24878222 .
- ^ McCorvy JD, Харланд AA, Maglathlin R, Nichols DE (2011). «Антагонист рецептора 5-НТ (2С) усиливает обусловленное амфетамином низкодозированное предпочтение условного места» . Письма неврологии . 505 (1): 10–3. DOI : 10.1016 / j.neulet.2011.07.036 . PMC 3213641 . PMID 21827831 .
- ↑ Stahl SM, Sommer B, Allers KA (январь 2011 г.). «Многофункциональная фармакология флибансерина: возможный механизм терапевтического действия при гипоактивном расстройстве полового влечения». Журнал сексуальной медицины . 8 (1): 15–27. DOI : 10.1111 / j.1743-6109.2010.02032.x . PMID 20840530 .
- ^ Dekeyne А, Brocco М, Луазо Ж, Гобер А, Заклепка JM, Ди Кара Б, Кремерса Т.И., Флик G, Fone KC, Уотсон ди - джей, Папп М, Sharp Т, Серес Р, Cespuglio Р, Оливье В, Чан JS, Лавьель Г., Миллан М.Дж. (март 2012 г.). «S32212, новый обратный агонист рецептора серотонина типа 2C / антагонист α2-адренорецептора и потенциальный антидепрессант: II. Поведенческая, нейрохимическая и электрофизиологическая характеристика». Журнал фармакологии и экспериментальной терапии . 340 (3): 765–80. DOI : 10,1124 / jpet.111.187534 . PMID 22178753 .
- ^ Бекамел C, Фигге A, Поляк S, Дюмуи A, Пелеш E, Бокерт Дж, Любберт Х, Ульмер C (апрель 2001 г.). «Взаимодействие серотониновых 5-гидрокситриптаминовых рецепторов типа 2C с PDZ10 мульти-PDZ-домена белка MUPP1» . Журнал биологической химии . 276 (16): 12974–82. DOI : 10.1074 / jbc.M008089200 . PMID 11150294 .
- ^ Ullmer C, Schmuck K, Figge A, Lübbert H (март 1998). «Клонирование и характеристика MUPP1, нового белка домена PDZ» . Письма FEBS . 424 (1–2): 63–8. DOI : 10.1016 / S0014-5793 (98) 00141-0 . PMID 9537516 .
- ^ a b c d e f g h Бернс К.М., Чу Х., Рутер С.М., Хатчинсон Л.К., Кантон Х., Сандерс-Буш Е., Эмесон РБ (май 1997 г.). «Регулирование связывания G-белка рецептора серотонина-2C путем редактирования РНК». Природа . 387 (6630): 303–8. Bibcode : 1997Natur.387..303B . DOI : 10.1038 / 387303a0 . PMID 9153397 .
- ^ a b Фитцджеральд Л.В., Айер Дж., Конклин Д.С., Краузе С.М., Маршалл А., Паттерсон Дж. П., Тран Д.П., Джонак Дж. Дж., Хартиг ПР (август 1999 г.). «Редактирование информационной РНК рецептора серотонина 5-HT2C человека» . Нейропсихофармакология . 21 (2 доп.): 82С – 90С. DOI : 10.1016 / S0893-133X (99) 00004-4 . PMID 10432493 .
- ^ a b Flomen R, Knight J, Sham P, Kerwin R, Makoff A (2004). «Доказательства того, что редактирование РНК модулирует выбор сайта сплайсинга в гене рецептора 5-HT2C» . Исследования нуклеиновых кислот . 32 (7): 2113–22. DOI : 10.1093 / NAR / gkh536 . PMC 407821 . PMID 15087490 .
- ^ Hackler Е.А., Эйри DC, Shannon CC, Sodhi MS, Сандерс-Буш E (май 2006). «Редактирование РНК рецептора 5-HT (2C) в миндалине мышей C57BL / 6J, DBA / 2J и BALB / cJ». Неврологические исследования . 55 (1): 96–104. DOI : 10.1016 / j.neures.2006.02.005 . PMID 16580757 .
- ^ a b c d Niswender CM, Copeland SC, Herrick-Davis K, Emeson RB, Sanders-Bush E (апрель 1999 г.). «Редактирование РНК человеческого серотонин-5-гидрокситриптамин 2С рецептора подавляет конститутивную активность» . Журнал биологической химии . 274 (14): 9472–8. DOI : 10.1074 / jbc.274.14.9472 . PMID 10092629 .
- ↑ a b Wang Q, O'Brien PJ, Chen CX, Cho DS, Murray JM, Nishikura K (март 2000 г.). «Измененные функции связывания G-белка изоформы редактирования РНК и варианта сплайсинга рецепторов серотонина 2С» . Журнал нейрохимии . 74 (3): 1290–300. DOI : 10.1046 / j.1471-4159.2000.741290.x . PMID 10693963 .
- ^ a b c Ян В., Ван Кью, Канес С.Дж., Мюррей Дж. М., Нишикура К. (апрель 2004 г.). «Редактирование измененной РНК рецептора серотонина 5-HT2C, индуцированное интерфероном: последствия для депрессии, связанной с терапией цитокинами». Исследование мозга. Молекулярное исследование мозга . 124 (1): 70–8. DOI : 10.1016 / j.molbrainres.2004.02.010 . PMID 15093687 .
- ^ Sukma M, Tohda M, Watanabe H, Мацумото K (август 2005). «Различия в экспрессии мРНК ферментов редактирования РНК в дифференцированных и недифференцированных клетках NG108-15» . Журнал фармакологических наук . 98 (4): 467–70. DOI : 10,1254 / jphs.SC0050074 . PMID 16082172 .
- ^ Tohda M, Sukma M, Watanabe H (октябрь 2004). «Редактирование РНК и короткий вариант мРНК рецептора серотонина 2C в нейронально дифференцированных клетках NG108-15» . Журнал фармакологических наук . 96 (2): 164–9. DOI : 10,1254 / jphs.FP0040227 . PMID 15492466 .
- ^ a b Hartner JC, Schmittwolf C, Kispert A, Müller AM, Higuchi M, Seeburg PH (февраль 2004 г.). «Распад печени у эмбриона мыши, вызванный дефицитом РНК-редактирующего фермента ADAR1» . Журнал биологической химии . 279 (6): 4894–902. DOI : 10.1074 / jbc.M311347200 . PMID 14615479 .
- Перейти ↑ Marion S, Weiner DM, Caron MG (январь 2004 г.). «Редактирование РНК вызывает изменение в десенсибилизации и транспортировке изоформ рецептора 5-гидрокситриптамина 2c» . Журнал биологической химии . 279 (4): 2945–54. DOI : 10.1074 / jbc.M308742200 . PMID 14602721 .
- Перейти ↑ Baxter G, Kennett G, Blaney F, Blackburn T (март 1995). «Подтипы рецепторов 5-HT2: воссоединилась семья?». Направления фармакологических наук . 16 (3): 105–10. DOI : 10.1016 / S0165-6147 (00) 88991-9 . PMID 7792930 .
- ^ a b Ивамото К., Като Т. (август 2003 г.). «Редактирование РНК рецептора серотонина 2C в человеческом посмертном мозге основных психических расстройств». Письма неврологии . 346 (3): 169–72. DOI : 10.1016 / S0304-3940 (03) 00608-6 . PMID 12853111 .
- ^ Гуревич I, Тамир H, Аранго V, Дворк AJ, Mann JJ, Schmauss C (апрель 2002). «Измененное редактирование пре-мРНК рецептора серотонина 2C в префронтальной коре головного мозга жертв суицида в депрессии». Нейрон . 34 (3): 349–56. DOI : 10.1016 / S0896-6273 (02) 00660-8 . PMID 11988167 .
- ^ Ивамото К, Накатани Н, Bundo М, Ёшикава Т, Като Т (сентябрь 2005 г.). «Измененное редактирование РНК рецептора серотонина 2C в модели депрессии на крысах». Неврологические исследования . 53 (1): 69–76. DOI : 10.1016 / j.neures.2005.06.001 . PMID 16005997 .
- ^ Гуревич I, Englander MT, Adlersberg M, Сигал NB, Schmauss C (декабрь 2002). «Модуляция редактирования рецептора серотонина 2C за счет устойчивых изменений серотонинергической нейротрансмиссии» . Журнал неврологии . 22 (24): 10529–32. DOI : 10.1523 / JNEUROSCI.22-24-10529.2002 . PMID 12486144 .
Внешние ссылки [ править ]
- Человек HTR2C место генома и HTR2C ген подробно страницу в браузере УСК генома .
- Обзор всей структурной информации, доступной в PDB для UniProt : P28335 (рецептор 5-гидрокситриптамина 2C) в PDBe-KB .
Дальнейшее чтение [ править ]
- Нисвендер CM, Сандерс-Буш Э., Эмесон РБ (декабрь 1998 г.). «Идентификация и характеристика событий редактирования РНК в рецепторе 5-HT2C». Летопись Нью-Йоркской академии наук . 861 (1): 38–48. Bibcode : 1998NYASA.861 ... 38N . DOI : 10.1111 / j.1749-6632.1998.tb10171.x . PMID 9928237 .
- Хойер Д., Хэннон Дж. П., Мартин Г. Р. (апрель 2002 г.). «Молекулярное, фармакологическое и функциональное разнообразие рецепторов 5-HT». Фармакология, биохимия и поведение . 71 (4): 533–54. DOI : 10.1016 / S0091-3057 (01) 00746-8 . PMID 11888546 .
- Раймонд Дж. Р., Мухин Ю. В., Геласко А., Тернер Дж., Коллинсворт Г., Gettys TW, Grewal JS, Гарновская М. Н. (2002). «Множественность механизмов передачи сигнала рецептора серотонина». Фармакология и терапия . 92 (2–3): 179–212. DOI : 10.1016 / S0163-7258 (01) 00169-3 . PMID 11916537 .
- Ван Оекелен Д., Луйтен У.Х., Лейсен Дж. Э. (апрель 2003 г.). «Рецепторы 5-HT2A и 5-HT2C и их свойства атипичной регуляции». Науки о жизни . 72 (22): 2429–49. DOI : 10.1016 / S0024-3205 (03) 00141-3 . PMID 12650852 .
- Рейнольдс Г.П., Темплман Л.А., Чжан З.Дж. (июль 2005 г.). «Роль полиморфизмов рецептора 5-HT2C в фармакогенетике лечения антипсихотическими препаратами». Прогресс в нейропсихофармакологии и биологической психиатрии . 29 (6): 1021–8. DOI : 10.1016 / j.pnpbp.2005.03.019 . PMID 15953671 .
- Миллан MJ (2006). «Рецепторы серотонина 5-HT2C как мишень для лечения депрессивных и тревожных состояний: внимание к новым терапевтическим стратегиям». Терапия . 60 (5): 441–60. DOI : 10,2515 / Терапи: 2005065 . PMID 16433010 .
- Милатович А., Сие К.Л., Бонаминио Г., Текотт Л., Юлиус Д., Франк Ю. (декабрь 1992 г.). «Ген рецептора серотонина 1c, относящийся к Х-хромосоме у человека (полоса q24) и мыши (полосы D-F4)». Молекулярная генетика человека . 1 (9): 681–4. DOI : 10.1093 / HMG / 1.9.681 . PMID 1302605 .
- Зальцман А.Г., Морс Б., Уитман М.М., Иванщенко Ю., Джей М., Фелдер С. (декабрь 1991 г.). «Клонирование подтипов человеческого серотонина 5-HT2 и 5-HT1C рецепторов». Сообщения о биохимических и биофизических исследованиях . 181 (3): 1469–78. DOI : 10.1016 / 0006-291X (91) 92105-S . PMID 1722404 .
- Лаппалайнен Дж., Чжан Л., Дин М., Оз М., Одзаки Н., Ю. Д.Х., Вирккунен М., Вес Ф, Линнойла М., Голдман Д. (май 1995 г.). «Идентификация, экспрессия и фармакология замены Cys23-Ser23 в гене рецептора 5-HT2c человека (HTR2C)» . Геномика . 27 (2): 274–9. DOI : 10.1006 / geno.1995.1042 . PMID 7557992 .
- Текотт Л.Х., Сан Л.М., Акана С.Ф., Страк А.М., Ловенштейн Д.Х., Даллман М.Ф., Джулиус Д. (апрель 1995 г.). «Расстройство пищевого поведения и эпилепсия у мышей, лишенных рецепторов серотонина 5-HT2c». Природа . 374 (6522): 542–6. Bibcode : 1995Natur.374..542T . DOI : 10.1038 / 374542a0 . PMID 7700379 .
- Стэм Нью-Джерси, Вандерхейден П., ван Алебек К., Кломп Дж., Де Бур Т., ван Делфт А.М., Олийве В. (ноябрь 1994 г.). «Геномная организация и функциональная экспрессия гена, кодирующего рецептор серотонина 5-HT2C человека». Европейский журнал фармакологии . 269 (3): 339–48. DOI : 10.1016 / 0922-4106 (94) 90042-6 . PMID 7895773 .
- Се Э, Чжу Л., Чжао Л., Чанг Л.С. (август 1996 г.). «Рецептор серотонина 5-HT2C человека: полная кДНК, геномная структура и альтернативно сплайсированный вариант». Геномика . 35 (3): 551–61. DOI : 10.1006 / geno.1996.0397 . PMID 8812491 .
- Бернс С.М., Чу Х., Рутер С.М., Хатчинсон Л.К., Кантон Х., Сандерс-Буш Э., Эмесон РБ (май 1997 г.). «Регулирование связывания G-белка рецептора серотонина-2C путем редактирования РНК». Природа . 387 (6630): 303–8. Bibcode : 1997Natur.387..303B . DOI : 10.1038 / 387303a0 . PMID 9153397 .
- Бреннан Т.Дж., Сили В.В., Килгард М., Шрейнер К.Э., Текотт Л.Х. (август 1997 г.). «Звук-индуцированные судороги у мышей с мутантным рецептором серотонина 5-HT2c». Генетика природы . 16 (4): 387–90. DOI : 10.1038 / ng0897-387 . PMID 9241279 .
- Ульмер К., Шмук К., Фигге А., Любберт Х. (март 1998 г.). «Клонирование и характеристика MUPP1, нового белка домена PDZ» . Письма FEBS . 424 (1–2): 63–8. DOI : 10.1016 / S0014-5793 (98) 00141-0 . PMID 9537516 .
- Самоховец Дж., Смолка М., Винтерер Дж., Роммельспахер Х., Шмидт Л.Г., Сандер Т. (апрель 1999 г.). «Анализ ассоциации между полиморфизмом замены Cys23Ser гена рецептора 5-HT2c человека и гипервозбудимостью нейронов». Американский журнал медицинской генетики . 88 (2): 126–30. DOI : 10.1002 / (SICI) 1096-8628 (19990416) 88: 2 <126 :: AID-AJMG6> 3.0.CO; 2-M . PMID 10206230 .
- Каргилл М., Альтшулер Д., Ирландия Дж., Склар П., Ардли К., Патил Н., Шоу Н., Лейн К.Р., Лим Э.П., Кальянараман Н., Немеш Дж., Зиаугра Л., Фридланд Л., Рольф А., Уоррингтон Дж., Липшутц Р., Дейли Г.К. , Lander ES (июль 1999 г.). «Характеристика однонуклеотидных полиморфизмов в кодирующих областях генов человека». Генетика природы . 22 (3): 231–8. DOI : 10,1038 / 10290 . PMID 10391209 .
- Marshall SE, Bird TG, Hart K, Welsh KI (декабрь 1999 г.). «Единый подход к анализу генетической изменчивости серотонинергических путей». Американский журнал медицинской генетики . 88 (6): 621–7. DOI : 10.1002 / (SICI) 1096-8628 (19991215) 88: 6 <621 :: AID-AJMG9> 3.0.CO; 2-H . PMID 10581480 .
- Бэкстрем Дж. Р., Прайс Р. Д., Ризонер Д. Т., Сандерс-Буш Е. (август 2000 г.). «Делеция мотива распознавания PDZ серотонинового 5-HT2C рецептора предотвращает фосфорилирование рецептора и задерживает повторную сенсибилизацию рецепторных ответов» . Журнал биологической химии . 275 (31): 23620–6. DOI : 10.1074 / jbc.M000922200 . PMID 10816555 .
Эта статья включает текст из Национальной медицинской библиотеки США , который находится в общественном достоянии .