 | |
| Клинические данные | |
|---|---|
| Произношение | / Eɪ ˌ п ɪ DJ ʊ л ə е ʌ п dʒ ɪ п / AY- NID -yuu-lə- ПОТЕХИ -jin |
| Торговые наименования | Эраксис, Экальта |
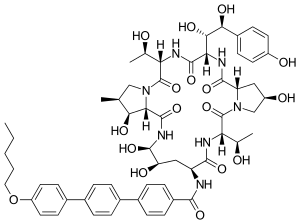
| Другие имена | (4 R , 5 S ) -4,5-Дигидрокси- N 2 - [[4 '' - (пентилокси) - пара- терфенил-4-ил] карбонил] - L -орнитил- L- треонил- транс- 4- гидрокси- L- пролил- ( S ) -4-гидрокси-4- ( п- гидроксифенил) - L- треонил- L- треонил- (3 S , 4 S ) -3-гидрокси-4-метил- L- пролин циклический (6 → 1) -пептид [1] 1 - [(4 R , 5 R ) -4,5-дигидрокси- N 2 - [[4 '' - (пентилокси) [1 ', 1': 4 ', 1 '' -терфенил] -4-ил] карбонил] -L -орнитин] эхинокандин B [2] |
| AHFS / Drugs.com | Монография |
| Данные лицензии |
|
| Пути администрирования | Внутривенный |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Биодоступность | 100% (только для внутривенного введения) |
| Связывание с белками | Широкий (> 99%) |
| Метаболизм | Печеночный метаболизм не наблюдается, система CYP не задействована |
| Ликвидация Период полураспада | 27 часов; 40–50 часов (терминал) |
| Экскреция | Кал (~ 30%), моча (<1%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ |
|
| Панель управления CompTox ( EPA ) |
|
| ECHA InfoCard | 100.184.856 |
| Химические и физические данные | |
| Формула | C 58 H 73 N 7 O 17 |
| Молярная масса | 1 140 .254 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
| | |
Анидулафунгин ( МНН ) [1] : 42 (торговые названия Eraxis , Ecalta ) - полусинтетический эхинокандин, используемый в качестве противогрибкового препарата . Ранее он был известен как LY303366. [3] [4] [5] Он также может применяться при лечении инвазивной инфекции Aspergillus при использовании в сочетании с вориконазолом . [6] Это представитель класса противогрибковых препаратов, известных как эхинокандины ; его механизм действия заключается в ингибировании (1 → 3) -β- D- глюканасинтаза, фермент, важный для синтеза клеточной стенки грибов. [7]
Показания [ править ]
- Кандидемия и другие формы инвазивных инфекций Candida (внутрибрюшной абсцесс и перитонит )
- Кандидоз пищевода
Анидулафунгин не изучался при эндокардите , остеомиелите и менингите, вызванном Candida , и не изучался на достаточном количестве пациентов с нейтропенией, чтобы определить эффективность в этой группе. [2]
Фармакодинамика и фармакокинетика [ править ]
Анидулафунгин значительно отличается от других противогрибковых средств тем, что подвергается химическому разложению до неактивных форм при pH и температуре тела . Поскольку он не зависит от ферментативной деградации или экскреции через печень или почки, препарат безопасен для применения у пациентов с любой степенью печеночной или почечной недостаточности. [8]
Объем распределения : 30–50 л.
Очевидно, анидулафунгин не метаболизируется в печени . Этот специфический препарат подвергается медленному химическому гидролизу до пептида с открытым кольцом, который не обладает противогрибковой активностью. Период полувыведения препарата составляет 27 часов. Около 30% выводится с калом (10% в неизмененном виде). Менее 1% выводится с мочой. [9] [10] [11]
Механизм действия [ править ]
Анидулафунгин ингибирует глюкансинтазу , фермент, важный в образовании (1 → 3) -β- D- глюкана, основного компонента клеточной стенки грибов. Глюкан-синтаза не присутствует в клетках млекопитающих, поэтому является привлекательной мишенью для противогрибковой активности. [12]
Полусинтез [ править ]
Анидулафунгин производится путем полусинтеза. Исходным материалом является эхинокандин B ( продукт ферментации липопептидов Aspergillus nidulans или близкородственных видов, A. rugulosus ), который подвергается деацилированию (расщеплению линолеоильной боковой цепи) под действием фермента деацилазы из бактерии Actinoplanes utahensis ; [13] за три последовательных этапа синтеза, включая химическое реацилирование, синтезируется противогрибковый препарат анидулафунгин [12] [14] .
История [ править ]
Анидулафунгин был первоначально открыт в лабораториях Lilly Тернером и Дебоно и лицензирован Vicuron Pharmaceuticals, которая представила его в FDA. [15] Pfizer приобрела препарат после приобретения Vicuron осенью 2005 г. [16] Pfizer получила одобрение Управления по контролю за продуктами и лекарствами (FDA) 21 февраля 2006 г. [17]
Ссылки [ править ]
- ^ a b «Международные непатентованные названия фармацевтических субстанций (МНН). Рекомендуемые международные непатентованные названия: Список 43» (PDF) . Всемирная организация здоровья. 2000 . Проверено 11 ноября +2016 .
- ^ a b «Eraxis (анидулафунгин) для инъекций, для внутривенного использования. Полная информация по назначению» . Рериг (подразделение Pfizer, Inc.), Нью-Йорк, 10017 . Проверено 11 ноября +2016 .
- ^ Krause DS, Реинхардт J Васкес JA, Reboli А, Голдстеин ВР, Wible М, Т Хенкель (2004). «Фаза 2, рандомизированное исследование с определением дозировки, оценивающее безопасность и эффективность анидулафунгина при инвазивном кандидозе и кандидемии» . Противомикробные агенты Chemother . 48 (6): 2021–4. DOI : 10,1128 / AAC.48.6.2021-2024.2004 . PMC 415613 . PMID 15155194 .
- ^ Pfaller MA, Boyken L, Холлис RJ, мессир SA, Tendolkar S, Diekema DJ (2005). «Активность анидулафунгина in vitro в отношении более чем 2500 клинических изолятов Candida spp., Включая 315 изолятов, устойчивых к флуконазолу» . J Clin Microbiol . 43 (11): 5425–7. DOI : 10.1128 / JCM.43.11.5425-5427.2005 . PMC 1287823 . PMID 16272464 .
- ^ Pfaller М.А., Diekema DJ, Boyken L, мессир SA, Tendolkar S, Холлис RJ, Goldstein BP (2005). «Эффективность анидулафунгина в искоренении видов Candida при инвазивном кандидозе» . Противомикробные агенты Chemother . 49 (11): 4795–7. DOI : 10,1128 / AAC.49.11.4795-4797.2005 . PMC 1280139 . PMID 16251335 .
- ^ Грау, Сантьяго; Азанза, Хосе Рамон; Руис, Изабель; Вальехо, Карлос; Менса, Хосеп; Мартенс, Йохан; Heinz, Werner J .; Барруэта, Джон Андони; Пераль, Кармен (01.01.2017). «Анализ экономической эффективности комбинированной противогрибковой терапии вориконазолом и анидулафунгином по сравнению с монотерапией вориконазолом для первичного лечения инвазивного аспергиллеза в Испании» . Клинико-экономика и исследования результатов . 9 : 39–47. DOI : 10,2147 / CEOR.S122177 . PMC 5221484 . PMID 28115858 .
- ^ Зида, А .; Bamba, S .; Yacouba, A .; Уэдраого-Траоре, Р .; Гигемде, RT (01.03.2017). «Натуральные продукты Anti-Candida albicans, источники новых противогрибковых препаратов: обзор». Journal de Mycologie Médicale . 27 (1): 1–19. DOI : 10.1016 / j.mycmed.2016.10.002 . ISSN 1773-0449 . PMID 27842800 .
- ^ "Eraxis в RxList" . 2009-06-24 . Проверено 1 августа 2009 .
- ^ Trissel LA и Ogundele AB, "Совместимость анидулафунгин с другими лекарственными средствами При имитации управления Y-сайта," Am J Health-Sys Pharm, 2005, 62: 834-7.
- ^ Васкес Дж. А., «Анидулафунгин: новый эхинокандин с новым профилем», Clin Ther, 2005, 27 (6): 657-73.
- ^ Walsh TJ, Anaissie EJ, Деннинг DW,др, "Лечение аспергиллеза: Руководствоклинической практике инфекционных заболеваний общества Америки". Clin Infect Dis 2008, 46 (3): 327-60
- ^ а б Деннинг DW (1997). «Эхинокандины и пневмокандины - новый класс противогрибковых средств с новым механизмом действия» . J Antimicrob Chemother . 40 (5): 611–614. DOI : 10,1093 / JAC / dkf045 . PMID 9421307 .
- ^ Лэй Шао; Цзянь Ли; Айзюань Лю; Цин Чанг; Хуэйминь Линь; Дайцзе Чен (2013). «Эффективная биоконверсия эхинокандина B в его ядро путем сверхэкспрессии генов деацилазы в различных штаммах-хозяевах» . Прикладная и экологическая микробиология . 79 (4): 1126–1133. DOI : 10,1128 / AEM.02792-12 . PMC 3568618 . PMID 23220968 .
- ^ "Anidulafungin EMA Europa" (PDF) .
- ^ PRNewswire. Vicuron Pharmaceuticals подает новую заявку на лекарственное средство (NDA) для анидулафунгина для лечения инвазивного кандидоза / кандидемии. Архивировано 16 мая 2012 г. на Wayback Machine 18.08.2005.
- ^ PRNewswire. Акционеры Vicuron Pharmaceuticals одобряют слияние с Pfizer Архивировано 16 мая 2012 г., на Wayback Machine 15.08.2005
- ^ «FDA одобряет новое лечение грибковых инфекций» . Выпуск новостей FDA . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов . 21 февраля 2006 г. Архивировано 10 июля 2009 года . Проверено 1 августа 2009 .