| Антиандрогены | |
|---|---|
| Класс препарата | |
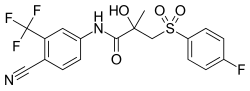 Бикалутамид , нестероидный антиандроген и наиболее широко используемый антагонист рецепторов андрогенов при лечении рака простаты . | |
| Идентификаторы класса | |
| Синонимы | Антагонисты андрогенов; Блокаторы андрогенов; Блокаторы тестостерона |
| Использовать | • Мужчины и мальчики: рак простаты ; Доброкачественная гиперплазия простаты ; Выпадение волос на коже головы ; Парафилии ; Гиперсексуальность ; Сексуальные преступники ; Преждевременное половое созревание ; Приапизм • Женщины и девушки: угри ; Себорея ; Гнойный гидраденит ; Гирсутизм ; Выпадение волос на коже головы ; Гиперандрогенизм ; Трансгендерная гормональная терапия |
| Код УВД | L02BB |
| Биологическая мишень | Рецептор андрогенов ; Рецептор прогестерона ; Рецептор эстрогена ; Рецептор GnRH ; 5α-редуктаза ; CYP17A1 (17α-гидроксилаза / |
| Химический класс | Стероидный ; Нестероидный ; Пептид |
| внешняя ссылка | |
| MeSH | D000726 |
| В Викиданных | |
Антиандрогены , также известные как антагонисты андрогенов или блокаторы тестостерона , представляют собой класс препаратов, которые не позволяют андрогенам, таким как тестостерон и дигидротестостерон (ДГТ), опосредовать их биологические эффекты в организме. Они действуют путем блокирования на андрогенного рецептора (AR) и / или ингибирования или подавления андрогенов производства . [1] [2] Их можно рассматривать как функциональные противоположности агонистов AR , например андрогенов и анаболических стероидов.(AAS), такие как тестостерон, DHT и нандролон, и селективные модуляторы рецепторов андрогенов (SARM), такие как энобосарм . Антиандрогены - это один из трех типов антагонистов половых гормонов , остальные - антиэстрогены и антипрогестагены . [3]
Антиандрогены используются для лечения ряда андроген-зависимых состояний . [4] У мужчин антиандрогены используются при лечении рака простаты , увеличения простаты , выпадения волос на коже головы , чрезмерно высокого полового влечения , необычных и проблематичных сексуальных побуждений и раннего полового созревания . [4] [5] У женщин антиандрогены используются для лечения акне , себореи , чрезмерного роста волос, выпадения волос на коже головы и высокого уровня андрогенов , например, при синдроме поликистозных яичников (СПКЯ).[4] Антиандрогены также используются в качестве компонента феминизирующей гормональной терапии для трансгендерных женщин и как блокаторы полового созревания у трансгендерных девушек . [4]
Побочные эффекты антиандрогенов зависят от типа антиандрогена и конкретного рассматриваемого антиандрогена. В любом случае, общие побочные эффекты антиандрогенов у мужчин включают болезненность груди , увеличение груди , феминизации , приливы , сексуальная дисфункция , бесплодие и остеопороз . У женщин антиандрогены переносятся намного лучше , а антиандрогены, которые действуют только путем прямого блокирования андрогенов, связаны с минимальными побочными эффектами. Однако, поскольку эстрогены производятся из андрогенов в организме, антиандрогены, подавляющие выработку андрогенов, могут вызыватьнизкий уровень эстрогена и связанные с ним симптомы, такие как приливы, нарушения менструального цикла и остеопороз у женщин в пременопаузе .
Есть несколько основных типов антиандрогенов. [6] К ним относятся антагонисты AR , ингибиторы синтеза андрогенов и антигонадотропины . [6] Антагонисты AR работают, напрямую блокируя эффекты андрогенов, в то время как ингибиторы синтеза андрогенов и антигонадотропины действуют, снижая уровни андрогенов. [6] Антагонисты AR можно далее разделить на стероидные антиандрогены и нестероидные антиандрогены ; ингибиторы синтеза андрогена могут быть дополнительно разделены на основном ингибиторы CYP17A1 и ингибиторы 5α-редуктазы ; и антигонадотропины можно разделить намодуляторы гонадотропин-рилизинг-гормона ( модуляторы гонадолиберина), прогестагены и эстрогены . [6] [7] [8]
Медицинское использование [ править ]
Антиандрогены используются при лечении ряда андроген-зависимых состояний как у мужчин, так и у женщин. [4] [9] Они используются для лечения мужчин с раком простаты , доброкачественной гиперплазией предстательной железы , типичным облысением , гиперсексуальностью , парафилиями и приапизмом , а также мальчиков с преждевременным половым созреванием . [9] [10] [11] У женщин и девочек антиандрогены используются для лечения акне , себореи , гнойного гидраденита , гирсутизма игиперандрогения . [9] [12] [13] Антиандрогены также используются у трансгендерных женщин в качестве компонента феминизирующей гормональной терапии и в качестве блокаторов полового созревания у трансгендерных девушек . [14] [15]
Мужчины и мальчики [ править ]
Рак простаты [ править ]
Андрогены, такие как тестостерон и особенно ДГТ, играют важную роль в развитии и прогрессировании рака простаты. [16] Они действуют как факторы роста в предстательной железе , стимулируя деление клеток и рост тканей . [16] В соответствии с этим терапевтические методы, которые снижают передачу сигналов андрогенов в предстательной железе, в совокупности именуемые терапией депривации андрогенов , способны значительно замедлить течение рака простаты и продлить жизнь у мужчин с этим заболеванием. [16]Хотя антиандрогены эффективны в замедлении прогрессирования рака простаты, обычно они не излечивают, и со временем болезнь адаптируется, и терапия андрогенной депривации в конечном итоге становится неэффективной. [17] Когда это происходит, можно рассмотреть другие подходы к лечению, такие как химиотерапия . [17]
Наиболее распространенными методами андрогенной депривации, применяемыми в настоящее время для лечения рака простаты, являются кастрация (с модулятором гонадолиберин или орхиэктомия ), прием нестероидных антиандрогенов и ингибитор синтеза андрогенов абиратерона ацетат . [16] Кастрацию можно использовать отдельно или в сочетании с одним из двух других методов лечения. [16] [18] Когда кастрация сочетается с нестероидными антиандрогенами, такими как бикалутамид , эта стратегия называется комбинированной андрогенной блокадой (также известной как полная или максимальная андрогенная блокада). [16] [19] Энзалутамид , апалутамид, и ацетат абиратерона специально одобрены для использования в сочетании с кастрацией для лечения устойчивого к кастрации рака простаты. [16] [20] Монотерапия нестероидным антиандрогеном бикалутамидом также используется при лечении рака простаты в качестве альтернативы кастрации с сопоставимой эффективностью, но с другим и потенциально благоприятным профилем побочных эффектов. [16] [21] [22]
Высокие дозы эстрогена были первым функциональным антиандрогеном, использованным для лечения рака простаты. Он широко использовался, но в основном от него отказались по этому показанию в пользу более новых агентов с улучшенными профилями безопасности и меньшим количеством феминизирующих побочных эффектов. [23] Ципротерона ацетат был разработан впоследствии на основе высоких доз эстрогена и является единственным стероидным антиандрогеном, который широко использовался при лечении рака простаты [24], но в значительной степени он был заменен нестероидными антиандрогенами, которые являются более новыми и более эффективными. эффективность, переносимость и безопасность. [25] [26] Бикалутамид, а также энзалутамид, в значительной степени заменили более ранние нестероидные антиандрогены флутамид инилутамид , которые сейчас мало используются. [19] [27] [28] [29] [30] Ранние ингибиторы синтеза андрогенов, аминоглутетимид и кетоконазол , только ограниченно использовались при лечении рака простаты из-за опасений токсичности и были заменены ацетатом абиратерона. [31]
Помимо активного лечения рака простаты, антиандрогены эффективны в качестве профилактики (превентивных средств), снижая риск развития рака простаты. [32] Антиандрогены для этой цели оценивались лишь ограниченно, но ингибиторы 5α-редуктазы финастерид и дутастерид и стероидный антагонист AR спиронолактон были связаны со значительным снижением риска рака простаты. [32] [33] Кроме того, следует отметить, что рак простаты крайне редко встречается у трансгендерных женщин, которые длительное время получали феминизирующую гормональную терапию. [34] [35] [36]
Увеличенная простата [ править ]
Ингибиторы 5α-редуктазы финастерид и дутастерид используются для лечения доброкачественной гиперплазии предстательной железы, состояния, при котором простата увеличивается в размерах, что приводит к непроходимости мочеиспускания и дискомфорту. [37] Они эффективны, потому что андрогены действуют как факторы роста в предстательной железе. [37] Антиандрогены хлормадинона ацетат и оксендолон, а также функциональные антиандрогены аллилестренол и гестонорон капроат также одобрены в некоторых странах для лечения доброкачественной гиперплазии простаты. [38] [39]
Выпадение волос на голове [ править ]
Ингибиторы 5α-редуктазы, такие как финастерид, дутастерид и альфатрадиол, а также местный нестероидный антагонист AR топилутамид (флуридил) одобрены для лечения типичного облысения, также известного как выпадение волос на коже головы или облысение. [40] Это состояние обычно вызывается андрогенами, поэтому антиандрогены могут замедлить или остановить его прогрессирование. [41] Системные антиандрогены, помимо ингибиторов 5α-редуктазы, обычно не используются для лечения выпадения волос на коже головы у мужчин из-за таких рисков, как феминизация (например, гинекомастия) и сексуальная дисфункция. [42] [43] [44] [45] [46] [47] [48]Однако они были оценены и признаны эффективными при этом показании. [42] [43] [49]
Акне [ править ]
Антиандрогены обычно не используются для лечения угрей у мужчин из-за высокого риска феминизации (например, гинекомастии) и сексуальной дисфункции. [50] [51] Тем не менее, они были изучены для лечения акне у мужчин и оказались эффективными. [52] [44] [45] [53] Класкотерон , антиандроген для местного применения, эффективен при угревой сыпи у мужчин и может быть одобрен для этого показания в будущем. [54] [55]
Сексуальные отклонения [ править ]
Андрогены увеличение полового влечения , [56] и по этой причине антиандрогены способны снижать половое влечение у мужчин. [57] [58] Соответственно, антиандрогены используются при лечении состояний сексуальных отклонений, таких как гиперсексуальность (чрезмерно высокое половое влечение) и парафилии (атипичные, а иногда и неприемлемые для общества сексуальные интересы), такие как педофилия (сексуальное влечение к детям). [57] [58] Они использовались для снижения полового влечения у сексуальных преступников, чтобы снизить вероятность рецидива (повторных преступлений). [59]Антиандрогены , используемые для этих показаний включают ципротерона ацетат , медроксипрогестерона ацетат и GnRH модуляторов. [60] [61]
Раннее половое созревание [ править ]
Антиандрогены используются для лечения преждевременного полового созревания у мальчиков. [62] [63] [64] [65] Они работают, противодействуя воздействию андрогенов и задерживая развитие вторичных половых признаков и начало изменений полового влечения и функций до более подходящего возраста. [62] [63] Антиандрогены , которые были использованы для этой цели , включают ципротерона ацетат , медроксипрогестерона ацетат , GnRH модуляторов, спиронолактон , бикалутамид и кетоконазол . [62] [65] [66][67] [68] [69] Спиронолактон и бикалутамид требуют комбинации с ингибитором ароматазы, чтобы предотвратить эффекты эстрогенов , которымне противодействуют , в то время как другие можно использовать отдельно. [62] [68] [69]
Длительная эрекция [ править ]
Антиандрогены эффективны при лечении рецидивирующего приапизма (потенциально болезненная эрекция полового члена, длящаяся более четырех часов). [70] [71] [72] [73] [74]
Женщины и девушки [ править ]
Состояние кожи и волос [ править ]
Антиандрогены используются для лечения андроген-зависимых состояний кожи и волос, включая угри, себорею, гнойный гидраденит, гирсутизм и типичное выпадение волос у женщин. [12] Все эти состояния зависят от андрогенов, и по этой причине антиандрогены эффективны при их лечении. [12] Наиболее часто используемыми антиандрогенами по этим показаниям являются ципротерона ацетат и спиронолактон . [75] Флутамид также широко изучался для таких целей, но потерял популярность из-за его связи с гепатотоксичностью . [76] Бикалутамид, который имеет относительно минимальный риск гепатотоксичности, был оценен для лечения гирсутизма и признан эффективным, как флутамид, и может использоваться вместо него. [77] [78] Помимо антагонистов AR, пероральные контрацептивы, содержащие этинилэстрадиол , эффективны при лечении этих состояний, и их можно комбинировать с антагонистами AR. [79] [80]
Высокий уровень андрогенов [ править ]
Гиперандрогения - это состояние у женщин, при котором уровни андрогенов чрезмерно и аномально высоки. [13] Это обычно наблюдается у женщин с СПКЯ, а также у женщин с интерсексуальными состояниями, такими как врожденная гиперплазия надпочечников . [13] Гиперандрогения связан с вирилизации - то есть, развитие мужских вторичных половых признаков , как рост мужскому типу лица и тела волос (или гирсутизм), голос углубления , увеличение мышечной массы и силы , и уширение плечи , среди других . [13]Андроген-зависимые состояния кожи и волос, такие как прыщи и облысение, также могут возникать при гиперандрогении и часто наблюдаются нарушения менструального цикла , такие как аменорея . [13] Хотя антиандрогены не лечат основную причину гиперандрогении (например, СПКЯ), они способны предотвратить и обратить вспять его проявления и эффекты. [13] Как и в случае андрогензависимых состояний кожи и волос, наиболее часто используемыми антиандрогенами при лечении гиперандрогении у женщин являются ципротерона ацетат и спиронолактон. [13] В качестве альтернативы можно использовать другие антиандрогены, такие как бикалутамид. [13]
Трансгендерная гормональная терапия [ править ]
Антиандрогены используются для предотвращения или обратного маскулинизация и способствовать феминизации в транссексуалов женщин , которые проходят гормональную терапию , и которые не подверглись операции по смене пола или орхэктомию . [14] Помимо эстрогенов, основными антиандрогенами, которые использовались для этой цели, являются ацетат ципротерона, спиронолактон и модуляторы гонадолиберина. [14] При этом показании также используются нестероидные антиандрогены, такие как бикалутамид. [81] [14] Помимо использования у трансгендерных женщин, антиандрогены, в основном модуляторы гонадолиберина, используются в качестве блокаторов полового созревания для предотвращенияполового созревания у трансгендерных девочек до тех пор, пока они не станут старше и не будут готовы начать гормональную терапию. [15]
Доступные формы [ править ]
Существует несколько различных типов антиандрогенов, в том числе следующие: [6]
- Антагонисты рецепторов андрогенов: препараты, которые напрямую связываются и блокируют АР. [82] [83] Эти препараты включают стероидные антиандрогены ципротерона ацетат , мегестрол ацетат , хлормадинона ацетат , спиронолактон , oxendolone , и осатерона ацетат (ветеринарный) и нестероидные антиандрогены , флутамид , бикалутамид , нилутамид , topilutamide , enzalutamide , и apalutamide . [82] [83] [7] [8]Помимо ципротерона ацетата и хлормадинона ацетата, некоторые другие прогестины, используемые в пероральных контрацептивах и / или в менопаузальной ЗГТ, включая диеногест , дроспиренон , медрогестон , номегестрола ацетат , промегестон и тримегестон, также обладают различной степенью антагонистической активности AR. [84] [85] [86]
- Ингибиторы синтеза андрогенов: препараты, которые напрямую подавляют ферментативный биосинтез андрогенов, таких как тестостерон и / или ДГТ. [87] [31] Примеры включают CYP17A1 ингибиторы Кетоконазол , ацетат абиратерона и seviteronel , [87] CYP11A1 (P450scc) ингибитор аминоглютетимид , [87] и 5 - альфа-редуктазы ингибиторы финастерид , дутастерид , эпристерид , alfatradiol и пальметто экстракт (Сереноа ползучая ). [88] Также известно, что ряд других антиандрогенов, включая ципротерона ацетат, спиронолактон, медрогестон, флутамид, нилутамид и бифлуранол , слабо подавляют синтез андрогенов.
- Antigonadotropins: Препараты , которые подавляют гонадотропин-рилизинг-гормон (ГнРГ) -индуцированное высвобождение гонадотропинов и последующей активации гонад производства андрогена. [2] [89] Примеры включают GnRH модуляторы , такие как лейпрорелин (а ГнРГ агонист ) и цетрореликс (а антагонист ГнРГа ), [90] прогестагены как аллилэстренол , хлормадинон ацетат, ацетат ципротерон, gestonorone капроит , гидроксипрогестерон капроит , медроксипрогестерон ацетат, мегестрола ацетат, осатерона ацетат (ветеринарный) и оксендолон, [91] [92] и эстрогены, такие как эстрадиол , сложные эфиры эстрадиола , этинилэстрадиол , конъюгированные эстрогены и диэтилстильбэстрол . [2] [91]
- Разное: препараты, которые препятствуют действию андрогенов другими способами, кроме указанных выше. Примеры включают эстрогены, особенно полости рта и синтетические (например, этинилэстрадиол , диэтилстилбестрол ), которые стимулируют гормон-связывающий глобулин секс (SHBG) производство в печени и тем самым уменьшить свободный и , следовательно , биологически активные уровни тестостерона и дигидротестостерона; антикортикотропины, такие как глюкокортикоиды , которые подавляют продукцию андрогенов надпочечников, индуцированную адренокортикотропным гормоном (АКТГ) ; и иммуногеныи вакцины против андростендиона, такие как овандротон-альбумин и андростендион-альбумин , которые снижают уровни андрогенов за счет образования антител против андрогенов и предшественников андрогенов андростендиона (используются только в ветеринарии ).
Некоторые антиандрогены сочетают в себе несколько вышеперечисленных механизмов. [6] [93] Примером является стероидный антиандроген ципротерона ацетат, который является мощным антагонистом AR, мощным прогестогеном и, следовательно, антигонадотропином, слабым глюкокортикоидом и, следовательно, антикортикотропином, а также слабым ингибитором синтеза андрогенов. [6] [93] [94] [95]
Побочные эффекты [ править ]
Побочные эффекты антиандрогенов варьируются в зависимости от типа антиандрогена, а именно от того, является ли он селективным антагонистом AR или понижает уровень андрогенов, а также от наличия нецелевой активности в рассматриваемом антиандрогене. [21] [96] Например, в то время как антигонадотропные антиандрогены, такие как модуляторы гонадолиберин и ципротерона ацетат, связаны с выраженной сексуальной дисфункцией и остеопорозом у мужчин, селективные антагонисты AR, такие как бикалутамид, не связаны с остеопорозом и связаны лишь с минимальной сексуальной дисфункцией. [21] [97] [98]Считается, что эти различия связаны с тем фактом, что антигонадотропины подавляют уровни андрогенов и за счет увеличения уровней биоактивных метаболитов андрогенов, таких как эстрогены и нейростероиды, тогда как селективные антагонисты AR аналогичным образом нейтрализуют эффекты андрогенов, но оставляют уровни андрогенов и, следовательно, их метаболитов нетронутыми (и фактически может даже увеличить их в результате их прогонадотропных эффектов). [21] В качестве другого примера, стероидные антиандрогены ципротерона ацетат и спиронолактон обладают нецелевым действием, включая прогестагенные , антиминералокортикоидные и / или глюкокортикоидные.активности в дополнение к их антиандрогенной активности, и эти нецелевые активности могут привести к дополнительным побочным эффектам. [96]
У мужчин основными побочными эффектами антиандрогенов являются демаскулинизация и феминизация . [99] Эти побочные эффекты включают боль / болезненность груди и гинекомастию ( развитие / увеличение груди ), снижение роста / плотности волос на теле , уменьшение мышечной массы и силы , женские изменения в массе и распределении жира , а также уменьшение длины полового члена и размера яичек . [99]Было обнаружено, что частота гинекомастии у мужчин при монотерапии селективными антагонистами AR составляет от 30 до 85%. [100] Кроме того, антиандрогены могут вызывать бесплодие , остеопороз , приливы , сексуальную дисфункцию (включая потерю либидо и эректильную дисфункцию ), депрессию , усталость , анемию и уменьшение объема семенной жидкости / эякулята у мужчин. [ неудачная проверка ] [99] И наоборот, побочные эффекты селективных антагонистов AR у женщин минимальны. [78] [101]Однако антигонадотропные антиандрогены, такие как ацетат ципротерона, могут вызывать гипоэстрогенизм , аменорею и остеопороз у женщин в пременопаузе, а также другие побочные эффекты. [79] [102] [103]
Некоторые антиандрогены связаны с гепатотоксичностью . [104] К ним относятся, в различной степени, ципротерона ацетат, флутамид, нилутамид, бикалутамид, аминоглутетимид и кетоконазол. [104] Напротив, спиронолактон, энзалутамид [105] и другие антиандрогены не связаны со значительными показателями гепатотоксичности. Однако, хотя спиронолактон не представляет риска гепатотоксичности, у него есть риск гиперкалиемии, а у энзалутамида - риск судорог .
У женщин , которые беременны , антиандрогены могут мешать андроген-опосредованных половой дифференцировки из гениталий и мозга мужских плодов . [106] Это проявляется в первую очередь как неоднозначные гениталии - то есть недовирилизованные или феминизированные гениталии, которые анатомически представляют собой нечто среднее между пенисом и влагалищем - а теоретически также как женственность . [106] [107] Таким образом, антиандрогены являются тератогенами , и беременным женщинам не следует лечить антиандрогенами. [80]Более того, женщинам, которые могут или могут забеременеть, настоятельно рекомендуется принимать антиандрогены только в сочетании с надлежащей контрацепцией . [80]
Передозировка [ править ]
Антиандрогены относительно безопасны при острой передозировке . [ необходима цитата ]
Взаимодействия [ править ]
Ингибиторы и индукторы из цитохрома Р450 ферментов могут взаимодействовать с различными антиандрогенами. [ необходима цитата ]
Механизм действия [ править ]
Антагонисты рецепторов андрогенов [ править ]
| Сложный | РБА [b] |
|---|---|
| Метриболон | 100 |
| Дигидротестостерон | 85 |
| Ципротерона ацетат | 7,8 |
| Бикалутамид | 1.4 |
| Нилутамид | 0,9 |
| Гидроксифлутамид | 0,57 |
| Флутамид | <0,0057 |
Примечания:
| |
| Антиандрогены | Относительная сила |
|---|---|
| Бикалутамид | 4.3 |
| Гидроксифлутамид | 3.5 |
| Флутамид | 3.3 |
| Ципротерона ацетат | 1.0 |
| Занотерон | 0,4 |
| Описание: Относительные потенции перорально антиандрогенов в антагонистического от 0,8 до 1,0 мг / кг подкожно тестостерон пропионат индуцированного вентральной простата увеличение веса в кастрируют незрелые самец крыс. Источники: см. Шаблон. | |
Антагонисты AR действуют путем прямого связывания и конкурентного вытеснения андрогенов, таких как тестостерон и DHT, из AR, тем самым предотвращая их активацию рецептора и опосредуя их биологические эффекты. [82] [83] Антагонисты AR делятся на два типа в зависимости от химической структуры : стероидные и нестероидные. [7] [8] [82] [83] [90] Антагонисты стероидных AR структурно родственны стероидным гормонам, таким как тестостерон и прогестерон , тогда как нестероидные антагонисты AR не являются стероидами и отличаются по своей структуре. Антагонисты стероидных AR, как правило, оказывают нецелевое гормональное действие.из-за их структурного сходства с другими стероидными гормонами. [90] Напротив, нестероидные антагонисты AR являются селективными в отношении AR и не обладают гормональной активностью, не являющейся мишенью. [90] По этой причине их иногда называют «чистыми» антиандрогенами. [90]
Хотя они описаны как антиандрогены и действительно проявляют только такие эффекты в целом, большинство или все стероидные антагонисты AR на самом деле не являются молчащими антагонистами AR, а скорее являются слабыми частичными агонистами и способны активировать рецептор в отсутствие более сильных агонистов AR, таких как тестостерон и ДГТ. [82] [31] [109] [110] Это может иметь клиническое значение в конкретном контексте лечения рака простаты. [82] [109] Например, стероидные антагонисты AR способны увеличивать вес простаты и ускорять рост клеток рака простаты в отсутствие более сильных агонистов AR, [82] [109]в отчетах о случаях было обнаружено, что спиронолактон ускоряет прогрессирование рака простаты. [111] [112] Кроме того, в то время как ацетат ципротерона вызывает неоднозначные гениталии за счет феминизации у плодов мужского пола при введении беременным животным [113] , было обнаружено, что он вызывает маскулинизацию гениталий женских плодов беременных животных. [82] В отличие от стероидных антагонистов AR, нестероидные антагонисты AR являются молчащими антагонистами AR и не активируют рецептор. [114] [31] [115] [109]Возможно, поэтому они обладают большей эффективностью, чем стероидные антагонисты АР при лечении рака простаты, и является важной причиной того, почему они в значительной степени заменили их по этому показанию в медицине. [114] [31] [115] [109]
Нестероидные антиандрогены имеют относительно низкое сродство к AR по сравнению со стероидными лигандами AR. [31] [115] [116] Например, бикалутамид имеет около 2% сродства DHT к AR и около 20% сродства CPA к AR. [116] Несмотря на их низкое сродство к AR, отсутствие слабой частичной агонистической активности NSAA, по-видимому, улучшает их эффективность по сравнению со стероидными антиандрогенами. [116] [117] Например, хотя флутамид имеет примерно в 10 раз меньшее сродство к AR, чем CPA, он показывает равную или немного большую эффективность с CPA в качестве антиандрогена в биоанализах . [116] [117]Кроме того, циркулирующие терапевтические концентрации нестероидных антиандрогенов очень высоки, в тысячи раз выше, чем у тестостерона и DHT, и это позволяет им эффективно конкурировать и блокировать передачу сигналов AR. [118]
Антагонисты AR могут не связываться или блокировать мембранные рецепторы андрогенов (mAR), которые отличаются от классических ядерных AR. [119] [120] [121] Однако, похоже, что mAR не участвуют в маскулинизации . Об этом свидетельствует совершенно женский фенотип женщин с синдромом полной нечувствительности к андрогенам . [122] [123] Эти женщины имеют кариотип 46, XY (т.е. генетически «мужские») и высокий уровень андрогенов, но обладают дефектным AR и по этой причине никогда не маскулинизируются. [122] [123]Их описывают как очень женственных, как физически, так и умственно и поведенчески. [124] [125] [126]
Антагонисты N-концевого домена [ править ]
Антагонисты AR N-концевого домена представляют собой новый тип антагонистов AR, которые, в отличие от всех продаваемых в настоящее время антагонистов AR, связываются с N-концевым доменом (NTD) AR, а не с лиганд-связывающим доменом (LBD). [127] В то время как обычные антагонисты AR связываются с LBD AR и конкурентно вытесняют андрогены, тем самым не позволяя им активировать рецептор, антагонисты AR NTD ковалентно связываются с NTD AR и предотвращают межбелковые взаимодействия после активации, которая требуется. для транскрипционной активности . [127] Как таковые, они неконкурентоспособны.и необратимые антагонисты АР. [128] Примеры антагонистов AR NTD включают диглицидиловый эфир бисфенола А (BADGE) и его производные EPI-001 , раланитен (EPI-002) и раланитен ацетат (EPI-506). [127] [129] AR NTD-антагонисты исследуются на предмет потенциального лечения рака простаты, и считается, что они могут иметь большую эффективность в качестве антиандрогенов по сравнению с обычными антагонистами AR. [127] В соответствии с этим представлением, антагонисты AR NTD активны против вариантов сплайсинга.AR, которыми не являются обычные антагонисты AR, и антагонисты AR NTD невосприимчивы к мутациям увеличения функции в AR LBD, которые превращают антагонисты AR в агонисты AR и обычно возникают при раке простаты. [127]
Разрушители рецепторов андрогенов [ править ]
Селективные деструкторы рецепторов андрогенов (SARD) - еще один новый тип антиандрогенов, который был недавно разработан. [130] Они работают путем усиления деградации АРА, и аналогичны селективные деструкторы рецептора эстрогена (SERDs) , как фулвестрант (препарат используется для лечения рецептора эстрогена-положительного рака молочной железы ). [130] Считается, что, подобно антагонистам AR NTD, SARD могут иметь большую эффективность, чем обычные антагонисты AR, и по этой причине они исследуются для лечения рака простаты. [131] Примером SARD является диметилкуркумин.(ASC-J9), который находится в стадии разработки в качестве местного лекарства для потенциального лечения акне. [132] SARD, такие как диметилкуркумин, отличаются от обычных антагонистов AR и антагонистов NTD тем, что они не обязательно могут напрямую связываться с AR. [131]
Ингибиторы синтеза андрогенов [ править ]
Ингибиторы синтеза андрогенов - это ингибиторы ферментов, которые предотвращают биосинтез андрогенов. [31] Этот процесс происходит в основном в половых железах и надпочечниках , но также происходит и в других тканях, таких как предстательная железа , кожа и волосяные фолликулы . Эти препараты включают аминоглютетимид, кетоконазол [133] и ацетат абиратерона. [87] [31] [134] Аминоглутетимид ингибирует фермент расщепления боковой цепи холестерина, также известный как P450scc или CYP11A1, который отвечает за превращение холестерина в прегненолон.и, как следствие, производство всех стероидных гормонов, включая андрогены. [87] Кетоконазол и абиратерона ацетат являются ингибиторами фермента CYP17A1, также известного как 17α-гидроксилаза / 17,20-лиаза, который отвечает за превращение прегнановых стероидов в андрогены, а также за превращение минералокортикоидов в глюкокортикоиды. [87] [31] Поскольку все эти препараты предотвращают образование глюкокортикоидов в дополнение к андрогенам, их необходимо сочетать с глюкокортикоидами, такими как преднизон, чтобы избежать надпочечниковой недостаточности . [134] В настоящее время разрабатывается новый препарат для лечения рака простаты - севитеронел., является селективным в отношении ингибирования 17,20-лиазной функциональности CYP17A1, и по этой причине, в отличие от более ранних препаратов, не требует сопутствующего лечения глюкокортикоидами. [135]
Ингибиторы 5α-редуктазы [ править ]
Ингибиторы 5α-редуктазы, такие как финастерид и дутастерид, являются ингибиторами 5α-редуктазы , фермента, который отвечает за образование DHT из тестостерона. [136] ДГТ в 2,5–10 раз более эффективен, чем тестостерон в качестве андрогена [137], и продуцируется ткане-селективным образом на основе экспрессии 5α-редуктазы. [138] Ткани, в которых ДГТ образуется с высокой скоростью, включают предстательную железу , кожу и волосяные фолликулы . [41] [138] Соответственно, DHT участвует в патофизиологиидоброкачественной гиперплазии предстательной железы, облысения и гирсутизма, а ингибиторы 5α-редуктазы используются для лечения этих состояний. [41] [138] [139]
Антигонадотропины [ править ]
Antigonadotropins препараты , которые подавляют ГнРГ-опосредованную секрецию из гонадотропинов из гипофиза . [89] Гонадотропины включают лютеинизирующий гормон (ЛГ) и фолликулостимулирующий гормон (ФСГ) и представляют собой пептидные гормоны, которые сигнализируют гонадам о выработке половых гормонов . Подавляя секрецию гонадотропинов, антигонадотропины подавляют выработку половых гормонов гонад и за счет увеличения уровней циркулирующих андрогенов. [89] GnRH модуляторы , включая как агонисты ГнРГ и антагонисты GnRH, являются мощными антигонадотропинами, которые способны подавлять уровень андрогенов на 95% у мужчин. [142] Кроме того, эстрогены и прогестагены являются антигонадотропинами за счет проявления отрицательной обратной связи по оси гипоталамус-гипофиз-гонад (ось HPG). [2] [91] [143] Высокие дозы эстрогенов способны подавлять уровни андрогенов, чтобы кастрировать уровни у мужчин аналогично модуляторам ГнРГ, [144] в то время как высокие дозы прогестагенов способны подавлять уровни андрогенов примерно на 70-80 % у мужчин. [145] [146]
Примеры агонистов GnRH включают лейпрорелин (лейпролид) и гозерелин , а примером антагониста GnRH является цетрореликс . [90] Эстрогены , которые являются или которые были использованы в качестве antigonadotropins включают эстрадиол, эстрадиола сложные эфиры , такие как эстрадиол валерат , эстрадиол undecylate и polyestradiol фосфат , конъюгированные эстрогены, этинилэстрадиол, диэтилстильбестрол (больше не широко не используется) и bifluranol . [147] [148] Прогестагены, которые используются в качестве антигонадотропинов, включают ацетат хлормадинона, ацетат ципротерона, гестоноронкапроат,[149] гидроксипрогестерона капроат , медроксипрогестерона ацетат, мегестрола ацетат и оксендолон. [2] [150] [151]
Разное [ править ]
Модуляторы SHBG [ править ]
В дополнение к их антигонадотропным эффектам, эстрогены также являются функциональными антиандрогенами за счет снижения свободных концентраций андрогенов за счет увеличения выработки печенью глобулина, связывающего половые гормоны (SHBG), и за счет увеличения уровней циркулирующего SHBG. [152] [153] [154] Было обнаружено, что комбинированные пероральные контрацептивы, содержащие этинилэстрадиол, повышают уровень циркулирующего ГСПГ в 2–4 раза у женщин и снижают концентрацию свободного тестостерона на 40–80%. [153] Однако было обнаружено , что комбинированные пероральные контрацептивы, содержащие особенно андрогенный прогестин левоноргестрел , повышают уровень SHBG только на 50–100%, [153]что, вероятно, связано с тем, что активация AR в печени имеет противоположный эффект эстрогена и подавляет выработку SHBG. [155] Левоноргестрел и некоторые другие прогестины 19-нортестостерона, используемые в комбинированных пероральных контрацептивах, таких как норэтистерон, также напрямую связываются и вытесняют андрогены из SHBG, что может дополнительно противодействовать функциональным антиандрогенным эффектам этинилэстрадиола. [155] [156]У мужчин исследование показало, что лечение относительно низкой дозировкой этинилэстрадиола 20 мкг / день в течение 5 недель увеличивало уровни циркулирующего SHBG на 150% и, из-за сопутствующего снижения уровней свободного тестостерона, увеличивало общие уровни циркулирующего тестостерона на 50% ( за счет уменьшения отрицательной обратной связи андрогенов по оси HPG). [152]
Антикортикотропины [ править ]
Антикортикотропины, такие как глюкокортикоиды и минералокортикоиды, работают, оказывая отрицательную обратную связь по оси гипоталамус-гипофиз-надпочечники ( ось HPA), тем самым подавляя секрецию кортикотропин-рилизинг-гормона (CRH) и, следовательно, адренокортикотропного гормона (ACTH; соответственно, подавляя выработку кортикотропина). из андрогенных прогормонов как дегидроэпиандростерон (ДГЭА), дегидроэпиандростерон сульфат (ДГЭА-с), и андростендионом в надпочечниках . [157] [158]Они редко используются в клинической практике в качестве функциональных антиандрогенов, но используются как таковые в случае врожденной гиперплазии надпочечников у девочек и женщин, при которых наблюдается чрезмерное производство и уровни андрогенов надпочечников из-за дефицита глюкокортикоидов и, следовательно, повышенной активности оси HPA. [157] [158]
Иммуногены и вакцины [ править ]
Овандротон-альбумин (Фекундин, Овастим) и Андровакс (андростендион-альбумин) - это иммуногены и вакцины против андростендиона , которые используются в ветеринарии для повышения плодовитости (репродуктивной способности) овец (взрослых самок овец). [159] [160] Считается, что образование антител против андростендиона этими агентами снижает циркулирующие уровни андростендиона и его метаболитов (например, тестостерона и эстрогенов), что, в свою очередь, увеличивает активность оси HPG за счет уменьшения отрицательной обратной связи и увеличения скорость овуляции , в результате чего большеплодородие и плодовитость. [159] [160]
Сенсибилизаторы инсулина [ править ]
У женщин с инсулинорезистентностью , например, с синдромом поликистозных яичников , уровень андрогенов часто повышен. [161] Метформин , лекарство , повышающее чувствительность к инсулину , оказывает на таких женщин непрямое антиандрогенное действие, снижая уровень тестостерона на 50% в результате его положительного воздействия на чувствительность к инсулину. [161]
Химия [ править ]
Антиандрогены можно разделить на несколько различных типов в зависимости от химической структуры , включая стероидные антиандрогены , нестероидные антиандрогены и пептиды . Стероидные антиандрогены включают такие соединения, как ацетат ципротерона , спиронолактон , эстрадиол , ацетат абиратерона и финастерид ; нестероидные антиандрогены включают такие соединения, как бикалутамид , элаголикс , диэтилстильбестрол , аминоглутетимид и кетоконазол ; и пептиды включают аналоги GnRHкак лейпрорелин и цетрореликс .
История [ править ]
Антигонадотропины, такие как эстрогены и прогестагены, были впервые представлены в 1930-х годах. [162] Благоприятные эффекты лишения андрогенов с помощью хирургической кастрации или терапии высокими дозами эстрогенов на рак простаты были обнаружены в 1941 году. [31] : 56 [163] Антагонисты AR были впервые обнаружены в начале 1960-х годов. [94] Стероидный антиандроген ципротерона ацетат был открыт в 1961 году и представлен в 1973 году и часто описывается как первый антиандроген, поступивший на рынок. [164] [60] Однако спиронолактон был представлен в 1959 году, [165] [166]хотя его антиандрогенные эффекты не были обнаружены и не использовались до тех пор, пока не были использованы, и изначально были непреднамеренным действием препарата не по назначению. [167] Помимо спиронолактона, хлормадинона ацетат и мегестрола ацетат являются стероидными антиандрогенами, которые более слабые, чем ципротерона ацетат, но также были введены ранее, в 1960-х годах. [168] [169] [170] Другие ранние стероидные антиандрогены, которые были разработаны примерно в это время, но никогда не продавались, включают бенортерон (SKF-7690; 17α-метил- B- нортестостерон), BOMT (Ro 7-2340), ципротерон (SH -80881) и триметилтриенолон (R-2956). [171] [172]
О нестероидном антиандрогене флутамиде впервые было сообщено в 1967 году. [24] Он был представлен в 1983 году и стал первым нестероидным антиандрогеном, поступившим на рынок. [173] [174] Другой ранний нестероидный антиандроген, [175] DIMP (Ro 7-8117), который структурно родственен талидомиду [176] и является относительно слабым антиандрогеном, [177] [178] был впервые описан в 1973 г. никогда не продавался. [179] За флутамидом последовали нилутамид в 1989 г. и бикалутамид в 1995 г. [180] В дополнение к этим трем препаратам, которые считались нестероидными антиандрогенами первого поколения, нестероидные антиандрогены второго поколенияэнзалутамид и апалутамид были представлены в 2012 и 2018 годах соответственно. [181] [182] [183] Они отличаются от более ранних нестероидных антиандрогенов, а именно тем, что они намного более эффективны по сравнению с ними. [182]
Ингибиторы синтеза андрогенов аминоглутетимид и кетоконазол были впервые представлены на рынке в 1960 и 1977 годах, соответственно [184] [185], а новый препарат абиратерона ацетат был представлен в 2011 году. [186] Модуляторы гонадолиберина были впервые представлены в 1980-х годах. [187] Ингибиторы 5α-редуктазы финастерид и дутастерид были введены в продажу в 1992 и 2002 годах соответственно. [188] [189] Elagolix , первый поступающий на рынок орально активный модулятор ГнРГ, был представлен в 2018 году. [190]
Хронология [ править ]
Ниже приводится хронология событий в истории антиандрогенов: [191]
- 1941: Хаджинс и Ходжес показывают, что депривация андрогенов с помощью терапии высокими дозами эстрогенов или хирургической кастрации лечит рак простаты.
- 1957: Впервые синтезирован стероидный антиандрогенный спиронолактон [192]
- 1960: Спиронолактон впервые представлен для медицинского применения как антиминералокортикоид [192]
- 1961: Впервые синтезирован стероидный антиандроген ципротерона ацетат [193]
- 1962: Впервые сообщается, что спиронолактон вызывает гинекомастию у мужчин [192] [194]
- 1963: Обнаружена антиандрогенная активность ципротерона ацетата [48] [195].
- 1966: Бенортерон - первый известный антиандроген, который будет изучен клинически для лечения акне и гирсутизма у женщин [196] [197]
- 1967: Впервые сообщается, что известный антиандроген, бенортерон, вызывает гинекомастию у мужчин [196]
- 1967: Впервые синтезирован нестероидный антиандрогенный флутамид первого поколения.
- 1967: Ципротерона ацетат впервые был исследован клинически для лечения сексуальных отклонений у мужчин [198]
- 1969: Ципротерона ацетат был впервые изучен для лечения акне, гирсутизма, себореи и выпадения волос на коже головы у женщин [199]
- 1969: Обнаружена антиандрогенная активность спиронолактона [200]
- 1972: Впервые сообщается об антиандрогенной активности флутамида [201] [202]
- 1973: Ципротерона ацетат был впервые использован в медицине для лечения сексуальных отклонений [203]
- 1977: Впервые описан антиандроген нилутамид первого поколения [204]
- 1978: Спиронолактон впервые исследован для лечения гирсутизма у женщин [63] [205]
- 1979: Впервые изучена комбинированная андрогенная блокада [206] [207]
- 1980: Впервые проведена медицинская кастрация аналогом гонадолиберина [ необходима цитата ]
- 1982: Впервые описан антиандрогенный бикалутамид первого поколения [208]
- 1982: Разработана комбинированная андрогенная блокада при раке простаты.
- 1983: Флутамид впервые представлен в Чили для медицинского применения для лечения рака простаты [209] [210]
- 1987: во Франции впервые представлен нилутамид для медицинского применения для лечения рака простаты [180]
- 1989: обнаружено, что комбинированная андрогенная блокада с помощью флутамида и аналога ГнРГ превосходит один только аналог ГнРГ при раке простаты.
- 1989: Флутамид впервые представлен для медицинского применения в США для лечения рака простаты [211]
- 1989: Флутамид впервые был изучен для лечения гирсутизма у женщин [9]
- 1992: Впервые описан ингибитор синтеза андрогенов абиратерона ацетат [212]
- 1995: Бикалутамид впервые используется в медицине для лечения рака простаты [180]
- 1996: Нилутамид впервые представлен для медицинского применения в США для лечения рака простаты [213]
- 2006: Впервые описан нестероидный антиандрогенный энзалутамид второго поколения [214]
- 2007: Впервые описан нестероидный антиандроген апалутамид второго поколения [215]
- 2011: Абиратерона ацетат впервые используется в медицине для лечения рака простаты [216]
- 2012: Энзалутамид впервые используется в медицине для лечения рака простаты [217]
- 2018: Апалутамид впервые используется в медицине для лечения рака простаты [218]
- 2018: Elagolix - первый пероральный активный антагонист ГнРГ, представленный для медицинского применения [190]
Общество и культура [ править ]
Этимология [ править ]
Термин « антиандрогены» обычно используется для обозначения конкретно антагонистов AR, как описано Dorfman (1970): [219] [220]
Антиандрогены - это вещества, которые не позволяют андрогенам проявлять свою активность на сайтах-мишенях. Следовательно, ингибирующее действие этих веществ следует дифференцировать от соединений, которые уменьшают синтез и / или высвобождение гипоталамических (высвобождающих) факторов, от гормонов передней доли гипофиза (гонадотропинов, особенно лютеинизирующего гормона) и от материала, который действует непосредственно на гонады, чтобы подавляют биосинтез и / или секрецию андрогенов. [219] [220]
Однако, несмотря на вышесказанное, этот термин может также использоваться для описания функциональных антиандрогенов, таких как ингибиторы синтеза андрогенов и антигонадотропины, включая даже эстрогены и прогестагены. [2] [6] [221] Например, прогестаген и, следовательно, антигонадотропин медроксипрогестерона ацетат иногда описывают как стероидный антиандроген, даже если он не является антагонистом AR. [222] [221]
Исследование [ править ]
Актуальное введение [ править ]
Большой интерес и усилия были направлены на разработку местных антагонистов AR для лечения андроген-зависимых состояний, таких как угри и типичное облысение у мужчин. [223] К сожалению, несмотря на то, что системное введение антиандрогенов очень эффективно при лечении этих состояний, местное введение, к сожалению, обычно имеет ограниченную и лишь умеренную эффективность, даже когда использовались высокоаффинные стероидные антагонисты AR, такие как ципротерона ацетат и спиронолактон. [223] Более того, в конкретном случае лечения акне местные антагонисты AR оказались гораздо менее эффективными по сравнению с общепринятыми методами лечения, такими как перекись бензоила и антибиотики . [223]
Разнообразные антагонисты AR были разработаны для местного применения, но еще не завершили разработку и, следовательно, никогда не поступали в продажу. К ним относятся стероидные антагонисты AR класкотерон , ципротерон , ростеролон и топтерон и нестероидные антагонисты AR циотеронел , инокотерона ацетат , RU-22930 , RU-58642 и RU-58841 . Тем не менее, один местный антагонист AR, топилутамид (флуридил), был представлен в нескольких европейских странах для лечения облысения у мужчин. [40] Кроме того, местный ингибитор 5α-редуктазы и слабый эстроген,альфатрадиол , также был введен в некоторых европейских странах по тому же показанию, хотя его эффективность неоднозначна. [40] Спиронолактон продавался в Италии в форме крема для местного применения под торговой маркой Spiroderm для лечения акне и гирсутизма, но этот состав был прекращен и, следовательно, больше не доступен. [224]
Мужская контрацепция [ править ]
Антиандрогены, такие как ацетат ципротерона, изучались на предмет потенциального использования в качестве мужских гормональных контрацептивов . [225] [226] [227] [228] [63] [229] [230] [231] Несмотря на то, что они эффективны в подавлении мужской фертильности , их использование в качестве монотерапии исключается из-за побочных эффектов, таких как андрогенная недостаточность (например, демасклинизация , сексуальная дисфункция , приливы , остеопороз ) и феминизация (например, гинекомастия ). [63] [229] [230] [232]Комбинация первичного антигонадотропина, такого как ацетат ципротерона, для предотвращения фертильности и андрогена, подобного тестостерону, для предотвращения системного андрогенного дефицита, приводящего к селективному антиандрогенному действию локально в яичках, была тщательно изучена и дала многообещающие результаты, но не была одобрена. для клинического использования в настоящее время. [230] [231] [233] [234] [232] Диметандролона ундеканоат (код развития CDB-4521), перорально активный двойной ААС и гестаген, исследуется в качестве потенциального мужского противозачаточного средства и в качестве первой противозачаточной таблетки для мужчин. . [235] [236]
Рак груди [ править ]
Антиандрогены, такие как бикалутамид , энзалутамид и абиратерона ацетат , исследуются на предмет потенциального лечения рака груди , включая AR-экспрессирующий тройной отрицательный рак молочной железы и другие типы AR-экспрессирующего рака молочной железы. [237] [238] [239] [240] [241]
Разное [ править ]
Антиандрогены могут быть эффективны при лечении обсессивно-компульсивного расстройства . [242]
См. Также [ править ]
- Синдром нечувствительности к андрогенам
- Антиандрогены в окружающей среде
- Андрогенная заместительная терапия
Ссылки [ править ]
- ^ Mowszowicz I (1989). «Антиандрогены. Механизмы и парадоксальные эффекты». Анна. Эндокринол . Париж. 50 (3): 50 (3): 189–99. PMID 2530930 .
- ^ a b c d e f Брюггемайер, Роберт У. (2006). «Половые гормоны (мужские): аналоги и антагонисты». Энциклопедия молекулярной клеточной биологии и молекулярной медицины . DOI : 10.1002 / 3527600906.mcb.200500066 . ISBN 3527600906.
- ^ Джуди Линдсли Нат (2006). Использование медицинской терминологии: практический подход . Липпинкотт Уильямс и Уилкинс. С. 977 -. ISBN 978-0-7817-4868-1.
- ^ a b c d e Студент S, Hejmo T, Poterała-Hejmo A, Leśniak A, Bułdak R (январь 2020 г.). «Антиандрогенная гормональная терапия рака и других заболеваний» . Евро. J. Pharmacol . 866 : 172783. DOI : 10.1016 / j.ejphar.2019.172783 . PMID 31712062 .
- ^ Gillatt D (2006). «Лечение антиандрогенами при местнораспространенном раке простаты: все ли они одинаковы?». J Cancer Res Clin Oncol . 1 : S17-26. DOI : 10.1007 / s00432-006-0133-5 . PMID 16845534 . S2CID 23888640 .
- ^ Б с д е е г ч Lieberman R (2001). «Андрогенная депривационная терапия для химиопрофилактики рака простаты: текущее состояние и будущие направления развития агентов». Урология . 58 (2 Дополнение 1): 83–90. DOI : 10.1016 / s0090-4295 (01) 01247-X . PMID 11502457 .
Существует несколько классов антиандрогенов, включая (1) антигонадотропины (например, агонисты / антагонисты LHRH, синтетические эстрогены [диэтилстильбестрол]); (2) нестероидные антагонисты рецепторов андрогенов (например, флутамид, бикалутамид, нилутамид); (3) стероидные агенты смешанного действия (например, ацетат ципротерона); (4) ингибиторы андрогенов надпочечников (например, кетоконазол, гидрокортизон); (5) стероидные агенты, которые ингибируют биосинтез андрогенов (например, ингибиторы 5α-редуктазы (тип II) и ингибиторы 5α-редуктазы двойного действия); [...]
- ^ a b c Schröder, Fritz H .; Радлмайер, Альберт (2009). «Стероидные антиандрогены». В В. Крейге Джордане; Баррингтон Дж. А. Ферр (ред.). Гормональная терапия рака груди и простаты . Humana Press. стр. 325 -346. DOI : 10.1007 / 978-1-59259-152-7_15 . ISBN 978-1-60761-471-5.
- ^ a b c Kolvenbag, Geert JCM; Ферр, Баррингтон Дж. А. (2009). «Нестероидные антиандрогены». В В. Крейге Джордане; Баррингтон Дж. А. Ферр (ред.). Гормональная терапия рака груди и простаты . Humana Press. С. 347 –368. DOI : 10.1007 / 978-1-59259-152-7_16 . ISBN 978-1-60761-471-5.
- ^ a b c d Sciarra F, Toscano V, Concolino G, Di Silverio F (1990). «Антиандрогены: клиническое применение». J. Steroid Biochem. Мол. Биол . 37 (3): 349–62. DOI : 10.1016 / 0960-0760 (90) 90484-3 . PMID 2147859 . S2CID 20274398 .
- ^ Бродерик Г.А., Кадиогл А, Bivalacqua TJ, Гханет Н, Нера А, Shamloul R (2010). «Приапизм: патогенез, эпидемиология и лечение». J Sex Med . 7 (1 Pt 2): 476–500. DOI : 10.1111 / j.1743-6109.2009.01625.x . PMID 20092449 .
- ^ Мартин Х. Стейнберг; Бернард Г. Забудьте; Дуглас Р. Хиггс; Дэвид Дж. Уэтеролл (17 августа 2009 г.). Нарушения гемоглобина: генетика, патофизиология и клиническое лечение . Издательство Кембриджского университета. С. 476–. ISBN 978-1-139-48080-2.
- ^ a b c Essah PA, Wickham EP, Nunley JR, Nestler JE (2006). «Дерматология андрогенных заболеваний». Clin. Дерматол . 24 (4): 289–98. DOI : 10.1016 / j.clindermatol.2006.04.004 . PMID 16828411 .
- ^ a b c d e f g h Rabe, T .; Grunwald, K .; Feldmann, K .; Раннебаум, Б. (2009). «Лечение гиперандрогении у женщин». Гинекологическая эндокринология . 10 (sup3): 1–44. DOI : 10.3109 / 09513599609045658 . ISSN 0951-3590 .
- ^ а б в г Боктинг В, Коулман Э, Де Кайпере Г (2011). «Уход за транссексуалами». N. Engl. J. Med . 364 (26): 2559–60, ответ автора 2560. doi : 10.1056 / NEJMc1104884 . PMID 21714669 .
- ^ а б Вэнс С.Р., Эрензафт Д., Розенталь С.М. (2014). «Психологическая и медицинская помощь гендерно неконформной молодежи» (PDF) . Педиатрия . 134 (6): 1184–92. DOI : 10.1542 / peds.2014-0772 . PMID 25404716 . S2CID 5743822 .
- ^ Б с д е е г ч Wadosky КМ, Koochekpour S (2016). «Терапевтические обоснования, успехи, неудачи и будущие направления для прогрессирующего рака простаты» . Int. J. Biol. Sci . 12 (4): 409–26. DOI : 10.7150 / ijbs.14090 . PMC 4807161 . PMID 27019626 .
- ^ a b Massard C, Fizazi K (2011). «Нацеливание на продолжение передачи сигналов рецептора андрогена при раке простаты» . Clin. Cancer Res . 17 (12): 3876–83. DOI : 10.1158 / 1078-0432.CCR-10-2815 . PMID 21680543 .
- ^ Msaouel P, Диаманти E, Tzanela M, Koutsilieris M (2007). «Антагонисты лютеинизирующего гормона-рилизинг-гормона в терапии рака простаты». Экспертное мнение Emerg Drugs . 12 (2): 285–99. DOI : 10.1517 / 14728214.12.2.285 . PMID 17604502 . S2CID 41988320 .
- ^ a b Akaza H (январь 2011 г.). «Комбинированная андрогенная блокада при раке простаты: обзор эффективности, безопасности и рентабельности» . Наука о раке . 102 (1): 51–6. DOI : 10.1111 / j.1349-7006.2010.01774.x . PMID 21091846 . S2CID 38486547 .
- Перейти ↑ Mateo J, Smith A, Ong M, de Bono JS (2014). «Новые лекарства, направленные на путь рецепторов андрогенов при раке простаты». Рак Метастазы Rev . 33 (2–3): 567–79. DOI : 10.1007 / s10555-013-9472-2 . PMID 24390422 . S2CID 13980764 .
- ^ a b c d Иверсен П., Мелезинек И., Шмидт А. (2001). «Нестероидные антиандрогены: терапевтический вариант для пациентов с запущенным раком простаты, которые хотят сохранить сексуальный интерес и функцию» . BJU Int . 87 (1): 47–56. DOI : 10.1046 / j.1464-410x.2001.00988.x . PMID 11121992 . S2CID 28215804 .
- ^ Kolvenbag GJ, Айверсен P, Newling DW (август 2001). «Монотерапия антиандрогенами: новая форма лечения больных раком простаты». Урология . 58 (2 Дополнение 1): 16–23. DOI : 10.1016 / s0090-4295 (01) 01237-7 . PMID 11502439 .
- ^ Mcleod DG (2003). «Гормональная терапия: историческая перспектива в будущих направлениях». Урология . 61 (2 Дополнение 1): 3–7. DOI : 10.1016 / s0090-4295 (02) 02393-2 . PMID 12667881 .
- ^ a b Смит HJ, Уильямс H (10 октября 2005 г.). Смит и Уильямс «Введение в принципы разработки и действия лекарств», четвертое издание . CRC Press. С. 489–. ISBN 978-0-203-30415-0.
- ^ Chabner BA Лонго DL (8 ноября 2010). Химиотерапия и биотерапия рака: принципы и практика . Липпинкотт Уильямс и Уилкинс. С. 679–680. ISBN 978-1-60547-431-1.
Со структурной точки зрения антиандрогены классифицируются как стероидные, включая ципротерон [ацетат] (Андрокур) и мегестрол [ацетат], или нестероидные, включая флутамид (Эулексин и другие), бикалутамид (Касодекс) и нилутамид (Ниландрон). Стероидные антиандрогены используются редко.
- ^ Каликс RA, Del Giglio A (2008). «Управление распространенным раком простаты» (PDF) . Revista da Associação Médica Brasileira . 54 (2): 178–82. DOI : 10.1590 / S0104-42302008000200025 . PMID 18506331 .
- ^ Chang S (10 марта 2010), Бикалутамид BPCA Drug Обзор использования в педиатрической популяции (PDF) , Министерство здравоохранения и службы человека , извлекаться +20 июлю +2016
- ^ Gulley JL (2011). Рак простаты . Demos Medical Publishing. С. 81–. ISBN 978-1-935281-91-7.
- ↑ Moser L (1 января 2008 г.). Споры в лечении рака простаты . Медицинские и научные издательства Karger. С. 41–42. ISBN 978-3-8055-8524-8.
- ^ Рак простаты . Demos Medical Publishing. 20 декабря 2011. С. 505–. ISBN 978-1-935281-91-7.
- ^ Б с д е е г ч я J William Фигга; Синди Х. Чау; Эрик Дж. Смолл (14 сентября 2010 г.). Медикаментозное лечение рака простаты . Springer Science & Business Media. С. 71–72, 75, 91–96. ISBN 978-1-60327-829-4.
- ^ а б Rittmaster RS (2011). «Химиопрофилактика рака простаты» . Acta Oncol . 50 Дополнение 1: 127–36. DOI : 10.3109 / 0284186X.2010.527367 . PMID 21604953 .
- ↑ Mackenzie IS, Morant SV, Wei L, Thompson AM, MacDonald TM (2016). «Использование спиронолактона и риск возникновения рака: ретроспективное когортное исследование» . Br J Clin Pharmacol . 83 (3): 653–663. DOI : 10.1111 / bcp.13152 . PMC 5306481 . PMID 27735065 .
- ^ Hembree туалет, Коген-Kettenis Р, Delemarre-ван де Ваал HA, Gooren LJ, Meyer WJ, Spack Н.П., Tangpricha V, Montori VM (2009). «Эндокринное лечение транссексуалов: руководство по клинической практике эндокринного общества» . J. Clin. Эндокринол. Метаб . 94 (9): 3132–54. DOI : 10.1210 / jc.2009-0345 . PMID 19509099 .
- ^ Gooren л, Morgentaler А (2014). «Заболеваемость раком предстательной железы у транссексуалов, подвергшихся орхидэктомии от мужчины к женщине, получавших эстрогены». Андрология . 46 (10): 1156–60. DOI : 10.1111 / and.12208 . PMID 24329588 . S2CID 1445627 .
- ^ Туро R, Jallad S, S Prescott, Cross WR (2013). «Метастатический рак простаты у транссексуалов диагностирован после трех десятилетий терапии эстрогенами» . Может Urol Assoc J . 7 (7–8): E544–6. DOI : 10,5489 / cuaj.175 . PMC 3758950 . PMID 24032068 .
- ^ Б Dörsam Дж, Altwein J (2009). «Лечение заболеваний предстательной железы ингибитором 5альфа-редуктазы: предпосылки и практическое значение» . Prostate Cancer Prostatic Dis . 12 (2): 130–6. DOI : 10.1038 / pcan.2008.56 . PMID 19030020 .
- ^ Ishizuka O, Нишизава O, Hirao Y, Ohshima S (2002). «Доказательный метаанализ фармакотерапии доброкачественной гипертрофии простаты» . Int. J. Urol . 9 (11): 607–12. DOI : 10.1046 / j.1442-2042.2002.00539.x . PMID 12534901 . S2CID 8249363 .
- ^ Г. Распе; В. Бросиг (22 октября 2013 г.). Международный симпозиум по лечению рака простаты, Берлин, 13-15 ноября 1969 г .: Монографии по естественным наукам . Эльзевир. С. 165–. ISBN 978-1-4831-8711-2.
- ^ a b c Ральф М. Труэб; Вон Су Ли (13 февраля 2014 г.). Мужская алопеция: руководство по успешному лечению . Springer Science & Business Media. С. 91–93. ISBN 978-3-319-03233-7.
- ^ a b c Жан Л. Болонья; Джозеф Л. Йориццо; Рональд П. Рапини. Дерматология . Gulf Professional Publishing. С. 1072–. ISBN 9789997638991.
- ^ a b Симпсон, NB (1989). «Влияние лекарств на волосы». Фармакология кожи II . Справочник по экспериментальной фармакологии. 87 / 2. С. 495–508. DOI : 10.1007 / 978-3-642-74054-1_37 . ISBN 978-3-642-74056-5. ISSN 0171-2004 .
- ^ Б Уолтер П. Унгер (1 февраля 1995). «Андрогенетическая алопеция и ее лечение. Исторический обзор». Трансплантация волос, третье издание . Тейлор и Фрэнсис. С. 1–33. ISBN 978-0-8247-9363-0.
- ^ a b Расмуссон, Гэри Х. (1986). Глава 18. Химический контроль действия андрогенов . Годовые отчеты по медицинской химии. 21 . С. 179–188. DOI : 10.1016 / S0065-7743 (08) 61128-8 . ISBN 9780120405213. ISSN 0065-7743 .
- ^ a b Корман, RH; ван дер Мерен, HLM (1981). «Ципротеронацетат в лечении тяжелых угрей у мужчин». Архив дерматологических исследований . 271 (2): 183–187. DOI : 10.1007 / BF00412545 . ISSN 0340-3696 . S2CID 12153042 .
- ^ Гильтая EJ, Gooren LJ (2009). «Возможные побочные эффекты лечения андрогенной депривации у лиц, совершивших сексуальные преступления». Варенье. Акад. Закон о психиатрии . 37 (1): 53–8. PMID 19297634 .
- ^ Лам, Сэмюэл М .; Хемпстед, Брайан Р .; Уильямс, Эдвин Ф. (2012). «Варианты лечения выпадения волос». Эстетическая медицина . С. 529–535. DOI : 10.1007 / 978-3-642-20113-4_41 . ISBN 978-3-642-20112-7.
- ^ a b Neumann, Фридмунд (1996). «Фармакология ацетата ципротерона - краткий обзор». Антиандрогены при раке простаты . С. 31–44. DOI : 10.1007 / 978-3-642-45745-6_3 . ISBN 978-3-642-45747-0.
- ^ Коски, Ральф Дж. (1984). «Дерматологическая терапия: декабрь 1982 г. - ноябрь 1983 г.». Журнал Американской академии дерматологии . 11 (1): 25–52. DOI : 10.1016 / S0190-9622 (84) 80163-2 . ISSN 0190-9622 . PMID 6376557 .
- ^ Г. Плевиг; А.М. Клигман (6 декабря 2012 г.). АКНЕ и РОЗАЦЕЯ . Springer Science & Business Media. С. 687–. ISBN 978-3-642-59715-2.
- ^ Брайан К. Олдридж; Робин Л. Корелли; Майкл Э. Эрнст (1 февраля 2012 г.). Прикладная терапия Кода-Кимбла и Янга: клиническое использование лекарств . Липпинкотт Уильямс и Уилкинс. С. 952–. ISBN 978-1-60913-713-7.
- ^ Уорд, А .; Brogden, RN; Каблук, RC; Speight, TM; Эйвери, GS (1984). «Изотретиноин». Наркотики . 28 (1): 6–37. DOI : 10.2165 / 00003495-198428010-00002 . ISSN 0012-6667 . PMID 6235105 .
- ^ Миш KJ, Dolman WF, Neild V, Rhodes EL (1986). «Ответ мужских угрей на антиандрогенную терапию ципротерона ацетатом». Dermatologica . 173 (3): 139–42. DOI : 10.1159 / 000249236 . PMID 2945742 .
- ^ Кирчик LH (июль 2019). «Что нового в лечении вульгарных угрей» . Кутис . 104 (1): 48–52. PMID 31487336 .
- ^ Hassoun Л.А., Chahal DS, Сивамани RK, Ларсен LN (июнь 2016). «Применение гормональных средств при лечении угревой сыпи». Semin Cutan Med Surg . 35 (2): 68–73. DOI : 10,12788 / j.sder.2016.027 . PMID 27416311 .
- ^ Ричард Э. Джонс; Кристин Х. Лопес (28 сентября 2013 г.). Репродуктивная биология человека . Академическая пресса. С. 77–. ISBN 978-0-12-382185-0.
- ^ а б Брэдфорд JM (2001). «Нейробиология, нейрофармакология и фармакологическое лечение парафилий и компульсивного сексуального поведения» . Может J Психиатрия . 46 (1): 26–34. DOI : 10.1177 / 070674370104600104 . PMID 11221487 .
- ^ a b Guay DR (2009). «Медикаментозное лечение парафильных и непарафильных сексуальных расстройств». Clin Ther . 31 (1): 1–31. DOI : 10.1016 / j.clinthera.2009.01.009 . PMID 19243704 .
- ^ Уильям Ламонт Маршалл; DR Законы; Ховард Э. Барбари (21 ноября 2013 г.). Справочник по сексуальному насилию: проблемы, теории и обращение с преступником . Springer Science & Business Media. С. 297–. ISBN 978-1-4899-0915-2.
- ^ а б Альберт Дж. Стункард; Эндрю Баум (1989). Еда, сон и секс . Психология Press. С. 209–. ISBN 978-0-8058-0280-1.
- ↑ Эми Феникс; Гарри М. Хоберман (7 декабря 2015 г.). Сексуальное оскорбление: предрасполагающие факторы, оценки и управление . Springer. С. 759–. ISBN 978-1-4939-2416-5.
- ^ a b c d Брито В. Н., Латронико А. С., Арнхольд И. Дж., Мендонса ВВ (февраль 2008 г.). «Обновленная информация по этиологии, диагностике и терапевтическому лечению преждевременной половой жизни» . Arq Bras Endocrinol Metabol . 52 (1): 18–31. DOI : 10.1590 / S0004-27302008000100005 . PMID 18345393 .
- ^ a b c d e Tindall DJ, Chang CH, Lobl TJ, Cunningham GR (1984). «Антагонисты андрогенов в тканях-мишенях андрогенов». Pharmacol. Ther . 24 (3): 367–400. DOI : 10.1016 / 0163-7258 (84) 90010-X . PMID 6205409 .
- ^ Namer M (октябрь 1988). «Клиническое применение антиандрогенов». J. Steroid Biochem . 31 (4B): 719–29. DOI : 10.1016 / 0022-4731 (88) 90023-4 . PMID 2462132 .
- ^ a b Fraser HM, Baird DT (февраль 1987 г.). «Клиническое применение аналогов LHRH». Клиника Байера. Эндокринол. Метаб . 1 (1): 43–70. DOI : 10.1016 / S0950-351X (87) 80052-6 . PMID 3109366 .
- ^ Ларон Z, Kauli R (июль 2000). «Опыт применения ципротерона ацетата в лечении преждевременного полового созревания». J. Pediatr. Эндокринол. Метаб . 13 Дополнение 1: 805–10. DOI : 10,1515 / jpem.2000.13.s1.805 . PMID 10969925 . S2CID 25398066 .
- Перейти ↑ Neumann F, Kalmus J (1991). «Ципротерона ацетат в лечении сексуальных расстройств: фармакологическая основа и клинический опыт». Exp. Clin. Эндокринол . 98 (2): 71–80. DOI : 10,1055 / с-0029-1211103 . PMID 1838080 .
- ^ a b Holland FJ (март 1991 г.). «Гонадотропин-независимое преждевременное половое созревание». Эндокринол. Метаб. Clin. North Am . 20 (1): 191–210. DOI : 10.1016 / s0889-8529 (18) 30288-3 . PMID 1903104 .
- ^ a b Reiter EO, Norjavaara E (декабрь 2005 г.). «Тестотоксикоз: современная точка зрения». Pediatr Эндокринол Rev . 3 (2): 77–86. PMID 16361981 .
- ^ Левея HR, Kutlu O, Bivalacqua TJ (2012). «Медицинское лечение приапизма ишемического заикания: современный обзор литературы» . Азиатский журнал андрологии . 14 (1): 156–63. DOI : 10.1038 / aja.2011.114 . PMC 3753435 . PMID 22057380 .
- ^ Бродерик Г.А., Кадиогл А, Bivalacqua TJ, Гханет Н, Нера А, Shamloul R (2010). «Приапизм: патогенез, эпидемиология и лечение». Журнал сексуальной медицины . 7 (1 Pt 2): 476–500. DOI : 10.1111 / j.1743-6109.2009.01625.x . PMID 20092449 .
- Перейти ↑ Chow K, Payne S (2008). «Фармакологическое лечение перемежающихся приапизмальных состояний» . BJU International . 102 (11): 1515–21. DOI : 10.1111 / j.1464-410X.2008.07951.x . PMID 18793304 . S2CID 35399393 .
- ^ Dahm P, Рао DS, Donatucci CF (2002). «Антиандрогены в лечении приапизма». Урология . 59 (1): 138. DOI : 10.1016 / S0090-4295 (01) 01492-3 . PMID 11796309 .
- ^ Юань J, Desouza R, Westney OL, Ван R (2008). «Понимание механизма приапизма и обоснования лечения рецидивирующего приапизма» . Азиатский журнал андрологии . 10 (1): 88–101. DOI : 10.1111 / j.1745-7262.2008.00314.x . PMID 18087648 .
- ↑ Роберт Баран; Ховард И. Майбах (1 октября 1998 г.). Учебник косметической дерматологии . CRC Press. С. 388–. ISBN 978-1-85317-478-0.
- ^ Ховард И. Майбах; Фарзам Гороуи (2011). Доказательная дерматология . PMPH-США. С. 526–. ISBN 978-1-60795-039-4.
- ^ Хиуэл Уильямс; Майкл Бигби; Томас Дипген; Эндрю Херксхаймер; Луиджи Нальди; Бертольд Рзани (22 января 2009 г.). Доказательная дерматология . Джон Вили и сыновья. С. 529–. ISBN 978-1-4443-0017-8.
- ^ а б Erem C (2013). «Новости об идиопатическом гирсутизме: диагностика и лечение». Acta Clin Belg . 68 (4): 268–74. DOI : 10,2143 / ACB.3267 . PMID 24455796 . S2CID 39120534 .
- ^ Б Кеннет Л. Беккер (2001). Принципы и практика эндокринологии и обмена веществ . Липпинкотт Уильямс и Уилкинс. стр. 1004, 1196. ISBN 978-0-7817-1750-2.
- ^ a b c Камачо; Хоссейн Гариб; Глен В. Сайзмор (2012). Доказательная эндокринология . Липпинкотт Уильямс и Уилкинс. С. 199–. ISBN 978-1-4511-1091-3.
- ^ Рэндольф JF (декабрь 2018). «Гендероподобная гормональная терапия для трансгендерных женщин». Clin Obstet Gynecol . 61 (4): 705–721. DOI : 10.1097 / GRF.0000000000000396 . PMID 30256230 .
- ^ Б с д е е г ч Singh С.М., Gauthier S, ЛаБри F (2000). «Антагонисты рецепторов андрогенов (антиандрогены): взаимосвязь структура-активность». Curr. Med. Chem . 7 (2): 211–47. DOI : 10.2174 / 0929867003375371 . PMID 10637363 .
- ^ a b c d Шен, Ховард К.; Таплин, Мэри-Эллен; Балк, Стивен П. (2010). «Антагонисты рецепторов андрогенов». Медикаментозное лечение рака простаты : 71–81. DOI : 10.1007 / 978-1-60327-829-4_6 . ISBN 978-1-60327-831-7.
- ^ Шауэр, Павел; Боржик, Адам; Головко, Оксана; Грабич, Роман; Войс Станова, Андреа; Валентова, Ольга; Стара, Альжбета; Шандова, Мари; Коджур Крупова, Хана (2018). «Способствуют ли прогестины (анти-) андрогенной активности в водной среде?». Загрязнение окружающей среды . 242 (Pt A): 417–425. DOI : 10.1016 / j.envpol.2018.06.104 . PMID 29990947 .
- ^ Raudrant D, Раба T (2003). «Прогестагены с антиандрогенными свойствами». Наркотики . 63 (5): 463–92. DOI : 10.2165 / 00003495-200363050-00003 . PMID 12600226 . S2CID 28436828 .
- ^ Шнайдер HP (2003). «Андрогены и антиандрогены». Анна. NY Acad. Sci . 997 : 292–306. DOI : 10.1196 / annals.1290.033 . PMID 14644837 . S2CID 8400556 .
- ^ a b c d e е Джером Ф. Штраус, III; Роберт Л. Барбьери (13 сентября 2013 г.). Репродуктивная эндокринология Йен и Джаффе . Elsevier Health Sciences. С. 90–. ISBN 978-1-4557-2758-2.
- ^ Аггарваль S, Thareja S, Верма A, Bhardwaj TR, Kumar M (2010). «Обзор ингибиторов 5альфа-редуктазы». Стероиды . 75 (2): 109–53. DOI : 10.1016 / j.steroids.2009.10.005 . PMID 19879888 . S2CID 44363501 .
- ^ a b c Питер Б. Фармер; Джон М. Уокер (6 декабря 2012 г.). Молекулярные основы рака . Springer Science & Business Media. С. 232–. ISBN 978-1-4684-7313-1.
- ^ a b c d e е Томас Л. Лемке; Дэвид А. Уильямс (24 января 2012 г.). Принципы медицинской химии Фуа . Липпинкотт Уильямс и Уилкинс. С. 228–231, 1371–1372. ISBN 978-1-60913-345-0.
- ^ a b c de Lignières B, Silberstein S (апрель 2000 г.). «Фармакодинамика эстрогенов и прогестагенов». Цефалгия: Международный журнал головной боли . 20 (3): 200–7. DOI : 10.1046 / j.1468-2982.2000.00042.x . PMID 10997774 . S2CID 40392817 .
- ^ Уильям Леджер; Уильям Д. Шлафф; Тьерри Г. Ванкаилли (11 декабря 2014 г.). Хроническая тазовая боль . Издательство Кембриджского университета. С. 55–. ISBN 978-1-316-21414-5.
- ^ a b Луиза Ханна; Том Кросби; Фергус Макбет (19 ноября 2015 г.). Практическая клиническая онкология . Издательство Кембриджского университета. С. 37–. ISBN 978-1-107-68362-4.
- ^ a b Георг Ф. Вебер (22 июля 2015 г.). Молекулярные методы лечения рака . Springer. стр. 314, 316. ISBN 978-3-319-13278-5.
- ^ Mahler C, Verhelst J, Denis L (май 1998). «Клиническая фармакокинетика антиандрогенов и их эффективность при раке простаты». Clin Pharmacokinet . 34 (5): 405–17. DOI : 10.2165 / 00003088-199834050-00005 . PMID 9592622 . S2CID 25200595 .
- ^ a b Джон А. Томас (12 марта 1997 г.). Эндокринная токсикология, второе издание . CRC Press. С. 152–. ISBN 978-1-4398-1048-4.
- ^ Андерсон J (2003). «Роль монотерапии антиандрогенами в лечении рака простаты» . BJU Int . 91 (5): 455–61. DOI : 10.1046 / j.1464-410x.2003.04026.x . PMID 12603397 . S2CID 8639102 .
- ^ Терренс Пристман (26 мая 2012). Химиотерапия рака в клинической практике . Springer Science & Business Media. С. 97–. ISBN 978-0-85729-727-3.
- ^ а б в Хигано С.С. (2003). «Побочные эффекты андрогенной депривационной терапии: мониторинг и минимизация токсичности». Урология . 61 (2 Дополнение 1): 32–8. DOI : 10.1016 / S0090-4295 (02) 02397-X . PMID 12667885 .
- ^ Di Lorenzo G, Autorino R, S Perdonà, De Placido S (декабрь 2005). «Лечение гинекомастии у пациентов с раком простаты: систематический обзор». Ланцет Онкол . 6 (12): 972–9. DOI : 10.1016 / S1470-2045 (05) 70464-2 . PMID 16321765 .
- ↑ Джерри Шапиро (12 ноября 2012 г.). Заболевания волос: современные концепции в патофизиологии, диагностике и лечении, выпуск дерматологических клиник . Elsevier Health Sciences. С. 187–. ISBN 978-1-4557-7169-1.
- ^ В. Futterweit (6 декабря 2012). Поликистоз яичников . Springer Science & Business Media. С. 282–. ISBN 978-1-4613-8289-8.
- ^ Katsambas AD, Dessinioti C (2010). «Гормональная терапия прыщей: почему не в качестве терапии первой линии? Факты и противоречия». Clin. Дерматол . 28 (1): 17–23. DOI : 10.1016 / j.clindermatol.2009.03.006 . PMID 20082945 .
- ^ a b Thole Z, Manso G, Salgueiro E, Revuelta P, Hidalgo A (2004). «Гепатотоксичность, вызванная антиандрогенами: обзор литературы». Урол. Int . 73 (4): 289–95. DOI : 10.1159 / 000081585 . PMID 15604569 . S2CID 24799765 .
- ^ Китинг GM (март 2015 г.). «Энзалутамид: обзор его использования при метастатическом устойчивом к кастрации раке простаты, ранее не полученном химиотерапией». Наркотики и старение . 32 (3): 243–9. DOI : 10.1007 / s40266-015-0248-у . PMID 25711765 . S2CID 29563345 .
- ^ a b Филлис Кэролайн Лепперт; Джеффри Ф. Пейпер (2004). Первичная помощь женщинам . Липпинкотт Уильямс и Уилкинс. С. 277–. ISBN 978-0-7817-3790-6.
- ^ Спенсер А. Ратус; Джеффри С. Невид; Лоис Фихнер-Ратус (2005). Человеческая сексуальность в мире разнообразия . Пирсон Аллин и Бэкон. п. 313. ISBN 978-0-205-40615-9.
- ^ Аюб М, Levell MJ (август 1989). «Влияние кетоконазол-родственных имидазольных препаратов и антиандрогенов на связывание [3H] R 1881 с рецептором андрогенов предстательной железы и связывание [3H] 5 альфа-дигидротестостерона и [3H] кортизола с белками плазмы». J. Steroid Biochem . 33 (2): 251–5. DOI : 10.1016 / 0022-4731 (89) 90301-4 . PMID 2788775 .
- ^ a b c d e Poyet P, Labrie F (октябрь 1985 г.). «Сравнение антиандрогенной / андрогенной активности флутамида, ципротерона ацетата и мегестрола ацетата». Молекулярная и клеточная эндокринология . 42 (3): 283–8. DOI : 10.1016 / 0303-7207 (85) 90059-0 . PMID 3930312 . S2CID 24746807 .
- ^ Luthy И.А., Begin DJ, ЛаБри F (1988). «Андрогенная активность синтетических прогестинов и спиронолактона в андроген-чувствительных клетках карциномы молочной железы мыши (Shionogi) в культуре». Журнал стероидной биохимии . 31 (5): 845–52. DOI : 10.1016 / 0022-4731 (88) 90295-6 . PMID 2462135 .
- ^ Сундара S, Дикинсон PD (2012). «Спиронолактон, возможный селективный модулятор рецепторов андрогенов, следует применять с осторожностью у пациентов с метастатической карциномой простаты» . BMJ Case Rep . 2012 : bcr1120115238. DOI : 10.1136 / bcr.11.2011.5238 . PMC 3291010 . PMID 22665559 .
- ^ Флинн Т, Guancial Е.А., Kilari М, Kilari D (2016). «Отчет о клиническом случае: отмена спиронолактона, связанная с драматической реакцией у пациента с метастатическим кастраторезистентным раком простаты». Clin Genitourin Cancer . 15 (1): e95 – e97. DOI : 10.1016 / j.clgc.2016.08.006 . PMID 27641657 . S2CID 38441469 .
- ^ Джеймс VH, Pasqualini JR (22 октября 2013). Гормональные стероиды: материалы Шестого Международного конгресса по гормональным стероидам . Elsevier Science. С. 391–. ISBN 978-1-4831-9067-9.
- ^ a b Caubet JF, Tosteson TD, Dong EW, Naylon EM, Whiting GW, Ernstoff MS, Ross SD (1997). «Максимальная андрогенная блокада при распространенном раке простаты: метаанализ опубликованных рандомизированных контролируемых исследований с использованием нестероидных антиандрогенов». Урология . 49 (1): 71–8. DOI : 10.1016 / S0090-4295 (96) 00325-1 . PMID 9000189 .
Поскольку стероидные антиандрогены, такие как ципротерона ацетат, обладают внутренней андрогенной активностью и более низкой антиандрогенной активностью, чем NSAA, такие как флутамид и нилутамид, 39–43, неудивительно, что два класса антиандрогенов могут иметь разную эффективность.
- ^ a b c Сингх С.М., Готье С., Лабри Ф. (февраль 2000 г.). «Антагонисты рецепторов андрогенов (антиандрогены): взаимосвязь структура-активность». Современная лекарственная химия . 7 (2): 211–47. DOI : 10.2174 / 0929867003375371 . PMID 10637363 .
- ^ a b c d Ayub M, Levell MJ (август 1989 г.). «Влияние кетоконазол-родственных имидазольных препаратов и антиандрогенов на связывание [3H] R 1881 с рецептором андрогенов предстательной железы и связывание [3H] 5 альфа-дигидротестостерона и [3H] кортизола с белками плазмы». J. Steroid Biochem . 33 (2): 251–5. DOI : 10.1016 / 0022-4731 (89) 90301-4 . PMID 2788775 .
- ^ a b Ямасаки К., Саваки М., Нода С., Мурои Т., Такакура С., Митома Н., Сакамото С., Накаи М., Якабе Ю. (2004). «Сравнение анализа Хершбергера и анализа связывания рецепторов андрогенов двенадцати химических веществ». Токсикология . 195 (2–3): 177–86. DOI : 10.1016 / j.tox.2003.09.012 . PMID 14751673 .
- ^ Уильям Б. Пратт (1994). Противораковые препараты . Издательство Оксфордского университета. С. 220–. ISBN 978-0-19-506739-2.
У пациентов, получающих флутамид в обычной дозировке 250 мг каждые 8 часов, минимальная концентрация гидроксифлутамида в плазме составляет около 5 мкМ, что в 5000 раз превышает плазменную концентрацию тестостерона (1 нМ) у пациентов, получавших агонист LHRH.127 As гидроксифлутамид. только на один процент эффективнее тестостерона в борьбе за связывание с рецептором андрогенов, 126 для обеспечения эффективной конкуренции требуется уровень 5 мкМ гидроксифлутамида в плазме127. [...] Ципротерона ацетат и флутамид оказались эффективной терапией. (примерно эквивалент эстрогену) при использовании отдельно для лечения рака простаты123.
- ^ Bennett NC, Гардинер RA, Хупер JD, Johnson DW, Gobe GC (2010). «Молекулярно-клеточная биология передачи сигналов рецептора андрогенов». Int. J. Biochem. Cell Biol . 42 (6): 813–27. DOI : 10.1016 / j.biocel.2009.11.013 . PMID 19931639 .
- Перейти ↑ Wang C, Liu Y, Cao JM (2014). «Рецепторы, связанные с G-белком: внеядерные медиаторы для негеномных действий стероидов» . Int J Mol Sci . 15 (9): 15412–25. DOI : 10.3390 / ijms150915412 . PMC 4200746 . PMID 25257522 .
- ^ Lang F, Alevizopoulos K, Stournaras C (2013). «Нацеливание на мембранные рецепторы андрогенов в опухолях». Мнение эксперта. Ther. Цели . 17 (8): 951–63. DOI : 10.1517 / 14728222.2013.806491 . PMID 23746222 . S2CID 23918273 .
- ^ a b Ора Хирш Песковиц; Эрика А. Эугстер (2004). Детская эндокринология: механизмы, проявления и лечение . Липпинкотт Уильямс и Уилкинс. С. 248–. ISBN 978-0-7817-4059-3.
- ^ a b Джузеппе Буонокоре; Родольфо Браччи; Майкл Вайндлинг (28 января 2012 г.). Неонатология: практический подход к неонатальным заболеваниям . Springer Science & Business Media. С. 1012–. ISBN 978-88-470-1405-3.
- ↑ Ребекка М. Джордан-Янг (7 января 2011 г.). Brain Storm . Издательство Гарвардского университета. С. 82–. ISBN 978-0-674-05879-8.
- ^ Джудит Э. Оуэн Блейкмор; Шери А. Беренбаум; Линн С. Либен (13 мая 2013 г.). Гендерное развитие . Психология Press. С. 115–. ISBN 978-1-135-07932-1.
- ↑ Марио Магги (30 января 2012 г.). Гормональная терапия мужской сексуальной дисфункции . Джон Вили и сыновья. С. 6–. ISBN 978-0-470-65760-7.
- ^ a b c d e Имамура, Юске; Садар, Марианна Д. (2016). «Терапия, направленная на рецепторы андрогенов при устойчивом к кастрации раке простаты: от места до клиники» . Международный журнал урологии . 23 (8): 654–665. DOI : 10.1111 / iju.13137 . ISSN 0919-8172 . PMC 6680212 . PMID 27302572 .
- ↑ Де Мол, Ева; Фенвик, Р. Брин; Панг, Кристофер Т.В.; Бузон, Виктор; Шульц, Эльжбета; де ла Фуэнте, Алекс; Эскобедо, Альберт; Гарсия, Хесус; Bertoncini, Carlos W .; Эстебанес-Перпинья, Ева; МакЭван, Иэн Дж .; Риера, Антони; Сальвателла, Ксавьер (2016). «EPI-001, соединение, активное против устойчивого к кастрации рака простаты, нацелено на блок трансактивации 5 рецептора андрогенов» . ACS Химическая биология . 11 (9): 2499–2505. DOI : 10.1021 / acschembio.6b00182 . ISSN 1554-8929 . PMC 5027137 . PMID 27356095 .
- ^ Мартинес-Арис G, Халй С (2015). «Последние достижения в области ингибиторов аллостерических рецепторов андрогенов для потенциального лечения резистентного к кастрации рака простаты». Pharm Pat Anal . 4 (5): 387–402. DOI : 10.4155 / ppa.15.20 . PMID 26389532 .
- ^ а б Лай, AC; Crews, CM (25 ноября 2016 г.). «Индуцированная деградация белка: новая парадигма открытия лекарств» . Обзоры природы. Открытие наркотиков . 16 (2): 101–114. DOI : 10.1038 / nrd.2016.211 . PMC 5684876 . PMID 27885283 .
- ^ а б Лай КП, Хуанг СК, Чанг YJ, Чунг CY, Ямасита С., Ли Л., Ли СО, Йе С., Чанг С. (2013). «Новый терапевтический подход к подавлению устойчивого к кастрации рака простаты с использованием ASC-J9 посредством нацеливания на рецептор андрогенов в селективных клетках простаты» . Являюсь. J. Pathol . 182 (2): 460–73. DOI : 10.1016 / j.ajpath.2012.10.029 . PMC 3562731 . PMID 23219429 .
- ^ http://adisinsight.springer.com/drugs/800028542
- ^ Witjes FJ, Debruyne FM, Фернандеса дель Мораль P, Geboers AD (май 1989). «Высокая доза кетоконазола для лечения пациентов с прогрессирующим метастатическим раком простаты, получающих гормональное лечение. Голландская юго-восточная урологическая кооперативная группа». Урология . 33 (5): 411–5. DOI : 10.1016 / 0090-4295 (89) 90037-X . PMID 2652864 .
- ^ a b Жанна Хельд-Вармкессель (2006). Современные проблемы рака простаты: перспективы медсестер . Джонс и Бартлетт Обучение. С. 275–. ISBN 978-0-7637-3075-8.
- Перейти ↑ Bird IM, Abbott DH (2016). «Охота на селективный ингибитор лиазы 17,20; уроки природы» . J. Steroid Biochem. Мол. Биол . 163 : 136–46. DOI : 10.1016 / j.jsbmb.2016.04.021 . PMC 5046225 . PMID 27154414 .
- ^ Flores E, Bratoeff E, Кабеса M, Рамирес E, Quiroz A, Heuze I (май 2003). «Ингибиторы стероид-5альфа-редуктазы». Миниобзоры по медицинской химии . 3 (3): 225–37. DOI : 10.2174 / 1389557033488196 . PMID 12570838 .
- ^ Ашраф Мозаяни; Лайонел Раймон (18 сентября 2011 г.). Справочник лекарственных взаимодействий: клиническое и судебно-медицинское руководство . Springer Science & Business Media. С. 656–. ISBN 978-1-61779-222-9.
- ^ a b c Н. В. Бхагаван (2002). Медицинская биохимия . Академическая пресса. С. 787–. ISBN 978-0-12-095440-7.
- ^ Hirshburg JM, Kelsey PA, Therrien CA, Gavino AC, Reichenberg JS (2016). «Побочные эффекты и безопасность ингибиторов 5-альфа редуктазы (финастерид, дутастерид): систематический обзор» . J Clin Aesthet Dermatol . 9 (7): 56–62. PMC 5023004 . PMID 27672412 .
- ^ Stege R, Гуннарссон ПО, Йоханссон CJ, Олссон Р, Pousette А, Карлстрём К (1996). «Фармакокинетика и подавление тестостерона однократной дозы полиэстрадиолфосфата (эстрадурина) у больных раком предстательной железы». Простаты . 28 (5): 307–10. DOI : 10.1002 / (SICI) 1097-0045 (199605) 28: 5 <307 :: AID-PROS6> 3.0.CO; 2-8 . PMID 8610057 .
- ^ Фуркад, R.-O .; Маклеод Д. (2015). «Переносимость антиандрогенов при лечении рака простаты». Уроонкология . 4 (1): 5–13. DOI : 10.1080 / 1561095042000191655 . ISSN 1561-0950 .
- ^ Urotext (1 января 2001). Уротекст-Лутс: Урология . Юротекст. С. 71–. ISBN 978-1-903737-03-3.
- Перейти ↑ Neumann F (1978). «Физиологическое действие прогестерона и фармакологические эффекты прогестагенов - краткий обзор». Последипломный медицинский журнал . 54 Дополнение 2: 11–24. PMID 368741 .
- ^ Jacobi GH, Altwein JE, Курта КН, Наметочная R, Хохенфелльнер R (1980). «Лечение распространенного рака предстательной железы парентеральным ципротерона ацетатом: рандомизированное исследование фазы III». Br J Urol . 52 (3): 208–15. DOI : 10.1111 / j.1464-410x.1980.tb02961.x . PMID 7000222 .
- ^ Wein AJ, Kavoussi LR, Новик AC, Partin AW, Петерс CA (25 августа 2011). Campbell-Walsh Urology: Expert Consult Premium Edition: Enhanced Online Features and Print, 4-Volume Set . Elsevier Health Sciences. С. 2938–. ISBN 978-1-4160-6911-9.
- ^ Кьелд JM, Фуа СМ, Кауфман В, Лоизу S, Vlotides Дж, Gwee НМ, Кан Р, Р Sood, Джоплин Г. Ф. (1979). «Влияние приема норгестрела и этинилэстрадиола на сывороточные уровни половых гормонов и гонадотропинов у мужчин». Клиническая эндокринология . 11 (5): 497–504. DOI : 10.1111 / j.1365-2265.1979.tb03102.x . PMID 519881 . S2CID 5836155 .
- ↑ Norman G, Dean ME, Langley RE, Hodges ZC, Ritchie G, Parmar MK, Sydes MR, Abel P, Eastwood AJ (2008). «Парентеральный эстроген в лечении рака простаты: систематический обзор» . Br. J. Рак . 98 (4): 697–707. DOI : 10.1038 / sj.bjc.6604230 . PMC 2259178 . PMID 18268497 .
- ^ Dekanski JB (1980). «Антипростатическая активность бифлуранола, фторированного бибензила» . Br. J. Pharmacol . 71 (1): 11–6. DOI : 10.1111 / j.1476-5381.1980.tb10903.x . PMC 2044395 . PMID 6258683 .
- ^ Sander S, Ниссен-Мейер R, Aakvaag А (1978). «О гестагеновом лечении прогрессирующей карциномы простаты». Сканд. J. Urol. Нефрол . 12 (2): 119–21. DOI : 10.3109 / 00365597809179977 . PMID 694436 .
- ^ Роберт Алан Прентки; Энн Уолберт Берджесс (31 июля 2000 г.). Судебно-медицинская экспертиза сексуальных преступников . Springer Science & Business Media. С. 219–. ISBN 978-0-306-46278-8.
- ^ Судо K, Ямадзаки I, Масуока M, Накаяма R (1979). «Антиандроген TSAA-291. IV. Влияние антиандрогена TSAA-291 (16 бета-этил-17 бета-гидрокси-4-эстрен-3-он) на секрецию гонадотропинов». Acta Endocrinol Suppl (Копен) . 229 : 53–66. DOI : 10,1530 / acta.0.092s053 . PMID 294107 .
- ^ a b Эберхард Нишлаг; Герман М. Бере; Сьюзан Нишлаг (26 июля 2012 г.). Тестостерон: действие, дефицит, замещение . Издательство Кембриджского университета. С. 62–. ISBN 978-1-107-01290-5.
- ^ a b c Рабочая группа МАИР по оценке канцерогенных рисков для людей; Всемирная организация здоровья; Международное агентство по изучению рака (2007 г.). Комбинированные эстроген-прогестагенные контрацептивы и комбинированная эстроген-прогестагенная терапия при менопаузе . Всемирная организация здоровья. С. 157–. ISBN 978-92-832-1291-1.
- ↑ Coss CC, Jones A, Parke DN, Narayanan R, Barrett CM, Kearbey JD, Veverka KA, Miller DD, Morton RA, Steiner MS, Dalton JT (2012). «Доклиническая характеристика нового селективного агониста ERα дифенилбензамида для гормональной терапии рака простаты» . Эндокринология . 153 (3): 1070–81. DOI : 10.1210 / en.2011-1608 . PMID 22294742 .
- ^ а б Кришна; Уша Р. (1 января 2000 г.). Подростковая гинекология (pb) . Ориент Блэксуан. стр. 121–. ISBN 978-81-250-1793-6.
- ^ Маркус Filshie; Джон Гийбо (22 октября 2013 г.). Контрацепция: наука и практика . Elsevier Science. С. 26–. ISBN 978-1-4831-6366-6.
- ^ a b Шломо Мелмед; Кеннет С. Полонски; П. Рид Ларсен; Генри М. Кроненберг (12 мая 2011 г.). Электронная книга "Учебник эндокринологии" Уильямса . Elsevier Health Sciences. С. 753–. ISBN 978-1-4377-3600-7.
- ^ a b Винай Кумар; Абул К. Аббас; Нельсон Фаусто; Джон К. Астер (10 июня 2009 г.). Электронная книга "Патологические основы болезней" Роббинса и Котрана . Elsevier Health Sciences. С. 1154–. ISBN 978-1-4377-2015-0.
- ^ а б Дж. М. Сринан; М.Г. Дискин (6 декабря 2012 г.). Эмбриональная смертность сельскохозяйственных животных . Springer Science & Business Media. С. 172–. ISBN 978-94-009-5038-2.
- ^ a b Сатиш Кумар Джиндал; MC Шарма (2010). Биотехнология в ветеринарии и производстве . Издательство Новой Индии. С. 77–. ISBN 978-93-80235-35-6.
- ^ a b Николакис, Георгиос; Киргидис, Афанасий; Зубулис, Христос К. (2019). «Есть ли роль антиандрогенной терапии суппуративного гидраденита? Систематический обзор опубликованных данных». Американский журнал клинической дерматологии . 20 (4): 503–513. DOI : 10.1007 / s40257-019-00442-ш . ISSN 1175-0561 . PMID 31073704 . S2CID 149443722 .
- ^ Марк А. Фриц; Леон Сперофф (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие . Липпинкотт Уильямс и Уилкинс. С. 750–751, 963. ISBN 978-1-4511-4847-3.
- ^ Kavoussi P, Костабиле RA, Salonia A (17 октября 2012). Клиническая урологическая эндокринология: принципы мужского здоровья . Springer Science & Business Media. С. 7–. ISBN 978-1-4471-4404-5.
- ^ Достижения в исследованиях лекарственных средств . Академическая пресса. 12 августа 1997. С. 34–. ISBN 978-0-08-052628-7.
- ^ Боого И. Jugdutt (19 февраля 2014). Старение и сердечная недостаточность: механизмы и управление . Springer Science & Business Media. С. 175–. ISBN 978-1-4939-0268-2.
- ^ Camille Georges Вермут (2 мая 2011). Практика мурлов = https://books.google.com/books?id=Qmt1_DQkCpEC&pg=PA34 . Академическая пресса. стр. 34–. ISBN 978-0-08-056877-5.
- ^ Рикардо Azziz (8 ноября 2007). Нарушения избытка андрогенов у женщин . Springer Science & Business Media. С. 382–. ISBN 978-1-59745-179-6.
- ^ Бенно Clemens Runnebaum; Томас Рабе; Людвиг Кизель (6 декабря 2012 г.). Женская контрацепция: обновление и тенденции . Springer Science & Business Media. С. 136–. ISBN 978-3-642-73790-9.
- ^ CE Орфанос; В. Монтанья; Г. Штюттген (6 декабря 2012 г.). Исследования волос: состояние и будущие аспекты; Материалы Первого Международного конгресса по исследованию волос, Гамбург, 13 марта-16, 1979 . Springer Science & Business Media. С. 587–. ISBN 978-3-642-81650-5.
- ^ Лара Маркс (2010). Сексуальная химия: история противозачаточных таблеток . Издательство Йельского университета. С. 76–78. ISBN 978-0-300-16791-7.
- ^ Дж. Хорски; Дж. Пресл (6 декабря 2012 г.). Функция яичников и ее нарушения: диагностика и терапия . Springer Science & Business Media. С. 112–. ISBN 978-94-009-8195-9.
- ^ Витамины и гормоны . Академическая пресса. 18 мая 1976. С. 682–. ISBN 978-0-08-086630-7.
- ^ Дэвид Э. Нил (6 декабря 2012 г.). Опухоли в урологии . Springer Science & Business Media. стр. 233–. ISBN 978-1-4471-2086-5.
- ^ Экхард Ottow; Хильмар Вайнманн (8 сентября 2008 г.). Ядерные рецепторы как мишени для лекарств . Джон Вили и сыновья. С. 255–. ISBN 978-3-527-62330-3.
- ^ Радхи Лал Сингхал; Джон А. Томас (1 января 1976 г.). Клеточные механизмы, регулирующие действие гонад . University Park Press. п. 239. ISBN 978-0-8391-0776-7.
- ^ Лю, Бо; Су, Лей; Гэн, Цзинкунь; Лю, Цзюньцзе; Чжао, Гуйсэн (2010). «Разработки нестероидных антиандрогенов, нацеленных на рецептор андрогенов». ChemMedChem . 5 (10): 1651–1661. DOI : 10.1002 / cmdc.201000259 . ISSN 1860-7179 . PMID 20853390 . S2CID 23228778 .
- ^ Heyns, W .; Г., Верховен; Де Моор, П. (1976). «Связывание андрогенов в цитозоле матки крысы. Исследование специфичности». Журнал стероидной биохимии . 7 (5): 335–343. DOI : 10.1016 / 0022-4731 (76) 90092-3 . ISSN 0022-4731 . PMID 180344 .
- ^ Годовые отчеты по медицинской химии . Академическая пресса. 16 сентября 1986. С. 182–. ISBN 978-0-08-058365-5.
- ^ Борис, А .; Скотт, JW; ДеМартино, Л .; Кокс, округ Колумбия (1973). «Эндокринный профиль нестероидного антиандрогена N- (3,5-диметил-4-изоксазолилметил) фталимида (Dimp)». Европейский журнал эндокринологии . 72 (3): 604–614. DOI : 10,1530 / acta.0.0720604 . ISSN 0804-4643 . PMID 4739363 .
- ^ a b c Жан-Пьер Беге; Даниэле Бонне-Делпон (2 июня 2008 г.). Биоорганическая и лекарственная химия фтора . Джон Вили и сыновья. стр. 327–. ISBN 978-0-470-28187-1.
- ^ Менон MP, Higano CS (2013). «Энзалутамид, антагонист рецепторов андрогенов второго поколения: разработка и клиническое применение при раке простаты». Curr Oncol Rep . 15 (2): 69–75. DOI : 10.1007 / s11912-013-0293-9 . PMID 23341368 . S2CID 8725297 .
- ^ а б Тран С, Оук С., Клегг, штат Нью-Джерси, Чен И, Уотсон, Пенсильвания, Арора В., Вонгвипат Дж., Смит-Джонс, П. М., Ю Д., Квон А., Василевска Т., Уэлсби Д., Чен С. Д., Хигано С. С., пиво TM, Хунг Д.Т., Шер Х.И., Юнг МЭ, Сойерс С.Л. (2009). «Разработка антиандрогена второго поколения для лечения запущенного рака простаты» . Наука . 324 (5928): 787–90. DOI : 10.1126 / science.1168175 . PMC 2981508 . PMID 19359544 .
- ^ https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm596768.htm
- ^ Вальтер Sneader (23 июня 2005). Открытие наркотиков: история . Джон Вили и сыновья. С. 367–. ISBN 978-0-471-89979-2.
- ^ Дэвид Э. Голан (2008). Принципы фармакологии: патофизиологические основы лекарственной терапии . Липпинкотт Уильямс и Уилкинс. стр. 624–. ISBN 978-0-7817-8355-2.
- ^ Рак простаты . Demos Medical Publishing. 20 декабря 2011. С. 518–. ISBN 978-1-935281-91-7.
- ^ Winsor Bowsher; Адам Картер (15 апреля 2008 г.). Проблемы при раке простаты . Джон Вили и сыновья. С. 138–. ISBN 978-1-4051-7177-9.
- ^ Гаутам Аллахбадия; Рина Агравал; Рубина Мерчант (2007). Синдром поликистозных яичников . Аньшань. С. 184–. ISBN 978-1-904798-74-3.
- ^ Границы медицинской химии . Издательство Bentham Science. 2010. С. 329–. ISBN 978-1-60805-208-0.
- ^ a b https://adisinsight.springer.com/drugs/800020238
- ^ Crawford ED, Schellhammer PF, McLeod DG, Moul JW, Higano CS, Shore N, Denis L, Iversen P, Eisenberger MA, Labrie F (ноябрь 2018 г.). «Целенаправленное лечение рака простаты на рецепторы андрогенов: 35 лет прогресса с антиандрогенами». J. Urol . 200 (5): 956–966. DOI : 10.1016 / j.juro.2018.04.083 . PMID 29730201 . S2CID 19162538 .
- ^ a b c Kolkhof P, Bärfacker L (июль 2017 г.). «30 ЛЕТ МИНЕРАЛОКОРТИКОИДНОГО РЕЦЕПТОРА: Антагонисты минералокортикоидных рецепторов: 60 лет исследований и разработок» . J. Endocrinol . 234 (1): T125 – T140. DOI : 10.1530 / JOE-16-0600 . PMC 5488394 . PMID 28634268 .
- ^ Pucci E, F Petraglia (декабрь 1997). «Лечение избытка андрогенов у женщин: вчера, сегодня, завтра». Гинеколь. Эндокринол . 11 (6): 411–33. DOI : 10.3109 / 09513599709152569 . PMID 9476091 .
- ^ Смит, WG (1962). «Спиронолактон и гинекомастия». Ланцет . 280 (7261): 886. DOI : 10.1016 / S0140-6736 (62) 90668-2 . ISSN 0140-6736 .
- ^ Хамада, H; Neumann, F; Junkmann, K (ноябрь 1963 г.). «Внутриутробный антимаскулин Beeinflussung von Rattenfeten Durch ein Stark Gestagen Wirksames Steroid» [Внутриутробное антимышечное влияние плодов крыс в результате рождения мощного стероида, действующего как гестаген]. Acta Endocrinologica (на немецком языке). 44 (3): 380–388. DOI : 10,1530 / acta.0.0440380 . ISSN 0804-4643 . PMID 14071315 .
- ^ a b Стюарт ME, Почи PE (апрель 1978 г.). «Антиандрогены и кожа». Int. J. Dermatol . 17 (3): 167–79. DOI : 10.1111 / j.1365-4362.1978.tb06057.x . PMID 148431 . S2CID 43649686 .
- ↑ Zarate A, Mahesh VB, Greenblatt RB (декабрь 1966 г.). «Влияние антиандрогена 17-альфа-метил-B-нортестостерона на угри и гирсутизм». J. Clin. Эндокринол. Метаб . 26 (12): 1394–8. DOI : 10,1210 / jcem-26-12-1394 . PMID 4225258 .
- ^ Тибо F, De La Barra F, H Гордон, Cosyns P, Брэдфорд JM (июнь 2010). «Рекомендации Всемирной федерации обществ биологической психиатрии (WFSBP) по биологическому лечению парафилий». Мир J. Biol. Психиатрия . 11 (4): 604–55. DOI : 10.3109 / 15622971003671628 . PMID 20459370 . S2CID 14949511 .
- ^ Хаммерштейн, J; Купчанку, Б. (апрель 1969 г.). "Behandlung des Hirsutismus mit Cyproteronacetat" [Лечение гирсутизма с использованием ацетата ципротерона]. Deutsche Medizinische Wochenschrift (на немецком языке). 94 (16): 829–34. DOI : 10,1055 / с-0028-1111126 . ISSN 0012-0472 . PMID 4304873 .
- ^ Steelman SL, Брукс JR, Morgan ER, Patanelli DJ (1969). «Антиандрогенная активность спиронолактона». Стероиды . 14 (4): 449–50. DOI : 10.1016 / s0039-128x (69) 80007-3 . PMID 5344274 .
- Перейти ↑ Neri R, Florance K, Koziol P, Van Cleave S (август 1972). «Биологический профиль нестероидного антиандрогена, SCH 13521 (4'-нитро-3'трифторметилизобутиранилид)». Эндокринология . 91 (2): 427–37. DOI : 10,1210 / эндо-91-2-427 . PMID 4264731 .
- ^ Neri RO, Монахан M (сентябрь 1972). «Влияние нового нестероидного антиандрогена на гиперплазию простаты у собак». Инвестируйте Урол . 10 (2): 123–30. PMID 4116667 .
- Перейти ↑ Neumann F (1994). «Антиандроген ципротерона ацетат: открытие, химия, фундаментальная фармакология, клиническое использование и инструмент в фундаментальных исследованиях». Exp. Clin. Эндокринол . 102 (1): 1–32. DOI : 10,1055 / с-0029-1211261 . PMID 8005205 .
- ^ Рейно ДП, Bonne С, Бутон ММ, Лагас л, Labrie F (1979). «Действие нестероидного антиандрогена RU 23908 на периферические и центральные ткани». J. Steroid Biochem . 11 (1A): 93–9. DOI : 10.1016 / 0022-4731 (79) 90281-4 . PMID 385986 .
- ^ Обер КП, Хеннесси JF (1978). «Спиронолактонная терапия гирсутизма у гиперандрогенной женщины». Анна. Междунар. Med . 89 (5 Pt 1): 643–4. DOI : 10.7326 / 0003-4819-89-5-643 . PMID 717935 .
- ↑ Klotz L (май 2006 г.). «Комбинированная андрогенная блокада: актуальная информация». Урол. Clin. North Am . 33 (2): 161–6, v – vi. DOI : 10.1016 / j.ucl.2005.12.001 . PMID 16631454 .
- ^ Лабри Ф, Дюпон А, Беланжер А, Кьюзан Л, Лакурсьер Y, Монфетт Дж, Лаберже Дж. Г., Эмонд Дж. П., Фазекас А. Т., Рейно Дж. П., Хассон Дж. М. (1982). «Новая гормональная терапия карциномы простаты: комбинированное лечение агонистом LHRH и антиандрогеном». Clin Invest Med . 5 (4): 267–75. PMID 6819101 .
- ^ Энгель Дж, Клееманн А, Б Кучер, Reichert D (2009). Фармацевтические субстанции: синтезы, патенты и применения наиболее актуальных API (5-е изд.). Тиме. С. 153–154. ISBN 978-3-13-179275-4.
- ↑ William Andrew Publishing (22 октября 2013 г.). Энциклопедия фармацевтического производства, 3-е издание . Эльзевир. стр. 1695–. ISBN 978-0-8155-1856-3.
- ^ Ирландские отчеты: содержащие отчеты о случаях, рассмотренных и решенных в Апелляционном суде, Высоком суде справедливости, Суде по делам о банкротстве в Ирландии и Ирландской земельной комиссии . Объединенный юридический совет по отчетности Ирландии. 1990. С. 501–502.
- ^ Вера Regitz-Zagrosek (2 октября 2012). Пол и гендерные различия в фармакологии . Springer Science & Business Media. С. 575–. ISBN 978-3-642-30725-6.
- ^ https://www.icr.ac.uk/news-features/latest-features/abiraterone-a-story-of-scientific-innovation-and-commercial-partnership
- ^ http://adisinsight.springer.com/drugs/800004379
- ^ Sawyers, К. Юнг, М. Чен, К., Оук С., Welsbie Д., Tran, C, ... & Yoo, D. (2006). Заявка на патент США № 11 / 433,829. https://www.google.com/patents/US20070004753
- ^ https://worldwide.espacenet.com/publicationDetails/originalDocument?FT=D&date=20071108&DB=EPODOC&locale=en_EP&CC=WO&NR=2007126765A2&KC=A2&ND=6
- ^ https://adisinsight.springer.com/drugs/800005133
- ^ https://adisinsight.springer.com/drugs/800026688
- ^ http://adisinsight.springer.com/drugs/800032695
- ^ a b Neumann F (январь 1977 г.). «Фармакология и возможности использования ацетата ципротерона». Horm. Метаб. Res . 9 (1): 1–13. DOI : 10,1055 / с-0028-1093574 . PMID 66176 .
- ^ a b Дорфман, Ральф I. (1970). «Биологическая активность антиандрогенов». Британский журнал дерматологии . 82 (s6): 3. DOI : 10.1111 / j.1365-2133.1970.tb07998.x . ISSN 0007-0963 . S2CID 71393789 .
- ^ a b Gräf, K.-J .; Brotherton, J .; Нойман, Ф. (1974). «Клиническое использование антиандрогенов». Андрогены II и антиандрогены / Андрогены II и антиандрогены . С. 485–542. DOI : 10.1007 / 978-3-642-80859-3_7 . ISBN 978-3-642-80861-6.
- ^ Николас Фогельзанг (2006). Комплексный учебник мочеполовой онкологии . Липпинкотт Уильямс и Уилкинс. С. 316–. ISBN 978-0-7817-4984-8.
- ^ a b c Ричард А. Хелмс; Дэвид Дж. Куан (2006). Учебник терапии: лекарства и лечение заболеваний . Липпинкотт Уильямс и Уилкинс. С. 211–. ISBN 978-0-7817-5734-8.
- ^ НАДИР Р. ФАРИД; Эвантия Диаманти-Кандаракис (27 февраля 2009 г.). Диагностика и лечение синдрома поликистозных яичников . Springer Science & Business Media. С. 235–. ISBN 978-0-387-09718-3.
- Перейти ↑ Neumann F, Diallo FA, Hasan SH, Schenck B, Traore I (1976). «Влияние фармацевтических препаратов на мужскую фертильность». Андрология . 8 (3): 203–35. DOI : 10.1111 / j.1439-0272.1976.tb02137.x . PMID 793446 . S2CID 24859886 .
- ^ Прасад М. Р., Rajalakshmi М (1976). «Целевые сайты для подавления фертильности у мужчин». Adv Sex Horm Res . 2 : 263–87. PMID 797248 .
- ^ Юинг LL, Robaire B (1978). «Эндогенные антисперматогенные средства: перспективы мужской контрацепции». Анну. Rev. Pharmacol. Toxicol . 18 : 167–87. DOI : 10.1146 / annurev.pa.18.040178.001123 . PMID 206192 .
- ↑ Gombe S (апрель 1983 г.). «Обзор текущего состояния исследований мужских контрацептивов». Восточный Афр Med J . 60 (4): 203–11. PMID 6354690 .
- ^ а б Шривастава Р.П., Бхадури А.П. (1989). «Новые концепции развития противозачаточных средств». Prog Drug Res . 33 : 267–315. DOI : 10.1007 / 978-3-0348-9146-2_9 . ISBN 978-3-0348-9925-3. PMID 2687939 .
- ^ a b c Wu FC (октябрь 1988 г.). «Мужская контрацепция: современное состояние и перспективы на будущее». Clin. Эндокринол. (Oxf) . 29 (4): 443–65. DOI : 10.1111 / j.1365-2265.1988.tb02894.x . PMID 3075164 . S2CID 36608203 .
- ^ a b Nieschlag E, Zitzmann M, Kamischke A (ноябрь 2003 г.). «Использование прогестинов в мужской контрацепции». Стероиды . 68 (10–13): 965–72. DOI : 10.1016 / s0039-128x (03) 00135-1 . PMID 14667989 . S2CID 22458746 .
- ^ а б Nieschlag E (2010). «Клинические испытания мужской гормональной контрацепции» (PDF) . Контрацепция . 82 (5): 457–70. DOI : 10.1016 / j.contraception.2010.03.020 . PMID 20933120 .
- ^ Rajalakshmi M (ноябрь 2005). «Мужская контрацепция: расширение репродуктивного выбора». Индийский J. Exp. Биол . 43 (11): 1032–41. PMID 16313066 .
- ↑ Chao JH, Page ST (июль 2016 г.). «Современное состояние мужской гормональной контрацепции». Pharmacol. Ther . 163 : 109–17. DOI : 10.1016 / j.pharmthera.2016.03.012 . PMID 27016468 .
- ^ Attardi BJ, Хильд SA, Reel JR (июнь 2006). «Ундеканоат диметандролона: новый мощный перорально активный андроген с прогестагенной активностью» . Эндокринология . 147 (6): 3016–26. DOI : 10.1210 / en.2005-1524 . PMID 16497801 .
- ^ АЙЮБ R, страница ST, Swerdloff RS, Лю PY, Эймори Ю.К., Leung А, Халл л, Блит D, Кристи А, Чао JH, Бремнер WJ, Ван С (март 2017 г.). «Сравнение фармакокинетики, фармакодинамики и безопасности однократной дозы двух новых пероральных препаратов диметандролона ундеканоата (DMAU): потенциального перорального мужского контрацептива» . Андрология . 5 (2): 278–285. DOI : 10.1111 / andr.12303 . PMC 5352517 . PMID 27907978 .
- ^ Fioretti FM, Сита-Лумсден A, Беван CL, Brooke GN (июнь 2014). «Пересмотр роли рецептора андрогена в раке груди» . J. Mol. Эндокринол . 52 (3): R257–65. DOI : 10.1530 / JME-14-0030 . PMID 24740738 .
- ^ Gucalp A, Traina TA (2016). «Ориентация на рецепторы андрогенов при тройном отрицательном раке груди» . Curr Probl Cancer . 40 (2–4): 141–150. DOI : 10.1016 / j.currproblcancer.2016.09.004 . PMC 5580391 . PMID 27816190 .
- Перейти ↑ Arce-Salinas C, Riesco-Martinez MC, Hanna W, Bedard P, Warner E (февраль 2016 г.). «Полный ответ метастатического рака молочной железы с положительным рецептором андрогенов на бикалутамид: отчет о болезни и обзор литературы». J. Clin. Онкол . 34 (4): e21–4. DOI : 10.1200 / JCO.2013.49.8899 . PMID 24888812 .
- ^ Héquet D, Mzoughi S, R Rouzier, Гуччионе Е (апрель 2017 г.). «[Рецепторы андрогенов при раке груди: выражение, значение и терапевтические перспективы]». Бычий рак (на французском языке). 104 (4): 363–369. DOI : 10.1016 / j.bulcan.2017.01.005 . PMID 28216075 .
- ^ Gerratana L, Basile D, Buono G, De Placido S, Giuliano M, Minichillo S, Coinu A, Martorana F, De Santo I, Del Mastro L, De Laurentiis M, Puglisi F, Arpino G (июнь 2018). «Рецептор андрогенов при тройном отрицательном раке груди: потенциальная мишень для бесцельного подтипа» . Лечение рака. Ред . 68 : 102–110. DOI : 10.1016 / j.ctrv.2018.06.005 . PMID 29940524 .
- ^ Nomani H, Mohammadpour AH, Moallem SM, YazdanAbad MJ, Barreto GE, Sahebkar A (декабрь 2019 г.). «Антиандрогенные препараты в лечении обсессивно-компульсивного расстройства: систематический обзор». Curr Med Chem . 27 (40): 6825–6836. DOI : 10.2174 / 0929867326666191209142209 . PMID 31814547 .
Дальнейшее чтение [ править ]
- Neumann, F .; Стейнбек, Х. (1974). «Антиандрогены». Андрогены II и антиандрогены / Андрогены II и антиандрогены . С. 235–484. DOI : 10.1007 / 978-3-642-80859-3_6 . ISBN 978-3-642-80861-6.
- Gräf, K.-J .; Brotherton, J .; Нойман, Ф. (1974). «Клиническое использование антиандрогенов». Андрогены II и антиандрогены / Андрогены II и антиандрогены . С. 485–542. DOI : 10.1007 / 978-3-642-80859-3_7 . ISBN 978-3-642-80861-6.