 | |
| Клинические данные | |
|---|---|
| Код УВД | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard | 100.051.864 |
| Химические и физические данные | |
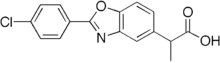
| Формула | C 16 H 12 Cl N O 3 |
| Молярная масса | 301,73 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| | |
Беноксапрофен , также известный как Беноксафен, представляет собой химическое соединение с формулой C 16 H 12 ClNO 3 . Это нестероидный противовоспалительный препарат (НПВП), который продавался под торговой маркой Oraflex в США и как Opren в Европе компанией Eli Lilly and Company . Lilly приостановила продажи Oraflex в 1982 году после сообщений от британского правительства и Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) о побочных эффектах и смертях, связанных с этим препаратом.
История [ править ]
Беноксапрофен был открыт группой химиков Lilly в ее британской лаборатории. Этой лаборатории было поручено исследовать новые антиартритные соединения в 1966 году. Лилли подала заявку на получение патента на беноксапрофен семь лет спустя, а также подала заявку на разрешение от FDA на начало испытаний препарата на людях. Он должен был пройти трехступенчатую процедуру клинического тестирования, требуемую федеральным правительством. [1]
Лилли начала Фазу I своего прогресса с тестирования нескольких здоровых добровольцев. Эти тесты должны были доказать, что препарат не представляет явной и непосредственной угрозы безопасности. На этапе II было протестировано большее количество людей, в том числе с незначительными заболеваниями. Главной целью этих испытаний была эффективность и безопасность препарата. Фаза III была крупнейшим испытанием и началась в 1976 году. Более чем 2 000 пациентов с артритом вводили препарат более чем 100 врачами. Врачи сообщили о результатах в компанию Lilly. [1]
Когда в январе 1980 года компания официально потребовала начать продажу препарата вместе с Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, документ содержал более 100 000 страниц с результатами тестов и записями пациентов. Беноксапрофен впервые был продан за границу: в 1980 году препарат был выпущен для продажи в Великобритании. Он появился на рынке в мае 1982 года в США. [2]
Когда беноксапрофен появился на рынке в США под названием Oraflex, компания Lilly Company впервые столкнулась с проблемой. British Medical Journal сообщила в мае 1982 года , что врачи в Великобритании полагают , что препарат был ответственен , по крайней мере , 12 человек, в основном , вызванных почечной и печеночной недостаточности. Было подано ходатайство об изъятии Oraflex с рынка. [1]
Четвертого августа 1982 года британское правительство временно приостановило продажу препарата в Великобритании «по соображениям безопасности». Британский комитет по безопасности лекарственных средств заявил в телеграмме в FDA, что он получил сообщения о более чем 3500 побочных эффектах у пациентов, которые использовали Oraflex. Также погиб 61 человек, в основном пожилые люди. Почти одновременно FDA сообщило, что у него есть сообщения об 11 случаях смерти в США среди пользователей Oraflex, большинство из которых были вызваны повреждением почек и печени. [1]
В тот же день компания Eli Lilly приостановила продажу беноксапрофена. [1]
Структура и реакционная способность [ править ]
Молекулярная формула беноксапрофена - C 16 H 12 ClNO 3, а систематическое (IUPAC) название - 2- [2- (4-хлорфенил) -1,3-бензоксазол-5-ил] пропионовая кислота. Молекула имеет молекулярную массу 301,050568 г / моль. [3]
Беноксапрофен - это, по сути, плоская молекула. Это происходит из-за копланарности бензоксазольного и фенильного колец, но молекула также имеет неплоскую боковую цепь, состоящую из фрагмента пропановой кислоты, который действует как группа-носитель. Эти данные были получены на основе рентгеновских кристаллографических измерений, проведенных в Исследовательском центре Лилли. [4]
Беноксапрофен очень фототоксичен. Свободнорадикальное декарбоксилированное производное лекарственного средства является токсичным агентом, который в присутствии кислорода дает синглетный кислород и супероксианион. Облучение беноксапрофена в водном растворе вызывает фотохимическое декарбоксилирование по радикальному механизму и в одноцепочечных разрывах ДНК. То же самое происходит с кетопрофеном и напроксеном, другими НПВП, которые в этом отношении даже более активны, чем беноксапрофен. [4]
Доступные формы [ править ]
Беноксапрофен представляет собой рацемическую смесь [(RS) -2- (п-хлорфенил-a-метил-5-бензоксазолуксусная кислота]. Двумя энантиомерами являются R (-) и S (+). [5]
Инверсия конъюгации R (-) энантиомера и глюкуронида будет метаболизировать беноксапрофен. Однако беноксапрофен не подвергается окислительному метаболизму. [4]
Однако возможно, что, когда цитохром P4501 является катализатором, происходит оксигенация 4-хлорофильного кольца. С энантиомером S (+) более вероятно, что происходит оксигенация ароматического кольца фрагмента 2-фенилпропионовой кислоты, здесь также используется цитохром P4501 в качестве катализатора. [4]
Токсикокинетика [ править ]
Беноксапрофен хорошо всасывается после приема внутрь в дозах от 1 до 10 мг / кг. В плазме обнаруживается только неизмененный препарат, в основном связанный с белками плазмы. [6] Уровни беноксапрофена в плазме у одиннадцати субъектов были точно предсказаны на основе двухкамерной открытой модели. Средний период полувыведения абсорбции составил 0,4 часа. Это означает, что в течение 25 минут половина дозы всасывается в организме. Средний период полувыведения составил 4,8 часа. Это означает, что в течение 5 часов половина дозы распределяется по всей системе. Средний период полувыведения составил 37,8 часа. Это означает, что в течение 40 часов половина дозы выводится из системы. [6]
У самок крыс после пероральной дозы 20 мг / кг концентрация беноксапрофена в тканях была самой высокой в печени, почках, легких, надпочечниках и яичниках. Распределение у беременных женщин такое же, хотя в более низких концентрациях он также может быть обнаружен у плода. Между видами существует большая разница в способах выведения из организма. У человека, макаки-резуса и кролика он в основном выводится с мочой, в то время как у крыс и собак он выводится через желчно-фекальную экскрецию. У человека и собаки соединение выделялось в виде глюкуронида сложного эфира, а у других видов - в неизмененном виде. Это означает, что не происходит серьезного метаболического превращения беноксапрофена. [7]
Токсикодинамика [ править ]
В отличие от других НПВП, беноксапрофен действует непосредственно на мононуклеарные клетки. Он подавляет их хемотаксический ответ путем ингибирования фермента липоксигеназы . [8]
Эффективность и побочные эффекты [ править ]
Эффективность [ править ]
Беноксапрофен - обезболивающее , жаропонижающее и противовоспалительное средство. [9] Беноксапрофен давали пациентам с ревматоидным артритом и остеоартритом из-за его противовоспалительного действия. Беноксапрофен также получали пациенты с болезнью Педжета , псориатическим артритом , анкилозирующим спондилитом , болезненным плечом, смешанным заболеванием соединительной ткани, ревматической полимиалгией , болями в спине и болезнью Бехчета. Для многих пациентов эффективна суточная доза 300–600 мг. [10]
Побочные эффекты [ править ]
Есть разные типы побочных эффектов. Большинство из них были кожными или желудочно-кишечными. Побочные эффекты со стороны центральной нервной системы проявляются редко, а различные побочные эффекты наблюдаются нечасто. Исследование показывает, что большинство побочных эффектов проявляется у пациентов с ревматоидным артритом [10]
Кожные побочные эффекты [ править ]
Кожные побочные эффекты беноксапрофена включают светочувствительность , онихолизис , сыпь , милиумы , усиление роста ногтей, зуд (зуд) и гипертрихоз . [10] Фоточувствительность приводит к жжению, зуду или покраснению, когда пациенты подвергаются воздействию солнечного света. [11] Исследование показывает, что беноксапрофен или другие агенты, ингибирующие липоксигеназу, могут быть полезны при лечении псориаза из-за подавления миграции воспалительных клеток ( лейкоцитов ) в кожу. [12]
Побочные эффекты со стороны желудочно-кишечного тракта [ править ]
Побочные эффекты беноксапрофена со стороны желудочно-кишечного тракта включают кровотечение, диарею, боль в животе, анорексию (симптом) , язвы во рту и изменение вкуса. [10] [13] Согласно исследованию, наиболее частыми побочными эффектами со стороны желудка являются рвота, изжога и боль в эпигастрии. [10]
Побочные эффекты в центральной нервной системе [ править ]
У небольшого числа людей прием беноксапрофена может вызвать депрессию, летаргию и плохое самочувствие. [10]
Разные побочные эффекты [ править ]
Обморок, головокружение, головная боль, сердцебиение , носовые кровотечения , помутнение зрения, позывы к мочеиспусканию и гинекомастия редко возникают у пациентов, принимающих беноксапрофен. [10] Беноксапрофен также вызывает гепатотоксичность , что привело к смерти некоторых пожилых пациентов. [14] [15] Это была основная причина, по которой препарат был изъят с рынка.
Токсичность [ править ]
После прекращения продаж в 1982 году токсические эффекты, которые беноксапрофен мог оказывать на людей, были изучены более тщательно. Довольно плоское соединение беноксапрофена, по-видимому, гепа- и фототоксично для человеческого организма. [4]
Беноксапрофен имеет довольно длительный период полураспада у человека (t 1/2 = 20-30 ч), подвергается желчному выздоровлению и энтерогепатической циркуляции, а также, как известно, имеет медленный плазменный клиренс (CL p = 4,5 мл / мин). Период полувыведения может быть увеличен у пожилых пациентов (> 80 лет) и у пациентов, у которых уже есть почечная недостаточность, возрастающая до 148 часов. [4]
Гепатотоксичность беноксапрофена для плода может быть связана с накоплением препарата после многократного приема, а также связана с медленным плазменным клиренсом. Накопление препарата в печени, по-видимому, является причиной повышения активности печеночного цитохрома P450I, который насыщает кислородом бенаксопрофен и продуцирует реактивные промежуточные соединения. Беноксапрофен, скорее всего, является субстратом и слабым индуктором цитохрома P450I и его семейства ферментов. Обычно он не метаболизируется посредством окислительных реакций, но с S (+) энантиомером беноксапрофена и цитохрома P450I в качестве катализатора кажется возможным оксигенация 4-хлорфенильного кольца и ароматического кольца 2-фенилпропионовой кислоты. Следовательно, индукция второстепенного метаболического пути приводит к образованию значительных количеств токсичных метаболитов.Токсичные метаболиты могут связываться с жизненно важными внутриклеточными макромолекулами и могут генерировать реактивные атомы кислорода за счет окислительно-восстановительного цикла, если образуется хинон.[4] Это также может привести к истощению защитного глутатиона, который отвечает за детоксикацию реактивных атомов кислорода. [16]
Наблюдаемую фототоксичность кожи пациентов, получавших беноксапрофен, можно объяснить, взглянув на структуру соединения. Существует значительное структурное сходство между бензоксазольным кольцом беноксапрофена и бензафурановым кольцом псоралена, соединения, которое, как известно, является фототоксичным. Свободное декарбоксилированное производное лекарственного средства может продуцировать синглетный кислород и супероксианионы в присутствии кислорода. Кроме того, возможными объяснениями фотохимического декарбоксилирования и образования кислородных радикалов могут быть накопление повторяющихся доз, индукция цитохрома P450I и появление реакционноспособных промежуточных продуктов с ковалентным связыванием. Фотохимический характер соединения может вызвать воспаление и серьезное повреждение тканей. [4]
У животных также наблюдается пролиферация пероксисом, но, по-видимому, у человека она незначительна. [4]
Воздействие на животных [ править ]
Эффекты Беноксапрофена на животных проверяли в серии экспериментов. [7] [17] Беноксапрофен обладал значительной противовоспалительной, обезболивающей и жаропонижающей активностью в этих тестах. [7] У всех шести испытанных животных, включая крыс, собак, макак-резусов, кроликов, морских свинок и мышей, препарат хорошо всасывался при пероральном приеме. У трех из шести видов беноксапрофен затем эффективно выводился из желудочно-кишечного тракта (после пероральных доз 1–10 мг / кг). [7]Было обнаружено, что период полужизни в плазме был разным: у собак, кроликов и обезьян он составлял менее 13 часов, а у мышей он был значительно больше. Кроме того, были обнаружены видовые различия в скорости и пути выведения соединения. В то время как беноксапрофен выводился с мочой кроликами и морскими свинками, выведение с желчью было способом выведения, обнаруженным у крыс и собак. У всех видов в плазме был обнаружен только неизмененный беноксапрофен, в основном связанный с белками. [7]
Выведение неизмененного соединения с желчью у крыс действительно происходило медленнее. Авторы интерпретируют это как доказательство отсутствия энтерогепатической циркуляции. [7] Другое исследование на крысах показало, что плазматическая мембрана гепатоцитов начала образовывать пузырьки после введения беноксапрофена. Предполагается, что это связано с нарушениями концентрации кальция, которые, возможно, являются результатом измененного окислительно-восстановительного состояния клеток, которое может влиять на функцию митохондрий и, следовательно, вызывать нарушения концентрации кальция. [17]Ни у одного из видов не было обнаружено значительных уровней метаболизма беноксапрофена. Только у собак глюкуронид может быть обнаружен в желчи, что является верным признаком метаболизма у этого вида. Также не было обнаружено различий в распределении соединения у нормальных и беременных крыс. На крысах было показано, что беноксапрофен распределялся внутри плода, но в значительно более низкой концентрации, чем в материнской ткани. [7]
Синтез [ править ]
Реакция зандмейера путем диазотирования 2- (4-аминофенил) пропаннитрил ( 1 ) с последующим кислотным гидролизом приводит к фенолу ( 2 ), который подвергается нитрования и сокращение , чтобы дать аминофенол ( 3 ). Гидролиз нитрила и этерификация дает сложный эфир 4 , который превращается в беноксапрофен ( 5 ) ацилированием п- хлорбензоилхлоридом с последующей циклизацией и затем омылением этилового эфира.
Ссылки [ править ]
- ^ Б с д е Lueck TJ (15 августа 1982). «В Lilly побочные эффекты Oraflex» . Нью-Йорк Таймс .
- ^ Грэхем R (ноябрь 1982). «Взлет и падение Беноксапрофена». Ревматология и реабилитация . XXI (4).
- ^ "Беноксапрофен" . ChemSpider .
- ^ a b c d e f g h i j Льюис Д. Ф., Иоаннидес К., Парк Д. В. (декабрь 1990 г.). «Ретроспективное исследование молекулярной токсикологии беноксапрофена». Токсикология . 65 (1–2): 33–47. DOI : 10.1016 / 0300-483x (90) 90077-т . PMID 2274968 .
- ^ Боппа RJ, Nash JF, Ridolfo А.С., Shepard ER (1979). «Стереоселективная инверсия (R) - (-) - беноксапрофена в (S) - (+) - энантиомер у человека». Метаболизм и утилизация лекарств: биологическая судьба химических веществ . 7 (6): 356–9. PMID 43219 .
- ^ Чатфилд DH, Таррант ME, Smith GL, Speirs CF (октябрь 1977). «Фармакокинетические исследования с беноксапрофеном на человеке: прогнозирование стабильных уровней на основе данных однократной дозы» . Британский журнал клинической фармакологии . 4 (5): 579–83. DOI : 10.1111 / j.1365-2125.1977.tb00789.x . PMC 1429156 . PMID 303114 .
- ^ a b c d e f g Chatfield DH, Green JN (март 1978 г.). «Распределение и метаболизм беноксапрофена у лабораторных животных и человека». Xenobiotica; Судьба чужеродных соединений в биологических системах . 8 (3): 133–44. DOI : 10.3109 / 00498257809060392 . PMID 418580 .
- ^ "Беноксапрофен" . Британский медицинский журнал (под ред. Клинических исследований). 285 (6340): 459–460. 14 августа 1982 г. DOI : 10.1136 / bmj.285.6340.459 . PMC 1499290 . PMID 6809122 .
- Перейти ↑ Dahl SL, Ward JR (1982). «Фармакология, клиническая эффективность и побочные эффекты нестероидного противовоспалительного агента беноксапрофена». Фармакотерапия . 2 (6): 354–66. DOI : 10.1002 / j.1875-9114.1982.tb03212.x . PMID 6762531 .
- ^ a b c d e f g Хэлси Дж. П., Кардо Н. (май 1982 г.). «Беноксапрофен: профиль побочных эффектов у 300 пациентов» . Британский медицинский журнал (под ред. Клинических исследований). 284 (6326): 1365–8. DOI : 10.1136 / bmj.284.6326.1365 . PMC 1498268 . PMID 6803978 .
- ^ Хиндсон С, Даймонд Т, Diffey В, Р Лолор (май 1982 г.). «Побочные эффекты беноксапрофена» . Британский медицинский журнал (под ред. Клинических исследований). 284 (6326): 1368–9. DOI : 10.1136 / bmj.284.6326.1368 . PMC 1498237 . PMID 6803979 .
- ↑ Аллен Б. Р., Литтлвуд С. М. (октябрь 1982 г.). «Беноксапрофен: влияние на кожные поражения при псориазе» . Британский медицинский журнал (под ред. Клинических исследований). 285 (6350): 1241. DOI : 10.1136 / bmj.285.6350.1241 . PMC 1499777 . PMID 6812822 .
- ↑ Somerville KW, Hawkey CJ (январь 1986). «Нестероидные противовоспалительные средства и желудочно-кишечный тракт» . Последипломный медицинский журнал . 62 (723): 23–8. DOI : 10.1136 / pgmj.62.723.23 . PMC 2418576 . PMID 3540919 .
- ^ Doube A (июль 1990). «Гепатит и нестероидные противовоспалительные средства» . Анналы ревматических болезней . 49 (7): 489–90. DOI : 10.1136 / ard.49.7.489 . PMC 1004125 . PMID 2200358 .
- ^ Таггарт HM, Alderdice JM (май 1982 г.). «Смертельная холестатическая желтуха у пожилых пациентов, принимающих беноксапрофен» . Британский медицинский журнал (под ред. Клинических исследований). 284 (6326): 1372. DOI : 10.1136 / bmj.284.6326.1372 . PMC 1498289 . PMID 6462187 .
- ↑ Ayrton AD, Ioannides C, Parke DV (июнь 1991 г.). «Индукция семейств цитохрома P450 I и IV и пролиферация пероксисом в печени крыс, получавших беноксапрофен. Возможные последствия его гепатотоксичности». Биохимическая фармакология . 42 (1): 109–15. DOI : 10.1016 / 0006-2952 (91) 90688-2 . PMID 2069584 .
- ^ a b Knights KM, Кэссиди MR, Дрю Р. (сентябрь 1986 г.). «Беноксапрофен вызвал токсичность в изолированных гепатоцитах крысы». Токсикология . 40 (3): 327–39. DOI : 10.1016 / 0300-483x (86) 90064-8 . PMID 3750332 .
- ^ Dunwell DW, Evans D, Хикс TA (январь 1975). «Производные 2-арил-5-бензоксазолеалкановой кислоты с заметной противовоспалительной активностью». Журнал медицинской химии . 18 (1): 53–8. DOI : 10.1021 / jm00235a012 . PMID 1109576 .