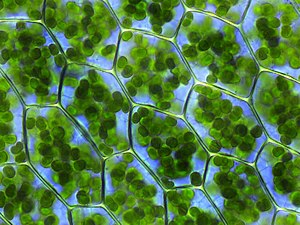
Хлорофилл (также хлорофилл ) является одной из нескольких смежных зеленых пигментов найдены в мезозе из цианобактерий и в хлоропластах из водорослей и растений . [2] Его название происходит от греческих слов χλωρός , khloros («бледно-зеленый») и φύλλον , phyllon («лист»). [3] Хлорофилл необходим для фотосинтеза , позволяя растениям поглощать энергию света.
Хлорофилл поглощает свет наиболее сильно в синей части от электромагнитного спектра , а также красной части. [4] И наоборот, он плохо поглощает зеленую и почти зеленую части спектра. Следовательно, ткани, содержащие хлорофилл, кажутся зелеными, потому что зеленый свет, диффузно отражаемый такими структурами, как клеточные стенки, меньше поглощается. [1] В фотосистемах зеленых растений существуют два типа хлорофилла: хлорофилл a и b . [5]
История
Хлорофилл был впервые выделен и назван Джозефом Бьенэме Кавенту и Пьером Жозефом Пеллетье в 1817 году. [6] Присутствие магния в хлорофилле было обнаружено в 1906 году [7] и было первым обнаружением этого элемента в живой ткани. [8]
После первоначальной работы, проделанной немецким химиком Ричардом Вильштеттером, охватывающей период с 1905 по 1915 годы, общая структура хлорофилла а была выяснена Гансом Фишером в 1940 году. К 1960 году, когда была известна большая часть стереохимии хлорофилла а , Роберт Бернс Вудворд опубликовал полный синтез молекулы. [8] [9] В 1967 году, последний оставшийся стереохимическая выяснение была завершена Яна Флеминга , [10] , а в 1990 Woodward и соавторами опубликовал обновленный синтез. [11] Было объявлено, что хлорофилл f присутствует в цианобактериях.и другие кислородные микроорганизмы, образующие строматолиты в 2010 г .; [12] [13] молекулярная формула C 55 H 70 O 6 N 4 Mg и структура (2- формил ) -хлорофилла а были выведены на основе ЯМР, оптических и масс-спектров. [14]
Фотосинтез
Хлорофилл жизненно важен для фотосинтеза , который позволяет растениям поглощать энергию света . [15]
Молекулы хлорофилла расположены внутри и вокруг фотосистем , которые встроены в тилакоидные мембраны хлоропластов . [16] В этих комплексах хлорофилл выполняет три функции. Функция подавляющего большинства хлорофилла (до нескольких сотен молекул на фотосистему) заключается в поглощении света. Сделав это, эти же центры выполняют свою вторую функцию: передачу этой световой энергии посредством резонансной передачи энергии определенной паре хлорофилла в реакционном центре фотосистем. Эта пара выполняет конечную функцию хлорофиллов, разделение зарядов, что приводит к биосинтезу. Два принятых в настоящее время блока фотосистемы - это фотосистема IIи фотосистема I , у которых есть свои собственные отдельные реакционные центры, названные P680 и P700 соответственно. Эти центры названы в честь длины волны (в нанометрах ) их максимума поглощения красного пика. Идентичность, функции и спектральные свойства типов хлорофилла в каждой фотосистеме различны и определяются друг другом и окружающей их белковой структурой. После извлечения из белка в растворитель (например, ацетон или метанол ) [17] [18] [19] эти пигменты хлорофилла могут быть разделены на хлорофилл а и хлорофилл b .
Функция реакционного центра хлорофилла - поглощать световую энергию и передавать ее другим частям фотосистемы. Поглощенная энергия фотона передается электрону в процессе, называемом разделением зарядов. Удаление электрона из хлорофилла - это реакция окисления. Хлорофилл отдает электрон высокой энергии ряду молекулярных промежуточных продуктов, называемых цепью переноса электронов . Заряженный реакционный центр хлорофилла (P680 + ) затем восстанавливается до своего основного состояния, принимая электрон, оторванный от воды. Электрон, который восстанавливает P680 +, в конечном итоге возникает в результате окисления воды до O 2 и H +.через несколько промежуточных звеньев. Эта реакция - это то, как фотосинтезирующие организмы, такие как растения, производят газ O 2 , и является источником практически всего O 2 в атмосфере Земли. Фотосистема I обычно работает последовательно с Фотосистемой II; таким образом, P700 + Фотосистемы I обычно уменьшается, поскольку она принимает электрон через многие промежуточные соединения в тилакоидной мембране, электронами, поступающими, в конечном счете, из Фотосистемы II. Однако реакции переноса электронов в тилакоидных мембранах сложны, и источники электронов, используемые для восстановления P700 +, могут варьироваться.
Электронный поток, производимый пигментами хлорофилла реакционного центра, используется для прокачки ионов H + через тилакоидную мембрану, устанавливая хемиосмотический потенциал, используемый в основном для производства АТФ (запасенной химической энергии) или для восстановления НАДФ + до НАДФН . НАДФН - универсальный агент, используемый для восстановления CO 2 до сахаров, а также для других биосинтетических реакций.
Хлорофилл-белковые комплексы реакционного центра способны непосредственно поглощать свет и выполнять процессы разделения зарядов без помощи других пигментов хлорофилла, но вероятность того, что это происходит при данной интенсивности света, мала. Таким образом, все другие хлорофиллы в фотосистеме и белки антенного пигмента совместно поглощают световую энергию и направляют ее в реакционный центр. Помимо хлорофилла а , в этих антенных комплексах пигмент-белок присутствуют и другие пигменты, называемые дополнительными пигментами .
Химическая структура
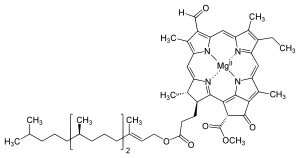
Хлорофиллы многочисленны по типам, но все они определяются наличием пятого кольца за четырьмя пирролоподобными кольцами. Большинство хлорофиллов классифицируются как хлорины , которые являются восстановленными родственниками порфиринов (обнаруженных в гемоглобине ). Они разделяют общий путь биосинтеза с порфиринами, включая предшественник уропорфириноген III . В отличие от гемов, у которых железо находится в центре тетрапиррольного кольца, хлорофиллы связывают магний . Для структур, изображенных в этой статье, некоторые лиганды, присоединенные к центру Mg 2+ , опущены для ясности. Хлориновое кольцо может иметь различные боковые цепи, обычно в том числе длинные.фитоловая цепь. Наиболее распространенной формой у наземных растений является хлорофилл а .
Структуры хлорофиллов кратко описаны ниже: [20] [14]
| Хлорофилл а | Хлорофилл b | Хлорофилл c1 | Хлорофилл c2 | Хлорофилл d | Хлорофилл f [14] | |
|---|---|---|---|---|---|---|
| Молекулярная формула | C 55 H 72 O 5 N 4 мг | C 55 H 70 O 6 N 4 мг | C 35 H 30 O 5 N 4 мг | C 35 H 28 O 5 N 4 мг | C 54 H 70 O 6 N 4 мг | C 55 H 70 O 6 N 4 мг |
| Группа C2 | −CH 3 | −CH 3 | −CH 3 | −CH 3 | −CH 3 | −CHO |
| Группа C3 | -CH = CH 2 | -CH = CH 2 | -CH = CH 2 | -CH = CH 2 | −CHO | -CH = CH 2 |
| Группа C7 | −CH 3 | −CHO | −CH 3 | −CH 3 | −CH 3 | −CH 3 |
| Группа C8 | −CH 2 CH 3 | −CH 2 CH 3 | −CH 2 CH 3 | -CH = CH 2 | −CH 2 CH 3 | −CH 2 CH 3 |
| Группа C17 | −CH 2 CH 2 COO − Phytyl | −CH 2 CH 2 COO − Phytyl | -CH = CHCOOH | -CH = CHCOOH | −CH 2 CH 2 COO − Phytyl | −CH 2 CH 2 COO − Phytyl |
| Связка C17-C18 | Одиночный (хлорин) | Одиночный (хлорин) | Двойной (порфирин) | Двойной (порфирин) | Одиночный (хлорин) | Одиночный (хлорин) |
| Вхождение | Универсальный | В основном растения | Различные водоросли | Различные водоросли | Цианобактерии | Цианобактерии |
- Структуры хлорофиллов
хлорофилл а
хлорофилл b
хлорофилл c1
хлорофилл c2
хлорофилл d
хлорофилл f
Измерение содержания хлорофилла
Измерение поглощения света [ как? ] осложняется растворителем, используемым для извлечения хлорофилла из растительного материала, что влияет на полученные значения,
- В диэтиловом эфире хлорофилл a имеет приблизительные максимумы поглощения 430 нм и 662 нм, а хлорофилл b имеет приблизительные максимумы 453 нм и 642 нм. [21]
- Пики поглощения хлорофилла а находятся при 465 нм и 665 нм. Хлорофилл а флуоресцирует при 673 нм (максимум) и 726 нм. Пик молярного коэффициента поглощения хлорофилла а превышает 10 5 М -1 см -1 , что является одним из самых высоких значений для низкомолекулярных органических соединений. [22]
- В смеси 90% ацетон-вода максимальные длины волн поглощения хлорофилла а составляют 430 нм и 664 нм; пики для хлорофилла b составляют 460 нм и 647 нм; пики для хлорофилла c 1 составляют 442 нм и 630 нм; пики для хлорофилла с 2 составляют 444 нм и 630 нм; пики для хлорофилла d составляют 401 нм, 455 нм и 696 нм. [23]
Измеряя поглощение света в красной и дальней красной областях, можно оценить концентрацию хлорофилла в листе. [24]
Коэффициент флуоресцентного излучения можно использовать для измерения содержания хлорофилла. За счет возбуждения флуоресценции хлорофилла а на более низкой длине волны отношение испускания флуоресценции хлорофилла при705 ± 10 нм и735 ± 10 нм может обеспечить линейную зависимость содержания хлорофилла по сравнению с химическим тестированием. Отношение F 735 / F 700 обеспечило значение корреляции r 2 0,96 по сравнению с химическим тестированием в диапазоне от 41 мг м -2 до 675 мг м -2 . Гительсон также разработал формулу для прямого считывания содержания хлорофилла в мг м -2 . Формула обеспечивает надежный метод измерения содержания хлорофилла от 41 мг / м 2 до 675 мг / м 2 со значением корреляции r 2 0,95. [25]
Биосинтез
В некоторых растениях хлорофилл происходит из глутамата и синтезируется по разветвленному биосинтетическому пути, который является общим с гемом и сирохемом . [26] [27] [28] Хлорофиллсинтаза [29] - это фермент, который завершает биосинтез хлорофилла а [30] [31] , катализируя реакцию EC 2.5.1.62
- хлорофиллид а + фитилдифосфат хлорофилл а + дифосфат
Это образует сложный эфир группы карбоновой кислоты в хлорофиллиде а с фитолом дитерпенового спирта с 20 атомами углерода . Хлорофилл b производится тем же ферментом, который действует на хлорофиллид b .
У покрытосеменных растений более поздние стадии биосинтетического пути зависят от света, и такие растения бледны ( этиолированы ), если выращиваются в темноте. [ необходима цитата ] Несосудистые растения и зеленые водоросли обладают дополнительным светонезависимым ферментом и становятся зелеными даже в темноте. [ необходима цитата ]
Сам хлорофилл связан с белками и может передавать поглощенную энергию в нужном направлении. Протохлорофиллид , один из промежуточных продуктов биосинтеза, встречается в основном в свободной форме и в условиях освещения действует как фотосенсибилизатор , образуя высокотоксичные свободные радикалы . Следовательно, растениям необходим эффективный механизм регулирования количества этого предшественника хлорофилла. У покрытосеменных это происходит на стадии аминолевулиновой кислоты (ALA), одного из промежуточных соединений в пути биосинтеза. Растения, которые питаются ALA, накапливают высокие и токсичные уровни протохлорофиллида; то же самое делают мутанты с поврежденной регуляторной системой. [32]
Старение и цикл хлорофилла
Процесс старения растений включает деградацию хлорофилла: например, фермент хлорофиллаза ( EC 3.1.1.14 ) гидролизует фитильную боковую цепь, чтобы обратить вспять реакцию, в которой хлорофиллы биосинтезируются из хлорофиллида a или b . Поскольку хлорофиллид a может быть преобразован в хлорофиллид b, а последний может быть повторно этерифицирован до хлорофилла b , эти процессы позволяют циклически переключаться между хлорофиллами a и b . Более того, хлорофилл b может быть восстановлен напрямую (через 7 1-гидроксихлорофилл а ) обратно в хлорофилл а , завершая цикл. [33] [34] На более поздних стадиях старения хлорофиллиды превращаются в группу бесцветных тетрапирролов, известных как нефлуоресцентные катаболиты хлорофилла (NCC) с общей структурой:
Эти соединения также были идентифицированы в созревания плодов , и они дают характерные цвета осени в лиственные растения. [34] [35]
Дефектная среда может вызвать хлороз
Хлороз - это состояние, при котором листья вырабатывают недостаточно хлорофилла, что приводит к их желтому. Хлороз может быть вызван дефицитом железа в питательных веществах, называемым хлорозом железа, или недостатком магния или азота . PH почвы иногда играет роль в хлорозе, вызванном питательными веществами; многие растения приспособлены к росту в почвах с определенным уровнем pH, и от этого может зависеть их способность поглощать питательные вещества из почвы. [36] Хлороз также может быть вызван патогенами, включая вирусы, бактерии и грибковые инфекции, или насекомыми, сосущими сок. [ необходима цитата ]
Дополнительное светопоглощение антоцианов
Антоцианы - другие пигменты растений . Характер поглощения, ответственный за красный цвет антоцианов, может быть дополнительным к таковому у зеленого хлорофилла в фотосинтетически активных тканях, таких как молодые листья Quercus coccifera . Он может защитить листья от нападения пожирателей растений, которых может привлечь зеленый цвет. [37]
Распределение
Карты хлорофилла показывают миллиграммы хлорофилла на кубический метр морской воды каждый месяц. Места, где количество хлорофилла было очень низким, что указывает на очень низкую численность фитопланктона , окрашены в синий цвет. Места, где концентрация хлорофилла была высокой, что означает рост многих фитопланктона, окрашены в желтый цвет. Наблюдения производятся спектрорадиометром среднего разрешения (MODIS) на спутнике НАСА Aqua. Земля темно-серая, а места, где MODIS не мог собрать данные из-за морского льда, полярной темноты или облаков, светло-серые. Самая высокая концентрация хлорофилла там, где процветают крошечные обитающие на поверхности океанские растения, находятся в холодных полярных водах или в местах, где океанские течения выносят холодную воду на поверхность, например, вокруг экватора и вдоль берегов континентов. Фитопланктон стимулируется не самой холодной водой. Вместо этого низкие температуры часто являются признаком того, что вода поднялась на поверхность из глубин океана, неся питательные вещества, накопившиеся с течением времени. В полярных водах питательные вещества накапливаются в поверхностных водах в темные зимние месяцы, когда растения не могут расти. Когда весной и летом возвращается солнечный свет, растения цветут в высокой концентрации. [38]
Кулинарное использование
Синтетический хлорофилл зарегистрирован как краситель для пищевых добавок, и его номер E составляет E140 . Повара используют хлорофилл для окрашивания в зеленый цвет различных продуктов и напитков, например пасты и спиртных напитков. Абсент приобретает свой зеленый цвет естественным образом за счет хлорофилла, который вводится через большое количество трав, используемых при его производстве. [39] Хлорофилл не растворяется в воде, и его сначала смешивают с небольшим количеством растительного масла, чтобы получить желаемый раствор . [ необходима цитата ]
Биологическое использование
Исследование 2002 года показало, что «листья, подвергшиеся воздействию сильного света, содержат разрушенные основные антенные белки , в отличие от тех, которые хранятся в темноте, что согласуется с исследованиями освещения изолированных белков ». Это показалось авторам подтверждением гипотезы о том, что « активные формы кислорода играют роль in vivo » в краткосрочном поведении растений. [40]
Смотрите также
| Викискладе есть медиафайлы по теме хлорофилла . |
- Бактериохлорофилл , родственные соединения фототрофных бактерий
- Хлорофиллин , полусинтетическое производное хлорофилла
- Максимум глубокого хлорофилла
- Расти свет , лампа, которая способствует фотосинтезу
- Флуоресценция хлорофилла для измерения стресса растений
Рекомендации
- ^ а б Виртанен, Олли; Константиниду, Эмануэлла; Tyystjärvi, Esa (2020). «Хлорофилл не отражает зеленый свет - как исправить заблуждение» . Журнал биологического образования : 1–8. DOI : 10.1080 / 00219266.2020.1858930 .
- ^ Мэй П. «Хлорофилл» . Бристольский университет .
- ^ «хлорофилл» . Интернет-словарь этимологии .
- ^ Muneer S, Ким Е.Ю., Парк JS, Lee JH (март 2014). «Влияние зеленых, красных и синих светодиодов на белки мультибелкового комплекса и фотосинтетическую активность при различной интенсивности света в листьях салата (Lactuca sativa L.)» . Международный журнал молекулярных наук . 15 (3): 4657–70. DOI : 10.3390 / ijms15034657 . PMC 3975419 . PMID 24642884 .
- ^ Шпеер BR (1997). «Фотосинтетические пигменты» . Глоссарий UCMP (онлайн) . Музей палеонтологии Калифорнийского университета . Проверено 17 июля 2010 .
- ^ См .:
- Делепин М (сентябрь 1951 г.). «Джозеф Пеллетье и Джозеф Кавенту». Журнал химического образования . 28 (9): 454. Bibcode : 1951JChEd..28..454D . DOI : 10.1021 / ed028p454 .
- Пеллетье и Кавенту (1817) «Notice sur la matière verte des feuilles» (Уведомление о зеленом материале в листьях), Journal de Pharmacie , 3 : 486-491. На стр. 490 авторы предлагают новое название хлорофиллу. С п. 490: "Nous n'avons aucun droit pour nommer une entity connue depuis long temps, et à l'histoire de laquelle nous n'avons ajouté que quelques faits; cependant nous proposerons, sans y mettre aucune value, le nom de chlorophyle , de chloros , couleur, et φυλλον , feuille: ce nom indiquerait le role qu'elle joue dans la nature ". (Мы не имеем права называть вещество, [которое] было известно давно и к истории которого мы добавили лишь несколько фактов; однако мы предлагаем, не придавая этому значения, название хлорофилл , от слова chloros , цвет и φυλλον , лист: это имя указывает на роль, которую он играет в природе.)
- ^ Вильштеттер R (1906). "Zur Kenntniss der Zusammensetzung des Chlorophylls" [Вклад в изучение состава хлорофилла]. Annalen der Chemie (на немецком языке). 350 (1–2): 48–82. DOI : 10.1002 / jlac.19063500103 .
С п. 49:
«Das Hauptproduct der alkalischen Hydrolyse bilden tiefgrüne Alkalisalze. In ihnen liegen complexe Magnesiumverbindungen vor, die das Metall in einer gegen Alkali auch bei hoher Temperatur merkwürdig widestandsfähigen Bindung.
(Глубокие зеленые щелочные соли образуют основной продукт щелочного гидролиза. В них присутствуют сложные соединения магния, которые содержат металл в связи, чрезвычайно устойчивой к щелочам даже при высокой температуре.)
- ^ а б Мотильва М (2008). «Хлорофиллы - от функциональности в продуктах питания до актуальности для здоровья». 5-й конгресс «Пигменты в продуктах питания» - за качество и здоровье (Печать). Университет Хельсинки. ISBN 978-952-10-4846-3.
- ^ Woodward RB, Ayer WA, Beaton JM, Bickelhaupt F, Bonnett R, Buchschacher P и др. (Июль 1960 г.). «Полный синтез хлорофилла» (PDF) . Журнал Американского химического общества . 82 (14): 3800–3802. DOI : 10.1021 / ja01499a093 .
- ↑ Флеминг I (14 октября 1967 г.). «Абсолютная конфигурация и структура хлорофилла». Природа . 216 (5111): 151–152. Bibcode : 1967Natur.216..151F . DOI : 10.1038 / 216151a0 . S2CID 4262313 .
- ^ Woodward RB, Ayer WA, Beaton JM, Bickelhaupt F, Bonnett R, Buchschacher P и др. (1990). «Полный синтез хлорофилла а». Тетраэдр . 46 (22): 7599–7659. DOI : 10.1016 / 0040-4020 (90) 80003-Z .
- ^ Джабер F (август 2010). "Новая форма хлорофилла?" . Scientific American .
- ^ Инфракрасный хлорофилл может стимулировать солнечные батареи . Новый ученый. 19 августа, 2010. Проверено 15 апреля 2012 г.
- ^ a b c Чен М., Шлип М., Уиллоуз Р.Д., Цай З.Л., Нейлан Б.А., Шеер Х. (сентябрь 2010 г.). «Хлорофилл с красным смещением». Наука . 329 (5997): 1318–9. Bibcode : 2010Sci ... 329.1318C . DOI : 10.1126 / science.1191127 . PMID 20724585 . S2CID 206527174 .
- ^ Картер Дж. С. (1996). «Фотосинтез» . Университет Цинциннати . Архивировано из оригинала на 2013-06-29.
- ^ Природа (5 июля 2013 г.). «Блок 1.3. Фотосинтетические клетки» . Основы клеточной биологии . nature.com.
- ^ Маркер AF (1972). «Использование ацетона и метанола в оценке хлорофилла в присутствии феофитина в растениях». Пресноводная биология . 2 (4): 361–385. DOI : 10.1111 / j.1365-2427.1972.tb00377.x .
- ^ Джеффри SW, Шибата (февраль 1969). «Некоторые спектральные характеристики хлорофилла c из Tridacna crocea Zooxanthellae». Биологический бюллетень . 136 (1): 54–62. DOI : 10.2307 / 1539668 . JSTOR 1539668 .
- ^ Гилпин L (21 марта 2001). «Методы анализа придонного фотосинтетического пигмента» . Школа наук о жизни, Университет Напьера . Архивировано из оригинального 14 апреля 2008 года . Проверено 17 июля 2010 .
- Перейти ↑ Scheer H (2006). «Обзор хлорофиллов и бактериохлорофиллов: биохимия, биофизика, функции и приложения». Хлорофиллы и бактериохлорофиллы . Достижения в фотосинтезе и дыхании. 25 . С. 1–26. DOI : 10.1007 / 1-4020-4516-6_1 . ISBN 978-1-4020-4515-8.
- Перейти ↑ Gross J (1991). Пигменты в овощах: хлорофиллы и каротиноиды . Ван Ностранд Рейнхольд. ISBN 978-0442006570.
- ^ Porra RJ, Thompson WA, Kriedemann PE (1989). «Определение точных коэффициентов экстинкции и одновременных уравнений для анализа хлорофиллов a и b, экстрагированных четырьмя различными растворителями: проверка концентрации стандартов хлорофилла с помощью атомно-абсорбционной спектроскопии». Biochimica et Biophysica Acta (BBA) - Биоэнергетика . 975 (3): 384–394. DOI : 10.1016 / S0005-2728 (89) 80347-0 .
- ^ Larkum AW, Douglas S, Raven JA, ред. (2003). Фотосинтез в водорослях . Лондон: Клувер. ISBN 978-0-7923-6333-0.
- Перейти ↑ Cate TM, Perkins TD (октябрь 2003 г.). «Мониторинг содержания хлорофилла в клене сахарном (Acer saccharum)» . Физиология деревьев . 23 (15): 1077–9. DOI : 10.1093 / treephys / 23.15.1077 . PMID 12975132 .
- ^ Gitelson AA, Buschmann C, Lichtenthaler HK (1999). "Коэффициент флуоресценции хлорофилла F 735 / F 700 как точный показатель содержания хлорофилла в растениях". Remote Sens. Enviro . 69 (3): 296–302. Bibcode : 1999RSEnv..69..296G . DOI : 10.1016 / S0034-4257 (99) 00023-1 .
- ^ Battersby AR (декабрь 2000). «Тетрапирролы: пигменты жизни». Отчеты о натуральных продуктах . 17 (6): 507–26. DOI : 10.1039 / B002635M . PMID 11152419 .
- Перейти ↑ Akhtar M (2007). «Модификация ацетатных и пропионатных боковых цепей во время биосинтеза гема и хлорофиллов: механистические и стереохимические исследования». Ciba Foundation Symposium 180 - Биосинтез тетрапиррольных пигментов . Симпозиумы Фонда Новартис. 180 . С. 131–155. DOI : 10.1002 / 9780470514535.ch8 . ISBN 9780470514535. PMID 7842850 .
- ^ Willows RD (июнь 2003 г.). «Биосинтез хлорофиллов из протопорфирина IX». Отчеты о натуральных продуктах . 20 (3): 327–41. DOI : 10.1039 / B110549N . PMID 12828371 .
- ↑ Schmid HC, Rassadina V, Oster U, Schoch S, Rüdiger W (ноябрь 2002 г.). «Предварительная загрузка хлорофиллсинтазы тетрапренилдифосфатом является обязательной стадией биосинтеза хлорофилла» (PDF) . Биологическая химия . 383 (11): 1769–78. DOI : 10.1515 / BC.2002.198 . PMID 12530542 . S2CID 3099209 .
- ^ Экхардт U, Гримм B, Hörtensteiner S (сентябрь 2004). «Последние достижения в биосинтезе и распаде хлорофилла у высших растений». Молекулярная биология растений . 56 (1): 1–14. DOI : 10.1007 / s11103-004-2331-3 . PMID 15604725 . S2CID 21174896 .
- ^ Bollivar DW (ноябрь 2006). «Последние достижения в биосинтезе хлорофилла». Фотосинтез Исследования . 90 (2): 173–94. DOI : 10.1007 / s11120-006-9076-6 . PMID 17370354 . S2CID 23808539 .
- ^ Meskauskiene R, Натер M, гусята D, F Kessler, оп ден Кэмп R, Апель K (октябрь 2001). «Грипп: негативный регулятор биосинтеза хлорофилла у Arabidopsis thaliana» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (22): 12826–31. Bibcode : 2001PNAS ... 9812826M . DOI : 10.1073 / pnas.221252798 . JSTOR 3056990 . PMC 60138 . PMID 11606728 .
- ^ «Цикл хлорофилла» . IUBMB. 2011 . Проверено 4 июня 2020 .
- ^ а б Hörtensteiner S (2006). «Деградация хлорофилла при старении». Ежегодный обзор биологии растений . 57 : 55–77. DOI : 10.1146 / annurev.arplant.57.032905.105212 . PMID 16669755 .
- Перейти ↑ Müller T, Ulrich M, Ongania KH, Kräutler B (2007). «Бесцветные тетрапиррольные катаболиты хлорофилла, обнаруженные в созревающих фруктах, являются эффективными антиоксидантами» . Angewandte Chemie . 46 (45): 8699–702. DOI : 10.1002 / anie.200703587 . PMC 2912502 . PMID 17943948 .
- ^ Duble RL. «Железный хлороз в дерновине» . Техасский университет A&M . Проверено 17 июля 2010 .
- ↑ Karageorgou P, Manetas Y (май 2006 г.). «Важность красного цвета в молодости: антоцианы и защита молодых листьев Quercus coccifera от травоядных насекомых и избытка света» . Физиология деревьев . 26 (5): 613–21. DOI : 10.1093 / treephys / 26.5.613 . PMID 16452075 .
- ^ Хлорофилл: Глобальные карты . Earthobservatory.nasa.gov. Проверено 2 февраля 2014.
- Перейти ↑ Adams J (2004). Ужасный абсент: история дьявола в бутылке . Соединенное Королевство: IBTauris, 2004. стр. 22. ISBN 978-1860649202.
- ^ Zolla L, Rinalducci S (декабрь 2002). «Вовлечение активных форм кислорода в деградацию светособирающих белков при легком стрессе». Биохимия . 41 (48): 14391–402. DOI : 10.1021 / bi0265776 . PMID 12450406 .