 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC 2-гидрокси- N , N , N- триметилэтан-1-аминий | |
| Другие имена 2-гидрокси- N , N , N- триметилэтанаминий, билинейрин (2-гидроксиэтил) триметиламмоний | |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| 1736748 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.487 |
| Номер ЕС |
|
| 324597 | |
| КЕГГ | |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| C 5 H 14 NO + | |
| Молярная масса | 104,17 г / моль |
| Внешность | вязкая расплывающаяся жидкость (гидроксид холина) [1] |
| очень растворим (гидроксид холина) [1] | |
| Растворимость | растворим в этаноле , [1] нерастворим в диэтиловом эфире и хлороформе (гидроксид холина) [2] |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Опасность |
Формулировки опасности GHS | H314 |
Меры предосторожности GHS | Р260 , Р264 , Р280 , Р301 + 330 + 331 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , P310 , P321 , P363 , P405 , P501 |
| NFPA 704 (огненный алмаз) |  COR |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 3–6 г / кг массы тела , крысы, перорально [1] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
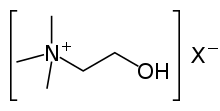
Холин / к ə ʊ л я п / [3] является условно важным питательным веществом для человека и многих других животных. [4] Холин присутствует в виде катиона, который образует различные соли (X - в изображенной формуле - неопределенный контрранион ). [5] Для поддержания здоровья его необходимо получать с пищей в виде холина или фосфолипидов холина , таких как фосфатидилхолин . [4] Люди и большинство животных вырабатывают холин de novo., но продукция у людей и большинства видов недостаточна. Холин часто классифицируют не как витамин , а как питательное вещество с метаболизмом, подобным аминокислотам . [2] У большинства животных холинфосфолипиды являются необходимыми компонентами клеточных мембран , мембран клеточных органелл и липопротеинов очень низкой плотности . [4] Холин необходим для производства ацетилхолина - нейромедиатора - и S- аденозилметионина , универсального донора метила, участвующего в синтезе гомоцистеина .[4]
Симптоматический дефицит холина, редко встречающийся у людей, вызывает неалкогольную жировую болезнь печени и повреждение мышц. [4] Чрезмерное потребление холина (более 7,5 г / день) может вызвать снижение артериального давления , потоотделение , диарею и запах тела, напоминающий рыбу, из-за триметиламина , который образуется в его метаболизме. [4] [6] Богатые диетические источники холина и холинфосфолипидов включают мясные субпродукты и яичные желтки , молочные продукты и овощи . [4]
Химия [ править ]
Холин - это семейство водорастворимых соединений четвертичного аммония . [5] холин гидроксид известен как холин основание. Он гигроскопичен и поэтому часто встречается в виде бесцветного вязкого гидратированного сиропа с запахом триметиламина (ТМА). Водные растворы холина стабильны, но соединение медленно распадается на этиленгликоль , полиэтиленгликоли и ТМА. [1]
Хлорид холина можно получить обработкой ТМА 2-хлорэтанолом : [1]
- (CH 3 ) 3 N + ClCH 2 CH 2 OH → (CH 3 ) 3 N + CH 2 CH 2 OH · Cl -
2-хлорэтанол может быть получен из окиси этилена . Холин исторически был произведен из природных источников, такие , как с помощью гидролиза из лецитина . [1]
Метаболизм [ править ]
Биосинтез [ править ]
В растениях, первый шаг в De Novo биосинтеза холина является декарбоксилированием из серина в этаноламин , который катализируемой серин декарбоксилазой . [7] Синтез холина из этаноламина может иметь место в трех параллельных путей, где три последовательных N -methylation стадии , катализируемой с помощью метил - трансферазы проводятся либо на свободное основание, [8] фосфо-основы, [9] или фосфатидил-основания. [10] Источником метильной группы является S- аденозил- L- метионин иS- аденозил- L- гомоцистеин образуется как побочный продукт. [11]
У людей и большинства других животных синтез холина de novo осуществляется по пути фосфатидилэтаноламин-N-метилтрансферазы (PEMT) [6], но биосинтеза недостаточно для удовлетворения потребностей человека. [12] При печеночном пути PEMT 3-фосфоглицерат (3PG) получает 2 ацильные группы от ацил-КоА, образуя фосфатидную кислоту . Он реагирует с цитидинтрифосфатом с образованием цитидиндифосфата-диацилглицерина. Его гидроксильная группа реагирует с серином с образованием фосфатидилсерина, который декарбоксилируется доформы этаноламина и фосфатидилэтаноламина (ПЭ). PEMT фермент перемещает три метильные группы из трех S -adenosyl метионинов (SAM) доноров к этаноламину группе фосфатидилэтаноламина с образованием холина в виде фосфатидилхолина. Три S- аденозилгомоцистеина (SAH) образуются как побочный продукт. [6]
Холин также может высвобождаться из более сложных молекул, содержащих холин. Например, фосфатидилхолины (PC) могут быть гидролизованы до холина (Chol) в большинстве типов клеток. Холин также может вырабатываться по пути ЦДФ-холин, цитозольные холинкиназы (СК) фосфорилируют холин с АТФ до фосфохолина (PChol). [2] Это происходит в некоторых типах клеток, таких как печень и почки. Холин-фосфатцитидилилтрансферазы (CPCT) превращают PChol в CDP-холин (CDP-Chol) с помощью цитидинтрифосфата (CTP). ЦДФ-холин и диглицерид трансформируются в ПК диацилглицеринхолинфосфотрансферазой (СРТ).[6]
У людей определенные мутации PEMT-фермента и дефицит эстрогена (часто из-за менопаузы ) увеличивают потребность в холине с пищей. У грызунов 70% фосфатидилхолинов образуются через путь PEMT и только 30% через путь CDP-холин. [6] У мышей с нокаутом инактивация PEMT делает их полностью зависимыми от пищевого холина. [2]
Поглощение [ править ]
У человека холин всасывается из кишечника через мембранный белок SLC44A1 (CTL1) посредством облегченной диффузии, регулируемой градиентом концентрации холина и электрическим потенциалом через мембраны энтероцитов . SLC44A1 имеет ограниченную способность транспортировать холин: при высоких концентрациях часть его остается неабсорбированной. Абсорбированный холин покидает энтероциты через воротную вену , проходит через печень и попадает в системный кровоток . Микробы кишечника разлагают неабсорбированный холин до триметиламина , который окисляется в печени до N- оксида триметиламина .[6]
Фосфохолин и глицерофосфохолины гидролизуются с помощью фосфолипаз до холина, который попадает в воротную вену. Из-за их водорастворимости некоторые из них в неизменном виде попадают в воротную вену. Жирорастворимые холиносодержащие соединения ( фосфатидилхолины и сфингомиелины ) либо гидролизуются фосфолипазами, либо попадают в лимфу, включенную в хиломикроны . [6]
Транспорт [ править ]
У людей холин переносится в крови в виде свободной молекулы. Холинсодержащие фосфолипиды и другие вещества, такие как глицерофосфохолины, переносятся липопротеинами крови . Уровни холина в плазме крови здоровых взрослых натощак составляют 7–20 микромоль на литр (мкмоль / л) и в среднем 10 мкмоль / л. Уровни регулируются, но потребление и дефицит холина изменяют эти уровни. Уровни повышаются примерно через 3 часа после приема холина. Уровень фосфатидилхолина в плазме взрослых натощак составляет 1,5–2,5 ммоль / л. Его потребление повышает уровень свободного холина примерно на 8–12 часов, но не оказывает значительного влияния на уровень фосфатидилхолина. [6]
Холин представляет собой водорастворимый ион и, следовательно, требует, чтобы переносчики проходили через жирорастворимые клеточные мембраны . Известны три типа переносчиков холина: [13]
- SLC5A7
- CTL: CTL1 ( SLC44A1 ), CTL2 ( SLC44A2 ) и CTL4 ( SLC44A4 )
- OCT: OCT1 ( SLC22A1 ) и OCT2 ( SLC22A2 )
SLC5A7 являются натрий- (Na + ) и АТФ- зависимыми переносчиками. [13] [6] Они обладают высокой аффинностью связывания с холином, транспортируют его в первую очередь к нейронам и косвенно связаны с производством ацетилхолина . [6] Их недостаточная функция вызывает у людей наследственную слабость в легочных и других мышцах из-за дефицита ацетилхолина. У мышей с нокаутом их дисфункция легко приводит к смерти от цианоза и паралича . [14]
CTL1 обладают умеренным сродством к холину и транспортируют его почти во все ткани, включая кишечник, печень, почки, плаценту и митохондрии . CTL1 поставляют холин для производства фосфатидилхолина и триметилглицина . [6] CTL2 встречаются особенно в митохондриях языка, почек, мышц и сердца. Они связаны с митохондриальным окислением холина до триметилглицина. CTL1 и CTL2 не связаны с производством ацетилхолина, но вместе транспортируют холин через гематоэнцефалический барьер.. На мозговой стороне барьера встречаются только CTL2. Они также удаляют избыток холина из нейронов обратно в кровь. CTL1 встречаются только на кровяной стороне барьера, но также на мембранах астроцитов и нейронов. [13]
OCT1 и OCT2 не связаны с производством ацетилхолина. [6] Они транспортируют холин с низким сродством. OCT1 транспортируют холин в основном в печень и почки; OCT2 в почках и головном мозге. [13]
Хранилище [ править ]
Холин хранится в клеточных мембранах и органеллах в виде фосфолипидов и внутри клеток в виде фосфатидилхолинов и глицерофосфохолинов . [6]
Экскреция [ править ]
Даже при дозах холина 2–8 г у человека с мочой выводится небольшое количество холина. Выведение происходит через транспортеры, которые происходят в почках (см. Транспорт ). Триметилглицин деметилируется в печени и почках до диметилглицина ( тетрагидрофолат получает одну из метильных групп). Формируется метилглицин , выводится с мочой или деметилируется до глицина . [6]
Функция [ править ]
Холин и его производные выполняют множество функций у людей и других организмов. Наиболее примечательной функцией является то, что холин служит синтетическим предшественником для других важных компонентов клетки и сигнальных молекул, таких как фосфолипиды, которые образуют клеточные мембраны, нейротрансмиттер ацетилхолин и осморегулятор триметилглицин ( бетаин ). Триметилглицин, в свою очередь, служит источником метильных групп , участвуя в биосинтезе S- аденозилметионина . [15] [16]
Предшественник фосфолипидов [ править ]
Холин превращается в различные фосфолипиды , такие как фосфатидилхолины и сфингомиелины . Они обнаружены во всех клеточных мембранах и в мембранах большинства клеточных органелл . [2] Фосфатидилхолины являются структурно важной частью клеточных мембран. У людей 40–50% фосфолипидов составляют фосфатидилхолины. [6]
Фосфолипиды холина также образуют липидные рафты в клеточных мембранах вместе с холестерином . Плоты являются центрами, например, для рецепторов и ферментов, передающих рецепторный сигнал . [2]
Фосфатидилхолины необходимы для синтеза ЛОНП : 70-95% их фосфолипидов фосфатидилхолины в организме человека. [6]
Холин также необходим для синтеза легочного сурфактанта , который представляет собой смесь, состоящую в основном из фосфатидилхолинов. Сурфактант отвечает за эластичность легких, то есть за способность ткани легких сокращаться и расширяться. Например, дефицит фосфатидилхолинов в тканях легких связан с острым респираторным дистресс-синдромом . [17]
Фосфатидилхолины выводятся с желчью и работают вместе с солями желчных кислот в качестве поверхностно-активных веществ в ней, тем самым способствуя всасыванию липидов в кишечнике . [2]
Синтез ацетилхолина [ править ]
Холин необходим для производства ацетилхолина . Это нейротрансмиттер, который, например, играет важную роль в сокращении мышц , памяти и нервном развитии . [6] Тем не менее, в организме человека мало ацетилхолина по сравнению с другими формами холина. [2] Нейроны также хранят холин в форме фосфолипидов на своих клеточных мембранах для производства ацетилхолина. [6]
Источник триметилглицина [ править ]
В организме человека холин окисляются необратима в митохондриях печени до глицинбетаина альдегида с холином оксидазами . Он окисляется митохондриальными или цитозольными бетаин-альдегиддегидрогеназами до триметилглицина . [6] Триметилглицин является необходимым осморегулятором . Он также работает как субстрат для BHMT- фермента, который метилирует гомоцистеин до метионина . Это предшественник S- аденозилметионина (SAM). SAM - обычный реагент в реакциях биологического метилирования . Например, он метилирует гуанидины.из ДНК и некоторых лизинов из гистонов . Таким образом, это часть экспрессии генов и эпигенетической регуляции . Таким образом, дефицит холина приводит к повышению уровня гомоцистеина и снижению уровня SAM в крови. [6]
Содержание в продуктах [ править ]
Холин содержится в пищевых продуктах в виде свободной молекулы и в форме фосфолипидов , особенно в виде фосфатидилхолинов . Больше всего холина содержится в мясных субстратах и яичных желтках, но в меньшей степени он содержится в мясе , не содержащем органических веществ , зерновых , овощах , фруктах и молочных продуктах . Кулинарные масла и другие пищевые жиры содержат около 5 мг / 100 г общего холина. [6] В Соединенных Штатах , пищевые этикетки выразить количество холина в порции в процентах от дневной нормы (DV%) на основеадекватное потребление 550 мг / день. 100% дневной нормы означает, что порция пищи содержит 550 мг холина. [18]
Грудное молоко человека богато холином. Исключительное грудное вскармливание соответствует примерно 120 мг холина в день для ребенка. Увеличение потребления холина матерью повышает содержание холина в грудном молоке, а низкое потребление снижает его. [6] Детские смеси могут содержать или не содержать достаточное количество холина. В ЕС и США в каждую детскую смесь обязательно добавлять не менее 7 мг холина на 100 килокалорий (ккал). В ЕС запрещены уровни выше 50 мг / 100 ккал. [6] [19]
Триметилглицин - функциональный метаболит холина. Он питательно заменяет холин, но только частично. [2] Высокое количество триметилглицина содержится, например, в пшеничных отрубях (1339 мг / 100 г), поджаренных зародышах пшеницы (1240 мг / 100 г) и шпинате (600–645 мг / 100 г). [20]
Содержание холина в продуктах питания (мг / 100 г) [a] [20] Мясо Овощи Бекон , приготовленный 124,89 Фасоль, оснастка 13,46 Говядина нарезанная, приготовленная 78,15 Свекла 6.01 Печень говяжья, обжаренная на сковороде 418,22 Брокколи 40,06 Цыпленок , жареный, с кожей 65,83 брюссельская капуста 40,61 Курица, жареная, без кожи 78,74 Капуста 15.45 Куриная печень 290,03 Морковь 8,79 Треска, атлантика 83,63 Цветная капуста 39,10 Говяжий фарш , 75–85% постный, жареный 79,32–82,35 Кукуруза , желтый 21,95 Свиная корейка приготовленная 102,76 Огурец 5,95 Креветки консервированные 70,60 Салат-латук , айсберг 6,70 Молочные продукты (корова) Салат-латук, ромэн 9,92 Сливочное масло соленое 18,77 Горох 27,51 Сыр 16,50–27,21 Квашеная капуста 10,39 Творог 18,42 Шпинат 22.08 Молоко цельное / обезжиренное 14.29–16.40 Сладкий картофель 13.11 Сметана 20,33 Помидор 6,74 Йогурт , простой 15.20 Цуккини 9,36 Зерна Фрукты Овсяные отруби сырые 58,57 яблоко 3,44 Овес , простой 7,42 Авокадо 14,18 Рис белый 2,08 Банан 9,76 Рис, коричневый 9,22 Черника 6,04 Пшеничные отруби 74,39 Мускусная дыня 7,58 Ростки пшеницы , поджаренные 152,08 Виноград 7,53 Другие Грейпфрут 5,63 Фасоль, темно-синий 26,93 апельсин 8,38 Яйцо, курица 251,00 Персик 6.10 Оливковое масло 0,29 Груша 5.11 Арахис 52,47 Чернослив 9,66 Соя , сырая 115,87 клубника 5,65 Тофу мягкий 27,37 Арбуз 4,07
- ^ Еда сырая, если не указано иное. Содержание представляет собой приблизительное количество свободного холина и холина, содержащего фосфолипиды.
Дневные значения [ править ]
В следующей таблице приведены обновленные источники холина, отражающие новую дневную норму и новые этикетки с фактами о питании и добавками. [18] Он отражает данные Службы сельскохозяйственных исследований Министерства сельского хозяйства США. FoodData Central, 2019. [18]
Избранные пищевые источники холина [18] Еда Миллиграммы (мг) на порцию Процент DV * Печень говяжья, обжаренная на сковороде, 85 г (3 унции) 356 65 Яйцо, сваренное вкрутую, 1 большое яйцо 147 27 Говяжий верх круглый , только разделимое постное мясо, тушеный, 3 унции (85 г) 117 21 год Соевые бобы , жареная, 1 / 2 чашки 107 19 Куриная грудка, жареная, 85 г (3 унции) 72 13 Говядина, фарш, 93% нежирного мяса, жареная, 3 унции (85 г) 72 13 Треска, атлантическая , приготовленная, сухой жар, 3 унции (85 г) 71 13 Грибы, шиитаке , вареные, 1 / 2 чашки штук 58 11 Картофель, красный , запеченный, мякоть и кожа, 1 большая картофелина 57 10 Ростки пшеницы , поджаренные, 1 унция (28 г) 51 9 Фасоль, почки , консервы, +1 / +2 чашки 45 8 Киноа , приготовленная, 1 стакан 43 8 Молоко , 1% жирности, 1 стакан 43 8 Йогурт , ваниль, обезжиренный, 1 стакан 38 7 Брюссельская капуста , вареная, 1 / 2 чашки 32 6 Брокколи , рубленые, вареные, осушенных, 1 / 2 чашки 31 год 6 Творог , обезжиренный, 1 стакан 26 5 Тунец , белый, консервированный в воде, сушеный, 3 унции (85 г) 25 5 Арахис , сухой жареный, 1 / 4 чашки 24 4 Цветная капуста , 1 в (2,5 см) куски, вареный, сушеный, 1 / 2 чашки 24 4 Горох, зеленый , вареные, 1 / 2 чашки 24 4 Семена подсолнечника , масло жареное, 1 / +4 чашки 19 3 Рис, коричневый , длиннозерный, вареный, 1 стакан 19 3 Хлеб, питы , из цельной пшеницы, 1 большой ( 6 1 / 2 или диаметром 17 см) 17 3 Капуста , вареные, 1 / 2 чашки 15 3 Tangerine ( мандарин ), секция, 1 / 2 чашки 10 2 Фасоль, оснастка , сырье, 1 / +2 чашки 8 1 Киви , сырье, 1 / 2 чашки нарезанного 7 1 Морковь , сырая, нарезанная, 1 / 2 чашки 6 1 Яблоки , сырье, с кожей, четвертинки или нарезанных, 1 / 2 чашки 2 0
DV = дневная стоимость. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) разработало DV, чтобы помочь потребителям сравнивать содержание питательных веществ в пищевых продуктах и пищевых добавках в контексте общей диеты. ДВ холина составляет 550 мг для взрослых и детей в возрасте от 4 лет и старше. [ необходима цитата ] FDA не требует, чтобы на этикетках пищевых продуктов было указано содержание холина, если холин не был добавлен в пищу. Продукты, обеспечивающие 20% или более DV, считаются богатыми источниками питательных веществ, но продукты, обеспечивающие более низкий процент DV, также вносят свой вклад в здоровое питание. [18]
В FoodData Central Министерства сельского хозяйства США (USDA) перечислено содержание питательных веществ во многих продуктах питания и представлен полный список продуктов, содержащих холин, с разбивкой по содержанию питательных веществ. [18]
Диетические рекомендации [ править ]
Рекомендации даны в миллиграммах в день (мг / день). В Европейский орган по безопасности пищевых продуктов рекомендации (EFSA) общие рекомендации для стран ЕС . EFSA не установило никаких верхних пределов потребления. [6] У отдельных стран ЕС могут быть более конкретные рекомендации. Национальная академия медицины (NAM) рекомендации применяются в Соединенных Штатах , [18] Австралия и Новая Зеландия . [21]
Рекомендации по холину (мг / день) Возраст Адекватное потребление EFSA [6] Адекватное потребление NAM США [18] Допустимые верхние уровни потребления в ДН США [18] Младенцы и дети 0–6 месяцев Не установлено 125 Не установлено 7–12 месяцев 160 150 Не установлено 1–3 года 140 200 1,000 4–6 лет 170 250 1,000 7–8 лет 250 250 1,000 9–10 лет 250 375 1,000 11–13 лет 340 375 2 000 Самцы 14 лет 340 550 3 000 15–18 лет 400 550 3 000 19+ лет 400 550 3500 Самки 14 лет 340 400 3 000 15–18 лет 400 400 3 000 19+ лет 400 425 3500 Если беременна 480 450 3500 (3000, если ≤18 лет) При грудном вскармливании 520 550 3500 (3000, если ≤18 лет)
Потребление населения [ править ]
Двенадцать исследований, проведенных в 9 странах ЕС в период с 2000 по 2011 год, оценили потребление холина взрослыми в этих странах на уровне 269–468 миллиграммов в день. Потребление составляло 269–444 мг / день для взрослых женщин и 332–468 мг / день для взрослых мужчин. Потребление составляло 75–127 мг / день для младенцев, 151–210 мг / день для детей от 1 до 3 лет, 177–304 мг / день для детей от 3 до 10 лет и 244–373 мг / день для детей. Дети от 10 до 18 лет. Средняя оценка общего потребления холина составляла 336 мг / день для беременных подростков и 356 мг / день для беременных женщин. [6]
Исследование, основанное на опросе NHANES 2009–2012, показало, что потребление холина в некоторых субпопуляциях США является слишком низким . Потребление было 315,2–318,8 мг / сут у детей в возрасте от 2 лет в этот период времени. Из детей 2+ лет только15,6 ± 0,8 % мужчин и6,1 ± 0,6 % женщин превышали допустимую норму потребления (AI). ИИ был превышен62,9 ± 3,1 % детей в возрасте от 2 до 3 лет,45,4 ± 1,6 % детей от 4 до 8 лет,9,0 ± 1,0 % детей от 9 до 13 лет,1,8 ± 0,4 % среди 14–18 и6,6 ± 0,5 % от 19 лет. Ни в одной из подгрупп не превышен верхний уровень потребления. [22]
Исследование NHANES, проведенное среди населения США в 2013–2014 гг., Показало, что потребление холина в возрасте от 2 до 19 лет составляет 256 ± 3,8 мг / сут и339 ± 3,9 мг / сут у взрослых от 20 лет и старше. Прием был402 ± 6,1 мг / сут у мужчин 20 лет и старше и 278 мг / сут у женщин 20 лет и старше. [23]
Дефицит [ править ]
Признаки и симптомы [ править ]
Симптоматический дефицит холина у людей встречается редко. Большинство из них получают его в достаточном количестве с пищей и способны биосинтезировать ограниченное количество. [2] Симптоматическая недостаточность часто вызывается определенными заболеваниями или другими косвенными причинами. Тяжелый дефицит вызывает повреждение мышц и неалкогольную жировую болезнь печени , которая может перерасти в цирроз . [24]
Помимо людей, жирная печень также является типичным признаком дефицита холина у других животных. У некоторых видов также может наблюдаться кровотечение из почек. Предполагается, что это связано с дефицитом триметилглицина , производного от холина , который действует как осморегулятор . [2]
Причины и механизмы [ править ]
Производство эстрогена является важным фактором, который предрасполагает людей к дефициту наряду с низким потреблением холина с пищей. Эстрогены активируют ферменты PEMT, продуцирующие фосфатидилхолин . У женщин до менопаузы потребность в холине ниже, чем у мужчин, из-за более высокой выработки эстрогена у женщин. Без терапии эстрогенами потребности женщин в постменопаузе в холине аналогичны потребностям мужчин. Также важны некоторые однонуклеотидные полиморфизмы (генетические факторы), влияющие на метаболизм холина и фолиевой кислоты. Некоторые кишечные микробы также расщепляют холин более эффективно, чем другие, поэтому они также важны. [24]
При дефиците снижается доступность фосфатидилхолинов в печени - они необходимы для образования ЛПОНП . Таким образом, опосредованный VLDL транспорт жирных кислот из печени снижается, что приводит к накоплению жира в печени. [6] Также были предложены другие одновременно возникающие механизмы, объясняющие наблюдаемое повреждение печени. Например, фосфолипиды холина также необходимы в митохондриальных мембранах. Их недоступность приводит к неспособности митохондриальных мембран поддерживать правильный электрохимический градиент , который, среди прочего, необходим для разложения жирных кислот посредством β-окисления . Следовательно, метаболизм жиров в печени снижается.[24]
Избыточное потребление [ править ]
Чрезмерные дозы холина могут иметь побочные эффекты. Например, было обнаружено, что ежедневные дозы холина 8–20 г вызывают низкое кровяное давление , тошноту , диарею и запах тела, напоминающий запах рыбы . Запах возникает из-за триметиламина (ТМА), который образуется микробами кишечника из неабсорбированного холина (см. Триметиламинурия ). [6]
Печень окисляет ТМА до N- оксида триметиламина (ТМАО). Повышенные уровни ТМА и ТМАО в организме связаны с повышенным риском атеросклероза и смертности. Таким образом, предполагается, что чрезмерное потребление холина увеличивает эти риски в дополнение к карнитину , который также образует ТМА и ТМАО. Тем не менее, потребление холина не увеличивает риск смерти от сердечно-сосудистых заболеваний . [25]Вполне вероятно, что повышенные уровни ТМА и ТМАО являются лишь симптомом других основных заболеваний или генетических факторов, которые предрасполагают людей к повышенной смертности. Такие факторы, возможно, не были должным образом учтены в некоторых исследованиях смертности, связанной с уровнями ТМА и ТМАО. Причинно-следственная связь может быть обратной или смешанной, а потребление большого количества холина может не увеличивать смертность людей. Например, дисфункция почек предрасполагает к сердечно-сосудистым заболеваниям , но также может снижать экскрецию ТМА и ТМАО. [26]
Воздействие на здоровье [ править ]
Закрытие нервной трубки [ править ]
Некоторые исследования на людях показали, что низкое потребление холина матерью значительно увеличивает риск дефектов нервной трубки (ДНТ) у новорожденных. [4] Дефицит фолиевой кислоты также вызывает NTD. Холин и фолат, взаимодействуя с витамином B 12 , действуют как доноры метила для гомоцистеина с образованием метионина , который затем может переходить к образованию SAM ( S- аденозилметионин ). [4] SAM является субстратом почти для всех реакций метилирования у млекопитающих. Было высказано предположение, что нарушенное метилирование посредством SAM может быть ответственным за связь между фолатом и NTD. [27] Это также может относиться к холину. [необходимая цитата ]Определенныемутации, нарушающие метаболизм холина, увеличивают распространенность NTD у новорожденных, но роль дефицита холина в пище остается неясной по состоянию на 2015 г.[4][Обновить]
Сердечно-сосудистые заболевания и рак [ править ]
Дефицит холина может вызвать ожирение печени , что увеличивает риск рака и сердечно-сосудистых заболеваний . Дефицит холина также снижает выработку SAM, которая участвует в метилировании ДНК - это снижение также может способствовать канцерогенезу . Таким образом, был изучен дефицит и его связь с такими заболеваниями. [6] Однако обсервационные исследования свободных популяций не показали убедительно связи между низким потреблением холина и сердечно-сосудистыми заболеваниями или большинством видов рака. [4] [6] Исследования рака простаты противоречивы. [28] [29]
Познание [ править ]
Исследования, наблюдающие за эффектом между повышенным потреблением холина и познавательной способностью , были проведены у взрослых людей с противоречивыми результатами. [4] [30] Подобные исследования на людях младенцев и детей были противоречивыми и также ограниченными. [4]
Перинатальное развитие [ править ]
Этот раздел требует дополнительных ссылок для проверки . ( Декабрь 2016 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
Как беременность, так и лактация резко увеличивают потребность в холине. Эта потребность может быть удовлетворена за счет активации PEMT за счет увеличения уровня эстрогена для выработки большего количества холина de novo , но даже при повышенной активности PEMT потребность в холине все еще настолько высока, что запасы холина в организме обычно истощаются. Примером этого является наблюдение, что мыши Pemt - / - (мыши с отсутствием функциональной PEMT) прерывают беременность через 9-10 дней, если не получают дополнительный холин. [31]
В то время как материнские запасы холина истощаются во время беременности и кормления грудью, плацента накапливает холин, перекачивая холин против градиента концентрации в ткань, где он затем сохраняется в различных формах, в основном в виде ацетилхолина . Концентрация холина в околоплодных водах может быть в десять раз выше, чем в крови матери. [31]
Функции у плода [ править ]
Холин пользуется большим спросом во время беременности в качестве субстрата для построения клеточных мембран (быстрое разрастание тканей плода и матери), повышенной потребности в одноуглеродных фрагментах (субстрат для метилирования ДНК и других функций), увеличения запасов холина в тканях плода и плаценты. , а также для увеличения производства липопротеинов (белков, содержащих «жировые» части). [32] [33] [34] В частности, есть интерес к влиянию потребления холина на мозг. Это связано с использованием холина в качестве материала для изготовления клеточных мембран (особенно при производстве фосфатидилхолина ). Рост человеческого мозга наиболее быстрый в третьем триместре.беременности и продолжает быть быстрым примерно до пяти лет. [35] В это время высок спрос на сфингомиелин , который производится из фосфатидилхолина (и, следовательно, из холина), потому что этот материал используется для миелинизации (изоляции) нервных волокон . [36] Холин также необходим для производства нейромедиатора ацетилхолина , который может влиять на структуру и организацию областей мозга, нейрогенез , миелинизацию и образование синапсов . Ацетилхолин даже присутствует в плаценте и может помочь контролировать пролиферацию и дифференцировку клеток.(увеличение числа клеток и превращение многоцелевых клеток в специализированные клеточные функции) и роды . [37] [38]
Захват холина в головном мозге контролируется транспортером с низким сродством, расположенным на гематоэнцефалическом барьере . [39] Транспорт происходит, когда концентрация холина в артериальной плазме увеличивается выше 14 мкмоль / л, что может произойти во время скачка концентрации холина после употребления богатой холином пищи. Нейроны , наоборот, приобретают холин с помощью транспортеров как с высоким, так и с низким сродством. Холин хранится в виде мембраносвязанного фосфатидилхолина, который впоследствии может быть использован для синтеза нейротрансмиттера ацетилхолина. Ацетилхолин образуется по мере необходимости, проходит через синапс и передает сигнал следующему нейрону. Впоследствии ацетилхолинэстеразаразрушает его, и свободный холин снова поглощается высокоаффинным транспортером в нейрон. [40]
Использует [ редактировать ]
Холин хлорид и холин битартрат используются в пищевых добавок . Битартрат используется чаще из-за его меньшей гигроскопичности . [2] Некоторые соли холина используются в качестве добавок для кур , индейки и некоторых других кормов для животных . Некоторые соли также используются в качестве промышленных химикатов: например, в фотолитографии для удаления фоторезиста . [1] Теофиллинат холина и салицилат холина используются в качестве лекарств [1] [41], а также в качестве структурных аналогов , таких какметахолин и карбахол . [42] Радиоактивно меченные холины, такие как 11 C-холин , используются в медицинской визуализации . [43] Другие коммерчески используемые соли включают цитрат трихолина и бикарбонат холина . [1]
Антагонисты и ингибиторы [ править ]
Сотни антагонистов холина и ингибиторов ферментов были разработаны в исследовательских целях. Аминометилпропанол одним из первых стал использоваться в качестве инструмента исследования. Он подавляет синтез холина и триметилглицина . Он может вызывать дефицит холина, что, в свою очередь, приводит к ожирению печени у грызунов. Диэтаноламин - еще одно такое соединение, но также загрязняет окружающую среду. N -циклогексилхолин подавляет захват холина в основном мозгом. Гемихолиний-3 является более общим ингибитором, но также умеренно ингибирует холинкиназы.. Также были разработаны более специфические ингибиторы холинкиназы. Также существуют ингибиторы синтеза триметилглицина: карбоксибутилгомоцистеин является примером специфического ингибитора BHMT . [2]
Холинергическая гипотеза о деменции не только приводит к лекарственным ингибиторам ацетилхолинэстеразы , но также и к различным ингибиторам ацетилхолина . Примерами таких химических веществ , ингибирующих исследовательских включают triethylcholine , homocholine и многие другие N - этил производные холина, которые являются ложные нейротрансмиттеров аналоги ацетилхолина. Также были разработаны ингибиторы холинацетилтрансферазы . [2]
История [ править ]
Открытие [ править ]
В 1849 году Адольф Стрекер первым выделил холин из желчи свиньи . [44] [45] В 1852 году Л. Бабо и М. Хиршбрунн извлекли холин из семян белой горчицы и назвали его синкалин . [45] В 1862 году Стрекер повторил свой эксперимент с желчью свиньи и быка, впервые назвав это вещество холином после греческого слова желчь, холе , и идентифицировав его с химической формулой C 5 H 13 NO. [46] [12] В 1850 году Теодор Николас Гобли извлек из мозгов и икрыиз карпов вещества он назвал лецитин после греческого слова для яичного желтка , lekithos , показывая в 1874 году , что это была смесь фосфатидилхолины . [47] [48]
В 1865 году Оскар Либрейх выделил « нейрин » из мозга животных. [49] [12] В структурные формулы из ацетилхолина и «нейрин» Liebreich были решены Адольф фон Байера в 1867. [50] [45] В том же году «нейрин» и sinkaline было показано, что одни и те же вещества , как холин STRECKER в. Таким образом, Байер первым разрешил структуру холина. [51] [52] [45] Соединение, известное как нейрин, не связано с холином. [12]
Открытие как питательное вещество [ править ]
В начале 1930 - х годов, Чарльз Лучший и его коллеги отметили , что жировая дистрофия печени у крыс на специальной диете и диабетических собак может быть предотвращено путем кормления их лецитина , [12] , доказав в 1932 году , что холин лецитином был исключительно ответственен за этот профилактический эффект. [53] В 1998 году Национальная академия медицины США представила свои первые рекомендации по содержанию холина в рационе человека. [54]
Ссылки [ править ]
- ^ Б с д е е г ч я J Кирк RE, и др. (2000). Энциклопедия химической технологии Кирка-Отмера . Том 6 (4-е изд.). Джон Вили и сыновья. С. 100–102. ISBN 9780471484943.
- ^ Б с д е е г ч я J к л м п Рукер РБ, Zempléni Дж, Suttie JW, McCormick БД (2007). Справочник витаминов (4-е изд.). Тейлор и Фрэнсис. стр. 459 -477. ISBN 9780849340222.
- ^ "Холин" . Словари Lexico . Дата обращения 9 ноября 2019 .
- ^ Б с д е е г ч я J к л м «Холин» . Информационный центр по микронутриентам, Институт Линуса Полинга, Государственный университет Орегона. Февраль 2015 . Дата обращения 11 ноября 2019 .
- ^ а б «Холин» . База данных человеческого метаболома . Центр инноваций в области метаболомики, Университет Альберты, Эдмонтон, Канада. 17 августа 2016 . Проверено 13 сентября 2016 года .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad "Диетические контрольные значения холина" . Журнал EFSA . 14 (8). 2016 DOI : 10,2903 / j.efsa.2016.4484 .
- ^ Rontein D, Нишиду I, Таширо G, Йошиока K, Wu WI, Фолькер DR, Бассет G, Hanson AD (сентябрь 2001). «Растения синтезируют этаноламин прямым декарбоксилированием серина с использованием пиридоксальфосфатного фермента» . Журнал биологической химии . 276 (38): 35523–9. DOI : 10.1074 / jbc.M106038200 . PMID 11461929 .
- ^ Prud'homme MP, Мур TS (ноябрь 1992). «Синтез фосфатидилхолина в эндосперме клещевины: свободные основания в качестве промежуточных продуктов» . Физиология растений . 100 (3): 1527–35. DOI : 10.1104 / pp.100.3.1527 . PMC 1075815 . PMID 16653153 .
- ^ Nuccio ML, Ziemak MJ, Генри С. А., Weretilnyk Е.А., Hanson AD (май 2000). «Клонирование кДНК фосфоэтаноламин N -метилтрансферазы из шпината путем комплементации в Schizosaccharomyces pombe и характеристики рекомбинантного фермента» . Журнал биологической химии . 275 (19): 14095–101. DOI : 10.1074 / jbc.275.19.14095 . PMID 10799484 .
- ^ McNeil SD, Nuccio ML, Ziemak MJ, Hanson AD (август 2001). «Повышенный синтез холина и бетаина глицина в трансгенных растениях табака, которые сверхэкспрессируют фосфоэтаноламин N-метилтрансферазу» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (17): 10001–5. Bibcode : 2001PNAS ... 9810001M . DOI : 10.1073 / pnas.171228998 . PMC 55567 . PMID 11481443 .
- ^ "Суперпути биосинтеза холина" . Коллекция базы данных BioCyc: MetaCyc . SRI International.
- ^ а б в г д Zeisel SH (2012). «Краткая история холина» . Анналы питания и метаболизма . 61 (3): 254–8. DOI : 10.1159 / 000343120 . PMC 4422379 . PMID 23183298 .
- ^ а б в г Иназу М (сентябрь 2019 г.). «Функциональная экспрессия транспортеров холина в гематоэнцефалическом барьере» . Питательные вещества . 11 (10): 2265. DOI : 10,3390 / nu11102265 . PMC 6835570 . PMID 31547050 .
- ^ Барвик К.Е., Райт Дж., Аль-Турки С., Макэнтагарт М.М., Наир А., Чиоза Б. и др. (Декабрь 2012 г.). «Нарушение пресинаптического транспорта холина лежит в основе наследственной моторной нейропатии» . Американский журнал генетики человека . 91 (6): 1103–7. DOI : 10.1016 / j.ajhg.2012.09.019 . PMC 3516609 . PMID 23141292 .
- Перейти ↑ Glier MB, Green TJ, Devlin AM (январь 2014 г.). «Метиловые нутриенты, метилирование ДНК и сердечно-сосудистые заболевания». Молекулярное питание и пищевые исследования . 58 (1): 172–82. DOI : 10.1002 / mnfr.201200636 . PMID 23661599 .
- ^ Barak AJ, Beckenhauer HC, Юннила M, Тума DJ (июнь 1993). «Диетический бетаин способствует выработке печеночного S- аденозилметионина и защищает печень от жировой инфильтрации, вызванной этанолом». Алкоголизм, клинические и экспериментальные исследования . 17 (3): 552–5. DOI : 10.1111 / j.1530-0277.1993.tb00798.x . PMID 8333583 .
- ^ Dushianthan A, Кьюсак R, Grocott MP, Postle AD (июнь 2018). «У пациентов с острым респираторным дистресс-синдромом выявлено нарушение синтеза фосфатидилхолина в печени» . Журнал липидных исследований . 59 (6): 1034–1045. DOI : 10.1194 / jlr.P085050 . PMC 5983399 . PMID 29716960 .
- ^ a b c d e f g h i "Холин" . Офис диетических добавок (ОРВ) в Национальных институтах здравоохранения . Дата обращения 19 мая 2020 .
 Эта статья включает текст из этого источника, который находится в общественном достоянии .
Эта статья включает текст из этого источника, который находится в общественном достоянии . - ^ «21 CFR 107.100: Детская смесь; Требования к питательным веществам; Характеристики питательных веществ; Содержание холина» . Свод федеральных правил, раздел 21; Управление по контролю за продуктами и лекарствами. 1 апреля 2019 . Проверено 24 октября 2019 года .
- ^ a b Zeisel SH, Mar MH, Howe JC, Holden JM (май 2003 г.). «Концентрации холинсодержащих соединений и бетаина в обычных пищевых продуктах» . Журнал питания . 133 (5): 1302–7. DOI : 10.1093 / JN / 133.5.1302 . PMID 12730414 .
- ^ Холин (17 марта 2014). «Холин» . www.nrv.gov.au . Проверено 22 октября 2019 года .
- ^ Уоллес ТС, Fulgoni В.Л. (2016). «Оценка общего потребления холина в США». Журнал Американского колледжа питания . 35 (2): 108–12. DOI : 10.1080 / 07315724.2015.1080127 . PMID 26886842 . S2CID 24063121 .
- ^ «Что мы едим в Америке, NHANES 2013-2014» (PDF) . Проверено 24 октября 2019 года .
- ^ a b c Корбин KD, Zeisel SH (март 2012). «Метаболизм холина позволяет по-новому взглянуть на неалкогольную жировую болезнь печени и ее прогрессирование» . Текущее мнение в гастроэнтерологии . 28 (2): 159–65. DOI : 10.1097 / MOG.0b013e32834e7b4b . PMC 3601486 . PMID 22134222 .
- ^ DiNicolantonio JJ, Маккарти М, OKeefe J (2019). « Связь умеренно повышенного уровня N- оксида триметиламина с риском сердечно-сосудистых заболеваний: является ли ТМАО маркером резистентности к инсулину печени» . Открытое сердце . 6 (1): e000890. DOI : 10.1136 / openhrt-2018-000890 . PMC 6443140 . PMID 30997120 .
- ↑ Jia J, Dou P, Gao M, Kong X, Li C, Liu Z, Huang T (сентябрь 2019). «Оценка причинно-следственной связи между кишечными микробиотозависимыми метаболитами и кардиометаболическим здоровьем: двунаправленный менделевский рандомизационный анализ» . Диабет . 68 (9): 1747–1755. DOI : 10,2337 / db19-0153 . PMID 31167879 .
- ^ Имбард А. и др. (2013). «Дефекты нервной трубки, фолиевая кислота и метилирование» . Международный журнал исследований окружающей среды и общественного здравоохранения . 10 (9): 4352–4389. DOI : 10.3390 / ijerph10094352 . PMC 3799525 . PMID 24048206 .
- ^ Richman Е.Л., Кенфилд С.А., Стампферы MJ, Giovannucci EL, Zeisel SH, Виллетты туалет, Чан JM (октябрь 2012). «Потребление холина и риск летального рака простаты: заболеваемость и выживаемость» . Американский журнал клинического питания . 96 (4): 855–63. DOI : 10,3945 / ajcn.112.039784 . PMC 3441112 . PMID 22952174 .
- ^ Хан П., Бидулеску А., Барбер-младший, Цейзель С.Х., Джошу С.Е., Призмент А.Е. и др. (Апрель 2019 г.). «Потребление холина и бетаина с пищей и риск общего и летального рака простаты в исследовании риска атеросклероза в сообществах (ARIC)» . Причины рака и борьба с ними . 30 (4): 343–354. DOI : 10.1007 / s10552-019-01148-4 . PMC 6553878 . PMID 30825046 .
- ↑ Wiedeman AM, Barr SI, Green TJ, Xu Z, Innis SM, Kitts DD (октябрь 2018 г.). «Диетическое потребление холина: современное состояние знаний на протяжении жизненного цикла» . Питательные вещества . 10 (10): 1513. DOI : 10,3390 / nu10101513 . PMC 6213596 . PMID 30332744 .
- ^ a b Zeisel SH (2006). «Холин: критическая роль во время развития плода и диетические требования у взрослых» . Ежегодный обзор питания . 26 : 229–50. DOI : 10.1146 / annurev.nutr.26.061505.111156 . PMC 2441939 . PMID 16848706 .
- ^ Институт медицины, пищевых продуктов и питания. Рекомендуемая диета для тиамина, рибофлавина, ниацина, витамина B 6 , фолиевой кислоты, витамина B 12 , пантотеновой кислоты, биотина и холина . Вашингтон, округ Колумбия: Пресса национальных академий. 1998 г.
- ^ Аллен LH (2006). «Беременность и период лактации». В Bowman BA, Russle RM (ред.). Настоящие знания в области питания . Вашингтон, округ Колумбия: ILSI Press. С. 529–543.
- ↑ King JC (май 2000 г.). «Физиология беременности и метаболизма питательных веществ» . Американский журнал клинического питания . 71 (5 доп.): 1218S – 25S. DOI : 10.1093 / ajcn / 71.5.1218s . PMID 10799394 .
- ^ Morgane PJ, Mokler DJ, Галлер JR (июнь 2002). «Влияние пренатальной белковой недостаточности на формирование гиппокампа». Неврология и биоповеденческие обзоры . 26 (4): 471–83. DOI : 10.1016 / s0149-7634 (02) 00012-X . PMID 12204193 . S2CID 7051841 .
- ^ Oshida K, Shimizu T, Takase M, Тамура Y, Shimizu T, Yamashiro Y (апрель 2003). «Влияние диетического сфингомиелина на миелинизацию центральной нервной системы у развивающихся крыс» . Педиатрические исследования . 53 (4): 589–93. DOI : 10,1203 / 01.pdr.0000054654.73826.ac . PMID 12612207 .
- ^ Шастри BV (июнь 1997). «Плацентарная холинергическая система человека». Биохимическая фармакология . 53 (11): 1577–86. DOI : 10.1016 / s0006-2952 (97) 00017-8 . PMID 9264309 .
- ^ Шастри BV, Sadavongvivad C (март 1978). «Холинергические системы в ненервных тканях». Фармакологические обзоры . 30 (1): 65–132. PMID 377313 .
- ^ Локман PR, Allen DD (август 2002). «Транспорт холина». Разработка лекарств и промышленная аптека . 28 (7): 749–71. DOI : 10.1081 / DDC-120005622 . PMID 12236062 . S2CID 34402785 .
- ^ Caudill MA (август 2010). «До- и послеродовое здоровье: свидетельства повышенной потребности в холине». Журнал Американской диетической ассоциации . 110 (8): 1198–206. DOI : 10.1016 / j.jada.2010.05.009 . PMID 20656095 .
- Перейти ↑ Rutter P (2017). Коммунальная аптека: симптомы, диагностика и лечение (4-е изд.). Эльзевир. п. 156. ISBN. 9780702069970.
- ↑ Howe-Grant M, Kirk RE, Othmer DF, ред. (2000). «C2-Хлороуглероды в технологии сжигания». Энциклопедия химической технологии Кирка-Отмера . Том 6 (4-е изд.). Джон Вили и сыновья. С. 100–102. ISBN 9780471484943.
- Перейти ↑ Guo Y, Wang L, Hu J, Feng D, Xu L (2018). «Диагностическая эффективность холина ПЭТ / КТ для обнаружения метастазов в кости при раке простаты: систематический обзор и метаанализ» . PLOS One . 13 (9): e0203400. Bibcode : 2018PLoSO..1303400G . DOI : 10.1371 / journal.pone.0203400 . PMC 6128558 . PMID 30192819 .
- Перейти ↑ Strecker A (1849). "Beobachtungen über die galle verschiedener thiere" . Justus Liebigs Ann Chem (на немецком языке). 70 (2): 149–197. DOI : 10.1002 / jlac.18490700203 .
- ^ а б в г Себрелл WH, Харрис RS, Алам SQ (1971). Витамины . 3 (2-е изд.). Академическая пресса. С. 4, 12. DOI : 10.1016 / B978-0-12-633763-1.50007-5 . ISBN 9780126337631.
- Перейти ↑ Strecker A (1862). "Üeber einige neue bestandtheile der schweinegalle" . Justus Liebigs Ann Chem (на немецком языке). 123 (3): 353–360. DOI : 10.1002 / jlac.18621230310 .
- ^ Gobley Т (1874 г.). "Sur la lécithine et la cérébrine" . J Pharm Chim (на французском языке). 19 (4): 346 -354.
- ^ Sourkes TL (2004). «Открытие лецитина, первого фосфолипида» (PDF) . Bull Hist Chem . 29 (1): 9–15. Архивировано 13 апреля 2019 года (PDF) .
- ^ Liebreich О (1865 г.). "Üeber die chemische beschaffenheit der gehirnsubstanz" . Justus Liebigs Ann Chem (на немецком языке). 134 (1): 29–44. DOI : 10.1002 / jlac.18651340107 .
- ^ Байеру A (1867). "I. Üeber das neinin" . Justus Liebigs Ann Chem (на немецком языке). 142 (3): 322–326. DOI : 10.1002 / jlac.18671420311 .
- ^ Dybkowsky W (1867). "Üeber die identityität des cholins und des nerins" [О идентичности холина и нейрина]. J Prakt Chem (на немецком языке). 100 (1): 153–164. DOI : 10.1002 / prac.18671000126 .
- ^ Клаус A, Кизе C (1867). «Убер нейрин унд синкалин» . J Prakt Chem (на немецком языке). 102 (1): 24–27. DOI : 10.1002 / prac.18671020104 .
- ↑ Best CH, Hershey JM, Huntsman ME (май 1932 г.). «Влияние лецитина на отложение жира в печени нормальной крысы» . Журнал физиологии . 75 (1): 56–66. DOI : 10.1113 / jphysiol.1932.sp002875 . PMC 1394511 . PMID 16994301 .
- ^ Постоянный комитет Института медицины (США) по научной оценке диетических рекомендаций и его группа по фолиевой кислоте, другим витаминам B. и холину . Национальная академия прессы (США). 1998. С. xi, 402–413. ISBN 9780309064118.