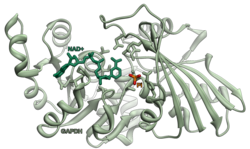
Глицеральдегид-3-фосфатдегидрогеназа
| GAPDH | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||
| Псевдонимы | GAPDH , GAPD, G3PD, HEL-S-162eP, глицеральдегид-3-фосфатдегидрогеназа | ||||||||||||||||||||||||
| Внешние идентификаторы | OMIM : 138400 MGI : 5434255 HomoloGene : 107053 GeneCards : GAPDH | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ортологи | |||||||||||||||||||||||||
| Разновидность | Человек | Мышь | |||||||||||||||||||||||
| Entrez |
|
| |||||||||||||||||||||||
| Ансамбль |
|
| |||||||||||||||||||||||
| UniProt |
|
| |||||||||||||||||||||||
| RefSeq (мРНК) |
|
| |||||||||||||||||||||||
| RefSeq (белок) |
|
| |||||||||||||||||||||||
| Расположение (UCSC) | Chr 12: 6.53 - 6.54 Мб | н / д | |||||||||||||||||||||||
| PubMed поиск | [2] | [3] | |||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Глицеральдегид-3-фосфатдегидрогеназа, NAD-связывающий домен | ||||||||
|---|---|---|---|---|---|---|---|---|
детерминанты термостабильности фермента, наблюдаемые в молекулярной структуре d-глицеральдегид-3-фосфатдегидрогеназы thermus aquaticus при разрешении 2,5 ангстрем | ||||||||
| Идентификаторы | ||||||||
| Условное обозначение | Gp_dh_N | |||||||
| Pfam | PF00044 | |||||||
| Клан пфам | CL0063 | |||||||
| ИнтерПро | IPR020828 | |||||||
| ПРОФИЛЬ | PDOC00069 | |||||||
| SCOP2 | 1gd1 / SCOPe / SUPFAM | |||||||
| ||||||||
| Глицеральдегид-3-фосфатдегидрогеназа, С-концевой домен | ||||||||
|---|---|---|---|---|---|---|---|---|
кристаллическая структура глицеральдегид-3-фосфатдегидрогеназы из Pyrococcus horikoshii ot3 | ||||||||
| Идентификаторы | ||||||||
| Условное обозначение | Gp_dh_C | |||||||
| Pfam | PF02800 | |||||||
| Клан пфам | CL0139 | |||||||
| ИнтерПро | IPR020829 | |||||||
| ПРОФИЛЬ | PDOC00069 | |||||||
| SCOP2 | 1gd1 / SCOPe / SUPFAM | |||||||
| ||||||||
Глицеральдегид-3-фосфатдегидрогеназа (сокращенно GAPDH ) ( EC 1.2.1.12 ) - это фермент с массой около 37 кДа, который катализирует шестую стадию гликолиза и, таким образом, служит для расщепления глюкозы для получения энергии и молекул углерода. Помимо этой давно установленной метаболической функции, GAPDH недавно был вовлечен в несколько неметаболических процессов, включая активацию транскрипции , инициацию апоптоза , [4] перемещение ER к пузырькам Гольджи и быстрый аксональный или аксоплазматический транспорт . [5] В сперме изофермент, специфичный для семенников. GAPDHS выражается.
Состав
В нормальных клеточных условиях цитоплазматический GAPDH существует в основном в виде тетрамера . Эта форма состоит из четырех идентичных субъединиц 37 кДа, каждая из которых содержит одну каталитическую тиоловую группу и имеет решающее значение для каталитической функции фермента. [6] [7] Ядерный GAPDH имеет повышенную изоэлектрическую точку (pI) pH 8,3–8,7. [7] Следует отметить, что остаток цистеина C152 в активном центре фермента необходим для индукции апоптоза под действием окислительного стресса . [7] В частности, посттрансляционные модификациицитоплазматического GAPDH вносят свой вклад в его функции вне гликолиза. [6]
GAPDH кодируется одним геном, который продуцирует один транскрипт мРНК с 8 вариантами сплайсинга, хотя изоформа действительно существует как отдельный ген, который экспрессируется только в сперматозоидах . [7]
Реакция
| глицеральдегид-3-фосфат | глицеральдегидфосфатдегидрогеназа | D - глицерат 1,3-бисфосфат | |
| НАД + + P i | НАДН + Н + | ||
| НАД + + P i | НАДН + Н + | ||
Соединение C00118 в базе данных KEGG Pathway. Фермент 1.2.1.12 в базе данных KEGG Pathway. Реакция R01063 в базе данных пути KEGG . Соединение C00236 в базе данных KEGG Pathway.
Двухэтапное преобразование G3P
Первая реакция - это окисление глицеральдегид-3-фосфата (G3P) в положении-1 (на диаграмме он показан как 4-й углерод от гликолиза), в котором альдегид превращается в карбоновую кислоту (ΔG ° '= - 50 кДж / моль (-12 ккал / моль)) и НАД + одновременно восстанавливается эндергонически до НАДН.
Энергия , выделяемая этих высокий экзэргонические приводы реакции окисления эндергонической второй реакции (ΔG ° '= + 50 кДж / моль (+ 12kcal / моль)), в котором молекула неорганического фосфата переносится в GAP промежуточной с образованием продукта с высокий потенциал переноса фосфорила: 1,3-бисфосфоглицерат (1,3-BPG).
Это пример фосфорилирования в сочетании с окислением, и общая реакция является несколько эндергонической (ΔG ° '= + 6,3 кДж / моль (+1,5)). Энергетическая связь здесь стала возможной благодаря GAPDH.
Механизм
GAPDH использует ковалентный катализ и общий основной катализ для уменьшения очень большой энергии активации второй стадии (фосфорилирования) этой реакции.
1: Окисление
Во-первых, остаток цистеина в активном центре GAPDH атакует карбонильную группу GAP, создавая полупродукт гемитиоацеталя (ковалентный катализ).
Гемитиоацеталь депротонируется остатком гистидина в активном центре фермента (общий щелочной катализ). Депротонирование способствует реформированию карбонильной группы в последующем промежуточном тиоэфире и выбросу гидрид-иона .
Затем соседняя, прочно связанная молекула НАД + принимает ион гидрида , образуя НАДН, в то время как гемитиоацеталь окисляется до тиоэфира .
Эта разновидность сложного тиоэфира имеет гораздо более высокую энергию (менее стабильна), чем разновидность карбоновой кислоты, которая могла бы возникнуть, если бы GAP был окислен в отсутствие GAPDH (разновидность карбоновой кислоты настолько низка по энергии, что энергетический барьер для второй стадии реакции (фосфорилирование) было бы слишком высоким, а следовательно, и слишком медленной и неблагоприятной для живого организма реакцией).
2: фосфорилирование
НАДН покидает активный центр и замещается другой молекулой НАД + , положительный заряд которой стабилизирует отрицательно заряженный карбонильный кислород в переходном состоянии следующей и последней стадии. Наконец, молекула неорганического фосфата атакует тиоэфир и образует тетраэдрический промежуточный продукт, который затем разрушается с высвобождением 1,3-бисфосфоглицерата и тиоловой группы остатка цистеина фермента.
Регулирование
Этот белок может использовать морфеиновую модель аллостерической регуляции . [8]
Функция
Метаболический
Как указывает его название, глицеральдегид - 3-фосфат - дегидрогеназы (GAPDH) катализирует превращение глицеральдегид 3-фосфата в D - глицерат 1,3-бисфосфат . Это шестой шаг в гликолитическом распаде глюкозы, важном пути снабжения энергией и молекулами углерода, который происходит в цитозоле эукариотических клеток. Преобразование происходит в два связанных этапа. Первый благоприятен и допускает второй неблагоприятный шаг.
Транскрипция и апоптоз
GAPDH может сам активировать транскрипцию . Комплекс транскрипционных коактиваторов OCA-S содержит GAPDH и лактатдегидрогеназу , два белка, которые ранее считались вовлеченными только в метаболизм . GAPDH перемещается между цитозолем и ядром и, таким образом, может связывать метаболическое состояние с транскрипцией гена. [9]
В 2005 году Hara et al. показали, что GAPDH инициирует апоптоз . Это не третья функция, но ее можно рассматривать как активность, опосредованную связыванием GAPDH с ДНК, как при активации транскрипции, обсуждавшейся выше. Исследование продемонстрировало, что GAPDH S-нитрозилируется NO в ответ на клеточный стресс, который заставляет его связываться с белком SIAH1 , убиквитинлигазой . Комплекс перемещается в ядро, где Siah1 нацеливается на ядерные белки для деградации , тем самым инициируя контролируемое отключение клеток. [10] В последующем исследовании группа продемонстрировала, что депренил , который использовался в клинических условиях для лечения болезни Паркинсона, сильно снижает апоптотическое действие GAPDH, предотвращая его S-нитрозилирование, и, таким образом, может использоваться в качестве лекарственного средства. [11]
Метаболический переключатель
GAPDH действует как обратимый метаболический переключатель при окислительном стрессе. [12] Когда клетки подвергаются действию оксидантов , они нуждаются в чрезмерном количестве кофактора антиоксиданта НАДФН . В цитозоле НАДФН восстанавливается из НАДФ + несколькими ферментами, три из которых катализируют первые шаги пентозофосфатного пути . Обработка окислителями вызывает инактивацию GAPDH. Эта инактивация временно перенаправляет метаболический поток с гликолиза на пентозофосфатный путь, позволяя клетке вырабатывать больше НАДФН. [13] В стрессовых условиях НАДФН необходим некоторым антиоксидантным системам, включая глутаредоксин и тиоредоксин.а также необходим для переработки глутатиона .
От скорой помощи до транспорта Гольджи
GAPDH также, по-видимому, участвует в транспорте везикул из эндоплазматического ретикулума (ER) в аппарат Гольджи, который является частью пути доставки секретируемых белков. Было обнаружено, что GAPDH рекрутируется rab2 в везикулярно-канальцевые кластеры ER, где он помогает формировать везикулы COP 1 . GAPDH активируется посредством фосфорилирования тирозина с помощью Src . [14]
Дополнительные функции
GAPDH, как и многие другие ферменты, выполняет несколько функций. Помимо катализа 6-й стадии гликолиза , недавние данные указывают на участие GAPDH в других клеточных процессах. Было описано, что GAPDH проявляет многофункциональность более высокого порядка в контексте поддержания клеточного гомеостаза железа [15], в частности, как белок-шаперон для лабильного гема внутри клеток. [16] Это стало неожиданностью для исследователей, но с эволюционной точки зрения имеет смысл повторно использовать и адаптировать существующие белки вместо того, чтобы создавать новый белок с нуля.
Использовать в качестве контроля загрузки
Поскольку ген GAPDH часто стабильно и постоянно экспрессируется на высоком уровне в большинстве тканей и клеток, он считается геном домашнего хозяйства . По этой причине GAPDH обычно используется биологическими исследователями в качестве контроля загрузки для вестерн-блоттинга и в качестве контроля для количественной ПЦР . Однако исследователи сообщили о различном регулировании GAPDH при определенных условиях. [17] Например, было показано , что фактор транскрипции MZF-1 регулирует ген GAPDH. [18] Гипоксия также сильно активирует GAPDH. [19] Таким образом, использование GAPDH для контроля загрузки следует тщательно продумать.
Сотовая связь
Все стадии гликолиза происходят в цитозоле, как и реакция, катализируемая GAPDH. В эритроцитах GAPDH и некоторые другие гликолитические ферменты собираются в комплексы на внутренней стороне клеточной мембраны . Этот процесс, по-видимому, регулируется фосфорилированием и оксигенацией. [20] Ожидается, что размещение нескольких гликолитических ферментов рядом друг с другом значительно увеличит общую скорость расщепления глюкозы. Недавние исследования также показали, что GAPDH экспрессируется железозависимым образом на внешней стороне клеточной мембраны, где он играет роль в поддержании гомеостаза клеточного железа. [21] [22]
Клиническое значение
Рак
GAPDH сверхэкспрессируется при множественных раковых заболеваниях человека, таких как меланома кожи , и его экспрессия положительно коррелирует с прогрессированием опухоли. [23] [24] Его гликолитические и антиапоптотические функции способствуют пролиферации и защите опухолевых клеток, способствуя онкогенезу . Примечательно, что GAPDH защищает от укорачивания теломер, вызванного химиотерапевтическими препаратами, которые стимулируют сфинголипид церамид . Между тем, такие условия, как окислительный стресс, нарушают функцию GAPDH, что приводит к старению и смерти клеток. [7] Кроме того, истощение GAPDH способствовало старению.в опухолевых клетках, тем самым представляя новую терапевтическую стратегию для контроля роста опухоли. [25]
Нейродегенерация
GAPDH причастен к нескольким нейродегенеративным заболеваниям и расстройствам, в основном через взаимодействия с другими белками, специфичными для этого заболевания или расстройства. Эти взаимодействия могут влиять не только на энергетический метаболизм, но и на другие функции GAPDH. [6] Например, взаимодействия GAPDH с белком - предшественником бета-амилоида (betaAPP) могут мешать его функции в отношении цитоскелета или мембранного транспорта, в то время как взаимодействия с хантингтином могут влиять на его функцию в отношении апоптоза, транспорта ядерной тРНК , репликации ДНК и ДНК. ремонт . Кроме того, сообщалось о ядерной транслокации GAPDH при болезни Паркинсона.(PD) и несколько антиапоптотических препаратов для лечения PD, таких как разагилин , действуют, предотвращая ядерную транслокацию GAPDH. Предполагается, что гипометаболизм может быть одним из факторов БП, но точные механизмы, лежащие в основе участия GAPDH в нейродегенеративном заболевании, еще предстоит выяснить. [26] SNP rs3741916 в 5' UTR из GAPDH гена может быть связано с поздним началом болезни Альцгеймера . [27]
Взаимодействия
Партнеры по связыванию белков
GAPDH участвует в ряде биологических функций через белок-белковые взаимодействия с:
- тубулин для облегчения связывания микротрубочек; [6]
- актин для облегчения полимеризации актина; [6]
- VDAC1 для индукции проницаемости митохондриальной мембраны (MMP) и апоптоза; [6]
- Инозитол-1,4,5-трифосфатный рецептор для регулирования внутриклеточной передачи сигналов Ca2 + ; [6]
- Окт-1 , чтобы сформировать коактиватор комплекс ОСА-S, который необходим для гистона H2B синтеза во время S фазы от клеточного цикла ; [7]
- p22, чтобы помочь организации микротрубочек ; [7]
- Rab2 для облегчения эндоплазматического ретикулума (ER) - транспорта Гольджи ; [7]
- Трансферрин на поверхности различных клеток и во внеклеточной жидкости; [7] [22] [28]
- Лактатдегидрогеназа ; [7]
- Лактоферрин; [29]
- Апуриновая / апиримидиновая эндонуклеаза ( APE1 ), таким образом превращая окисленный APE1 в его восстановленную форму, чтобы возобновить его эндонуклеазную активность; [7]
- Белок промиелоцитарного лейкоза (PML) РНК- зависимым образом; [7]
- Rheb для секвестрации GTPase в условиях низкого уровня глюкозы; [7]
- Siah1 с образованием комплекса, который перемещается в ядро, где он убиквитинирует и разрушает ядерные белки в условиях нитрозативного стресса; [7]
- Конкурент GAPDH белка Siah увеличивает жизнь (GOSPEL), чтобы блокировать взаимодействие GAPDH с Siah1 и, таким образом, гибель клеток в ответ на окислительный стресс; [7]
- p300 / CREB-связывающий белок (CBP), который ацетилирует GAPDH и, в свою очередь, усиливает ацетилирование дополнительных апоптотических мишеней; [7]
- Са2 + / кальмодулин-зависимая протеинкиназа, специфичная для скелетных мышц; [7]
- Акт ; [7]
- Белок - предшественник бета-амилоида (бетаАПП); [26]
- Хантингтин . [26]
- GAPDH может самоассоциироваться в гомотипные олигомеры / агрегаты.
Партнеры по связыванию нуклеиновых кислот
GAPDH связывается с одноцепочечной РНК [30] и ДНК, и был идентифицирован ряд партнеров по связыванию нуклеиновых кислот: [7]
- тРНК ,
- РНК вируса гепатита А ,
- РНК вируса гепатита В ,
- РНК вируса гепатита С ,
- HPIV3,
- мРНК лимфокинов ,
- МРНК IFN-γ ,
- МРНК JEV и
- теломерная ДНК.
Ингибиторы
- Конингиновая кислота
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи. [§ 1]
- ^ Интерактивную карту путей можно отредактировать на WikiPathways: " GlycolysisGluconeogenesis_WP534 " .
использованная литература
- ^ a b c GRCh38: Ensembl, выпуск 89: ENSG00000111640 - Ensembl , май 2017 г.
- ^ "Human PubMed Reference:" . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Tarze А, Deniaud А, Le Bras M, Maillier E, D Molle, Larochette N, N Zamzami, Ян G, G Кремер, Brenner C (апрель 2007). «GAPDH, новый регулятор проапоптотической проницаемости митохондриальной мембраны» . Онкоген . 26 (18): 2606–20. DOI : 10.1038 / sj.onc.1210074 . PMID 17072346 .
- ^ Zala D, Hinckelmann М.В., Ю Н, Лира - да - Кунья М.М., Liot G, Cordelières FP, Marco S, Saudou F (январь 2013). «Везикулярный гликолиз обеспечивает бортовую энергию для быстрого аксонального транспорта» . Cell . 152 (3): 479–91. DOI : 10.1016 / j.cell.2012.12.029 . PMID 23374344 .
- ^ Б с д е е г Тристан C, N, Шахани Sedlak TW, Sawa A (февраль 2011 г.). «Разнообразные функции GAPDH: взгляды из разных субклеточных компартментов» . Сотовая связь . 23 (2): 317–23. DOI : 10.1016 / j.cellsig.2010.08.003 . PMC 3084531 . PMID 20727968 .
- ^ a b c d e f g h i j k l m n o p q r s Николлс К., Ли Х., Лиу Дж. П. (август 2012 г.). «GAPDH: обычный фермент с необычными функциями». Клиническая и экспериментальная фармакология и физиология . 39 (8): 674–9. DOI : 10.1111 / j.1440-1681.2011.05599.x . PMID 21895736 . S2CID 23499684 .
- ^ Selwood T, Джаффе EK (март 2012). «Динамические диссоциирующие гомоолигомеры и контроль функции белка» . Архивы биохимии и биофизики . 519 (2): 131–43. DOI : 10.1016 / j.abb.2011.11.020 . PMC 3298769 . PMID 22182754 .
- ↑ Zheng L, Roeder RG, Luo Y (июль 2003 г.). «Активация S-фазы промотора гистона H2B с помощью OCA-S, коактиваторного комплекса, который содержит GAPDH в качестве ключевого компонента» . Cell . 114 (2): 255–66. DOI : 10.1016 / S0092-8674 (03) 00552-X . PMID 12887926 . S2CID 5543647 .
- ^ Hara MR, Agrawal N, Kim SF, Cascio MB, Fujimuro M, Ozeki Y, Takahashi M, Cheah JH, Tankou SK, Hester LD, Ferris CD, Hayward SD, Snyder SH, Sawa A (июль 2005 г.). «S-нитрозилированный GAPDH инициирует апоптотическую гибель клеток путем ядерной транслокации после связывания Siah1». Природа клеточной биологии . 7 (7): 665–74. DOI : 10.1038 / ncb1268 . PMID 15951807 . S2CID 1922911 .
- ^ Hara MR, Thomas B, Cascio MB, Bae BI, Hester LD, Dawson VL, Dawson TM, Sawa A, Snyder SH (март 2006). «Нейропротекция фармакологической блокадой каскада смерти GAPDH» . Труды Национальной академии наук Соединенных Штатов Америки . 103 (10): 3887–9. Bibcode : 2006PNAS..103.3887H . DOI : 10.1073 / pnas.0511321103 . PMC 1450161 . PMID 16505364 .
- ^ Агарвал Р., Чжао л, Sancheti Н, Сундар И.К., Рахман I, Каденас Е (ноябрь 2012 года). «Кратковременное воздействие сигаретного дыма вызывает обратимые изменения в энергетическом обмене и окислительно-восстановительном статусе клеток, независимо от воспалительных реакций в легких мыши». Американский журнал физиологии. Клеточная и молекулярная физиология легких . 303 (10): L889–98. DOI : 10,1152 / ajplung.00219.2012 . PMID 23064950 .
- ^ Ральсер М, Вамелинк ММ, Ковальд А, Гериш Б, Херен Г, Струйс Э.А., Клипп Э., Якобс С, Брайтенбах М, Лехрах Х, Кробич С (2007). «Динамическое изменение маршрута потока углеводов является ключом к противодействию окислительному стрессу» . Журнал биологии . 6 (4): 10. DOI : 10,1186 / jbiol61 . PMC 2373902 . PMID 18154684 .
- ^ Тисдейл EJ, Artalejo CR (июнь 2007). «Мутант GAPDH, дефектный по Src-зависимому фосфорилированию тирозина, препятствует Rab2-опосредованным событиям» . Трафик . 8 (6): 733–41. DOI : 10.1111 / j.1600-0854.2007.00569.x . PMC 3775588 . PMID 17488287 .
- ^ Boradia В.М., Raje M, Raje CI (декабрь 2014). «Белок подрабатывает метаболизмом железа: глицеральдегид-3-фосфатдегидрогеназа (GAPDH)». Труды биохимического общества . 42 (6): 1796–801. DOI : 10.1042 / BST20140220 . PMID 25399609 .
- ^ Суини Э.А., Сингх А.Б., Чакраварти Р., Мартинес-Гусман О, Сайни А., Хак М.М. и др. (Июль 2018). «Глицеральдегид-3-фосфатдегидрогеназа - шаперон, выделяющий лабильный гем в клетки» . Журнал биологической химии . 293 (37): 14557–14568. DOI : 10.1074 / jbc.RA118.004169 . PMC 6139559 . PMID 30012884 .
- ^ Barber RD, Хармера DW, Coleman RA, Кларк BJ (май 2005). «GAPDH как ген домашнего хозяйства: анализ экспрессии мРНК GAPDH в панели из 72 тканей человека». Физиологическая геномика . 21 (3): 389–95. CiteSeerX 10.1.1.459.7039 . DOI : 10.1152 / physiolgenomics.00025.2005 . PMID 15769908 .
- ^ Piszczatowski RT, Рафферти BJ, Rozado A, S Тобак, Ленц NH (август 2014). «Ген глицеральдегид-3-фосфатдегидрогеназы (GAPDH) регулируется миелоидным цинковым пальцем 1 (MZF-1) и индуцируется кальцитриолом». Сообщения о биохимических и биофизических исследованиях . 451 (1): 137–41. DOI : 10.1016 / j.bbrc.2014.07.082 . PMID 25065746 .
- ^ Ян, Инчжун; Фан, Венхонг; Чжу, Линлинг; Чжао, Тонг; Ма, Лан; Ву, Ян; Ге, Рили; Вентилятор, Мин (2008). «Влияние гипоксии на экспрессию мРНК генов домашнего хозяйства в ткани мозга крыс и первичных культивируемых нервных клетках». Границы медицины в Китае . 2 (3): 239–243. DOI : 10.1007 / s11684-008-0045-7 . S2CID 85327763 .
- Перейти ↑ Campanella ME, Chu H, Low PS (февраль 2005 г.). «Сборка и регуляция комплекса гликолитических ферментов на мембране эритроцитов человека» . Труды Национальной академии наук Соединенных Штатов Америки . 102 (7): 2402–7. Bibcode : 2005PNAS..102.2402C . DOI : 10.1073 / pnas.0409741102 . PMC 549020 . PMID 15701694 .
- ^ Sirover MA (декабрь 2014). «Структурный анализ функционального разнообразия глицеральдегид-3-фосфатдегидрогеназы» . Международный журнал биохимии и клеточной биологии . 57 : 20–6. DOI : 10.1016 / j.biocel.2014.09.026 . PMC 4268148 . PMID 25286305 .
- ^ a b Кумар С., Шеоканд Н., Мхадешвар М.А., Радже С.И., Радже М. (январь 2012 г.). «Характеристика глицеральдегид-3-фосфатдегидрогеназы как нового рецептора трансферрина». Международный журнал биохимии и клеточной биологии . 44 (1): 189–99. DOI : 10.1016 / j.biocel.2011.10.016 . PMID 22062951 .
- ^ Рамос Д, Пеллин-Carcelén А, Agustí Дж, Murgui А, Жорды Е, Пеллин А, С Монтеагудо (январь 2015). «Нарушение регуляции экспрессии глицеральдегид-3-фосфатдегидрогеназы во время опухолевой прогрессии меланомы кожи человека». Противораковые исследования . 35 (1): 439–44. PMID 25550585 .
- ^ Ван D, Moothart DR, Лоуи DR, Цянь X (2013). «Экспрессия генов связанного с глицеральдегид-3-фосфатдегидрогеназой клеточного цикла (GACC) коррелирует со стадией рака и плохой выживаемостью у пациентов с солидными опухолями» . PLOS ONE . 8 (4): e61262. Bibcode : 2013PLoSO ... 861262W . DOI : 10.1371 / journal.pone.0061262 . PMC 3631177 . PMID 23620736 .
- ^ Пхадка М, Krynetskaia Н, Мишр А, Krynetskiy Е (июль 2011 года). «Фенотип ускоренного клеточного старения GAPDH-истощенных клеток карциномы легких человека» . Сообщения о биохимических и биофизических исследованиях . 411 (2): 409–15. DOI : 10.1016 / j.bbrc.2011.06.165 . PMC 3154080 . PMID 21749859 .
- ^ a b c Mazzola JL, Sirover MA (октябрь 2002 г.). «Изменение внутриклеточной структуры и функции глицеральдегид-3-фосфатдегидрогеназы: общий фенотип нейродегенеративных расстройств?». Нейротоксикология . 23 (4–5): 603–9. DOI : 10.1016 / s0161-813x (02) 00062-1 . PMID 12428732 .
- ^ Аллен M, Кокс C, Белбин O, Ma L, Bisceglio GD, Wilcox SL, Howell CC, Hunter TA, Culley O, Walker LP, Carrasquillo MM, Dickson DW, Petersen RC, Graff-Radford NR, Younkin SG, Ertekin- Танер Н (январь 2012 г.). «Ассоциация и гетерогенность в локусе GAPDH при болезни Альцгеймера» . Нейробиология старения . 33 (1): 203.e25–33. DOI : 10.1016 / j.neurobiolaging.2010.08.002 . PMC 3017231 . PMID 20864222 .
- ^ Raje CI, Kumar S, Harle A, Нанда JS, Raje M (февраль 2007). «Глицеральдегид-3-фосфатдегидрогеназа на поверхности клеток макрофагов является новым рецептором трансферрина» . Журнал биологической химии . 282 (5): 3252–61. DOI : 10.1074 / jbc.M608328200 . PMID 17121833 .
- ^ Секретируемая многофункциональная глицеральдегид-3-фосфатдегидрогеназа секвестрирует лактоферрин и железо в клетки неканоническим путем. Ануп С. Чаухан, Пуджа Рават, Химаншу Малхотра, Навдип Шеоканд, Манодж Кумар, Анил Патидар, Сурбхи Чаудхари, Приянка Джахар, Чая И. Радже и Манодж Радже Scientific Reports 5, 18465; DOI: 10.1038 / srep18465 (2015)
- ^ Белого М. Р., Хан М., Deredge Д, Росс CR, Квинтин R, Zucconi BE, Высоцкий В.Х., Wintrode ЛП, Уилсон Г.М., Гарсен ЭД (январь 2015). «Мутация интерфейса димера в глицеральдегид-3-фосфатдегидрогеназе регулирует его связывание с AU-богатой РНК» . Журнал биологической химии . 290 (3): 1770–85. DOI : 10.1074 / jbc.M114.618165 . PMC 4340419 . PMID 25451934 .
дальнейшее чтение
- Воет Д., Воет Дж. Г. (2010). Биохимия . Нью-Йорк: Вили. ISBN 978-0-470-57095-1.
- Страйер Л., Берг Дж. М., Тимочко Дж. Л. (2002). Биохимия, пятое издание и лекционная тетрадь . Сан-Франциско: WH Freeman. ISBN 978-0-7167-9804-0.
- диаграмма механизма реакции GAPDH от Lodish MCB на книжной полке NCBI
- похожая диаграмма из Альберта Клетка на книжной полке NCBI
внешние ссылки
- PDBe-KB предоставляет обзор всей информации о структуре, доступной в PDB для глицеральдегид-3-фосфатдегидрогеназы человека.
| vте Путь метаболизма гликолиза |
|---|
Глюкоза Гексокиназа АТФ ADP Глюкозо-6-фосфат Глюкозо-6-фосфат- изомераза Фруктоза 6-фосфат Фосфофруктокиназа-1 АТФ ADP 1,6-бисфосфат фруктозы Фруктозо-бисфосфат альдолаза Дигидроксиацетонфосфат + + Глицеральдегид 3-фосфат Триозофосфат изомераза 2 × Глицеральдегид-3-фосфат 2 × Глицеральдегид-3- фосфатдегидрогеназа НАД + + P i НАДН + Н + НАД + + P i НАДН + Н + 2 × 1,3-бисфосфоглицерат 2 × Фосфоглицераткиназа ADP АТФ ADP АТФ 2 × 3-фосфоглицерат 2 × Фосфоглицератмутаза 2 × 2-фосфоглицерат 2 × Phosphopyruvate гидратаз ( енолаз ) H 2 O H 2 O 2 × Фосфоенолпируват 2 × Пируваткиназа ADP АТФ 2 × Пируват 2 × |
- Гены на хромосоме 12 человека
- Гликолиз
- EC 1.2.1
- Ферменты гликолиза

