| GSN | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||
| Псевдонимы | ГСН , ГСН, АДФ, АГЕЛ, гельсолин | ||||||||||||||||||||||||
| Внешние идентификаторы | OMIM : 137350 MGI : 95851 HomoloGene : 147 GeneCards : GSN | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ортологи | |||||||||||||||||||||||||
| Разновидность | Человек | Мышь | |||||||||||||||||||||||
| Entrez |
|
| |||||||||||||||||||||||
| Ансамбль |
|
| |||||||||||||||||||||||
| UniProt |
|
| |||||||||||||||||||||||
| RefSeq (мРНК) |
|
| |||||||||||||||||||||||
| RefSeq (белок) |
|
| |||||||||||||||||||||||
| Расположение (UCSC) | н / д | Chr 2: 35.26 - 35.31 Мб | |||||||||||||||||||||||
| PubMed поиск | [2] | [3] | |||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Гельсолин - это актин- связывающий белок, который является ключевым регулятором сборки и разборки актиновых филаментов. Гельсолин является одним из самых эффективных членов суперсемейства гельсолин / виллин , расщепляющих актин , поскольку он разделяет с почти 100% эффективностью. [4] [5]
Клеточный гельсолин, обнаруженный в цитозоле и митохондриях , [6] имеет близкую секретируемую форму, плазменный гельзолин , который содержит дополнительные 24 АА N-концевых удлинения. [7] [8] Способность плазменного гельсолина разъединять актиновые волокна помогает организму оправиться от болезней и травм, которые вызывают утечку клеточного актина в кровь. Кроме того, он играет важную роль в врожденном иммунитете хозяина , активации макрофагов и локализации воспаления .
Структура [ править ]
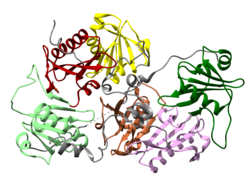
Гельсолин представляет собой белок массой 82 кДа с шестью гомологичными субдоменами, обозначаемый как S1-S6. Каждый субдомен состоит из пятицепочечного β-листа , окруженного двумя α-спиралями , одна из которых расположена перпендикулярно нитям, а другая - параллельно. Β-листы трех N-концевых субдоменов (S1-S3) соединяются, чтобы сформировать расширенный β-лист, как и β-листы C-концевых субдоменов (S4-S6). [9]
Регламент [ править ]
Среди липид- связывающих регуляторных белков актина гельсолин (как и кофилин ) предпочтительно связывает полифосфоинозитид (PPI). [10] Связывающие последовательности в гельсолине очень похожи на мотивы в других PPI-связывающих белках. [10]
Активность Гельсолина стимулируется ионами кальция (Ca 2+ ). [5] Хотя белок сохраняет свою общую структурную целостность как в активированном, так и в деактивированном состояниях, спиральный хвост S6 движется как защелка в зависимости от концентрации ионов кальция. [11] С-конец определяет концентрацию кальция в клетке. Когда Ca 2+ отсутствует, хвост S6 экранирует сайты связывания актина на одной из спиралей S2. [9] Когда ион кальция прикрепляется к хвосту S6, он выпрямляется, обнажая актин-связывающие участки S2. [11]N-конец непосредственно участвует в разделении актина. S2 и S3 связываются с актином до того, как связывание S1 разрывает связи актин-актин и закрывает зазубренный конец. [10]
Гельсолин может подавляться локальным повышением концентрации фосфатидилинозитол (4,5) -бисфосфата (PIP 2 ), PPI. Это двухэтапный процесс. Во-первых, (PIP 2 ) связывается с S2 и S3, ингибируя связывание гельсолина на стороне актина. Затем (PIP 2 ) связывается с S1 гельсолина, не позволяя гельсолину расщеплять актин, хотя (PIP 2 ) не связывается напрямую с актин-связывающим сайтом гельсолина. [10]
Разделение актина Гельсолином , в отличие от разделения микротрубочек катанином , не требует дополнительных затрат энергии.
Сотовая связь [ править ]
Как важный регулятор актина, гельзолин играет роль в образовании подосом (наряду с Arp3, кортактином и Rho GTPases). [12]
Гельсолин также подавляет апоптоз , стабилизируя митохондрии . [6] Перед смертью клетки митохондрии обычно теряют мембранный потенциал и становятся более проницаемыми. Гельсолин может препятствовать высвобождению цитохрома С , препятствуя усилению сигнала, которое могло бы привести к апоптозу. [13]
Актин может быть поперечно сшит в гель с помощью протеинов, сшивающих актин. Гельсолин может превратить этот гель в золь , отсюда и название гельсолин.
Исследования на животных [ править ]
Исследования на мышах показывают, что гельзолин, как и другие белки, расщепляющие актин, не экспрессируется в значительной степени до окончания ранней эмбриональной стадии - примерно 2 недели у эмбрионов мышей . [14] Однако во взрослых образцах гельзолин особенно важен для подвижных клеток, таких как тромбоциты . Мыши с нулевыми gelsolin-кодирующих генов претерпевают нормальное развитие эмбриона , но деформация их тромбоцитов крови снижается их подвижность, в результате чего более медленный ответ на заживление ран. [14]
Также было показано, что недостаточность гельсолина у мышей вызывает повышенную проницаемость сосудистого легочного барьера, что позволяет предположить, что гельсолин играет важную роль в ответе на повреждение легких. [15]
Связанные белки [ править ]
| Гельсолин-подобный домен | |
|---|---|
3FG7 ; Домен виллина-1 6: гельсолиноподобный домен. Длинная спираль прямая, что соответствуетформе гельсолина, активированнойCa 2+ . [16] | |
| Идентификаторы | |
| Условное обозначение | ? |
Сравнение последовательностей указывает на эволюционную взаимосвязь между гельсолином, виллином , фрагмином и северином . [17] Шесть больших повторяющихся сегментов встречаются в гельсолине и виллине, а 3 аналогичных сегмента - в северине и фрагмине. Множественные повторы связаны по структуре (но не последовательно) с доменом ADF-H , образуя суперсемейство ( InterPro : IPR029006 ). Семьи по- видимому, развивались из родового последовательности от 120 до 130 аминокислотных остатков . [17] [4]
Археи Асгарда кодируют многие функциональные гельсолины. [18]
Взаимодействия [ править ]
Гельсолин представляет собой цитоплазматический , регулируемый кальцием, модулирующий актин белок, который связывается с зазубренными концами актиновых филаментов, предотвращая обмен мономеров (блокирование концов или кэппинг). [19] Он может способствовать зародышеобразованию (сборке мономеров в филаменты), а также разъединять существующие филаменты . Кроме того, этот белок с высоким сродством связывается с фибронектином . Плазменный гельзолин и цитоплазматический гельзолин происходят из одного гена путем чередования сайтов инициации и дифференциального сплайсинга . [7]
Гельсолин взаимодействует с:
- Белок-предшественник амилоида , [20]
- Рецептор андрогенов , [21]
- PTK2B , [22] и
- VDAC1 . [13]
См. Также [ править ]
- Плазменный гельзолин
- Кортактин
- Виллин
- Супервиллин
- Амилоидоз финского типа
Ссылки [ править ]
- ^ a b c GRCm38: выпуск Ensembl 89: ENSMUSG00000026879 - Ensembl , май 2017 г.
- ^ "Human PubMed Reference:" . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ a b Ghoshdastider U, Popp D, Burtnick LD, Robinson RC (ноябрь 2013 г.). «Расширяющееся суперсемейство белков домена гомологии гельсолина». Цитоскелет . 70 (11): 775–95. DOI : 10.1002 / cm.21149 . PMID 24155256 . S2CID 205643538 .
- ^ a b Sun HQ, Ямамото М., Мехиллано М., Инь Х.Л. (ноябрь 1999 г.). «Гельсолин, многофункциональный белок, регулирующий актин» . Журнал биологической химии . 274 (47): 33179–82. DOI : 10.1074 / jbc.274.47.33179 . PMID 10559185 .
- ^ a b Koya RC, Fujita H, Shimizu S, Ohtsu M, Takimoto M, Tsujimoto Y, Kuzumaki N (май 2000 г.). «Гельсолин подавляет апоптоз, блокируя потерю потенциала митохондриальной мембраны и высвобождение цитохрома с» . Журнал биологической химии . 275 (20): 15343–9. DOI : 10.1074 / jbc.275.20.15343 . PMID 10809769 .
- ^ a b Kwiatkowski DJ, Stossel TP, Orkin SH, Mole JE, Colten HR, Yin HL (1986-10-02). «Гельсолины плазмы и цитоплазмы кодируются одним геном и содержат дублированный актин-связывающий домен». Природа . 323 (6087): 455–8. Bibcode : 1986Natur.323..455K . DOI : 10.1038 / 323455a0 . PMID 3020431 . S2CID 4356162 .
- ^ Наг S, M Ларссон, Robinson RC, Burtnick LD (июль 2013). «Гельсолин: хвост молекулярной гимнастки» . Цитоскелет . 70 (7): 360–84. DOI : 10.1002 / cm.21117 . PMID 23749648 . S2CID 23646422 .
- ^ a b Kiselar JG, Janmey PA, Almo SC, Chance MR (апрель 2003 г.). «Визуализация Ca2 + -зависимой активации гельсолина с помощью синхротронного отпечатка стопы» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (7): 3942–7. Bibcode : 2003PNAS..100.3942K . DOI : 10.1073 / pnas.0736004100 . PMC 153027 . PMID 12655044 .
- ^ a b c d Yu FX, Sun HQ, Janmey PA, Yin HL (июль 1992 г.). «Идентификация полифосфоинозитид-связывающей последовательности в актиновом мономер-связывающем домене гельсолина». Журнал биологической химии . 267 (21): 14616–21. PMID 1321812 .
- ^ a b Буртник Л.Д., Уросев Д., Ироби Э., Нараян К., Робинсон Р.К. (июль 2004 г.). «Структура N-концевой половины гельсолина, связанного с актином: роль в разделении, апоптозе и FAF» . Журнал EMBO . 23 (14): 2713–22. DOI : 10.1038 / sj.emboj.7600280 . PMC 514944 . PMID 15215896 .
- ^ Варон С, Tatin Ж, Moreau В, Ван Obberghen-Шиллинг Е, Фернандес-Соз S, Reuzeau Е, и др. (Май 2006 г.). «Трансформирующий фактор роста бета индуцирует розетки подосом в первичных эндотелиальных клетках аорты» . Молекулярная и клеточная биология . 26 (9): 3582–94. DOI : 10.1128 / MCB.26.9.3582-3594.2006 . PMC 1447430 . PMID 16611998 .
- ^ а б Кусано Х., Симидзу С., Коя Р.С., Фудзита Х., Камада С., Кузумаки Н., Цудзимото Ю. (октябрь 2000 г.). «Человеческий гельзолин предотвращает апоптоз, подавляя апоптотические митохондриальные изменения посредством закрытия VDAC» . Онкоген . 19 (42): 4807–14. DOI : 10.1038 / sj.onc.1203868 . PMID 11039896 .
- ^ a b Witke W, Sharpe AH, Hartwig JH, Azuma T, Stossel TP, Kwiatkowski DJ (апрель 1995 г.). «Гемостатический, воспалительный и фибробластный реакции притуплены у мышей, лишенных гельсолина» . Cell . 81 (1): 41–51. DOI : 10.1016 / 0092-8674 (95) 90369-0 . PMID 7720072 .
- ^ Becker PM, Кази AA, Wadgaonkar R, Пирса DB, Квятковский D, Гарсиа JG (апрель 2003). «Легочная сосудистая проницаемость и ишемическое повреждение у мышей с дефицитом гельсолина». Американский журнал респираторной клетки и молекулярной биологии . 28 (4): 478–84. DOI : 10,1165 / rcmb.2002-0024OC . PMID 12654637 .
- ^ Ван Х, Чумнарнсилпа С., Лунчанта А., Ли Кью, Куан Ю.М., Робин С. и др. (Август 2009 г.). «Выпрямление спирали как механизм активации в суперсемействе гельсолинов регуляторных белков актина» . Журнал биологической химии . 284 (32): 21265–9. DOI : 10.1074 / jbc.M109.019760 . PMC 2755850 . PMID 19491107 .
- ^ a b Way M, Weeds A (октябрь 1988 г.). «Нуклеотидная последовательность гельсолина плазмы свиньи. Сравнение белковой последовательности гельсолина человека и других актин-расщепляющих белков показывает сильную гомологию и доказательства наличия больших внутренних повторов». Журнал молекулярной биологии . 203 (4): 1127–33. DOI : 10.1016 / 0022-2836 (88) 90132-5 . PMID 2850369 .
- ^ Akıl C, Tran LT, Orhant-Prioux M, Баскаран Y, Manser E, Blanchoin L, Robinson RC (август 2020). «Понимание эволюции регулируемой динамики актина посредством характеристики примитивных белков гельсолина / кофилина из архей Асгарда» . Труды Национальной академии наук Соединенных Штатов Америки . 117 (33): 19904–19913. DOI : 10.1073 / pnas.2009167117 . PMC 7444086 . PMID 32747565 .
- Перейти ↑ Weeds AG, Gooch J, Pope B, Harris HE (ноябрь 1986). «Приготовление и характеристика свиной плазмы и гельсолинов тромбоцитов» . Европейский журнал биохимии . 161 (1): 69–76. DOI : 10.1111 / j.1432-1033.1986.tb10125.x . PMID 3023087 .
- ^ Чаухан В.П., Луч I, Чаухан A, Вишневский HM (май 1999). «Связывание гельсолина, секреторного белка, с бета-амилоидным белком». Сообщения о биохимических и биофизических исследованиях . 258 (2): 241–6. DOI : 10.1006 / bbrc.1999.0623 . PMID 10329371 .
- ^ Nishimura K, Ting HJ, Harada Y, Tokizane T, Nonomura N, Kang HY и др. (Август 2003 г.). «Модуляция трансактивации рецептора андрогена гелзолином: недавно идентифицированный корегулятор рецептора андрогена». Исследования рака . 63 (16): 4888–94. PMID 12941811 .
- ^ Ван Q, Xie Y, Du QS, Wu XJ, Feng X, Mei L и др. (Февраль 2003 г.). «Регулирование образования остеокластических колец актина с помощью богатой пролином тирозинкиназы 2, взаимодействующей с гельсолином» . Журнал клеточной биологии . 160 (4): 565–75. DOI : 10,1083 / jcb.200207036 . PMC 2173747 . PMID 12578912 .
Внешние ссылки [ править ]
- Gelsolin в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- http://www.bioaegistherapeutics.com