 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Лорбрена, Лорвика |
| Другие названия | PF-6463922 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a619005 |
| Данные лицензии |
|
Категория беременности |
|
| Пути администрирования | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Биодоступность | 81% |
| Связывание с белками | 66% |
| Метаболизм | В основном CYP3A4 и UGT1A4 |
| Ликвидация Период полураспада | 24 часа (разовая доза) |
| Экскреция | 48% мочи (<1% без изменений), 41% фекалий (9% без изменений) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ECHA InfoCard | 100.245.079 |
| Химические и физические данные | |
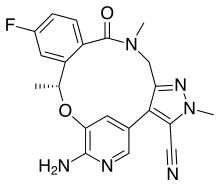
| Формула | C 21 H 19 F N 6 O 2 |
| Молярная масса | 406,421 г · моль -1 |
| 3D модель ( JSmol ) |
|
Улыбки
| |
ИнЧИ
| |
Лорлатиниб , продаваемый под торговой маркой Lorbrena в США, Канаде и Японии, и Lorviqua в Европейском союзе, представляет собой противораковый препарат, разработанный Pfizer . Это пероральный ингибитор ALK и ROS1 , двух ферментов, которые играют роль в развитии рака. [1]
Медицинское использование [ править ]
Лорлатиниб одобрен в США и Европе для лечения второй или третьей линии ALK-положительного метастатического немелкоклеточного рака легкого (НМРЛ). [2] [3] [1]
Противопоказания [ править ]
Лорлатиниб нельзя комбинировать с сильными индукторами (т.е. активаторами) печеночных ферментов CYP3A4 / 5, если этого можно избежать, поскольку наблюдались серьезные случаи токсического воздействия на печень при комбинации с рифампицином, индуктором CYP3A4 / 5 . [4] [5]
Побочные эффекты [ править ]
Наиболее частыми побочными эффектами в исследованиях были высокий уровень холестерина в крови (84% пациентов), высокий уровень триглицеридов в крови (67%), отеки (55%), периферическая невропатия (48%), когнитивные эффекты (29%), усталость (28%). ), набор веса (26%) и эффекты настроения (23%). Серьезные побочные эффекты привели к снижению дозы у 23% пациентов и к прекращению лечения лорлатинибом у 3% пациентов. [4] [5]
Взаимодействия [ править ]
Лорлатиниб метаболизируется ферментами CYP3A4 / 5. Следовательно, индукторы CYP3A4 / 5, такие как рифампицин, карбамазепин или зверобой, снижают его концентрацию в плазме крови и могут снизить его эффективность. Кроме того, в исследованиях комбинация лорлатиниба с рифампицином показала токсичность для печени. Ингибиторы этих ферментов, такие как кетоконазол или грейпфрутовый сок, увеличивают концентрацию лорлатиниба в плазме, что приводит к более высокой токсичности. Лорлатиниб также является (умеренным) индуктором CYP3A4 / 5, поэтому препараты, метаболизируемые этими ферментами, расщепляются быстрее в сочетании с лорлатинибом. Примеры включают мидазолам и циклоспорин .[4] [5]
Взаимодействие через другие ферменты изучено только in vitro . Согласно этим результатам, лорлатиниб может ингибировать CYP2C9 , UGT1A1 и некоторые транспортные белки , индуцировать CYP2B6 и, вероятно, не оказывает существенного влияния на CYP1A2 . [5]
Фармакология [ править ]
Механизм действия [ править ]
Lorlatinib является небольшая молекула ингибитора киназы из ALK и ROS1 , а также ряд других киназ . Он активен in vitro против многих мутировавших форм ALK. [4]
Фармакокинетика [ править ]
Препарат принимают внутрь в виде таблеток. Максимальная концентрация в плазме крови достигается через 1,2 часа после однократного приема или через 2 часа после приема при регулярном приеме. Его абсолютная биодоступность составляет 80,8%. Прием с жирной пищей увеличивает ее доступность на 5%, что не считается клинически значимым. Находясь в кровотоке, 66% вещества связывается с белками плазмы . [4] [5] Лорлатиниб способен преодолевать гематоэнцефалический барьер . [7]
Лорлатиниб инактивируется путем окисления , главным образом, через CYP3A4, и путем глюкуронизации , в основном, через UGT1A4 . Другие CYP и UGT играют второстепенную роль. Лорлатиниб и его метаболиты выводятся с периодом полувыведения 23,6 часа после однократного приема; 47,7% в мочу (из которых менее 1% в неизмененном виде) и 40,9% в фекалии (9,1% в неизмененном виде). [5]
Химия [ править ]
Лорлатиниб представляет собой порошок от белого до кремового цвета. Он имеет высокую растворимость в 0,1 М соляной кислоте и очень низкую растворимость при pH более 4,5. [6]
История [ править ]
Клинические исследования [ править ]
Этот раздел необходимо обновить . ( Сентябрь 2019 г. ) |
Несколько клинических испытаний продолжаются. Ожидается, что в конце 2017 года будет завершено исследование фазы II, сравнивающее авелумаб отдельно и в комбинации с лорлатинибом или кризотинибом для лечения немелкоклеточного рака легкого. Ожидается, что исследование фазы II по сравнению лорлатиниба с кризотинибом будет завершено в середине 2018 года. [8] Испытания фазы II по лечению ALK-положительного или ROS1-положительного немелкоклеточного рака легкого с метастазами в центральную нервную систему не будут завершены до 2023 года. [9] Доклинические исследования изучают лорлатиниб для лечения нейробластомы. .
В 2017 году компания Pfizer объявила, что лорлатиниб обладает активностью в отношении опухолей легких и головного мозга у людей с ALK или ROS1-положительным распространенным немелкоклеточным раком легкого. [10]
Утверждение [ править ]
В 2015 году FDA предоставило Pfizer статус орфанного препарата лорлатинибу для лечения НМРЛ. [11] В 2018 году FDA одобрило лорталиниб для лечения ALK-положительного метастатического НМРЛ второй или третьей линии. [2] В феврале 2019 года Европейский ЧМП из ЕМА рекомендовал предоставление условного разрешения на продажу. [12] В мае 2019 года Европейская комиссия одобрила лорлатиниб для 28 стран ЕС, а также в качестве препарата второй или третьей линии. [3] [13]
Ссылки [ править ]
- ^ а б Нагасака М., Гэ Й, Сукари А., Кукреджа Г., Оу С.И. (июль 2020 г.). «Руководство пользователя лорлатиниба» . Критические обзоры в онкологии / гематологии . 151 : 102969. DOI : 10.1016 / j.critrevonc.2020.102969 . PMID 32416346 .
- ^ a b «FDA одобряет лорлатиниб для лечения ALK-положительного метастатического НМРЛ второй или третьей линии» . FDA . 2019-12-20.
- ^ a b «Европейская комиссия одобряет LORVIQUA (лорлатиниб) для некоторых взрослых пациентов с ранее леченным ALK-положительным продвинутым немелкоклеточным раком легкого, PM Pfizer, 7 мая 2019 г.» . pfizer.com . Дата обращения 15 мая 2019 .
- ^ a b c d e FDA Professional Drug Information on Lorbrena.
- ^ a b c d e f "Lorviqua: EPAR - Информация о продукте" (PDF) . Европейское агентство по лекарственным средствам . 2019-06-17.
- ^ a b «Lorviqua: EPAR - Отчет об общественной оценке» (PDF) . Европейское агентство по лекарственным средствам . 2019-06-17.
- ^ "Лорлатиниб" . Словарь лекарств NCI . Национальный институт рака. 2011-02-02.
- ^ Номер клинического испытания NCT01970865 для "Изучение ингибитора ALK / ROS1 PF-06463922 у пациентов с развитым немелкоклеточным раком легкого со специфическими молекулярными изменениями" на ClinicalTrials.gov
- ^ Номер клинического испытания NCT02927340 "Исследование лорлатиниба при раке легких с перестройкой ALK и ROS1 с метастазами в ЦНС при отсутствии поддающихся измерению экстракраниальных поражений" на ClinicalTrials.gov
- ^ "IASLC 2017: Лорлатиниб в ALK- положительном и ROS1-положительном позднем немелкоклеточном раке легкого" . Почта ASCO . 17 октября 2017.
- ^ "Лорлатиниб" . drugspider.com .
- ^ «Положительное мнение EMA - Lorviqua, 28 февраля 2019 г.» . ema.europa.eu . Дата обращения 15 мая 2019 .
- ^ Syed YY (январь 2019). «Лорлатиниб: первое глобальное одобрение». Наркотики . 79 (1): 93–98. DOI : 10.1007 / s40265-018-1041-0 . PMID 30604291 .
Внешние ссылки [ править ]
- «Лорлатиниб» . Информационный портал о наркотиках . Национальная медицинская библиотека США.