Азотный цикл представляет собой биохимический цикл , по которому азот превращается в нескольких химических формах , как она циркулирует среди атмосферы , наземных и морских экосистем . Конверсия азота может осуществляться как биологическими, так и физическими способами. Важные процессы в азотном цикле включают фиксацию , аммонификацию , нитрификацию и денитрификацию . Большинство атмосферы Земли (78%) является атмосферным азотом , [16]что делает его крупнейшим источником азота. Однако атмосферный азот имеет ограниченную доступность для биологического использования, что приводит к нехватке пригодного для использования азота во многих типах экосистем .
Азотный цикл представляет особый интерес для экологов, потому что доступность азота может влиять на скорость основных экосистемных процессов, включая первичное производство и разложение . Деятельность человека, такая как сжигание ископаемого топлива, использование искусственных азотных удобрений и выброс азота в сточные воды, резко изменила глобальный цикл азота . [17] [18] [19] Изменение глобального круговорота азота человеком может отрицательно сказаться на системе окружающей среды, а также на здоровье человека. [20] [21]
Процессы
Азот присутствует в окружающей среде в самых разных химических формах, включая органический азот, аммоний (NH+
4), нитрит (NO-
2), нитрат (NO-
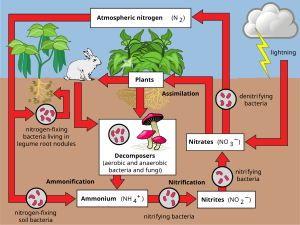
3), закись азота (N 2 O), оксид азота (NO) или неорганический газообразный азот (N 2 ). Органический азот может находиться в форме живого организма, гумуса или в промежуточных продуктах разложения органических веществ. Процессы в круговороте азота заключаются в преобразовании азота из одной формы в другую. Многие из этих процессов выполняются микробами , стремясь собрать энергию или накапливать азот в форме, необходимой для их роста. Например, азотсодержащие отходы в моче животных расщепляются нитрифицирующими бактериями.в почве для использования растениями. На диаграмме показано, как эти процессы сочетаются друг с другом и образуют азотный цикл.
Фиксация азота
Преобразование газообразного азота (N 2 ) в нитраты и нитриты посредством атмосферных, промышленных и биологических процессов называется азотфиксацией. Атмосферный азот должен быть переработан, или « закреплен », в пригодную для использования форму, чтобы растения могли усвоить его. От 5 до 10 миллиардов кг в год фиксируется ударами молнии , но большая часть фиксации осуществляется свободноживущими или симбиотическими бактериями, известными как диазотрофы . У этих бактерий есть фермент нитрогеназа, который объединяет газообразный азот с водородом для производства аммиака , который бактерии превращают в другие органические соединения.. В большинстве случаев биологическая фиксация азота происходит за счет активности Mo-нитрогеназы, обнаруженной у самых разных бактерий и некоторых архей . Mo-нитрогеназа - это сложный двухкомпонентный фермент, который имеет несколько металлсодержащих простетических групп. [22] Примером свободноживущих бактерий является Azotobacter . Симбиотические азотфиксирующие бактерии, такие как Rhizobium, обычно живут в корневых клубеньках бобовых (таких как горох, люцерна и деревья акации). Здесь они образуют мутуалистические отношения с растением, производя аммиак в обмен на углеводы.. Из-за этой связи бобовые часто повышают содержание азота в бедных азотом почвах. Некоторые небобовые растения также могут образовывать такие симбиозы . На сегодняшний день, около 30% от общего фиксированного азота производится в промышленности с использованием Haber-Bosch процесса, [23] , который использует высокие температуры и давление газа для преобразования азота и источник водорода (природный газ или нефти) в аммиак. [24]
Ассимиляция
Растения могут поглощать нитраты или аммоний из почвы корневыми волосками. Если нитрат абсорбируется, он сначала восстанавливается до нитрит-ионов, а затем до ионов аммония для включения в аминокислоты, нуклеиновые кислоты и хлорофилл. У растений, которые находятся в симбиотических отношениях с ризобиями, часть азота ассимилируется в виде ионов аммония непосредственно из клубеньков. Теперь известно, что существует более сложный круговорот аминокислот между бактероидами Rhizobia и растениями. Растение обеспечивает бактероидами аминокислоты, поэтому ассимиляция аммиака не требуется, и бактероиды передают аминокислоты (с вновь зафиксированным азотом) обратно в растение, таким образом формируя взаимозависимые отношения. [25] Хотя многие животные, грибы и другие гетеротрофныеорганизмы получают азот путем проглатывания аминокислот , нуклеотидов и других небольших органических молекул, другие гетеротрофы (включая многие бактерии ) способны использовать неорганические соединения, такие как аммоний, в качестве единственных источников азота. Использование различных источников азота тщательно регулируется всеми организмами.
Аммонификация
Когда растение или животное умирает, или животное выбрасывает отходы, исходная форма азота - органическая . Бактерии или грибки превращают органический азот в останках обратно в аммоний ( ), этот процесс называется аммонификацией или минерализацией . Участвующие ферменты:
- GS: Gln-синтетаза (цитозольная и пластическая)
- GOGAT: Glu 2-оксоглутарат аминотрансфераза ( ферредоксин и НАДН-зависимая)
- GDH: Glu дегидрогеназа:
- Незначительная роль в усвоении аммония.
- Важен в катаболизме аминокислот.
Нитрификация
Превращение аммония в нитрат осуществляется прежде всего почвенными бактериями и другими нитрифицирующими бактериями. На первичной стадии нитрификации окисление аммония (NH+
4) осуществляется такими бактериями, как виды Nitrosomonas , которые превращают аммиак в нитриты ( NO- 2). Другие виды бактерий, такие как Nitrobacter , ответственны за окисление нитритов ( NO- 2) в нитраты ( NO- 3). Это важно для аммиака ( NH
3) для преобразования в нитраты или нитриты, поскольку газообразный аммиак токсичен для растений.
Из-за их очень высокой растворимости и из-за того, что почвы очень неспособны удерживать анионы , нитраты могут попадать в грунтовые воды . Повышенное содержание нитратов в грунтовых водах вызывает беспокойство при использовании питьевой воды, поскольку нитраты могут влиять на уровень кислорода в крови у младенцев и вызывать метгемоглобинемию или синдром голубого ребенка. [28] Там, где грунтовые воды пополняют сток ручья, обогащенные нитратами грунтовые воды могут способствовать эвтрофикации., процесс, который приводит к высокой популяции и росту водорослей, особенно популяций сине-зеленых водорослей. Хотя нитрат не является прямым токсичным для рыб, как аммиак, он может оказывать косвенное воздействие на рыбу, если способствует эвтрофикации. Азот вызывает серьезные проблемы эвтрофикации в некоторых водоемах. С 2006 года внесение азотных удобрений все больше контролируется в Великобритании и США. Это происходит по той же схеме, что и контроль фосфорных удобрений, ограничение которых обычно считается необходимым для восстановления заболоченных водоемов.
Денитрификация
Денитрификация - это восстановление нитратов обратно в газообразный азот (N 2 ), завершающее азотный цикл. Этот процесс выполняется такими видами бактерий, как Pseudomonas и Paracoccus , в анаэробных условиях. Они используют нитрат в качестве акцептора электронов вместо кислорода во время дыхания. Эти факультативно (то есть необязательно) анаэробные бактерии также могут жить в аэробных условиях. Денитрификация происходит в анаэробных условиях, например, в заболоченных почвах. Денитрифицирующие бактерии используют нитраты в почве для дыхания и, следовательно, производят газообразный азот, который инертен и недоступен для растений.
Диссимиляционное восстановление нитрата до аммония
Диссимиляционное восстановление нитратов до аммония (DNRA) или аммификация нитратов / нитритов - это анаэробный процесс дыхания . Микробы, которые участвуют в DNRA, окисляют органическое вещество и используют нитрат в качестве акцептора электронов, восстанавливая его до нитрита , а затем до аммония (NO 3 - → NO 2 - → NH 4 + ). [29] Как денитрифицирующие, так и нитратные аммонифицирующие бактерии будут конкурировать за нитраты в окружающей среде, хотя DNRA стремится сохранить биодоступный азот в виде растворимого аммония, а не производить газообразный азот. [30]
Анаэробное окисление аммиака
В этом биологическом процессе нитрит и аммиак превращаются непосредственно в газообразный молекулярный азот (N 2 ). Этот процесс составляет основную долю превращения азота в океанах. Сбалансированная формула этой химической реакции " анаммокс ": NH+
4 + НЕТ-
2→ N 2 + 2H 2 O (Δ G ° =−357 кДж⋅моль −1 ). [31]
Другие процессы
Хотя азотфиксация является основным источником доступного для растений азота в большинстве экосистем , в районах с богатыми азотом коренными породами разрушение этой породы также служит источником азота. [32] [33] [34] Восстановление нитратов также является частью цикла железа. В бескислородных условиях Fe (II) может отдавать электрон NO 3 - и окисляется до Fe (III), а NO 3 - восстанавливается до NO. 2 - , N 2 O, N 2 и NH 4 + в зависимости от условий и затронутых видов микробов. [35]
Морской азотный цикл
Круговорот азота также является важным процессом в океане. Хотя общий цикл похож, существуют различные участники [36] и способы переноса азота в океане. Азот входит в воду через осадки, сток, или как Н 2 из атмосферы. Фитопланктон не может использовать азот в виде N 2, поэтому он должен подвергаться азотфиксации, которая осуществляется преимущественно цианобактериями . [37] Без поставок фиксированного азота, входящего в морской цикл, фиксированный азот будет израсходован примерно через 2000 лет. [38]Фитопланктону необходим азот в биологически доступных формах для первоначального синтеза органического вещества. Аммиак и мочевина попадают в воду в результате выделения из планктона. Источники азота удаляются из эвфотической зоны за счет нисходящего движения органического вещества. Это может происходить в результате опускания фитопланктона, вертикального перемешивания или опускания отходов вертикальных мигрантов. В результате опускания аммиак попадает на более низкие глубины ниже эвфотической зоны. Бактерии способны превращать аммиак в нитриты и нитраты, но они подавляются светом, поэтому это должно происходить ниже эвфотической зоны. [39] Аммонификация или минерализация осуществляется бактериями для преобразования органического азота в аммиак. Нитрификациязатем может произойти преобразование аммония в нитрит и нитрат. [40] Нитраты могут быть возвращены в эвфотическую зону путем вертикального перемешивания и апвеллинга, где они могут быть поглощены фитопланктоном для продолжения цикла. N 2 можно вернуть в атмосферу посредством денитрификации .
Аммоний считается предпочтительным источником фиксированного азота для фитопланктона, поскольку его ассимиляция не включает окислительно-восстановительную реакцию и поэтому требует мало энергии. Для ассимиляции нитратов требуется окислительно-восстановительная реакция, но их больше, поэтому большинство фитопланктона адаптировались к ферментам, необходимым для этого восстановления ( нитратредуктаза ). Есть несколько примечательных и хорошо известных исключений, среди которых большинство Prochlorococcus и некоторые Synechococcus, которые могут поглощать только азот в виде аммония. [38]
Питательные вещества в океане распределены неравномерно. Области апвеллинга обеспечивают поступление азота снизу эвфотической зоны. Прибрежные зоны обеспечивают азотом сток, и вдоль побережья легко происходит апвеллинг. Однако скорость поглощения азота фитопланктоном снижается в олиготрофных водах круглый год и в умеренных водах летом, что приводит к снижению первичной продукции. [41] Распределение различных форм азота также варьируется в океанах.
Нитраты обеднены в приповерхностных водах, за исключением районов апвеллинга. Прибрежные районы апвеллинга обычно имеют высокий уровень нитратов и хлорофилла в результате увеличения производства. Однако есть области с высоким содержанием нитратов на поверхности, но с низким содержанием хлорофилла, которые называются областями HNLC (с высоким содержанием азота и низким содержанием хлорофилла). Лучшее объяснение для регионов HNLC связано с дефицитом железа в океане, который может играть важную роль в динамике океана и круговоротах питательных веществ. Поступление железа варьируется в зависимости от региона и доставляется в океан с пылью (от пыльных бурь) и выщелачивается из горных пород. Железо рассматривается как истинный элемент, ограничивающий продуктивность экосистемы океана.
Аммоний и нитрит показывают максимальную концентрацию на высоте 50–80 м (нижний конец эвфотической зоны) с уменьшающейся концентрацией ниже этой глубины. Это распределение можно объяснить тем фактом, что нитрит и аммоний являются промежуточными частицами. Они оба быстро производятся и потребляются через толщу воды. [38] Количество аммония в океане примерно на 3 порядка меньше, чем нитрата. [38] Среди аммония, нитрита и нитрата нитрит имеет самую быструю скорость оборота. Может образовываться при ассимиляции нитратов, нитрификации и денитрификации; однако он сразу же снова потребляется.
Новый и регенерированный азот
Азот, поступающий в эвфотическую зону, называется новым азотом, потому что он вновь поступает из-за пределов продуктивного слоя. [37] Новый азот может поступать из-под эвфотической зоны или из внешних источников. Внешние источники поднимаются из-за глубокой воды и азотфиксации. Если органическое вещество съедается, вдыхается, доставляется в воду в виде аммиака и повторно включается в органическое вещество фитопланктоном, это считается переработанным / регенерированным продуктом.
Новое производство - важная составляющая морской среды. Одна из причин заключается в том, что только постоянное поступление нового азота может определить общую способность океана производить устойчивый улов рыбы. [41] Промысел рыбы на участках с регенерированным азотом приведет к уменьшению азота и, следовательно, к снижению первичной продукции. Это отрицательно скажется на системе. Однако, если рыбу вылавливают с участков с новым азотом, азот будет восполнен.
Влияние человека на круговорот азота
В результате экстенсивного выращивания бобовых (особенно сои , люцерны и клевера ), растущего использования процесса Габера – Боша при создании химических удобрений и загрязнения от транспортных средств и промышленных предприятий, человечество более чем вдвое увеличило годовой объем производства. перевод азота в биологически доступные формы. [28] Кроме того, люди внесли значительный вклад в перенос газовых примесей азота с Земли в атмосферу и с суши в водные системы. Изменения человеком глобального азотного цикла наиболее интенсивны в развитых странах и в Азии, где выбросы транспортных средств и промышленное сельское хозяйство наиболее высоки. [42]
Производство Nr, реактивного азота , увеличилось более чем в 10 раз за последнее столетие из-за глобальной индустриализации . [2] [43] Эта форма азота каскадом проходит через биосферу с помощью различных механизмов и накапливается по мере того, как скорость его образования превышает скорость денитрификации . [44]
Закись азота (N 2 O) поднялась в атмосфере в результате сельскохозяйственных удобрений, сжигания биомассы, скота и откормочных площадок, а также промышленных источников. [45] N 2 O оказывает пагубное воздействие на стратосферу , где он разрушается и действует как катализатор разрушения атмосферного озона . Закись азота также является парниковым газом и в настоящее время является третьим по величине источником глобального потепления после диоксида углерода и метана.. Хотя он не так богат в атмосфере, как углекислый газ, при эквивалентной массе он почти в 300 раз сильнее по своей способности согревать планету. [46]
Аммиак (NH 3 ) в атмосфере утроился в результате деятельности человека. Это реагент в атмосфере, где он действует как аэрозоль , ухудшая качество воздуха и цепляясь за капли воды, что в конечном итоге приводит к образованию азотной кислоты ( H NO 3 ), которая вызывает кислотный дождь . Атмосферный аммиак и азотная кислота также повреждают органы дыхания.
Очень высокая температура молнии, естественно, производит небольшие количества NO x , NH 3 и HNO 3 , но высокотемпературное горение способствовало увеличению потока NO x в атмосферу в 6 или 7 раз . Его образование зависит от температуры сгорания: чем выше температура, тем больше NO x образуется. Основной вклад вносит сжигание ископаемого топлива , но также биотопливо и даже сжигание водорода. Однако скорость, с которой водород непосредственно впрыскивается в камеры сгорания двигателей внутреннего сгорания, можно регулировать, чтобы предотвратить более высокие температуры сгорания, которые производят NO x .
Аммиак и оксиды азота активно изменяют химию атмосферы . Они являются предшественниками образования озона в тропосфере (нижние слои атмосферы), который способствует образованию смога и кислотных дождей , повреждает растения и увеличивает поступление азота в экосистемы. Экосистемные процессы могут усиливаться за счет азотных удобрений , но антропогенное воздействие может также привести к насыщению азотом, что снижает продуктивность и может нанести ущерб здоровью растений, животных, рыб и людей. [28]
Уменьшение биоразнообразия может также произойти, если более высокая доступность азота увеличивает потребность в азоте трав, вызывая деградацию бедных азотом пустошей с разнообразием видов . [47]
Последствия модификации азотного цикла у человека
Воздействие на природные системы
Показано, что возрастающие уровни осаждения азота имеют ряд негативных последствий как для наземных, так и для водных экосистем. [48] [49] Азотные газы и аэрозоли могут быть непосредственно токсичными для определенных видов растений, влияя на наземную физиологию и рост растений вблизи крупных точечных источников загрязнения азотом. Изменения видов растений также могут происходить, поскольку накопление соединений азота увеличивает их доступность в данной экосистеме, в конечном итоге изменяя видовой состав, разнообразие растений и круговорот азота. Аммиак и аммоний - две восстановленные формы азота - со временем могут нанести вред из-за повышенной токсичности для чувствительных видов растений [50].особенно те, которые привыкли использовать нитраты в качестве источника азота, вызывая плохое развитие их корней и побегов. Повышенное осаждение азота также приводит к подкислению почвы, что увеличивает выщелачивание основных катионов в почве и количество алюминия и других потенциально токсичных металлов, наряду с уменьшением количества происходящей нитрификации и увеличением растительного опада. Из-за продолжающихся изменений, вызванных высоким уровнем осаждения азота, восприимчивость окружающей среды к экологическому стрессу и нарушениям, таким как вредители и патогены, может увеличиваться, что делает ее менее устойчивой к ситуациям, которые в противном случае оказали бы незначительное влияние на ее долгосрочную жизнеспособность.
Дополнительные риски, связанные с повышением доступности неорганического азота в водных экосистемах, включают подкисление воды; эвтрофикация пресноводных и морских систем; и вопросы токсичности для животных, включая человека. [51] Эвтрофикация часто приводит к снижению уровня растворенного кислорода в водной толще, включая гипоксические и аноксические условия, которые могут вызвать гибель водной фауны. Относительно сидячий бентос, или живущие на дне существа, особенно уязвимы из-за своей малоподвижности, хотя массовая гибель рыбы не является редкостью. Океанические мертвые зоны около устья Миссисипи в Мексиканском заливе являются хорошо известным примером гипоксии, вызванной цветением водорослей .[52] [53] Озера Адирондак в Нью-Йорке, Катскиллс , Гудзонское нагорье, плато Ренсселер и некоторые части Лонг-Айленда демонстрируют влияние выпадения азотно-кислотных дождевых осадков, в результате чего погибает рыба и многие другие водные виды. [54]
Аммиак (NH 3 ) очень токсичен для рыб, поэтому необходимо тщательно контролировать уровень аммиака, сбрасываемого из очистных сооружений. Чтобы предотвратить гибель рыб, часто желательна нитрификация путем аэрации перед сливом. Применение земли может быть привлекательной альтернативой аэрации.
Воздействие на здоровье человека: накопление нитратов в питьевой воде.
Утечка Nr (реактивного азота) в результате деятельности человека может вызвать накопление нитратов в естественной водной среде, что может оказать вредное воздействие на здоровье человека. Чрезмерное использование азотных удобрений в сельском хозяйстве было одним из основных источников загрязнения нитратами подземных и поверхностных вод. [55] [56] Благодаря своей высокой растворимости и низкому удерживанию почвой, нитраты могут легко уходить из подпочвенного слоя в грунтовые воды, вызывая загрязнение нитратами. Некоторые другие неточечные источникив качестве источника загрязнения грунтовых вод нитратами являются кормление скота, заражение животных и людей, а также бытовые и промышленные отходы. Поскольку грунтовые воды часто служат основным источником бытовой воды, загрязнение нитратами может распространяться от грунтовых вод на поверхностные и питьевые воды в процессе производства питьевой воды , особенно для небольших коммунальных систем водоснабжения, где используются плохо регулируемые и антисанитарные воды. [57]
Стандарт ВОЗ для питьевой воды составляет 50 мг NO 3 - л -1 для кратковременного воздействия и 3 мг NO 3 - л -1 для хронических эффектов. [58] После того, как он входит в человеческое тело, нитрат может вступать в реакцию с органическими соединениями через нитрозирование реакции в желудке , чтобы сформировать нитрозамин и nitrosamides , которые участвуют в некоторых видах рака (например, рак полости рта и рак желудка ). [59]
Воздействие на здоровье человека: качество воздуха
Деятельность человека также резко изменила глобальный круговорот азота за счет производства азотистых газов, что связано с глобальным загрязнением атмосферы азотом. Существует несколько источников атмосферных потоков химически активного азота (Nr). Сельскохозяйственные источники реактивного азота могут вызывать выбросы в атмосферу аммиака (NH 3) , оксидов азота (NO x ) и закиси азота (N 2 O). Процессы сжигания в производстве энергии, на транспорте и в промышленности также могут привести к образованию нового реактивного азота через выбросы NO x., непреднамеренные отходы. Когда эти химически активные атомы азота выбрасываются в нижние слои атмосферы, они могут вызвать образование смога, твердых частиц и аэрозолей, которые вносят основной вклад в неблагоприятное воздействие загрязнения воздуха на здоровье человека. [60] В атмосфере NO 2 может окисляться до азотной кислоты (HNO 3 ), и он может далее реагировать с NH 3 с образованием нитрата аммония, который способствует образованию определенного нитрата. Кроме того, NH 3 может реагировать с другими кислыми газами ( серной и соляной кислотами.) с образованием аммонийсодержащих частиц, которые являются предшественниками вторичных органических аэрозольных частиц в фотохимическом смоге . [61]
Смотрите также
- Планетарные границы
- Цикл фосфора - биогеохимический цикл, который описывает движение фосфора через литосферу, гидросферу и биосферу.
Рекомендации
- ↑ Фаулер, Дэвид; Койл, Мхайри; Скиба, Юте; Саттон, Марк А .; Кейп, Дж. Нил; Рейс, Стефан; Шеппард, Люси Дж .; Дженкинс, Алан; Гризетти, Бруна; Galloway, JN; Vitousek, P; Выщелачивание, А; Бауман, AF; Butterbach-Bahl, K; Дентенер, F; Стивенсон, Д; Аманн, М; Восс, М. (5 июля 2013 г.). «Глобальный круговорот азота в XXI веке» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 368 (1 621): 20130164. DOI : 10.1098 / rstb.2013.0164 . PMC 3682748 . PMID 23713126 .
- ^ a b Галлоуэй, Дж. Таунсенд, штат Арканзас; Эрисман, JW; Бекунда, М .; Cai, Z .; Френей, младший; Мартинелли, Луизиана; Зейтцингер, ИП; Саттон, Массачусетс (2008). «Трансформация цикла азота: последние тенденции, вопросы и возможные решения» (PDF) . Наука . 320 (5878): 889–892. Bibcode : 2008Sci ... 320..889G . DOI : 10.1126 / science.1136674 . ISSN 0036-8075 . PMID 18487183 . S2CID 16547816 . Архивировано (PDF) из оригинала 08.11.2011 . Получено 2019-09-23 .
- ^ Vitousek, PM; Менге, ДНЛ; Рид, Южная Каролина; Кливленд, CC (2013). «Биологическая фиксация азота: скорости, закономерности и экологический контроль в наземных экосистемах» . Философские труды Королевского общества B: биологические науки . 368 (1621): 20130119. DOI : 10.1098 / rstb.2013.0119 . ISSN 0962-8436 . PMC 3682739 . PMID 23713117 .
- ^ a b Voss, M .; Банге, HW; Диппнер, JW; Мидделбург, JJ; Монтойя, JP; Уорд, Б. (2013). «Морской азотный цикл: недавние открытия, неопределенности и потенциальное значение изменения климата» . Философские труды Королевского общества B: биологические науки . 368 (1 621): 20130121. DOI : 10.1098 / rstb.2013.0121 . ISSN 0962-8436 . PMC 3682741 . PMID 23713119 .
- ^ a b Фаулер, Дэвид; Койл, Мхайри; Скиба, Юте; Саттон, Марк А .; Кейп, Дж. Нил; Рейс, Стефан; Шеппард, Люси Дж .; Дженкинс, Алан; Гризетти, Бруна; Galloway, JN; Vitousek, P; Выщелачивание, А; Бауман, AF; Butterbach-Bahl, K; Дентенер, F; Стивенсон, Д; Аманн, М; Восс, М. (5 июля 2013 г.). «Глобальный круговорот азота в XXI веке» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 368 (+1621): 20130164. DOI : 10.1098 / rstb.2013.0164 . PMC 3682748 . PMID 23713126 .
- ^ Вуурен, Детлеф П. ван; Бауман, Лекс Ф; Смит, Стивен Дж; Дентенер, Франк (2011). «Глобальные прогнозы антропогенных выбросов химически активного азота в атмосферу: оценка сценариев в научной литературе». Текущее мнение в области экологической устойчивости . 3 (5): 359–369. DOI : 10.1016 / j.cosust.2011.08.014 . hdl : 1874/314192 . ISSN 1877-3435 .
- ^ Pilegaard, К. (2013). «Процессы регулирования выбросов оксида азота из почв» . Философские труды Королевского общества B: биологические науки . 368 (одна тысяча шестьсот двадцать один): 20130126. DOI : 10.1098 / rstb.2013.0126 . ISSN 0962-8436 . PMC 3682746 . PMID 23713124 .
- ^ Леви, H .; Moxim, WJ; Kasibhatla, PS (1996). «Глобальный трехмерный зависящий от времени источник молнии тропосферных NOx». Журнал геофизических исследований: атмосферы . 101 (D17): 22911–22922. Bibcode : 1996JGR ... 10122911L . DOI : 10.1029 / 96jd02341 . ISSN 0148-0227 .
- ^ Саттон, Массачусетс; Reis, S .; Риддик, С. Н.; Драгосиц, У .; Nemitz, E .; Теобальд, MR; Тан, Ю.С.; Брабан, CF; Виено, М. (2013). «На пути к парадигме выбросов и осаждения аммиака, зависящей от климата» . Философские труды Королевского общества B: биологические науки . 368 (тысяча шестьсот двадцать один): 20130166. DOI : 10.1098 / rstb.2013.0166 . ISSN 0962-8436 . PMC 3682750 . PMID 23713128 .
- ^ Дентенер, Ф .; Drevet, J .; Lamarque, JF; Бей, I .; Eickhout, B .; Fiore, AM; Hauglustaine, D .; Горовиц, LW; Крол, М. (2006). «Осаждение азота и серы в региональном и глобальном масштабе: многомодельная оценка». Глобальные биогеохимические циклы . 20 (4): н / д. Bibcode : 2006GBioC..20.4003D . DOI : 10.1029 / 2005GB002672 .
- ^ a b c Дуче, РА; LaRoche, J .; Altieri, K .; Арриго, КР; Бейкер, АР; Capone, DG; Cornell, S .; Дентенер, Ф .; Галлоуэй, Дж. (2008). «Воздействие атмосферного антропогенного азота на открытый океан» . Наука . 320 (5878): 893–897. Bibcode : 2008Sci ... 320..893D . DOI : 10.1126 / science.1150369 . ISSN 0036-8075 . PMID 18487184 . S2CID 11204131 .
- ^ Bouwman, L .; Goldewijk, KK; Ван дер Хук, KW; Beusen, AHW; Ван Вуурен, Д.П .; Willems, J .; Руфино, MC; Стефест, Э. (16 мая 2011 г.). «Изучение глобальных изменений в циклах азота и фосфора в сельском хозяйстве, вызванных животноводством за период 1900-2050 годов» . Труды Национальной академии наук . 110 (52): 20882–20887. DOI : 10.1073 / pnas.1012878108 . ISSN 0027-8424 . PMC 3876211 . PMID 21576477 .
- ^ Соломон, Сьюзен (2007). Изменение климата 2007: основы физических наук . Опубликовано для Межправительственной группы экспертов по изменению климата [издано] Cambridge University Press. ISBN 9780521880091. OCLC 228429704 .
- ^ Саттон, Марк А., редактор (2011-04-14). Европейская оценка азота: источники, эффекты и перспективы политики . ISBN 9781107006126. OCLC 690090202 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Дойч, Кертис; Сармьенто, Хорхе Л .; Сигман, Дэниел М .; Грубер, Николас; Данн, Джон П. (2007). «Пространственная взаимосвязь поступления и потерь азота в океане» . Природа . 445 (7124): 163–167. Bibcode : 2007Natur.445..163D . DOI : 10,1038 / природа05392 . ISSN 0028-0836 . PMID 17215838 . S2CID 10804715 .
- ^ Стивен Б. Кэрролл; Стивен Д. Солт (2004). Экология для садоводов . Timber Press. п. 93. ISBN 978-0-88192-611-8. Архивировано 01 февраля 2018 года . Проверено 23 октября 2016 .
- ^ Кайперс, МММ; Маршан, Гонконг; Картал, Б (2011). "Сеть микробного цикла азота" . Обзоры природы микробиологии . 1 (1): 1–14. DOI : 10.1038 / nrmicro.2018.9 . PMID 29398704 . S2CID 3948918 .
- ↑ Galloway, JN; и другие. (2004). «Азотные циклы: прошлые, настоящие и будущие поколения» . Биогеохимия . 70 (2): 153–226. DOI : 10.1007 / s10533-004-0370-0 . S2CID 98109580 .
- ^ Рейс, Стефан; Бекунда, Матите; Ховард, Клэр М; Каранджа, Нэнси; Винивартер, Вильфрид; Ян, Сяоюань; Бликер, Альберт; Саттон, Марк А (01.12.2016). «Обобщение и обзор: решение проблемы управления азотом: от глобального до местного масштаба» . Письма об экологических исследованиях . 11 (12): 120205. Bibcode : 2016ERL .... 11l0205R . DOI : 10.1088 / 1748-9326 / 11/12/120205 . ISSN 1748-9326 .
- ^ Гу, Баоцзин; Ге, Инь; Рен, юань; Сюй, Бен; Ло, Вэйдун; Цзян, Хун; Гу, Биньхэ; Чанг, Джи (17 августа 2012 г.). «Атмосферный реактивный азот в Китае: источники, последние тенденции и стоимость ущерба». Наука об окружающей среде и технологии . 46 (17): 9420–9427. Bibcode : 2012EnST ... 46.9420G . DOI : 10.1021 / es301446g . ISSN 0013-936X . PMID 22852755 .
- ^ Ким, Харьюн; Ли, Китак; Лим, Донг-Ил; Нам, Сын-Иль; Ким, Тэ Ук; Ян, Цзинь-Ю Т .; Ко, Ён Хо; Шин, Кён-Хун; Ли, Юнил (2017-05-11). «Широкое распространение антропогенного азота в отложениях северо-западной части Тихого океана». Наука об окружающей среде и технологии . 51 (11): 6044–6052. Bibcode : 2017EnST ... 51.6044K . DOI : 10.1021 / acs.est.6b05316 . ISSN 0013-936X . PMID 28462990 .
- ^ Мойр, JWB (редактор) (2011). Круговорот азота в бактериях: молекулярный анализ . Caister Academic Press . ISBN 978-1-904455-86-8.CS1 maint: дополнительный текст: список авторов ( ссылка )
- ^ Смит, Б., Р. Л. Ричардс и В. Е. Ньютон. 2004. Катализаторы азотфиксации: нитрогеназы, соответствующие химические модели и коммерческие процессы. Kluwer Academic Publishers, Дордрехт; Бостон.
- ^ Smil V (2000). Циклы жизни . Научная американская библиотека, Нью-Йорк.
- ^ Уилли, Joanne M. (2011). Микробиология Прескотта, 8-е изд . Нью-Йорк, штат Нью-Йорк: Макгроу Хилл. п. 705. ISBN 978-0-07-337526-7.
- ^ Спарацино-Уоткинс, Кортни; Штольц, Джон Ф .; Басу, Партха (2013-12-16). «Нитрат и периплазматические нитратредуктазы» . Chem. Soc. Ред . 43 (2): 676–706. DOI : 10.1039 / c3cs60249d . ISSN 1460-4744 . PMC 4080430 . PMID 24141308 .
- ^ Саймон, Йорг; Клотц, Мартин Г. (2013). «Разнообразие и эволюция биоэнергетических систем, вовлеченных в трансформации микробных соединений азота» . Biochimica et Biophysica Acta (BBA) - Биоэнергетика . 1827 (2): 114–135. DOI : 10.1016 / j.bbabio.2012.07.005 . PMID 22842521 .
- ^ a b c Витаусек, П.М. Абер, Дж; Ховарт, RW; Likens, GE; Matson, PA; Шиндлер, DW; Шлезингер, WH; Тильман, GD (1997). «Антропогенное изменение глобального круговорота азота: источники и последствия» (PDF) . Экологические приложения . 1 (3): 1–17. DOI : 10,1890 / 1051-0761 (1997) 007 [0737: HAOTGN] 2.0.CO; 2 . ЛВП : 1813/60830 . ISSN 1051-0761 .
- ^ Лам, Филлис и Кайперс, Марсель MM (2011). «Микробные азотные процессы в зонах минимального содержания кислорода». Ежегодный обзор морской науки . 3 : 317–345. Bibcode : 2011ARMS .... 3..317L . DOI : 10.1146 / annurev-marine-120709-142814 . PMID 21329208 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Маршант, HK, Lavik, Г., Holtappels, М. и Kuypers, МММ (2014). «Судьба нитратов в приливных проницаемых отложениях» . PLOS ONE . 9 (8): e104517. Bibcode : 2014PLoSO ... 9j4517M . DOI : 10.1371 / journal.pone.0104517 . PMC 4134218 . PMID 25127459 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ "Anammox" . Anammox - MicrobeWiki . MicrobeWiki. Архивировано 27 сентября 2015 года . Дата обращения 5 июля 2015 .
- ^ «Исследование азота может« потрясти »мир растений» . 2011-09-06. Архивировано 05 декабря 2011 года . Проверено 22 октября 2011 .
- ^ Schuur ЕАГ (2011). «Экология: азот из глубины» . Природа . 477 (7362): 39–40. Bibcode : 2011Natur.477 ... 39S . DOI : 10.1038 / 477039a . PMID 21886152 . S2CID 2946571 .
- ^ Морфорд, SL; Houlton, BZ; Дальгрен, РА (2011). «Увеличение запасов углерода и азота в лесных экосистемах из богатых азотом коренных пород» . Природа . 477 (7362): 78–81. Bibcode : 2011Natur.477 ... 78M . DOI : 10,1038 / природа10415 . PMID 21886160 . S2CID 4352571 .
- ^ Бургин, Эми Дж .; Ян, Венди Х .; Гамильтон, Стивен К .; Сильвер, Whendee L. (2011). «Помимо углерода и азота: как микробная энергетическая экономика объединяет элементарные циклы в различных экосистемах». Границы экологии и окружающей среды . 9 (1): 44–52. DOI : 10.1890 / 090227 . hdl : 1808/21008 . ISSN 1540-9309 .
- ^ Moulton, Орисса M; Altabet, Mark A; Беман, Дж. Майкл; Диган, Линда А; Льорет, Хавьер; Lyons, Meaghan K; Нельсон, Джеймс А; Пфистер, Кэтрин А (май 2016 г.). «Микробные ассоциации с макробиотой в прибрежных экосистемах: закономерности и последствия для круговорота азота». Границы экологии и окружающей среды . 14 (4): 200–208. DOI : 10.1002 / fee.1262 . hdl : 1912/8083 . ISSN 1540-9295 .
- ^ a b Миллер, Чарльз (2008). Биологическая океанография . 350 Main Street, Malden, MA 02148 США: Blackwell Publishing Ltd., стр. 60–62. ISBN 978-0-632-05536-4.CS1 maint: location ( ссылка )
- ^ a b c d Грубер, Николас (2008). Азот в морской среде . Корпоративный драйв 30, Suite 400, Берлингтон, Массачусетс 01803: Эльзевир. С. 1–35. ISBN 978-0-12-372522-6.CS1 maint: location ( ссылка )
- ^ Миллер, Чарльз (2008). Биологическая океанография . 350 Main Street, Malden, MA 02148 США: Blackwell Publishing Ltd., стр. 60–62. ISBN 978-0-632-05536-4.CS1 maint: location ( ссылка )
- ^ Бойс, Эллиот, Сьюзен, Майкл. «Учебный блок: морская среда с азотным циклом» . Архивировано из оригинального 15 апреля 2012 года . Проверено 22 октября 2011 года .
- ^ a b Лалли, Парсонс, Кэрол, Тимоти (1997). Биологическая океанография: Введение . Баттерворт-Хайнеманн. ISBN 978-0-7506-3384-0.
- ^ Голландия, Элизабет А.; Дентенер, Франк Дж .; Braswell, Bobby H .; Сульцман, Джеймс М. (1999). «Современные и доиндустриальные глобальные бюджеты химически активного азота». Биогеохимия . 46 (1-3): 7. DOI : 10.1007 / BF01007572 . S2CID 189917368 .
- ^ Гу, Баоцзин; Ге, Инь; Рен, юань; Сюй, Бен; Ло, Вэйдун; Цзян, Хун; Гу, Биньхэ; Чанг, Джи (04.09.2012). «Атмосферный реактивный азот в Китае: источники, последние тенденции и стоимость ущерба». Наука об окружающей среде и технологии . 46 (17): 9420–9427. Bibcode : 2012EnST ... 46.9420G . DOI : 10.1021 / es301446g . ISSN 0013-936X . PMID 22852755 .
- ^ Косби, Б. Джек; Каулинг, Эллис Б.; Ховарт, Роберт В .; Seitzinger, Sybil P .; Эрисман, Ян Виллем; Абер, Джон Д .; Галлоуэй, Джеймс Н. (2003-04-01). «Азотный каскад». Бионаука . 53 (4): 341–356. DOI : 10,1641 / 0006-3568 (2003) 053 [0341: УЧПУ] 2.0.CO; 2 . ISSN 0006-3568 .
- Перейти ↑ Chapin, SF III, Matson, PA, Mooney HA 2002. Принципы экологии наземных экосистем. Архивировано 28 июня 2014 г. в Wayback Machine Springer, Нью-Йорк, 2002 ISBN 0-387-95443-0 , стр. 345.
- ^ Труды Научного комитета по проблемам окружающей среды (SCOPE) International Biofuels Project Rapid Assessment, 22-25 сентября 2008 г., Гуммерсбах, Германия, редакторы Р. У. Ховарт и С. Бринджезу. Краткое содержание 2009 г. , стр. 3 Архивировано 6 июня 2009 г. в Wayback Machine.
- ^ Аэртс, Rien & Berendse, Frank (1988). «Влияние увеличения доступности питательных веществ на динамику растительности во влажных пустошах». Vegetatio . 76 (1/2): 63–69. JSTOR 20038308 .
- ^ Bobbink, R .; Hicks, K .; Galloway, J .; Spranger, T .; Alkemade, R .; Ashmore, M .; Bustamante, M .; Cinderby, S .; Дэвидсон, Э. (01.01.2010). «Глобальная оценка воздействия осаждения азота на разнообразие наземных растений: синтез» (PDF) . Экологические приложения . 20 (1): 30–59. DOI : 10.1890 / 08-1140.1 . ISSN 1939-5582 . PMID 20349829 . Архивировано (PDF) из оригинала 30.09.2019 . Проверено 30 сентября 2019 .
- ^ Лю, Сюэцзюнь; Дуань, Лэй; Мо, Цзянмин; Ду, Энзай; Шен, Цзяньлинь; Лу, Сянькай; Чжан, Инь; Чжоу, Сяобин; Он, Чуне (2011). «Отложение азота и его экологическое воздействие в Китае: обзор». Загрязнение окружающей среды . 159 (10): 2251–2264. дои : 10.1016 / j.envpol.2010.08.002 . PMID 20828899 .
- ^ Бритто, Дев Т .; Кронзукер, Герберт Дж. (2002). «Токсичность NH4 + для высших растений: критический обзор». Журнал физиологии растений . 159 (6): 567–584. DOI : 10.1078 / 0176-1617-0774 .
- ^ Камаргоа, Хулио А .; Алонсо, Альваро (2006). «Экологические и токсикологические последствия загрязнения неорганическим азотом в водных экосистемах: глобальная оценка». Environment International . 32 (6): 831–849. DOI : 10.1016 / j.envint.2006.05.002 . PMID 16781774 .
- ^ Rabalais, Нэнси Н. Р. Юджин Тернер, Уильям Дж Wiseman, младший (2002). «Гипоксия в Мексиканском заливе, она же« Мертвая зона » ». Анну. Rev. Ecol. Syst . 33 : 235–63. DOI : 10.1146 / annurev.ecolsys.33.010802.150513 . JSTOR 3069262 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Дайбас, Шерил Лин. (2005). «Мертвые зоны, распространяющиеся в Мировом океане» . Бионаука . 55 (7): 552–557. DOI : 10,1641 / 0006-3568 (2005) 055 [0552: DZSIWO] 2.0.CO; 2 .
- ^ Охрана окружающей среды штата Нью-Йорк, Воздействие кислотного осаждения на окружающую среду: Озера [1] Архивировано 24ноября2010 г. в Wayback Machine.
- ^ Мощность, JF; Schepers, JS (1989). «Загрязнение нитратами подземных вод в Северной Америке». Сельское хозяйство, экосистемы и окружающая среда . 26 (3–4): 165–187. DOI : 10.1016 / 0167-8809 (89) 90012-1 . ISSN 0167-8809 .
- ^ Strebel, O .; Duynisveld, WHM; Бёттчер, Дж. (1989). «Загрязнение грунтовых вод нитратами в Западной Европе». Сельское хозяйство, экосистемы и окружающая среда . 26 (3–4): 189–214. DOI : 10.1016 / 0167-8809 (89) 90013-3 . ISSN 0167-8809 .
- ^ Fewtrell, Лорна (2004). «Нитраты питьевой воды, метгемоглобинемия и глобальное бремя болезней: обсуждение» . Перспективы гигиены окружающей среды . 112 (14): 1371–1374. DOI : 10.1289 / ehp.7216 . ISSN 0091-6765 . PMC 1247562 . PMID 15471727 .
- ^ Глобальная обсерватория здравоохранения: (GHO) . Всемирная организация здоровья. OCLC 50144984 .
- ^ Canter, Larry W. (2019-01-22), "Иллюстрации нитратного загрязнения подземных вод", Нитраты в грунтовых водах , Routledge, стр 39-71,. DOI : 10,1201 / 9780203745793-3 , ISBN 9780203745793
- ^ Кампа, Марилена; Кастанас, Элиас (2008). «Влияние загрязнения воздуха на здоровье человека». Загрязнение окружающей среды . 151 (2): 362–367. DOI : 10.1016 / j.envpol.2007.06.012 . ISSN 0269-7491 . PMID 17646040 .
- ^ Эрисман, JW; Galloway, JN; Зейтцингер, S .; Bleeker, A .; Dise, NB; Петреску, AMR; Выщелачивание, AM; де Фрис, В. (27 мая 2013 г.). «Последствия модификации глобального азотного цикла человеком» . Философские труды Королевского общества B: биологические науки . 368 (+1621): 20130116. DOI : 10.1098 / rstb.2013.0116 . ISSN 0962-8436 . PMC 3682738 . PMID 23713116 .