| Часть серии по |
| Генетика |
|---|
 |
| Ключевые компоненты |
| История и темы |
| Исследование |
| Персонализированная медицина |
| Персонализированная медицина |
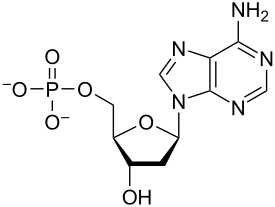
Нуклеотиды - это органические молекулы, состоящие из нуклеозида и фосфата . Они служат мономерными единицами полимеров нуклеиновых кислот дезоксирибонуклеиновой кислоты (ДНК) и рибонуклеиновой кислоты (РНК), которые являются важными биомолекулами для всех форм жизни на Земле. Нуклеотиды поступают с пищей, а также синтезируются печенью из обычных питательных веществ. [1]
Нуклеотиды состоят из трех субъединичных молекул: азотистого основания , пятиуглеродного сахара ( рибоза или дезоксирибоза ) и фосфатной группы, состоящей из одного-трех фосфатов . Четыре азотистых основания в ДНК - это гуанин , аденин , цитозин и тимин ; в РНК вместо тимина используется урацил .
Нуклеотиды также играют центральную роль в метаболизме на фундаментальном, клеточном уровне. Они обеспечивают химическую энергию - в форме нуклеозидтрифосфатов , аденозинтрифосфата (АТФ), гуанозинтрифосфата (GTP), цитидинтрифосфата (CTP) и уридинтрифосфата (UTP) - через клетку для многих клеточных функций, требующих энергии, включая : синтез аминокислот , белков и клеточных мембран , перемещение клеток и их частей (как внутри, так и между клетками), деление клеток и т. д. [2] Кроме того, нуклеотиды участвуют в передаче сигналов клетки (циклический гуанозинмонофосфат или цГМФ и циклический аденозинмонофосфат или цАМФ) и включены в важные кофакторы ферментативных реакций (например, кофермент A , FAD , FMN , NAD и NADP + ).
В экспериментальной биохимии нуклеотиды могут быть помечены радиоактивным изотопом с использованием радионуклидов для получения радионуклеотидов.
Структура [ править ]
Нуклео прилив состоит из трех отличительных химических субъединиц: молекулы сахара в пять-углероде, нуклеиновых -Какие два вместе называются нуклео стороны -А одна фосфатной группы . С всеми три присоединился, нуклеотидный также называют «Nucleo бокового моно фосфат», «нуклеозид - ди - фосфат» или «нуклеозид три фосфатом», в зависимости от того , сколько фосфатов составляют группу фосфата.
В нуклеиновых кислотах нуклеотиды содержат пуриновое или пиримидиновое основание, то есть молекулу азотистого основания, также известную как азотистое основание, и называются рибонуклеотидами, если сахар представляет собой рибозу, или дезоксирибонуклеотидами, если сахар представляет собой дезоксирибозу. Отдельные молекулы фосфата повторно соединяют молекулы сахарного кольца в двух соседних нуклеотидных мономерах, таким образом соединяя нуклеотидные мономеры нуклеиновой кислоты от конца к концу в длинную цепь. Эти цепные соединения молекул сахара и фосфата создают «основу» для одинарной или двойной спирали . В любой из цепей химическая ориентация ( направленность) соединений цепи проходит от 5'-конца к 3'-концу ( читай : от 5 простых концов до 3 простых концов), имея в виду пять углеродных сайтов на молекулах сахара в соседних нуклеотидах. В двойной спирали две нити ориентированы в противоположных направлениях, что позволяет создавать пары оснований и комплементарность между парами оснований, что важно для репликации или транскрипции кодированной информации, обнаруженной в ДНК.
Тогда нуклеиновые кислоты представляют собой полимерные макромолекулы, собранные из нуклеотидов, мономерных единиц нуклеиновых кислот . Пуриновые основания аденин и гуанин и цитозин пиримидинового основания встречаются как в ДНК, так и в РНК, в то время как пиримидиновые основания тимин (в ДНК) и урацил (в РНК) встречаются только в одном. Аденин образует пару оснований с тимином с двумя водородными связями, тогда как пары гуанина с цитозином с тремя водородными связями.
Помимо того, что они являются строительными блоками для создания полимеров нуклеиновых кислот, единичные нуклеотиды играют роль в хранении и обеспечении клеточной энергии, передаче клеточных сигналов, в качестве источника фосфатных групп, используемых для модуляции активности белков и других сигнальных молекул, а также в качестве ферментных кофакторов. , часто проводя окислительно-восстановительные реакции. Сигнальные циклические нуклеотиды образуются путем двойного связывания фосфатной группы с одной и той же молекулой сахара, соединяя 5'- и 3'- гидроксильные группы сахара. [2] Некоторые сигнальные нуклеотиды отличаются от стандартной конфигурации с одной фосфатной группой тем, что несколько фосфатных групп присоединены к разным положениям на сахаре. [3] Кофакторы нуклеотидов включают более широкий спектр химических групп, связанных с сахаром через гликозидную связь , включая никотинамид и флавин , и в последнем случае сахар рибозы является линейным, а не образующим кольцо, наблюдаемое в других нуклеотидах.
- Примеры нуклеотидов, не являющихся нуклеиновыми кислотами
цАМФ , циклическая нуклеотидная сигнальная молекула с одним фосфатом, связанным как с 5-, так и с 3-положениями.
pppGpp , нуклеотидная сигнальная молекула с 5'- и 3'-фосфатами.
НАДФ , ферментативный кофактор динуклеотидов .
FAD , динуклеотидный ферментативный кофактор, в котором один из сахаров рибозы принимает линейную конфигурацию, а не кольцо.
)
Синтез [ править ]
Нуклеотиды можно синтезировать различными способами как in vitro, так и in vivo .
In vitro защитные группы можно использовать во время лабораторного получения нуклеотидов. Очищенный нуклеозид защищен для создания фосфорамидита , который затем можно использовать для получения аналогов, не встречающихся в природе, и / или для синтеза олигонуклеотида .
In vivo нуклеотиды можно синтезировать de novo или рециркулировать по путям спасения . [1] Компоненты, используемые в синтезе нуклеотидов de novo, получены из биосинтетических предшественников углеводов и аминокислот.метаболизм, а также от аммиака и углекислого газа. Печень является основным органом синтеза всех четырех нуклеотидов de novo. Синтез пиримидинов и пуринов de novo происходит двумя разными путями. Пиримидины сначала синтезируются из аспартата и карбамоилфосфата в цитоплазме до обычной кольцевой структуры-предшественника оротовой кислоты, с которой ковалентно связано фосфорилированное рибозильное звено. Однако пурины сначала синтезируются из сахарной матрицы, на которой происходит синтез кольца. Для справки: синтез пуриновых и пиримидиновых нуклеотидов осуществляется несколькими ферментами в цитоплазме клетки, а не в определенной органелле.. Нуклеотиды подвергаются разрушению, так что полезные части можно повторно использовать в реакциях синтеза для создания новых нуклеотидов.
Синтез пиримидин рибонуклеотидов [ править ]
Синтез пиримидинов CTP и UTP происходит в цитоплазме и начинается с образования карбамоилфосфата из глутамина и CO 2 . Далее, аспартат карбамоилтрансферазу катализируют реакцию конденсации между аспартатой и карбамоильный фосфат с образованием карбамоильной аспарагиновой кислоты , который подвергает циклизации в 4,5-дигидрооротовые кислоты по дигидрооротазу . Последний превращают оротат по дигидрооротат - оксидазы . Чистая реакция:
- ( S ) -Дигидрооротат + O 2 → оротат + H 2 O 2
Оротат ковалентно связан с фосфорилированным рибозильным звеном. Ковалентная связь между рибозой и пиримидином происходит в положении C 1 [4] от рибозы блока, который содержит пирофосфат , и N 1 из пиримидинового кольца. Оротатфосфорибозилтрансфераза (трансфераза PRPP) катализирует чистую реакцию с образованием монофосфата оротидина (OMP):
- Оротат + 5-фосфо-α-D-рибозо-1-дифосфат (PRPP) → Оротидин 5'-фосфат + пирофосфат
Оротидин-5'-монофосфат декарбоксилируется оротидин-5'-фосфатдекарбоксилазой с образованием уридинмонофосфата (UMP). Трансфераза PRPP катализирует реакции как рибозилирования, так и декарбоксилирования, образуя UMP из оротовой кислоты в присутствии PRPP. Именно из UMP происходят другие пиримидиновые нуклеотиды. UMP фосфорилируется двумя киназами до уридинтрифосфата (UTP) посредством двух последовательных реакций с ATP. Сначала образуется дифосфат из UDP, который, в свою очередь, фосфорилируется до UTP. Обе стадии подпитываются гидролизом АТФ:
- ATP + UMP → ADP + UDP
- UDP + ATP → UTP + ADP
CTP впоследствии образуется в результате аминирования UTP каталитической активностью CTP-синтетазы . Глутамин является донором NH 3, и реакция также поддерживается гидролизом АТФ:
- UTP + глутамин + ATP + H 2 O → CTP + ADP + P i
Цитидинмонофосфат (CMP) является производным цитидинтрифосфата (CTP) с последующей потерей двух фосфатов. [5] [6]
Синтез пуриновых рибонуклеотидов [ править ]
Атомы, которые используются для создания пуриновых нуклеотидов, происходят из различных источников:
| В биосинтетическом происхождении пуринового кольца атомов N 1 возникает из амина группы Asp С 2 и С 8 происходят из формиата N 3 и N 9 , предоставлено амидной группой Gln C 4 , C 5 и N 7 получают из Gly C 6 происходит из HCO 3 - (CO 2 ) |
De Novo синтеза из пуриновых нуклеотидов , с помощью которого эти предшественники включены в пуринового кольца протекает по 10-ступенчатой пути к отводной точке промежуточного IMP , нуклеотидная базовой гипоксантин . AMP и GMP впоследствии синтезируются из этого промежуточного продукта отдельными двухэтапными путями. Таким образом, пуриновые фрагменты первоначально образуются как часть рибонуклеотидов, а не как свободные основания .
В синтезе ИМФ принимают участие шесть ферментов. Три из них многофункциональные:
- GART (реакции 2, 3 и 5)
- PAICS (реакции 6 и 7)
- ATIC (реакции 9 и 10)
Путь начинается с образования PRPP . PRPS1 - это фермент, который активирует R5P , который образуется в основном пентозофосфатным путем , в PRPP путем его реакции с АТФ . Реакция является необычным в том , что pyrophosphoryl группа непосредственно передается от АТФ к C 1 из R5P и что продукт имеет альфа конфигурацию относительно C1. Эта реакция также является общей с путями синтеза Trp , His и пиримидиновых нуклеотидов.. Находясь на важном метаболическом перекрестке и требуя много энергии, эта реакция строго регулируется.
В первой реакции , уникальной для пуриновых нуклеотидов биосинтез, PPAT катализирует перемещение ФРПФ «ы пирофосфата группы (ПП я ) с помощью амидного азота донорской либо из глутамина (N), глицина (N & С), аспартат (N), фолиевая кислота (C 1 ) или CO 2 . Это обязательный этап синтеза пуринов. Реакция происходит с инверсией конфигурации рибозы C 1 , в результате чего образуется β - 5-фосфорибозиламин (5-PRA) и устанавливается аномерная форма будущего нуклеотида.
Затем включается глицин за счет гидролиза АТФ, и карбоксильная группа образует аминовую связь с ранее введенным NH 2 . Одноуглеродное звено кофермента N 10 -формил-ТГФ фолиевой кислоты затем добавляется к аминогруппе замещенного глицина с последующим замыканием имидазольного кольца. Затем вторая группа NH 2 переносится с глутамина на первый атом углерода глициновой единицы. Одновременно добавляется карбоксилирование второго атома углерода глициновой единицы. Этот новый углерод модифицирован добавлением третьего NH 2.единица, на этот раз перенесенная из остатка аспартата. Наконец, второе одноуглеродное звено формил-ТГФ добавляется к азотной группе, и кольцо ковалентно замыкается с образованием общего предшественника пурина инозинмонофосфата (ИМФ).
Монофосфат инозина превращается в монофосфат аденозина в два этапа. Во-первых, гидролиз ГТФ способствует добавлению аспартата к ИМФ аденилосукцинатсинтазой, замещая атом азота карбонильным кислородом и образуя промежуточный аденилосукцинат. Затем фумарат отщепляется с образованием аденозинмонофосфата. Эта стадия катализируется аденилосукцинатлиазой.
Монофосфат инозина превращается в монофосфат гуанозина путем окисления IMP с образованием ксантилата с последующим введением аминогруппы в C 2 . НАД + является акцептором электронов в реакции окисления. Перенос амидной группы из глутамина происходит за счет гидролиза АТФ.
Разложение пиримидинов и пуринов [ править ]
У человека пиримидиновые кольца (C, T, U) могут полностью разлагаться до CO 2 и NH 3 (экскреция мочевины). Как уже было сказано, пуриновые кольца (G, A) не могут. Вместо этого они разлагаются до метаболически инертной мочевой кислоты.который затем выводится из организма. Мочевая кислота образуется при расщеплении GMP на основной гуанин и рибозу. Гуанин дезаминируется до ксантина, который, в свою очередь, окисляется до мочевой кислоты. Эта последняя реакция необратима. Точно так же мочевая кислота может образовываться, когда АМФ дезаминируется до ИМФ, из которого удаляется рибозная единица с образованием гипоксантина. Гипоксантин окисляется до ксантина и, наконец, до мочевой кислоты. Вместо секреции мочевой кислоты гуанин и ИМФ можно использовать для целей рециркуляции и синтеза нуклеиновых кислот в присутствии PRPP и аспартата ( донора NH 3 ).
Пребиотический синтез нуклеотидов [ править ]
Теории о том, как возникла жизнь , требуют знания химических путей, которые позволяют формировать ключевые строительные блоки жизни в вероятных пребиотических условиях . Гипотеза мира РНК утверждает, что в изначальном супе существовали свободно плавающие рибонуклеотиды , основные молекулы, которые последовательно соединяются, образуя РНК . Сложные молекулы, подобные РНК, должны были возникнуть из небольших молекул, реакционная способность которых определялась физико-химическими процессами. РНК состоит из пуриновых и пиримидиновых нуклеотидов, которые необходимы для надежной передачи информации и, следовательно, для дарвиновской эволюции.. Becker et al. показали, как пиримидиновые нуклеозиды могут быть синтезированы из малых молекул и рибозы , только за счет циклов «влажный-сухой». [7] Пуриновые нуклеозиды могут быть синтезированы аналогичным путем. 5'-моно- и дифосфаты также селективно образуются из фосфатсодержащих минералов, что позволяет одновременное образование полирибонуклеотидов как с пуриновыми, так и с пиримидиновыми основаниями. Таким образом, сеть реакций по отношению к строительным блокам пуриновой и пиримидиновой РНК может быть создана, начиная с простых атмосферных или вулканических молекул. [7]
Неестественная пара оснований (UBP) [ править ]
Неестественная пара оснований (UBP) - это разработанная субъединица (или нуклеиновое основание ) ДНК, которая создается в лаборатории и не встречается в природе. [8] Примеры включают d5SICS и dNaM . Эти искусственные нуклеотиды, несущие гидрофобные азотистые основания , содержат два слитых ароматических кольца, которые образуют (d5SICS – dNaM) комплекс или пару оснований в ДНК. [9] [10] E. coli были индуцированы к репликации плазмиды, содержащей UBP, через несколько поколений. [11] Это первый известный пример передачи живым организмом расширенного генетического кода последующим поколениям. [9] [12]
Медицинское применение синтетических нуклеотидов [ править ]
Некоторые производные нуклеотидов использовались в качестве противовирусных средств против гепатита и ВИЧ . [13] Тенофовир дизопроксил , Тенофовир алафенамид и Софосбувир являются примерами НИОТ, используемых против гепатита. В то время как некоторые препараты , как Mericitabine , ламивудин , Entecavir и Telbivudine , например , являются нуклеозиды, но они метаболизируется в свои биоактивные нуклеотидных форм через фосфорилирования.
Единица длины [ править ]
В этом разделе не процитировать любые источники . ( Март 2021 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
Нуклеотид (сокращенно «нт») - это обычная единица длины для одноцепочечных нуклеиновых кислот, подобно тому, как пара оснований является единицей длины для двухцепочечных нуклеиновых кислот.
Коды сокращений для вырожденных оснований [ править ]
IUPAC назначил символы для нуклеотидов. [14] Помимо пяти (A, G, C, T / U) оснований, часто используются вырожденные основания, особенно для создания праймеров для ПЦР . Эти коды нуклеотидов перечислены здесь. Некоторые последовательности праймеров могут также включать символ «I», который кодирует нестандартный нуклеотид- инозин . Инозин входит в состав тРНК и соединяется с аденином, цитозином или тимином. Однако этот символ не появляется в следующей таблице, потому что он не представляет собой вырождение. Хотя инозин может выполнять ту же функцию, что и вырождение «D», он является действительным нуклеотидом, а не представлением смеси нуклеотидов, охватывающей каждую возможную необходимую пару.
| Символ [14] | Описание | Представленные базы | ||||
|---|---|---|---|---|---|---|
| А | Денин | А | 1 | |||
| C | с ytosine | C | ||||
| грамм | г уанин | грамм | ||||
| Т | т hymine | Т | ||||
| U | у racil | U | ||||
| W | ж ЕАК | А | Т | 2 | ||
| S | s Чонг | C | грамм | |||
| M | м иных | А | C | |||
| K | k eto | грамм | Т | |||
| р | пу г ине | А | грамм | |||
| Y | р у -пиримидина | C | Т | |||
| B | не A ( B идет после A) | C | грамм | Т | 3 | |
| D | не C ( D идет после C) | А | грамм | Т | ||
| ЧАС | не G ( H идет после G) | А | C | Т | ||
| V | не T ( V идет после T и U) | А | C | грамм | ||
| N | п у основания (не пробел) | А | C | грамм | Т | 4 |
См. Также [ править ]
- Биология
- Хромосома
- Ген
- Генетика
- Аналоги нуклеиновой кислоты
- Последовательность нуклеиновой кислоты
- Нуклеооснование
Ссылки [ править ]
- ^ a b Захаревиц Д.В., Андерсон Л.В., Малиновский Н.М., Хайман Р., Стронг Дж.М., Цисик Р.Л. (ноябрь 1992 г.). «Вклад de-novo и спасения синтеза в пул нуклеотидов урацила в тканях мышей и опухолях in vivo» . Европейский журнал биохимии . 210 (1): 293–6. DOI : 10.1111 / j.1432-1033.1992.tb17420.x . PMID 1446677 .
- ^ a b Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К. и Уолтер П. (2002). Молекулярная биология клетки (4-е изд.). Наука о гирляндах. ISBN 0-8153-3218-1 . С. 120–121.
- ^ Смит, AD, изд. (2000). Оксфордский словарь биохимии и молекулярной биологии, исправленное издание . Оксфорд: Издательство Оксфордского университета. п. 460.
- ^ См. Номенклатуру органической химии ИЮПАК для получения подробной информации о нумерации остатков углерода.
- Перейти ↑ Jones ME (1980). «Биосинтез пиримидиновых нуклеотидов у животных: гены, ферменты и регуляция биосинтеза UMP». Ежегодный обзор биохимии . 49 (1): 253–79. DOI : 10.1146 / annurev.bi.49.070180.001345 . PMID 6105839 .
- ^ МакМурри JE, Бегли TP (2005). Органическая химия биологических путей . Робертс и Компания. ISBN 978-0-9747077-1-6.
- ^ a b Беккер С., Фельдманн Дж., Видеманн С., Окамура Х., Шнайдер С., Иван К., Крисп А., Росса М., Аматов Т., Карелл Т. Унифицированный пребиотически вероятный синтез пиримидиновых и пуриновых рибонуклеотидов РНК. Наука. 2019 4 октября; 366 (6461): 76-82. DOI: 10.1126 / science.aax2747. PMID: 31604305
- ^ Малышев Д.А., дхами К, Quach НТ, Лавернь Т, Ordoukhanian Р, Torkamani А, Romesberg ИП (июль 2012). «Эффективная и независимая от последовательности репликация ДНК, содержащей третью пару оснований, устанавливает функциональный шестибуквенный генетический алфавит» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (30): 12005–10. Bibcode : 2012PNAS..10912005M . DOI : 10.1073 / pnas.1205176109 . PMC 3409741 . PMID 22773812 .
- ^ a b Малышев Д.А., Дхами К., Лаверн Т., Чен Т., Дай Н., Фостер Дж. М., Корреа И. Р., Ромесберг Ф. Э. (май 2014 г.). «Полусинтетический организм с расширенным генетическим алфавитом» . Природа . 509 (7500): 385–8. Bibcode : 2014Natur.509..385M . DOI : 10,1038 / природа13314 . PMC 4058825 . PMID 24805238 .
- ↑ Callaway E (7 мая 2014 г.). «Ученые создают первый живой организм с« искусственной »ДНК» . Новости природы . Huffington Post . Проверено 8 мая 2014 .
- ^ Файкс BJ (8 мая 2014). «Жизнь, созданная с помощью расширенного генетического кода» . Сан-Диего Юнион Трибьюн . Проверено 8 мая 2014 .
- ↑ Образец I (7 мая 2014 г.). «Первые формы жизни, передающие искусственную ДНК, созданную учеными США» . Хранитель . Проверено 8 мая 2014 .
- ^ Рамеш, Дипти; Виджаякумар, Баладжи Говривел; Каннан, Тараниккарасу (12 февраля 2021 г.). «Достижения в области нуклеозидов и аналогов нуклеотидов в борьбе с вирусами иммунодефицита человека и вирусными инфекциями гепатита» . ChemMedChem . DOI : 10.1002 / cmdc.202000849 . Проверено 13 марта 2021 года .
- ^ a b Номенклатурный комитет Международного союза биохимиков (NC-IUB) (1984). «Номенклатура не полностью определенных оснований в последовательностях нуклеиновых кислот» . Проверено 4 февраля 2008 .
Дальнейшее чтение [ править ]
- Сигель А, Operschall BP, Сигель Х (2017). «Глава 11. Комплексное образование свинца (II) с нуклеотидами и их составляющими». В Astrid S, Helmut S, Sigel RK (ред.). Свинец: его влияние на окружающую среду и здоровье . Ионы металлов в науках о жизни. 17 . де Грюйтер. С. 319–402. DOI : 10.1515 / 9783110434330-011 . ISBN 9783110434330. PMID 28731304 .
- Фрайзингер, Э. и Сигель, Р.К. (2007). От нуклеотидов до рибозимов - сравнение их свойств связывания с ионами металлов . Coordination Chemistry Reviews , 251 (13-14), 1834-1851.
Внешние ссылки [ править ]
- Аббревиатуры и символы для нуклеиновых кислот, полинуклеотидов и их компонентов ( IUPAC )
- Предварительные рекомендации 2004 г. (IUPAC)
- Химическое объяснение структуры нуклеотидов