 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Хинолин [2] | |||
Систематическое название ИЮПАК
| |||
Другие имена
| |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 3DMet | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100,001,865 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
| MeSH | Хинолины | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2656 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 9 H 7 N | |||
| Молярная масса | 129,16 г / моль | ||
| Внешность | Бесцветная маслянистая жидкость | ||
| Плотность | 1,093 г / мл | ||
| Температура плавления | -15 ° С (5 ° F, 258 К) | ||
| Точка кипения | 237 ° С (459 ° F, 510 К), 760 мм рт. 108–110 ° C (226–230 ° F), 11 мм рт. | ||
| Слабо растворим | |||
| Растворимость | Растворим в спирте, эфире и сероуглероде | ||
| Кислотность (p K a ) | 4,85 (сопряженная кислота) [3] | ||
Магнитная восприимчивость (χ) | −86,0 · 10 −6 см 3 / моль | ||
| Термохимия | |||
Std энтальпия формации (Δ F H ⦵ 298 ) | 174,9 кДж · моль -1 | ||
| Опасности | |||
| R-фразы (устаревшие) | R21 , R22 | ||
| S-фразы (устарели) | S26 , S27 , S28 , S29 , S30 , S31, S32, S33 , S34, S35 , S36 | ||
| NFPA 704 (огненный алмаз) |  1 2 0 | ||
| точка возгорания | 101 ° С (214 ° F, 374 К) | ||
самовоспламенения температуру | 400 ° С (752 ° F, 673 К) | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD 50 ( средняя доза ) | 331 мг / кг | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
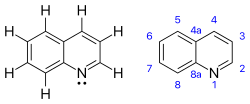
Хинолин представляет собой гетероциклическое ароматическое органическое соединение с химической формулой C 9 H 7 N. Это бесцветная гигроскопичная жидкость с сильным запахом. Старые образцы, особенно под воздействием света, становятся желтыми, а затем коричневыми. Хинолин слабо растворяется в холодной воде, но легко растворяется в горячей воде и большинстве органических растворителей. [4] Сам по себе хинолин имеет несколько применений, но многие из его производных используются в самых разных областях. Ярким примером является хинин , алкалоид, содержащийся в растениях. Более 200 биологически активных хинолина и хиназолинаалкалоиды идентифицированы. [5] [6] 4-Гидрокси-2-алкилхинолины (HAQ) участвуют в устойчивости к антибиотикам .
Возникновение и изоляция [ править ]
Хинолин был впервые извлечен из каменноугольной смолы в 1834 году немецким химиком Фридлибом Фердинандом Рунге ; [4] он назвал хинолин лейкол («белое масло» по-гречески). [7] Каменноугольная смола остается основным источником коммерческого хинолина. [8] В 1842 году французский химик Шарль Герхардт получил соединение путем сухой перегонки хинина , стрихнина или цинхонина с гидроксидом калия ; [4] он назвал соединение хиноилином или хинолеином . [9] Соединения Рунге и Гепардта казались разными изомерами, потому что они по-разному реагировали. Однако немецкий химик Август Хоффманн в конце концов осознал, что различия в поведении были связаны с присутствием загрязнителей и что эти два соединения фактически идентичны. [10] Единственное сообщение о хинолине как о натуральном продукте поступило от перуанского палочника Oreophoetes peruana . У них есть пара грудных желез, из которых они выделяют зловонную жидкость, содержащую хинолин, когда их беспокоят. (Eisner, T; Morgan, RC; Attygalle AB, Smedley, SR; Herath, KB, Meinwald, J. (1997) «Защитное производство хинолина фазмидным насекомым (Oreophoetes peruana)» J. Exp. Biol. 200, 2493– 2500).
Как и другие азотсодержащие гетероциклические соединения, такие как производные пиридина , хинолин часто упоминается как загрязнитель окружающей среды, связанный с предприятиями по переработке горючего сланца или угля, а также был обнаружен на старых участках обработки древесины. Благодаря своей относительно высокой растворимости в воде хинолин обладает значительным потенциалом мобильности в окружающей среде, что может способствовать загрязнению воды. Хинолин легко разлагается некоторыми микроорганизмами, такими как штамм Q1 вида Rhodococcus , который был изолирован из почвы и ила бумажных фабрик. [11]
Хинолины в небольших количествах присутствуют в сырой нефти в первичной дизельной фракции. Его можно удалить с помощью процесса, называемого гидроденитрификацией .
Синтез [ править ]
Хинолины часто синтезируют из простых анилинов с использованием ряда названных реакций .
По часовой стрелке сверху это:
- Объединяет синтез хинолина с использованием анилинов и β- дикетонов .
- Синтез Конрада-Лимпаха с использованием анилинов и β-кетоэфиров.
- Реакция Дебнера с использованием анилинов с альдегидом и пировиноградной кислотой с образованием хинолин-4-карбоновых кислот
- Реакция Дебнера-Миллера с использованием анилинов и α, β-ненасыщенных карбонильных соединений.
- Реакция Гульда-Якобса, исходя из анилина и этилэтоксиметиленмалоната
- Синтез Скраупа с использованием сульфата железа , глицерина , анилина , нитробензола и серной кислоты .
Существует ряд других процессов, для которых требуются специально замещенные анилины или родственные соединения:
- Синтез хинолина по лагерю с использованием о-ациламиноацетофенона и гидроксида
- Синтез Фридлендера с использованием 2-аминобензальдегида и ацетальдегида
- Синтез хинолина Knorr с использованием β-кетоанилида и серной кислоты
- Синтез хинолина Нементовского с использованием антраниловой кислоты и кетонов
- Реакция Пфитцингера с использованием изатина с основанием и карбонильным соединением с образованием замещенных хинолин-4-карбоновых кислот
- Реакция Поварова с использованием анилина , бензальдегида и активированного алкена
Приложения [ править ]
Хинолин используется в производстве красителей , препаратах гидроксихинолина сульфата и ниацина . Он также используется в качестве растворителя для смол и терпенов .
Хинолин в основном используется, как и в производстве других специальных химикатов . Согласно отчету, опубликованному в 2005 году, ежегодно производится около 4 тонн . [8] Его основное применение - это предшественник 8-гидроксихинолина , который является универсальным хелатирующим агентом и предшественником пестицидов. Его 2- и 4-метилпроизводные являются предшественниками цианиновых красителей . Окисление хинолина дает хинолиновую кислоту (пиридин-2,3-дикарбоновую кислоту), предшественник гербицида, продаваемого под названием «Assert». [8]
Восстановление хинолина с боргидридом натрия в присутствии уксусной кислоты , как известно, производит Kairoline A . [12] ( ср. Кайрин )
У хинолина есть несколько противомалярийных производных, включая хинин , хлорохин , амодиахин и примахин .
Хинолины восстанавливаются до тетрагидрохинолинов энантиоселективно с использованием нескольких каталитических систем. [13] [14]
См. Также [ править ]
- Хинолиновые алкалоиды
- 4-аминохинолин
- 8-гидроксихинолин
- Пирролохинолинхинон (PQQ), редокс-кофактор и сомнительная пищевая добавка
- Хиназолин , аза производное хинолина
- Хинин
- Подобные простые ароматические кольца
- Изохинолин , аналог с атомом азота в положении 2
- Пиридин , аналог без конденсированного бензольного кольца
- Нафталин , аналог с углеродом вместо азота
- Индол , аналог только с пятичленным азотным кольцом
Ссылки [ править ]
- ^ «ХИНОЛИН (БЕНЗОПИРИДИН)» . Chemicalland21.com . Проверено 14 июня 2012 .
- ^ Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга) . Кембридж: Королевское химическое общество . . 2014. С. 4, 211. DOI : 10.1039 / 9781849733069-FP001 . ISBN 978-0-85404-182-4.
Название «хинолин» - это сохраненное название, которое предпочтительнее альтернативных систематических названий слияния «1-бензопиридин» или «бензо [ b ] пиридин».
- ^ Brown, HC, et al., В Baude, EA и Nachod, FC, Определение органических структур физическими методами , Academic Press, New York, 1955.
- ^ a b c Чисхолм, Хью, изд. (1911). . Encyclopdia Britannica . 22 (11-е изд.). Издательство Кембриджского университета. п. 759.
- ^ Шан, XF; Моррис-Натшке, SL; Лю, YQ; Guo, X; Сюй, XS; Гото, М; Li, JC; Ян, GZ; Ли, К. Х. (май 2018 г.). «Биологически активные хинолиновые и хиназолиновые алкалоиды часть I.» Обзоры медицинских исследований . 38 (3): 775–828. DOI : 10.1002 / med.21466 . PMC 6421866 . PMID 28902434 .
- ^ Шан, Сяо-Фэй; Morris-Natschke, Susan L .; Ян, Гуань-Чжоу; Лю Инь-Цянь; Го, Сяо; Сюй, Сяо-Шань; Гото, Масуо; Ли, Цзюнь-Цай; Чжан, Цзи-Ю; Ли, Куо-Сюн (сентябрь 2018 г.). «Биологически активные хинолиновые и хиназолиновые алкалоиды часть II» . Обзоры медицинских исследований . 38 (5): 1614–1660. DOI : 10.1002 / med.21492 . PMC 6105521 . PMID 29485730 .
- ^ FF Рунге (1834) «Ueber einige Produkte der Steinkohlendestillation» (О некоторых продуктах перегонки угля), Annalen der Physik und Chemie , 31 (5): 65–78; особенно см. стр. 68: «3. Leukol oder Weissöl» (3. Белое масло [по-гречески] или белое масло [по-немецки]). С п. 68: "Diese dritte Basis habe ich Leukol oder Weissöl genannt, weil sie keine farbigen Reactionen zeigt." (Эту третью основу я назвал лейкол или белое масло, потому что она не проявляет цветных реакций.)
- ^ a b c Герд Коллин; Хартмут Хёке. «Хинолин и изохинолин». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a22_465 .
- ^ Герхардт, гл. (1842) «Untersuchungen über die organischen Basen» (Исследования органических оснований), Annalen der Chemie und Pharmacie , 42 : 310-313. См. Также: (Редактор) (1842 г.) «Chinolein oder Chinoilin» (хинолин или хиноилин), Annalen der Chemie und Pharmacie , 44 : 279-280.
- ^ Первоначально Хоффман считалчто Рунге Leukol и Герхардт в Chinolein были различны. (См .: Hoffmann, August Wilhelm (1843) «Chemische Untersuchungen der organischen Basen im Steinkohlen-Theeröl» (Химические исследования органических оснований в каменноугольном масле), Annalen der Chemie und Pharmacie , 47 : 37-87; особенно см. Стр. 76 -78.) Однако после дополнительной очистки егообразца Leukol Хоффманн определил, что они действительно идентичны. (См .: (Редактор) (1845) "Vorläufige Notiz über die Identität des Leukols und Chinolins" (Предварительное уведомление о идентичности лейкола и хинолина), Annalen der Chemie und Pharmacie, 53 : 427-428.)
- ^ О'Лафлин, Эдвард Дж .; Kehrmeyer, Staci R .; Симс, Джеральд К. (1996). «Выделение, характеристика и использование субстрата бактерии, разлагающей хинолин». Международный биоразложение и биоразложение . 38 (2): 107. DOI : 10.1016 / S0964-8305 (96) 00032-7 .
- ^ ГРИББЛ, Гордон W .; ЗДОРОВЬЕ, Питер В. (1975). «Реакции боргидрида натрия в кислой среде; III. Восстановление и алкилирование хинолина и изохинолина карбоновыми кислотами». Синтез . 1975 (10): 650–652. DOI : 10,1055 / с-1975-23871 . ISSN 0039-7881 .
- ^ Xu, L .; Лам, KH; Ji, J .; Wu, J .; Fan, Q.-H .; Lo, W.-H .; Chan, ASC Chem. Commun. 2005 , 1390.
- ^ Reetz, MT; Li, X. Chem. Commun. 2006 , 2159.
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме хинолина . |
- Международная карта химической безопасности 0071
- Новые методы синтеза хинолинов