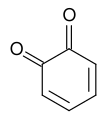
В хинонах представляют собой класс органических соединений , которые формально «получены из ароматических соединений , такие как [ бензол или нафталин ] путем превращения четного числа -СНО = групп в -C (= O) - группы с любой необходимой перегруппировкой двойных связей , что приводит к «полностью сопряженной структуре циклического диона ». [1] [2] [3] Типичным представителем этого класса является 1,4-бензохинон или циклогексадиендион, часто называемый просто «хиноном» (отсюда и название класса) . Другими важными примерами являются 1,2-бензохинон ( орто-хинон ), 1,4-нафтохинон и 9,10-антрахинон .
Свойства [ править ]
Хиноны представляют собой окисленные производные ароматических соединений и часто легко получаются из реакционноспособных ароматических соединений с электронодонорными заместителями, такими как фенолы и катехины , которые увеличивают нуклеофильность кольца и вносят свой вклад в большой окислительно-восстановительный потенциал, необходимый для разрушения ароматичности. (Хиноны конъюгированы, но не ароматичны). Хиноны представляют собой электрофильные акцепторы Михаэля, стабилизированные конъюгацией. В зависимости от хинона и участка восстановления восстановление может реоматизировать соединение или нарушить конъюгацию. Добавление конъюгата почти всегда нарушает конъюгацию.
Термин хинон также используется в более общем смысле для большого класса соединений, формально полученных из ароматических хинонов путем замены некоторых атомов водорода другими атомами или радикалами.
Хлоранил , реагент в органической химии
Lawsone , краситель, присутствующий в листьях растения хны.
Ализарин , распространенный красный краситель
DDQ , реагент в органической химии
Даунорубицин , противораковый препарат
Возникновение и использование [ править ]
Производство перекиси водорода [ править ]
Хиноны широко используются в промышленности для производства перекиси водорода . 2-Алкилантрахиноны гидрируются до соответствующих гидрохинонов (хинизаринов), которые затем переносят H
2 к кислороду:
- дигидроантрахинон + O
2 → антрахинон + H
2О
2
таким образом, несколько миллионов метрических тонн H
2О
2выпускаются ежегодно. [4]
1,4- Нафтохинон , полученный окислением нафталина триоксидом хрома . [5] Это предшественник антрахинона.
Биохимия [ править ]
Убихинон -1 - это 1,4-бензохинон природного происхождения, который участвует в дыхательном аппарате.
Предполагается, что они встречаются у всех дышащих организмов. [6] Некоторые из них служат акцепторами электронов в цепях переноса электронов, например, при фотосинтезе ( пластохинон , филлохинон ) и аэробном дыхании ( убихинон ). Филлохинон также известен как витамин К 1, поскольку он используется животными для карбоксилирования определенных белков, которые участвуют в свертывании крови , формировании костей и других процессах. И наоборот, токсичность парацетамола связана с его метаболизмом в хинонимин., который затем вступает в реакцию с белками печени, вызывая печеночную недостаточность.
В брызгах жуков-бомбардиров гидрохинон реагирует с перекисью водорода, образуя огненный поток пара, сдерживающий мир животных.
Автоокисление нейротрансмиттера дофамина и его предшественника L-Dopa генерирует сравнительно стабильный дофаминовый хинон, который подавляет функционирование переносчика дофамина (DAT) и фермента TH, что приводит к снижению выработки митохондриального АТФ . [7]
Другие натуральные продукты [ править ]
Бензохинон blattellaquinone является секс феромонов в тараканами .
Лекарственное [ править ]
Некоторые хиноны представляют фармакологический интерес. Они образуют основной класс цитотоксинов, используемых в борьбе с раком. Одним из примеров является даунорубицин , обладающий противолейкозом. [6] Некоторые из них проявляют противоопухолевую активность. Они воплощают некоторые претензии в фитотерапии . Эти приложения включают слабительное ( Sennosides ), антимикробное и противопаразитарное ( реин и saprorthoquinone , атовакон ), противоопухолевое ( эмодин и юглон ), ингибирование PGE2 биосинтеза ( arnebinone и arnebifuranone ) и антисердечно-сосудистые заболевания ( таншинон ). [8]
Другим препаратом, содержащим хинон, является Мекарбинат ( димекарбин ), получаемый при реакции этил- N-метил-β-аминокротоната с пара-бензохиноном. Другие включают Амендол , Оксифемедол , Фемедол, все в FR5142 (M) - 1967-06-05. [ требуется разъяснение ] Примечание: все это индолы, полученные в результате синтеза индола Неницеску . Противоопухолевый препарат Апазиквон .
Бензохиноновые соединения являются метаболитом парацетамола . [9]
Красители [ править ]
Многие натуральные и искусственные красящие вещества ( красители и пигменты ) являются производными хинона. По важности красителей они уступают только азокрасителям , с особым акцентом на синие цвета. Ализарин (1,2-дигидрокси-9,10-антрахинон), экстрагированный из марены , был первым природным красителем, синтезированным из каменноугольной смолы.
Реагенты в органической химии [ править ]
Бензохинон используется в органической химии как окислитель . Сильно окисляющие хиноны включают хлоранил и 2,3-дихлор-5,6-дициано-1,4-бензохинон (также известный как DDQ). [10]
Носитель заряда аккумулятора [ править ]
9,10-Антрахинон-2,7-дисульфоновая кислота (AQDS), хинон, подобный хинону, встречающемуся в природе в ревене , использовался в качестве носителя заряда в безметалловых проточных батареях . [11]
Номенклатура [ править ]
Хиноны обычно называются с префиксом, который указывает на исходный ароматический углеводород («бензо-» для бензола, «нафто-» для нафталина, «антра-» для антрацена и т. Д.) И суффикс «-хинон». Инфиксные множители «-di-», «-tri-», «-tetra-» (и т. Д.) Используются, когда имеется 4, 6, 8 (т. Д.) Карбонилов. Положение карбонильных групп может быть указано перед префиксом (например, «1,4,5,8-нафтодихинон») или после него («антра-1,4-хинон»).
См. Также [ править ]
- Антрахинон
- Бензохинон
- Нафтохинон
- Пластохинон
- Пирролохинолинхинон
- Хинон метид
- Хинондиимин - аналог азота, проиллюстрированный антисептиком Амбазон
- Malbranchea cinnamomea
Ссылки [ править ]
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) « Хиноны ». DOI : 10,1351 / goldbook.Q05015
- ^ Патай, Савл; Раппопорт, Цви, ред. (1988). Хиноноидные соединения: Vol. 1 (1988) . DOI : 10.1002 / 9780470772119 . ISBN 9780470772119.
- ^ Патай, Савл; Раппопорт, Цви, ред. (1988). Хиноноидные соединения: Vol. 2 (1988) . DOI : 10.1002 / 9780470772126 . ISBN 9780470772126.
- ^ Gustaaf Гур, Юрген Glenneberg, Сильвия Jacobi "Перекись водорода" в энциклопедии Ульмана промышленной химии 2007, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a13_443.pub2 .
- ^ Braude EA; Фосетт, Дж. С. (1953). «1,4-Нафтохинон». Органический синтез . 33 : 50. DOI : 10,15227 / orgsyn.033.0050 .; Сборник , 4 , с. 698
- ^ а б О'Брайен, П.Дж. (1991). «Молекулярные механизмы цитотоксичности хинонов». Химико-биологические взаимодействия . 80 (1): 1–41. DOI : 10.1016 / 0009-2797 (91) 90029-7 . PMID 1913977 .
- ^ Доршевска, Иоланта; Прендеки, Михал; Козубски, Маргарита Лианери и Войцех (2014-01-31). «Молекулярные эффекты терапии L-допа при болезни Паркинсона» . Текущая геномика . 15 (1): 11–17. DOI : 10.2174 / 1389202914666131210213042 . PMC 3958954 . PMID 24653659 .
- ^ Лю Х., «Извлечение и выделение соединений из лекарственных растений» в «Методы исследования традиционных лекарственных трав» под редакцией Уиллоу Дж. Х. Лю, 2011 г., John Wiley and Sons, Inc.
- ^ Далин, округ Колумбия; Miwa, GT; Лу, AY; Нельсон, SD (1984). «N-ацетил-п-бензохинонимин: продукт окисления ацетаминофена, опосредованный цитохромом P-450» . Труды Национальной академии наук Соединенных Штатов Америки . 81 (5): 1327–1331. Полномочный код : 1984PNAS ... 81.1327D . DOI : 10.1073 / pnas.81.5.1327 . PMC 344826 . PMID 6424115 .
- Перейти ↑ March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3 ed.), New York: Wiley, ISBN 0-471-85472-7
- ^ Хускинсон, Брайан; Маршак, Майкл П .; Су, Чангвон; Эр, Сулейман; Герхардт, Майкл Р .; Галвин, Купер Дж .; Чен, Сюйдун; Аспуру-Гузик, Алан; Гордон, Рой Дж .; Азиз, Майкл Дж. (9 января 2014 г.). "Безметалловая органо-неорганическая проточная батарея на водной основе" (PDF) . Природа . 505 (7482): 195–198. Bibcode : 2014Natur.505..195H . DOI : 10,1038 / природа12909 . PMID 24402280 . S2CID 4459692 .
Внешние ссылки [ править ]
- Хиноны в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)