Ретосибан, также известный как GSK-221,149-A [1] [2], представляет собой пероральный препарат, который действует как антагонист рецепторов окситоцина . Он разрабатывается GlaxoSmithKline для лечения преждевременных родов . [3] [4] Ретосибан имеет высокое сродство к рецептору окситоцина (K i = 0,65 нМ) и имеет более чем 1400-кратную селективность [5] по сравнению с родственными рецепторами вазопрессина.
Механизм действия [ править ]
Ретосибан является конкурентным антагонистом рецепторов окситоцина, который блокирует опосредованное окситоцином сокращение гладкой мускулатуры матки в женской матке, которое происходит во время начала преждевременных родов. Это использовалось для предотвращения преждевременных родов и преждевременных родов .
Фармакология [ править ]
Было доказано, что ретосибан является эффективным токолитиком . При внутривенном и пероральном введении он вызывает дозозависимое уменьшение вызванных окситоцином сокращений матки у небеременных самок крыс. У крыс на поздних сроках беременности он значительно снижает спонтанные сокращения матки в зависимости от дозы при внутривенном введении. [5]У человека ретозибан продлевает беременность и снижает вероятность преждевременных родов. Внутривенное введение ретозибана женщинам со спонтанными преждевременными родами было связано с увеличением времени до родов более чем на 1 неделю по сравнению с плацебо, значительным сокращением преждевременных родов, незначительным увеличением периода покоя матки и благоприятным профилем безопасности. Результаты демонстрируют доказательство концепции лечения угрозы самопроизвольных преждевременных родов [6]
Фармакокинетика [ править ]
Пероральная биодоступность ретозибана у крыс составляет порядка 100% с периодом полураспада 1,4 часа. Он имеет внутренний клиренс от низкого до умеренного в микросомах трех доклинических видов (крысы, собаки, яванские макаки) и низкий внутренний клиренс в микросомах человека. Он имеет хороший профиль цитохрома P450 (Cyp450) без значительного ингибирования, с IC50> 100 мкм, низким связыванием с белками (<80%) и низким прогнозируемым проникновением в ЦНС. [4]
Физические и химические свойства [ править ]
При физиологическом pH ретозибан существует в незаряженном состоянии. Он имеет хорошую растворимость (> 0,22 мг / мл) с logd 2,2. [4]
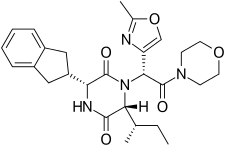
Retosiban состоит из центральной 2,5 дикетопиперазина кольца с R - инданил группой в положении 3 и R ( S -secButyl) в 6 - положении, как цис друг к другу, и с R -2-метил - оксазол кольцо на положение 7 в ациклическом амиде присоединено к положению N1. Ретосибан представляет собой (3 R , 6 R , 7 R ) -изомер и является суб-наномолярным (Ki = 0,65 нМ) антагонистом рецептора окситоцина , в то время как (3 R , 6 R , 7 S) -изомер, в котором стереохимия в боковой цепи амида у C-7 инвертирована, в 10 раз менее эффективен. Обычно в этой серии антагонистов 2,5 дикетопиперазина окситоцина (3 S , 6 S , 7 S ) изомер более чем на 500 менее активен, чем (3 R , 6 R , 7 R ) -изомер. Помимо основного ядра 2,5 дикетопиперазина, ретозибан также содержит несколько структурных характеристик, которые повышают его эффективность и безопасность. инданилгруппа в положении 3 является лучшим выбором с точки зрения активности антагониста рецептора окситоцина, ее замена фенэтильной и бензильной группами привела к прогрессивному ослаблению активности. Показано, что для C-3 предпочтительным является 4-углеродный разветвленный алкил, причем R ( S- втор-бутил) является лучшим; меньшие алкильные группы приводят к снижению активности антагонистов. [4] 2-метилоксазольное кольцо в положении 7 обеспечивает хорошую растворимость в воде, низкое связывание с белками и минимальное взаимодействие с Cyp450. Эта взаимосвязь структура-активность (SAR) подтверждается кристаллической структурой рецептора окситоцина человека в комплексе с ретозибаном [7].где липофильный инданильный заместитель проникает в глубокую, в основном гидрофобную щель на дне связывающего кармана, в то время как оксазол-морфолиновый амидный фрагмент находится ближе всего к внеклеточной поверхности. Оксазольное кольцо является заместителем, наиболее подверженным воздействию растворителя, а морфолиновое кольцо не взаимодействует напрямую с рецептором. Ядро 2,5-дикетопиперазина специфически взаимодействует с рецептором через полярный интерфейс взаимодействия.
Синтез [ править ]
Ретосибан представляет собой циклический дипептид или 2,5-дикетопиперазин, и они образуются путем циклизации соответствующего линейного дипептида. В коротком лабораторном масштабе и высоко стереоселективного синтеза из Retosiban 8 линейный пептид 5 образован четырехкомпонентной реакции Уги на карбоксибензил (Cbz) , защищенный R-indanylglycine 1 , D-аллоизолейцин гидрохлорид метилового эфира 2 , 2-methyloxazole- 4-карбоксальдегид 3 и 2-бензилоксифенилизонитрил 4 . Гидрирование для удаления защитных групп Cbz и бензила позволило циклизовать линейный пептид 5.происходить с образованием фенольного циклического дипептида 6 . Гидролиз фенольного амида реакцией с карбонилдиимидазолом (CDI) с последующим добавлением водной соляной кислоты дает кислоту 7, которая превращается в амид ретосибан 8 путем активации кислоты пептидным связывающим реагентом PyBOP (бензотриазол-1-илокситрипирролидинофосфоний гексафторфосфоний ) с последующим добавлением морфолина . [4] Хотя линейный пептид 5 и циклический дипептид 6 представляют собой смесь диастереоизомеров (7 RS) в экзоциклическом амиде гидролиз активированного фенольного амида соляной кислотой вызывает эпимеризацию в экзоциклическом положении и дает кислоту 7 с требуемой (7 R ) -стереохимией в качестве основного продукта.
См. Также [ править ]
- Атосибан
- Барусибан
- Эпельсибан
- L-368 899
- L-371,257
Ссылки [ править ]
- ^ Лиддл Дж, Аллен MJ, Бортвик А.Д., Брукс Д.П., Дэвис Д.Е., Эдвардс Р.М. и др. (Январь 2008 г.). «Открытие GSK221149A: мощного и селективного антагониста окситоцина». Письма по биоорганической и медицинской химии . 18 (1): 90–4. DOI : 10.1016 / j.bmcl.2007.11.008 . PMID 18032036 .
- ^ Бортвик AD, Liddle J (январь 2013). «Ретосибан и Эпельсибан: сильнодействующие и селективные пероральные антагонисты окситоцина». В Domling A (ред.). Методы и принципы медицинской химии: белок-белковые взаимодействия в открытии лекарств . Вайнхайм: Wiley-VCH. С. 225–256. DOI : 10.1002 / 9783527648207.ch10 . ISBN 978-3-527-33107-9.
- ^ Совет USAN (2007). «Заявление о непатентованном названии, принятое Советом USAN» (PDF) .
- ^ Б с д е е Бортвик AD, Liddle J (июль 2011). «Дизайн пероральных биодоступных антагонистов окситоцина 2,5-дикетопиперазина: от концепции до клинического кандидата на преждевременные роды». Обзоры медицинских исследований . 31 (4): 576–604. DOI : 10.1002 / med.20193 . PMID 20027670 .
- ^ a b McCafferty GP, Pullen MA, Wu C, Edwards RM, Allen MJ, Woollard PM, Borthwick AD, Liddle J, Hickey DM, Brooks DP, Westfall TD (2007). «Использование нового и высокоселективного антагониста рецепторов окситоцина для характеристики сокращений матки у крыс». Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология . 293 (1): R299–305. DOI : 10,1152 / ajpregu.00057.2007 . PMID 17395790 .
- ^ Торнтон S, Миллер Н, Валенсуэла G, J Snidow, Стиэр В, Fossler МДж, Монтегью TH, Пауэлл М, Пляж КДж (октябрь 2015). «Лечение спонтанных преждевременных родов ретозибаном: исследование фазы 2, подтверждающее концепцию» . Британский журнал клинической фармакологии . 80 (4): 740–749. DOI : 10.1111 / bcp.12646 . PMC 4594710 . PMID 25819462 .
- ^ Waltenspühl Y, Schoppe J, J Ehrenmann, куммерова л, Pluckthun А (июль 2020). «Кристаллическая структура рецептора окситоцина человека» . Наука продвигается . 6 (29): 1–11. DOI : 10.1126 / sciadv.abb5419 . PMID 32832646 .