Реакция замещения (также известная как одной реакция замещения или одной реакции замещения) представляет собой химическая реакция , в течение которого одна функциональной группы в химическом соединении заменена другой функциональной группой. [1] [2] Реакции замещения имеют первостепенное значение в органической химии . Реакции замещения в органической химии классифицируются как электрофильные или нуклеофильные в зависимости от задействованного реагента, независимо от того, является ли реакционноспособный промежуточный продукт, участвующий в реакции, карбокатион , карбанион.или свободный радикал , и является ли субстрат является алифатическим или ароматическим . Детальное понимание типа реакции помогает предсказать результат реакции. Это также полезно для оптимизации реакции с учетом таких переменных, как температура и выбор растворителя .
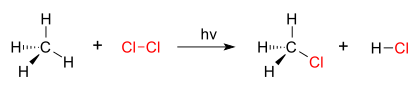
Хорошим примером реакции замещения является галогенирование . При облучении газообразного хлора (Cl 2 ) некоторые молекулы расщепляются на два радикала хлора (Cl •), свободные электроны которых сильно нуклеофильны . Один из них разрывает ковалентную связь C – H в CH 4 и захватывает атом водорода с образованием электрически нейтральной HCl. Другой радикал восстанавливает ковалентную связь с CH 3 • с образованием CH 3 Cl ( метилхлорид ).
| хлорирование метана хлором |
|---|
Нуклеофильное замещение [ править ]
В органической (и неорганической) химии нуклеофильное замещение является фундаментальным классом реакций, в которых нуклеофил избирательно связывается или атакует положительный или частично положительный заряд на атоме или группе атомов. При этом он заменяет более слабый нуклеофил, который затем становится уходящей группой ; Оставшийся положительный или частично положительный атом становится электрофилом . Вся молекулярная структура, частью которой являются электрофил и уходящая группа, обычно называется субстратом. [1] [2]
Наиболее общая форма реакции может быть дана как где R-LG указывает субстрат.
- Nuc : + R-LG → R-Nuc + LG :
Пара электронов ( : ) от нуклеофила (NUC :) атака субстрат (R-LG) формирование новой ковалентной связи Nuc-R-LG. Прежнее состояние заряда восстанавливается, когда уходящая группа (LG) уходит с электронной парой. Основным продуктом в этом случае является R-Nuc. В таких реакциях нуклеофил обычно электрически нейтрален или заряжен отрицательно, тогда как субстрат обычно нейтрален или заряжен положительно.
Примером нуклеофильного замещения является гидролиз алкилбромида , R-Br, в основных условиях, где атакующий нуклеофил представляет собой основание ОН -, а уходящей группой является Br - .
- R-Br + OH - → R-OH + Br -
Реакции нуклеофильного замещения являются обычным явлением в органической химии, и их можно в широком смысле классифицировать как происходящие на атоме углерода насыщенного алифатического соединения или (реже) на ароматическом или другом ненасыщенном углеродном центре. [1]
Механизмы [ править ]
Нуклеофильные замены на алифатических углеродных центрах могут происходить по двум различным механизмам: мономолекулярному нуклеофильному замещению ( S N 1 ) и бимолекулярному нуклеофильному замещению ( S N 2 ).
Механизм S N 1 состоит из двух ступеней. На первом этапе уходящая группа уходит, образуя карбокатион C + . На втором этапе нуклеофильный реагент (Nuc :) присоединяется к карбокатиону и образует ковалентную сигма-связь. Если субстрат имеет хиральный углерод, этот механизм может привести либо к инверсии стереохимии, либо к сохранению конфигурации. Обычно оба варианта происходят без предпочтений. Результат - рацемизация .
Механизм S N 2 имеет всего один шаг. Атака реагента и изгнание уходящей группы происходят одновременно. Этот механизм всегда приводит к инверсии конфигурации. Если субстрат, который подвергается нуклеофильной атаке, является хиральным, реакция, следовательно, приведет к инверсии его стереохимии , называемой инверсией Вальдена .
Атака S N 2 может происходить, если обратный путь атаки стерически не затруднен заместителями на субстрате. Следовательно, этот механизм обычно имеет место в беспрепятственном первичном углеродном центре. Если существует стерическое скопление на субстрате рядом с уходящей группой, например, в третичном углеродном центре, замещение будет включать механизм S N 1, а не S N 2; S N 1 также будет более вероятным в этом случае, потому что может быть образован достаточно стабильный карбокатионный промежуточный продукт.
Когда субстрат представляет собой ароматическое соединение, тип реакции представляет собой нуклеофильное ароматическое замещение , которое протекает с различными механизмами. Производные карбоновых кислот реагируют с нуклеофилами путем нуклеофильного ацильного замещения . Такой тип реакции может быть полезен при получении соединений.
Электрофильное замещение [ править ]
Электрофилы участвуют в реакциях электрофильного замещения , особенно в электрофильных ароматических замещениях .
В этом примере структура электронного резонанса бензольного кольца подвергается атаке электрофила E + . Резонирующая связь разрывается, и в результате образуется резонирующая структура карбокатиона. Наконец, выталкивается протон и образуется новое ароматическое соединение.
| Электрофильное ароматическое замещение |
|---|
Электрофильные реакции с другими ненасыщенными соединениями, кроме аренов, обычно приводят к электрофильному присоединению, а не замещению.
Радикальная подмена [ править ]
В реакции радикального замещения участвуют радикалы . Примером может служить реакция Хунсдикера .
Металлоорганическое замещение [ править ]
Реакции связывания представляют собой класс реакций, катализируемых металлами, с участием металлоорганического соединения RM и органического галогенида R'X, которые вместе реагируют с образованием соединения типа RR 'с образованием новой углерод-углеродной связи . Примеры включают реакцию Хека , реакцию Ульмана , и реакцию Вюрца-Fittig . Существует множество вариаций. [3]
Замещенные соединения [ править ]
Замещенные соединения - это химические соединения, в которых один или несколько атомов водорода в структуре ядра были заменены функциональной группой, такой как алкил , гидрокси или галоген , или более крупными группами заместителей .
Например, бензол представляет собой простое ароматическое кольцо . Бензолы, подвергшиеся замещению, представляют собой гетерогенную группу химических веществ с широким спектром применения и свойств:
| Примеры замещенных бензольных соединений | ||
| сложный | общая формула | общая структура |
| Бензол | С 6 Н 6 | |
| Толуол | C 6 H 5 -CH 3 | |
| о-ксилол | С 6 Н 4 (-СН 3 ) 2 | |
| Мезитилен | С 6 Н 3 (-СН 3 ) 3 | |
| Фенол | С 6 Н 5 -ОН | |
Ссылки [ править ]
- ^ a b c Марч, Джерри (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3 ed.), New York: Wiley, ISBN 0-471-85472-7
- ^ a b Имянитов, Наум С. (1993). «Является ли эта реакция замещением, окислением-восстановлением или переносом?». J. Chem. Educ . 70 (1): 14–16. Bibcode : 1993JChEd..70 ... 14I . DOI : 10.1021 / ed070p14 .
- ^ Elschenbroich, C .; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 3-527-28165-7.