 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Lanvis, Tabloid, другие |
| AHFS / Drugs.com | Международные названия лекарств |
| MedlinePlus | a682099 |
| Пути администрирования | устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетические данные | |
| Биодоступность | 30% (от 14% до 46%) |
| Метаболизм | Внутриклеточный |
| Ликвидация Период полураспада | 80 минут (диапазон 25–240 минут) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard | 100.005.299 |
| Химические и физические данные | |
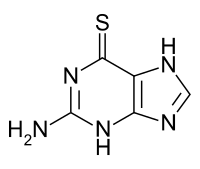
| Формула | C 5 H 5 N 5 S |
| Молярная масса | 167,19 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| | |
Тиогуанин , также известный как тиогуанин или 6-тиогуанин ( 6-TG ), представляет собой лекарство, используемое для лечения острого миелоидного лейкоза (AML), острого лимфоцитарного лейкоза (ALL) и хронического миелоидного лейкоза (CML). [1] Не рекомендуется длительное использование. [1] Принимается внутрь. [1]
Общие побочные эффекты включают подавление костного мозга , проблемы с печенью и воспаление ротовой полости . [1] [2] Во время приема лекарств рекомендуется еженедельно проверять ферменты печени . [1] Люди с генетическим дефицитом тиопурин-S-метилтрансферазы подвержены более высокому риску побочных эффектов. [2] Избегать беременности во время приема лекарств рекомендуется как мужчинам, так и женщинам. [1] Тиогуанин входит в группу антиметаболитов . [2] Это пурина аналог из гуанинаи работает, разрушая ДНК и РНК . [3]
Тиогуанин был разработан между 1949 и 1951 годами. [4] [5] Он включен в Список основных лекарственных средств Всемирной организации здравоохранения , наиболее безопасных и эффективных лекарств, необходимых в системе здравоохранения . [6]
Медицинское использование [ править ]
- Острые лейкозы как у взрослых, так и у детей
- Хронический миелолейкоз
- Воспалительное заболевание кишечника , особенно язвенный колит
- Псориаз [7]
Побочные эффекты [ править ]
- Лейкопения и нейтропения
- Тромбоцитопения
- Анемия
- Анорексия
- Тошнота и рвота
- Гепатотоксичность : проявляется как:
Веноокклюзионная болезнь печени [ править ]
Основное беспокойство, препятствующее использованию тиогуанина, - это веноокклюзионное заболевание (VOD) и его гистологическая предшественница узловая регенеративная гиперплазия (NRH). Сообщалось, что частота НРГ с тиогуанином составляет 33–76%. [8] Риск последующей VOD серьезен и часто необратим, поэтому этот побочный эффект вызывает серьезную озабоченность. Однако недавние данные с использованием модели животных для индуцированного тиогуанином NRH / VOD показали, что, вопреки предыдущим предположениям, NRH / VOD зависит от дозы, и механизм этого был продемонстрирован. [9] Это было подтверждено испытаниями на людях, в которых тиогуанин оказался безопасным, но эффективным при глютеновой болезни при использовании в дозах ниже обычно назначаемых. [10]Это привело к возрождению интереса к тиогуанину из-за его более высокой эффективности и более быстрого действия по сравнению с другими тиопуринами и иммунодепрессантами, такими как микофенилат. [11]
Противопоказания [ править ]
- Беременность
- Лактация : Предупреждение о безопасности грудного вскармливания могло быть консервативной оценкой, но данные исследований показывают, что тиопурины не проникают в грудное молоко. [12]
Взаимодействия [ править ]
Раковые опухоли, которые не реагируют на лечение меркаптопурином, не реагируют на тиогуанин. С другой стороны, некоторые случаи ВЗК, устойчивые к меркаптопурину (или его пролекарству азатиоприну), могут реагировать на тиогуанин.
Фармакогенетика [ править ]
Фермент тиопурин-S-метилтрансфераза (TPMT) отвечает за прямую инактивацию тиогуанина до его метилтиогуанинового основания - это метилирование предотвращает дальнейшее превращение тиогуанина в активные цитотоксические метаболиты тиогуаниновых нуклеотидов (TGN). [13] [14] [15] Определенные генетические вариации в гене TPMT могут приводить к снижению или отсутствию активности фермента TPMT, а у лиц, гомозиготных или гетерозиготных по этим типам генетических вариаций, могут быть повышенные уровни метаболитов TGN и повышенный риск тяжелого угнетения костного мозга ( миелосупрессия) при приеме тиогуанина. [13] Во многих этнических группах полиморфизмы TPMT, которые приводят к снижению или отсутствию активности TPMT, встречаются с частотой примерно 5%, что означает, что около 0,25% пациентов являются гомозиготными по этим вариантам. [13] [16] Однако анализ активности TPMT в эритроцитах или генетический тест TPMT может идентифицировать пациентов со сниженной активностью TPMT, что позволяет скорректировать дозу тиопурина или полностью отказаться от препарата. [13] [17] На этикетке тиогуанина, одобренной FDA, отмечается, что пациенты с дефицитом TPMT могут быть предрасположены к развитию миелосупрессии.и что лаборатории предлагают тестирование на дефицит TPMT. [18] Действительно, тестирование активности TPMT в настоящее время является одним из немногих примеров фармакогенетики, применяемой в повседневной клинической помощи. [19]
Метаболизм и фармакокинетика [ править ]
Однократная пероральная доза тиогуанина имеет неполный метаболизм, всасывание и высокую индивидуальную вариабельность. Биодоступность тиогуанина составляет в среднем 30% (диапазон 14-46%). Максимальная концентрация в плазме после однократного приема внутрь достигается через 8 часов.
Тиогуанин, как и другие тиопурины, цитотоксичен для лейкоцитов; в результате он оказывает иммуносупрессивное действие при более низких дозах и противолейкозный / противоопухолевый при более высоких дозах. Тиогуанин включен в клетки костного мозга человека, но, как и другие тиопурины, неизвестно, проникает ли он через гематоэнцефалический барьер. Тиогуанин не может быть обнаружен в спинномозговой жидкости , как и близкородственное соединение 6-меркаптопурин, которое также не может проникать в мозг.
Период полувыведения тиогуанина из плазмы короткий из-за быстрого всасывания в печень и клетки крови и превращения в 6-TGN. Средний период полувыведения из плазмы составляет 80 минут с диапазоном 25–240 минут. Тиогуанин выводится в основном через почки с мочой, но в основном в виде метаболита, 2-амино-6-метилтиопурина. Однако внутриклеточные тио-нуклеотидные метаболиты тиогуанина (6-TGN) имеют более длительный период полураспада и, следовательно, могут быть измерены после удаления тиогуанина из плазмы.
Тиогуанин катаболизируется (расщепляется) двумя путями. [20] Один путь заключается в дезаминировании ферментом гуаниндезаминазой до 6-тиоксантина, который имеет минимальную противоопухолевую активность, а затем путем окисления тиоксантина ксантиноксидазой до тиуровой кислоты.. Этот метаболический путь не зависит от эффективности ксантиноксидазы, поэтому ингибитор ксантиноксидазы, лекарственный препарат аллопуринол, не блокирует распад тиогуанина, в отличие от его ингибирования распада родственного тиопурин-6-меркаптопурина. Второй путь - это метилирование тиогуанина до 2-амино-6-метилтиопурина, который минимально эффективен в качестве противоопухолевого средства и значительно менее токсичен, чем тиогуанин. Этот путь также не зависит от ферментативной активности ксантиноксидазы.
Механизм действия [ править ]
6-Тиогуанин является тио аналогом природного пуринового основания гуанина. 6-тиогуанин использует фермент гипоксантин-гуанинфосфорибозилтрансферазу (HGPRTase), который превращается в 6-тиогуанозинмонофосфат (TGMP). Высокие концентрации TGMP могут накапливаться внутри клетки и препятствовать синтезу гуаниновых нуклеотидов с помощью фермента инозинмонофосфатдегидрогеназы ( IMP-дегидрогеназа ). [21]
TGMP превращается путем фосфорилирования в тиогуанозиндифосфат (TGDP) и тиогуанозинтрифосфат (TGTP). Одновременно образуются дезоксирибозильные аналоги с помощью фермента рибонуклеотидредуктазы . TGMP, TGDP и TGTP вместе называются 6-тиогуаниновыми нуклеотидами (6-TGN). 6-TGN цитотоксичны для клеток за счет: (1) включения в ДНК во время фазы синтеза (S-фаза) клетки; и (2) посредством ингибирования GTP-связывающего белка ( G-белка ) Rac1 , который регулирует путь Rac / Vav. [22]
Химия [ править ]
Это бледно-желтый кристаллический порошок без запаха.
Имена [ править ]
Тиогуанин ( INN , BAN , AAN ) или тиогуанин ( USAN ).
Тиогуанин принимают внутрь (в таблетках - «Ланвис»).
Ссылки [ править ]
- ^ a b c d e f Британский национальный формуляр: BNF 69 (изд. 69). Британская медицинская ассоциация. 2015. С. 588, 592. ISBN. 9780857111562.
- ^ a b c «Таблетки тиогуанина 40 мг - Сводка характеристик продукта (SPC) - (eMC)» . www.medicines.org.uk . Архивировано 21 декабря 2016 года . Проверено 21 декабря +2016 .
- ^ Голан, Дэвид Э .; Ташджян, Армен Х .; Армстронг, Эрин Дж. (2011). Принципы фармакологии: патофизиологические основы медикаментозной терапии . Липпинкотт Уильямс и Уилкинс. п. 686. ISBN. 9781608312702. Архивировано 21 декабря 2016 года.
- ^ Сигель, Астрид; Сигель, Хельмут (1996). Ионы металлов в биологических системах: Том 32: Взаимодействие ионов металлов с нуклеотидами: нуклеиновые кислоты и их составляющие . CRC Press. п. 302. ISBN. 9780824795498. Архивировано 21 декабря 2016 года.
- ^ Ландау, Ральф; Ахилладелис, Василий; Скрябин, Александр (1999). Фармацевтические инновации: революция в здоровье человека . Фонд химического наследия. п. 342. ISBN. 9780941901215. Архивировано 21 декабря 2016 года.
- ^ Всемирная организация здравоохранения (2019). Примерный перечень Всемирной организации здравоохранения основных лекарственных средств: список двадцать первых 2019 . Женева: Всемирная организация здравоохранения. ЛВП : 10665/325771 . WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- Перейти ↑ Mason C, Krueger GG (январь 2001 г.). «Тиогуанин при рефрактерном псориазе: 4-летний опыт». Варенье. Акад. Дерматол . 44 (1): 67–72. DOI : 10.1067 / mjd.2001.109296 . PMID 11148479 .
- ^ Дубинский MC, Василяускас Э.А., Сингх Х. и др. (2003). «6-тиогуанин может вызвать серьезное повреждение печени у пациентов с воспалительными заболеваниями кишечника». Гастроэнтерология . 125 (2): 298–303. DOI : 10.1016 / S0016-5085 (03) 00938-7 . PMID 12891528 .
- ^ Oancea я, Png CW, Дас I, R Лурье, Винклер И.Г., и др. (Июль 2012 г.). «Новая модель веноокклюзионного заболевания на мышах обеспечивает стратегии предотвращения токсичности для печени, вызванной тиогуанином». Кишечник . 62 (4): 594–605. DOI : 10.1136 / gutjnl-2012-302274 . PMID 22773547 . S2CID 29585979 .
- ^ Tack GJ ван Asseldonk DP ван Wanrooij RL, и др. (Август 2012 г.). «Тиогуанин в лечении рефрактерной целиакии - опыт единственного центра». Алимент Pharmacol Ther . 36 (3): 274–81. DOI : 10.1111 / j.1365-2036.2012.05154.x . PMID 22646133 . S2CID 24811114 .
- ^ Ван Asseldonk DP, Oancea I, Jharap B, и др. (Март 2012 г.). «Можно ли избежать синдрома синусоидальной обструкции, связанного с тиогуанином? Уроки, извлеченные из лечения воспалительного заболевания кишечника 6-тиогуанином и модели на мышах». Бюстгальтеры Rev Assoc Med . 58 (Дополнение 1): S8–13.
- ^ Гардинер SJ, Gearry RB, Робертс RL и др. (2006). «Воздействие тиопуриновых препаратов через грудное молоко невелико, исходя из концентраций метаболитов в парах мать-младенец» . Br J Clin Pharmacol . 62 (4): 453–6. DOI : 10.1111 / j.1365-2125.2006.02639.x . PMC 1885151 . PMID 16995866 .
- ^ a b c d Реллинг М. В., Гарднер Э. Э., Сандборн В. Дж., Шмигелоу К., Пуи Ч., Йи С. В., Стейн С. М., Каррильо М., Эванс В. Е., Кляйн Т. Е.; Консорциум по внедрению клинической фармакогенетики (март 2011 г.). «Рекомендации Консорциума по внедрению клинической фармакогенетики для определения генотипа тиопуринметилтрансферазы и дозирования тиопурина» . Clin Pharmacol Ther . 89 (3): 387–91. DOI : 10.1038 / clpt.2010.320 . PMC 3098761 . PMID 21270794 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Заза G, Чеок M, N Krynetskaia, Thorn C, Stocco G, Эбер JM, Маклеод H, Weinshilboum RM, Relling М.В., Evans WE, Klein TE, Альтман RB (сентябрь 2010). «Тиопуриновый путь» . Pharmcogenet Genomics . 20 (9): 573–4. DOI : 10.1097 / FPC.0b013e328334338f . PMC 3098750 . PMID 19952870 .
- ↑ Fujita K, Sasaki Y (август 2007 г.). «Фармакогеномика в ферментах, метаболизирующих лекарства, катализирующих противоопухолевые препараты для персонализированной химиотерапии рака» . Curr. Drug Metab . 8 (6): 554–62. DOI : 10.2174 / 138920007781368890 . PMID 17691917 . Архивировано 12 января 2013 года.
- ^ Мучлер, Эрнст; Шефер-Кортинг, Моника (2001). Arzneimittelwirkungen (на немецком языке) (8-е изд.). Штутгарт: Wissenschaftliche Verlagsgesellschaft. С. 107, 936. ISBN 3-8047-1763-2.
- ^ Payne, K .; Newman, W .; Fargher, E .; Tricker, K .; Брюс, Индиана; Оллер, WER (2007). «Тестирование TPMT в ревматологии: что лучше, чем рутинный мониторинг?» . Ревматология . 46 (5): 727–729. DOI : 10.1093 / ревматологических / kel427 . PMID 17255139 .
- ^ "ТАБЛОИД-тиогуанин таблетка" . DailyMed . Проверено 17 марта 2015 года .
- ^ Ван L, Pelleymounter L, R Weinshilboum, Johnson JA, Эбер JM, Altman RB, Кляйн TE (июнь 2010). «Очень важное резюме фармакогена: тиопурин-S-метилтрансфераза» . Pharmacogenet Genomics . 20 (6): 401–5. DOI : 10.1097 / FPC.0b013e3283352860 . PMC 3086840 . PMID 20154640 .
- ^ Oncea I; Дулей Дж. (2008). «Глава 38. Фармакогенетика тиопуринов». В Брантоне, LL; Лазо, JS; Паркер, К. (ред.). Гудман и Гилман Фармакологические основы терапии (11-е изд.). McGraw-Hill's Access Medicine (он-лайн).
- ^ Эванс МЫ. (2004). «Фармакогенетика тиопурин-S-метилтрансферазы и тиопуриновая терапия» . Ther Drug Monit . 26 (2): 186–91. DOI : 10.1097 / 00007691-200404000-00018 . PMID 15228163 . S2CID 34015182 .
- ^ де Бур Н.К., ван Бодегравен А.А., Джарап Б. и др. (Декабрь 2007 г.). «Drug Insight: фармакология и токсичность тиопуриновой терапии у пациентов с ВЗК». Нат Клин Практ Гастроэнтерол Гепатол . 4 (12): 686–94. DOI : 10.1038 / ncpgasthep1000 . PMID 18043678 . S2CID 23686284 .
Дальнейшее чтение [ править ]
- Дин Л. (2012). «Тиогуаниновая терапия и генотип TPMT» . В Pratt VM, McLeod HL, Rubinstein WS, et al. (ред.). Резюме по медицинской генетике . Национальный центр биотехнологической информации (NCBI). PMID 28520351 . Код книжной полки: NBK100663.
Внешние ссылки [ править ]
- «Тиогуанин» . Информационный портал о наркотиках . Национальная медицинская библиотека США.