| Тригональная бипирамидальная молекулярная геометрия | |
|---|---|
 | |
| Примеры | ПФ 5 , Fe (CO) 5 |
| Группа точек | Д 3ч |
| Координационный номер | 5 |
| Угол крепления | 90 °, 120 ° |
| μ (полярность) | 0 |
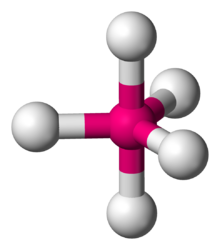
В химии образование тригональной бипирамиды представляет собой молекулярную геометрию с одним атомом в центре и еще 5 атомами в углах треугольной бипирамиды . Это та геометрия, для которой валентные углы, окружающие центральный атом, не идентичны (см. Также пентагональную бипирамиду ), потому что не существует геометрического расположения с пятью концевыми атомами в эквивалентных положениях. Примерами такой молекулярной геометрии являются пентафторид фосфора (PF 5 ) и пентахлорид фосфора (PCl 5 ) в газовой фазе. [1]
Осевое (или апикальное) и экваториальное положения [ править ]
Не все пять атомов, связанных с центральным атомом, эквивалентны, и определены два разных типа положения. Для пентахлорида фосфора, например, атом фосфора имеет общую плоскость с тремя атомами хлора, расположенными под углом 120 ° друг к другу в экваториальных положениях, и еще двумя атомами хлора выше и ниже плоскости ( осевое или апикальное положения).
Согласно теории геометрии молекул VSEPR , осевое положение более тесно, потому что осевой атом имеет три соседних экваториальных атома (на одном центральном атоме) под углом связи 90 °, тогда как экваториальный атом имеет только два соседних осевых атома на Угол крепления 90 °. Для молекул с пятью идентичными лигандами длины аксиальных связей имеют тенденцию быть больше, потому что атом лиганда не может приближаться к центральному атому так близко. Например, в PF 5 осевая длина связи P-F составляет 158 пм, а экваториальная - 152 пм, а в PCl 5 аксиальная и экваториальная длина составляют 214 и 202 пм соответственно. [1]
В смешанном галогениде PF 3 Cl 2 хлор занимает два экваториальных положения [1], что указывает на то, что фтор имеет большую апикофильность или тенденцию занимать аксиальное положение. В общем, апикофильность лиганда увеличивается с электроотрицательностью, а также со способностью акцептировать пи-электрон, как в последовательности Cl <F <CN. [2] Оба фактора уменьшают концентрацию электронов в области связи около центрального атома, так что скученность в осевом положении менее важна.
Связанные геометрии с одинокими парами [ править ]
Теория VSEPR также предсказывает, что замещение лиганда в центральном атоме неподеленной парой валентных электронов оставляет общую форму расположения электронов неизменной, и неподеленная пара теперь занимает одну позицию. Для молекул с пятью парами валентных электронов, включая как связывающие пары, так и неподеленные пары, электронные пары по-прежнему расположены в тригональной бипирамиде, но одно или несколько экваториальных положений не прикреплены к атому лиганда, так что геометрия молекулы (только для ядер) отличается.
Качелей молекулярная геометрия находится в тетрафторида серы (SF 4 ) с центральным атомом серы окружен четырьмя атомами фтора , занимающих два осевых и двух экваториальных положениях, а также один экваториальной неподеленной пары, что соответствует АХ 4 молекулы Е в AX обозначениях . Т-образная молекулярная геометрия находится в трехфтористом хлоре (CLF 3 ), в АХ 3 Е 2 молекулы с атомами фтора в двух осевых и одного экваториальном положении, а также два экваториальных неподеленного пара. Наконец, трииодид- ион ( I-
3) также основан на тригональной бипирамиде, но реальная молекулярная геометрия линейна с концевыми атомами йода только в двух аксиальных положениях и тремя экваториальными позициями, занятыми неподеленными парами электронов (AX 2 E 3 ); Другой пример такой геометрии - дифторид ксенона XeF 2 .
Псевдовращение ягод [ править ]
Изомеры с тригонально-бипирамидальной геометрией способны взаимопревращаться посредством процесса, известного как псевдовращение Берри . Псевдовращение похоже на концепцию движения конформационного диастереомера, хотя полных оборотов не происходит. В процессе псевдовращения два экваториальных лиганда (оба имеют более короткую длину связи, чем третий) «смещаются» к оси молекулы, в то время как аксиальные лиганды одновременно «смещаются» к экватору, создавая постоянное циклическое движение. Псевдовращение особенно заметно в простых молекулах, таких как пентафторид фосфора (PF 5 ).
См. Также [ править ]
Ссылки [ править ]
- ^ a b c Housecroft, CE; Шарп, AG (2004). Неорганическая химия (2-е изд.). Прентис Холл. п. 407. ISBN. 978-0-13-039913-7.
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) « Апикофильность ». DOI : 10,1351 / goldbook.AT06990
Внешние ссылки [ править ]
- Центр молекулярной структуры Университета Индианы
- Интерактивные молекулярные примеры для точечных групп
- Молекулярное моделирование
- Анимированный тригональный планарный визуал
