 | |
 | |
| Имена | |
|---|---|
| Другие имена Карбид циркония (I) | |
| Идентификаторы | |
| ECHA InfoCard | 100.031.920 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| Номер ООН | 3178 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| ZrC | |
| Молярная масса | 103,235 г · моль -1 |
| Внешность | Серое тугоплавкое твердое тело |
| Запах | Без запаха |
| Плотность | 6,73 г / см 3 (24 ° C) [1] |
| Температура плавления | 3,532–3,540 ° C (6,390–6,404 ° F; 3,805–3,813 K) [1] [2] |
| Точка кипения | 5 100 ° C (9 210 ° F, 5 370 К) [2] |
| Нерастворимый | |
| Растворимость | Растворим в концентрированной H 2 SO 4 , HF , [1] HNO 3. |
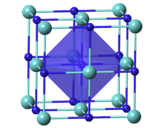
| Структура | |
| Кубическая , cF8 [3] | |
| Fm 3 m, № 225 [3] | |
а = 4,6976 (4) Å [3] α = 90 °, β = 90 °, γ = 90 ° | |
| Октаэдрический [3] | |
| Термохимия | |
Теплоемкость ( C ) | 37,442 Дж / моль · К [4] |
Стандартная мольная энтропия ( S | 33,14 Дж / моль · К [4] |
Std энтальпия формации (Δ F H ⦵ 298 ) | −207 кДж / моль (экстраполировано на стехиометрический состав) [5] −196,65 кДж / моль [4] |
| Опасности | |
| Основные опасности | Пирофорный |
| Пиктограммы GHS | [6] |
| Сигнальное слово GHS | Опасность |
Положения об опасности GHS | H228 , H302 , H312 , H332 [6] |
Меры предосторожности GHS | P210 , P280 [6] |
| NFPA 704 (огненный алмаз) |  0 0 0 |
| Родственные соединения | |
Другие анионы | Нитрид циркония Оксид циркония |
Другие катионы | Карбид титана Карбид гафния Карбид ванадия Карбид ниобия Карбид тантала Карбид хрома Карбид молибдена Карбид вольфрама |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Карбид циркония ( Zr C ) - чрезвычайно твердый тугоплавкий керамический материал [7], коммерчески используемый в насадках для режущих инструментов. Обычно его обрабатывают спеканием .
Свойства [ править ]
Коэффициенты теплового расширения ZrC [2] | |
|---|---|
| Т | α V |
| 100 ° С | 0,141 |
| 200 ° С | 0,326 |
| 400 ° С | 0,711 |
| 800 ° С | 1,509 |
| 1200 ° С | 2,344 |
Он имеет вид серого металлического порошка с кубической кристаллической структурой . Он очень устойчив к коррозии . Этот карбид переходного металла внедрения группы IV также входит в состав сверхвысокотемпературной керамики или (UHTC). Благодаря наличию металлической связи ZrC имеет теплопроводность 20,5 Вт / м · К и электрическую проводимость (удельное сопротивление ~ 43 мкОм · см), которые аналогичны таковым для металлического циркония. Прочная ковалентная связь Zr-C придает этому материалу очень высокую температуру плавления (~ 3530 ° C), высокий модуль (~ 440 ГПа) и твердость (25 ГПа). ZrC имеет более низкую плотность (6,73 г / см 3) по сравнению с другими карбидами, такими как WC (15,8 г / см 3 ), TaC (14,5 г / см 3 ) или HfC (12,67 г / см 3 ). ZrC кажется подходящим для использования в космических аппаратах , ракетных / прямоточных реактивных двигателях или сверхзвуковых транспортных средствах, для которых критически важны несущие способности при низкой плотности и высоких температурах . [ необходима цитата ]
Как и большинство карбидов тугоплавких металлов, карбид циркония субстехиометрический, т. Е. Содержит углеродные вакансии. При содержании углерода выше, чем приблизительно ZrC 0,98, материал содержит свободный углерод. [5] ZrC стабилен при соотношении углерода к металлу от 0,65 до 0,98.
Карбиды металлов группы IVA , TiC , ZrC и SiC практически инертны по отношению к воздействию сильных водных кислот (HCl) и сильных водных оснований (NaOH) даже при 100 ° C, однако ZrC реагирует с HF.
Смесь карбида циркония и карбида тантала является важным металлокерамическим материалом. [ необходима цитата ]
Использует [ редактировать ]
Не содержащий гафния карбид циркония и карбид ниобия могут использоваться в качестве тугоплавких покрытий в ядерных реакторах . Из-за малого сечения поглощения нейтронов и слабой чувствительности к повреждению при облучении он находит применение в качестве покрытия из диоксида урана и частиц диоксида тория в ядерном топливе . Покрытие обычно наносят термическим химическим осаждением из паровой фазы в реакторе с псевдоожиженным слоем . Он также обладает высоким коэффициентом излучения и высокой токовой нагрузкой при повышенных температурах, что делает его многообещающим материалом для использования в термофотовольтаических радиаторах, наконечниках и массивах полевых эмиттеров. [ необходима цитата ]
Он также используется в качестве абразивного материала , в облицовке , в металлокерамику , раскаленных нитей и режущие инструменты. [ необходима цитата ]
Производство [ править ]
Карбид циркония можно получить несколькими способами. Один из методов - карботермическая реакция диоксида циркония графитом. В результате получается порошок. Затем можно получить уплотненный ZrC путем спекания порошка ZrC при температуре выше 2000 ° C. Горячее прессование ZrC может снизить температуру спекания и, следовательно, способствует получению полностью уплотненного мелкозернистого ZrC. Искровое плазменное спекание также использовалось для получения полностью уплотненного ZrC. [8]
Карбид циркония также может быть получен путем обработки на основе раствора. [9] Это достигается кипячением оксида металла с ацетилацетоном.
Другой метод изготовления - химическое осаждение из газовой фазы. [10] Это достигается нагреванием циркониевой губки и пропусканием через нее галогенидного газа.
Плохая стойкость к окислению при температуре выше 800 ° C ограничивает применение ZrC. Одним из способов повышения стойкости ZrC к окислению является создание композитов. Важными предлагаемыми композитами являются композит ZrC-ZrB 2 и ZrC-ZrB 2 -SiC. Эти композиты могут работать при температуре до 1800 ° C. [ необходима цитата ] Другой способ улучшить это - использовать другой материал в качестве барьерного слоя, например, в топливных частицах TRISO.
Ссылки [ править ]
- ^ a b c Лиде, Дэвид Р., изд. (2009). CRC Справочник по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0.
- ^ a b c Перри, Дейл Л. (2011). Справочник неорганических соединений (2-е изд.). CRC Press. п. 472. ISBN. 978-1-4398-1461-1.
- ^ а б в г Кемптер, CP; Фрайз, Р.Дж. (1960). «Кристаллографические данные. 189. Карбид циркония». Аналитическая химия . 32 (4): 570. DOI : 10.1021 / ac60160a042 .
- ^ a b c Карбид циркония в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (получено 30 июня 2014 г.)
- ^ a b Бейкер, FB; Штормы, ЭК; Холли, CE (1969). «Энтальпия образования карбида циркония». Журнал химических и технических данных . 14 (2): 244. DOI : 10.1021 / je60041a034 .
- ^ a b c Sigma-Aldrich Co. , карбид циркония (IV) . Проверено 30 июня 2014.
- ^ Измерение и теория твердости карбидов переходных металлов, особенно карбида тантала. Schwab, GM; Krebs, A. Phys.-Chem. Inst., Univ. Мюнхен, Мюнхен, Фед. Rep. Ger. Planseeberichte fuer Pulvermetallurgie (1971), 19 (2), 91-110.
- ^ Вэй, Сялу; Назад, Кристина; Ижванов, Олег; Хейнс, Кристофер; Олевский, Евгений (2016). «Карбид циркония, полученный методом искрового плазменного спекания и горячего прессования: кинетика уплотнения, рост зерен и тепловые свойства» . Материалы . 9 (7): 577. Bibcode : 2016Mate .... 9..577W . DOI : 10,3390 / ma9070577 . PMC 5456903 . PMID 28773697 .
- ^ Мешки, Майкл Д .; Ван, Чан-Ань; Ян, Чжаохуэй; Джайн, Анубхав (2004). «Карботермический восстановительный синтез нанокристаллических порошков карбида циркония и карбида гафния с использованием прекурсоров на основе растворов». Журнал материаловедения . 39 (19): 6057–6066. DOI : 10,1023 / Б: JMSC.0000041702.76858.a7 .
- ^ https://www.researchgate.net/publication/229653039_Deposition_Mechanism_for_Chemical_Vapor_Deposition_of_Zirconium_Carbide_Coatings