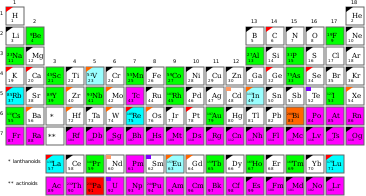
Моноизотопная элемент является элементом , который имеет только один стабильный изотоп (нуклидов). Всего 26 элементов обладают этим свойством. Список приведен в следующем разделе.
Стабильность химических элементов определяется экспериментально, поскольку существует ряд стабильных нуклидов с атомными номерами более ~ 40, которые теоретически нестабильны, но, по-видимому, имеют настолько длительный период полураспада, что они не наблюдались прямо или косвенно (по результатам измерения продуктов). разлагаться.
Моноизотопные элементы характеризуются, за исключением единственного случая, нечетным числом протонов (нечетное Z ) и четным числом нейтронов. Из-за увеличения энергии за счет эффектов спаривания ядер нечетное число протонов придает нестабильность изотопам с нечетным Z , что в более тяжелых элементах требует полностью спаренного набора нейтронов, чтобы компенсировать эту тенденцию к стабильности. (Четыре стабильных нуклида с нечетным Z и нечетным числом нейтронов - это водород-2, литий-6, бор-10 и азот-14.)
Единственным мононуклидным исключением из правила нечетных Z является бериллий; его единственный стабильный первичный изотоп, бериллий-9, имеет 4 протона и 5 нейтронов. Этот элемент не имеет стабильного изотопа с равным числом нейтронов и протонов ( бериллий-8 , по 4 каждого из них) из-за его нестабильности к альфа-распаду , чему способствует чрезвычайно прочное связывание ядер гелия-4 . Он не может иметь стабильный изотоп с 4 протонами и 6 нейтронами из-за очень большого несоответствия в соотношении протон / нейтрон для такого легкого элемента. (Тем не менее, бериллий-10 имеет период полураспада 1,36 миллиона лет, что слишком мало, чтобы быть изначальным., но все же указывает на необычную стабильность для легкого изотопа с таким дисбалансом.)
Дифференциация от мононуклидных элементов [ править ]
Набор моноизотопных элементов перекрывается, но не совпадает с набором из 21 мононуклидного элемента , которые характеризуются наличием только одного изотопа (нуклида), встречающегося в природе. [1] Причиной этого является наличие в природе некоторых долгоживущих радиоактивных первичных нуклидов , которые могут образовывать примеси с моноизотопами и, таким образом, препятствовать тому, чтобы они были естественными мононуклидами. Это происходит в случаях 7 ( 26 - 19 = 7 ) моноизотопных элементов. Эти изотопы являются моноизотопами, но из-за присутствия долгоживущего радиоактивного первичного нуклида не являются мононуклидами. Эти элементы: ванадий , рубидий , индий ,лантан , европий , рений и лютеций . См. Список ниже; в двух отмеченных случаях (индий и рений) долгоживущий радионуклид на самом деле является наиболее распространенным изотопом в природе, а стабильный изотоп - менее распространенным.
В 2 дополнительных случаях ( висмут [2] и протактиний ) изначально присутствуют мононуклидные элементы, которые не являются моноизотопами, потому что встречающийся в природе нуклид радиоактивен, и, таким образом, элемент вообще не имеет стабильных изотопов. Чтобы элемент был моноизотопным, он должен иметь один стабильный нуклид.
Список (стабильных с точки зрения наблюдений) моноизотопных элементов, упорядоченных по атомному номеру и весу [ править ]
Немононуклидные элементы отмечены звездочкой и дан долгоживущий первичный радиоизотоп . В двух примечательных случаях (индий и рений) наиболее распространенным изотопом природного происхождения является умеренно радиоактивный изотоп, а в случае европия - почти половина.
- Бериллий-9
- Фтор-19
- Натрий-23
- Алюминий-27
- Фосфор-31
- Скандий-45
- Ванадий-51 * в природе встречается с 0,25% радиоактивного ванадия-50.
- Марганец-55
- Кобальт-59
- Мышьяк-75
- Рубидий-85 * в природе встречается с 27,835% радиоактивного рубидия-87.
- Иттрий-89
- Ниобий-93
- Родий-103
- Индий-113 * в природе встречается с большинством (95,7%) радиоактивного изотопа индия-115.
- Йод-127
- Цезий-133
- Лантан-139 * в природе встречается с 0,09% радиоактивного лантана-138.
- Празеодим-141
- Европий-153 * в природе встречается с 47,8% радиоактивного европия-151.
- Тербий-159
- Гольмий-165
- Тулий-169
- Лютеций-175 * в природе встречается с 2,59% радиоактивного лютеция-176.
- Рений-185 * в природе встречается с большинством (62,6%) радиоактивного изотопа рений-187.
- Золото-197
См. Также [ править ]
- Первородный нуклид
- Список нуклидов (отсортированный по периодам полураспада)
- Таблица нуклидов
- Изотопная геохимия
- Радионуклид
- Мононуклидный элемент
- Стабильный изотоп
- Список элементов по стабильности изотопов
Ссылки [ править ]
- ^ Н.Э. Холден, "Стандартные значения атомного веса для мононуклидных элементов - 2001", BNL-NCS-68362 , Брукхейвенская национальная лаборатория (2001)
- ↑ До 2003 годасчиталось, что 209 Bi относились к первой категории. Затем было обнаружено, что его период полураспада составляет 10 19 лет, что примерно в миллиард раз превышает возраст Вселенной. См. Висмут
Внешние ссылки [ править ]
- Атомный вес элементов по состоянию на 2000 год, с разделом о моноизотопах, начинающейся на странице 708