Ноцицептор
| Ноцицептор | |
|---|---|
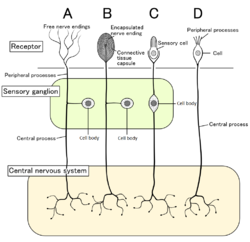 Четыре типа сенсорных нейронов и их рецепторных клеток. Ноцицепторы показаны как свободные нервные окончания типа А. | |
| Идентификаторы | |
| МеШ | D009619 |
| Анатомическая терминология | |
Ноцицептор ( « болевой рецептор») — это сенсорный нейрон , который реагирует на повреждающие или потенциально повреждающие стимулы, посылая сигналы «возможная угроза» [1] [2] [3] [4] в спинной и головной мозг. Если мозг воспринимает угрозу как реальную, он создает ощущение боли, чтобы привлечь внимание к части тела, поэтому можно надеяться, что угрозу можно смягчить; этот процесс называется ноцицепцией .
История
Ноцицепторы были открыты Чарльзом Скоттом Шеррингтоном в 1906 году. В прежние века ученые полагали, что животные подобны механическим устройствам, преобразующим энергию сенсорных раздражителей в двигательные реакции. Шеррингтон провел много разных экспериментов, чтобы продемонстрировать, что разные типы стимуляции рецептивного поля афферентного нервного волокна приводят к разным реакциям. Некоторые интенсивные раздражители вызывают рефлекторное отторжение , определенные вегетативные реакции и боль . Специфические рецепторы для этих интенсивных раздражителей были названы ноцицепторами. [5]
Место расположения
У млекопитающих ноцицепторы находятся в любой области тела, способной воспринимать вредные раздражители. Внешние ноцицепторы находятся в таких тканях , как кожа ( кожные ноцицепторы ), роговица и слизистая оболочка . Внутренние ноцицепторы находятся в различных органах, таких как мышцы , суставы , мочевой пузырь , внутренние органы и пищеварительный тракт. Тела этих нейронов расположены либо в ганглиях задних корешков , либо в ганглиях тройничного нерва . [6]Ганглии тройничного нерва являются специализированными нервами для лица, тогда как ганглии задних корешков связаны с остальной частью тела. Аксоны проходят в периферическую нервную систему и оканчиваются ветвями, образуя рецептивные поля.
Разработка
Ноцицепторы развиваются из стволовых клеток нервного гребня . Нервный гребень отвечает за большую часть раннего развития позвоночных. Он конкретно отвечает за развитие периферической нервной системы (ПНС). Стволовые клетки нервного гребня отделяются от нервной трубки, когда она закрывается, и ноцицепторы вырастают из дорсальной части этой ткани нервного гребня. Они формируются поздно во время нейрогенеза. Ранее формирующиеся клетки из этой области могут стать нечувствительными к боли рецепторами, либо проприорецепторами , либо низкопороговыми механорецепторами . Все нейроны, происходящие из нервного гребня, включая эмбриональные ноцицепторы, экспрессируют TrkA, который является рецептором фактора роста нервов .(НГФ). Однако факторы транскрипции, определяющие тип ноцицептора, остаются неясными. [7]
После сенсорного нейрогенеза происходит дифференцировка и формируются два типа ноцицепторов. Они классифицируются как пептидергические или непептидергические ноцицепторы, каждый из которых экспрессирует отдельный репертуар ионных каналов и рецепторов. Их специализация позволяет рецепторам иннервировать различные центральные и периферические мишени. Эта дифференциация происходит как в перинатальном, так и в постнатальном периоде. Непептидергические ноцицепторы выключают киназу рецептора тропомиозина A или TrkA и начинают экспрессировать Ret, который является трансмембранным сигнальным компонентом, который обеспечивает экспрессию нейротрофического фактора глиальной клеточной линии .(ГДНФ). Этому переходу помогает Runx1, жизненно важный для развития непептидергических ноцицепторов. Напротив, пептидергические ноцицепторы продолжают использовать TrkA и экспрессируют совершенно другой тип фактора роста. В настоящее время проводится много исследований о различиях между ноцицепторами. [7]
Типы и функции
Периферический терминал зрелого ноцицептора - это место, где повреждающие раздражители обнаруживаются и преобразуются в электрическую энергию. [8] Когда электрическая энергия достигает порогового значения, индуцируется потенциал действия , направляемый в центральную нервную систему .(ЦНС). Это приводит к череде событий, которые позволяют сознательно осознавать боль. Сенсорная специфичность ноцицепторов определяется высоким порогом только к отдельным признакам раздражителей. Ноцицепторы срабатывают только тогда, когда достигается высокий порог химической, термической или механической среды. Большинство ноцицепторов классифицируются по тому, на какие модальности окружающей среды они реагируют. Некоторые ноцицепторы реагируют более чем на одну из этих модальностей и, следовательно, называются полимодальными. Другие ноцицепторы не реагируют ни на одну из этих модальностей (хотя они могут реагировать на стимуляцию в условиях воспаления) и называются спящими или молчащими.
Ноцицепторы имеют два разных типа аксонов. Первыми являются аксоны волокон Aδ . Они миелинизированы и могут позволить потенциалу действия двигаться со скоростью около 20 метров в секунду по направлению к ЦНС. Другой тип — более медленно проводящие аксоны С-волокна . Они работают только со скоростью около 2 метров в секунду. [9]Это связано со светлой или без миелинизации аксона. В результате боль проходит в две фазы. Первая фаза опосредована быстропроводящими Aδ-волокнами, а вторая часть – (полимодальными) C-волокнами. Боль, связанная с волокнами Aδ, может быть связана с начальной чрезвычайно острой болью. Вторая фаза — более продолжительное и несколько менее интенсивное ощущение боли в результате острого повреждения. Если есть массивное или продолжительное входное отверстие для С-волокна, в спинном роге спинного мозга происходит прогрессирующее наращивание; это явление похоже на столбняк в мышцах, но называется завыванием . Если происходит заводнение, существует вероятность повышенной чувствительности к боли. [10]
Термальный
Термические ноцицепторы активируются вредным теплом или холодом при различных температурах. Существуют специфические ноцицепторные преобразователи, которые отвечают за то, как конкретное нервное окончание реагирует на температурный раздражитель. Первым был обнаружен TRPV1 , порог которого совпадает с температурой тепловой боли 43 °C. Другая температура в диапазоне теплого-горячего опосредована более чем одним каналом TRP . Каждый из этих каналов экспрессирует определенный С-концевой домен, который соответствует тепло-горячей чувствительности. Взаимодействия между всеми этими каналами и то, как определяется уровень температуры выше болевого порога, в настоящее время неизвестны. Прохладные стимулы воспринимаются TRPM8 .каналы. Его С-концевой домен отличается от термочувствительных TRP. Хотя этот канал соответствует холодовым раздражителям, пока неизвестно, способствует ли он также обнаружению сильного холода. Интересное открытие, связанное с холодовыми раздражителями, заключается в том, что тактильная чувствительность и двигательная функция ухудшаются, в то время как восприятие боли сохраняется.
механический
Механические ноцицепторы реагируют на избыточное давление или механическую деформацию. Они также реагируют на надрезы, которые нарушают поверхность кожи. Реакция на раздражитель обрабатывается корой как боль, точно так же, как химические и температурные реакции. Эти механические ноцицепторы часто имеют полимодальные характеристики. Таким образом, возможно, что некоторые преобразователи тепловых раздражителей одинаковы и для механических раздражителей. То же самое относится и к химическим раздражителям, поскольку TRPA1, по-видимому, обнаруживает как механические, так и химические изменения. Некоторые механические раздражители могут вызывать высвобождение промежуточных химических веществ, таких как АТФ , который может быть обнаружен пуринергическими рецепторами P2 , или фактор роста нервов , который может быть обнаружен киназой рецептора тропомиозина A (TrkA).. [11]
Химическая
Химические ноцицепторы имеют каналы TRP, которые реагируют на широкий спектр специй. Тот, который вызывает наибольший отклик и очень широко тестируется, — это капсаицин . Другие химические стимуляторы являются раздражителями окружающей среды, такими как акролеин , химическое оружие времен Первой мировой войны и компонент сигаретного дыма. Помимо этих внешних стимуляторов, химические ноцицепторы способны обнаруживать эндогенные лиганды и определенные амины жирных кислот, возникающие в результате изменений во внутренних тканях. Как и в термических ноцицепторах, TRPV1 может обнаруживать такие химические вещества, как капсаицин, а также токсины и кислоты пауков. [7] [11] Кислотно-чувствительные ионные каналы (ASIC) также обнаруживают кислотность. [11]
Спящий/молчаливый
Хотя каждый ноцицептор может иметь множество возможных пороговых уровней, некоторые из них вообще не реагируют на химические, термические или механические раздражители, если на самом деле не произошло повреждение. Их обычно называют молчащими или спящими ноцицепторами, поскольку их реакция проявляется только в начале воспаления окружающих тканей. [6]
Полимодальный
Многие нейроны выполняют только одну функцию; поэтому нейроны, выполняющие эти функции в комплексе, получают классификацию «полимодальные». [12]
Путь
по возрастанию
Афферентные ноцицептивные волокна (те, которые посылают информацию в головной мозг , а не из него) возвращаются в спинной мозг , где образуют синапсы в его дорсальных рогах . Это ноцицептивное волокно (расположенное на периферии) является нейроном первого порядка. Клетки спинного рога разделены на физиологически обособленные слои, называемые пластинками . Различные типы волокон образуют синапсы в разных слоях и используют либо глутамат , либо вещество P в качестве нейротрансмиттера. Волокна Aδ образуют синапсы в пластинках I и V, волокна C соединяются с нейронами в пластинках II, волокна Aβ соединяются с пластинками I, III и V. [6] Достигнув определенной пластинки в спинном мозге, ноцицептивные нейроны первого порядка проецируются на нейроны второго порядка, которые пересекают среднюю линию у передней белой спайки. Нейроны второго порядка затем посылают свою информацию через два пути в таламус : медиально-лемнисковую систему дорсального столба и переднебоковую систему . Первый предназначен больше для регулярных безболезненных ощущений, а второй - для болевых ощущений. Достигнув таламуса, информация обрабатывается в вентральном заднем ядре и отправляется в кору головного мозга по волокнам задней ножки внутренней капсулы.
По убыванию
Поскольку существует восходящий путь к мозгу, который инициирует сознательное осознание боли, существует также и нисходящий путь, модулирующий болевые ощущения. Мозг может запросить высвобождение определенных гормонов или химических веществ, которые могут оказывать обезболивающее действие, уменьшая или подавляя болевые ощущения. Область мозга, стимулирующая выброс этих гормонов, называется гипоталамус . [13] Этот эффект нисходящего торможения можно продемонстрировать при электрической стимуляции периакведуктальной серой области среднего мозга или перивентрикулярного ядра . Они оба, в свою очередь, проецируются на другие области, участвующие в регуляции боли, такие как большое ядро шва.который также получает аналогичные афференты от парагигантоцеллюлярного ретикулярного ядра (NPG). В свою очередь, большое ядро шва проецируется в область желатинозного вещества заднего рога и опосредует ощущение спиноталамических входов. Сначала это осуществляется большим швом ядра , который посылает серотонинергические нейроны к нейронам спинного мозга, которые, в свою очередь, секретируют энкефалин к интернейронам, отвечающим за восприятие боли. [14] Энкефалин действует путем связывания опиоидных рецепторов , вызывая ингибирование постсинаптических нейронов, тем самым подавляя боль. [11] Околоакведуктальный серый цвет также содержитопиоидных рецепторов, что объясняет один из механизмов обезболивающего действия опиоидов, таких как морфин и диацетилморфин .
Чувствительность
Чувствительность ноцицепторных нейронов модулируется большим количеством медиаторов во внеклеточном пространстве. [15] Периферическая сенсибилизация представляет собой форму функциональной пластичности ноцицептора. Ноцицептор может превратиться из простого детектора вредных раздражителей в детектор невредных раздражителей. В результате стимулы низкой интенсивности от регулярной деятельности вызывают болезненные ощущения. Это широко известно как гипералгезия . Воспаление является одной из частых причин, приводящих к сенсибилизации ноцицепторов. Обычно гипералгезия прекращается, когда воспаление стихает, однако иногда генетические дефекты и/или повторные травмы могут привести к аллодинии.: совершенно безвредный раздражитель, такой как легкое прикосновение, вызывает сильную боль. Аллодиния также может быть вызвана повреждением ноцицептора в периферических нервах. Это может привести к деафферентации, что означает развитие различных центральных отростков из сохранившегося афферентного нерва. В этой ситуации выжившие аксоны задних корешков ноцицепторов могут контактировать со спинным мозгом, тем самым изменяя нормальный вход. [10]
Другие животные
Ноцицепция была зарегистрирована у немлекопитающих животных, включая рыб [16] и широкий спектр беспозвоночных , включая пиявок , [17] червей - нематод , [18] морских слизней [ 19] и личинок плодовых мушек . [20] Хотя эти нейроны могут иметь другие пути и связи с центральной нервной системой, чем ноцицепторы млекопитающих, ноцицептивные нейроны у немлекопитающих часто возбуждаются в ответ на такие же стимулы, как и у млекопитающих, такие как высокая температура (40 градусов по Цельсию или более), низкая рН , капсаицин и повреждение тканей.
Терминология
Из-за исторического неправильного понимания боли ноцицепторы также неуместно называют болевыми рецепторами . Хотя любая боль реальна, психологические факторы могут сильно влиять на субъективную интенсивность. [21]
Смотрите также
- Капсаицин и его механизм действия на ноцицепторы.
- Пиперин из черного перца
- Ионный канал TRPC
использованная литература
- ^ http://www.bodyinmind.org/what-is-pain/
- ^ "НОИ - Нейроортопедический институт" . www.noigroup.com . Архивировано из оригинала 17 октября 2018 г. . Проверено 13 октября 2017 г. .
- ^ «Ноцицепция и боль: в чем разница и почему это важно? - Массаж Сент-Луис, Сент-Луис, Миссури» . www.massage-stlouis.com .
- ↑ Животные, Комитет Национального исследовательского совета (США) по распознаванию и облегчению боли в лаборатории (8 декабря 2017 г.). Механизмы Боли . National Academy Press (США) – через www.ncbi.nlm.nih.gov.
- ^ Шеррингтон С. Интегративное действие нервной системы. Оксфорд: Издательство Оксфордского университета; 1906 г.
- ^ a b c Джессел, Томас М .; Кандел, Эрик Р .; Шварц, Джеймс Х. (1991). Принципы нейронауки . Норуолк, Коннектикут: Appleton & Lange. стр. 472–79 . ISBN 978-0-8385-8034-9.
- ^ a b c Вульф CJ, Ma Q (август 2007 г.). «Ноцицепторы - детекторы вредных раздражителей» . Нейрон . 55 (3): 353–64. doi : 10.1016/j.neuron.2007.07.016 . PMID 17678850 . S2CID 13576368 .
- ^ Fein, A Ноцицепторы: клетки, которые чувствуют боль http://cell.uchc.edu/pdf/fein/nociceptors_fein_2012.pdf
- ^ Уильямс, SJ; Первес, Дейл (2001). Неврология . Сандерленд, Массачусетс: Sinauer Associates. ISBN 978-0-87893-742-4.
- ^ a b Филдс Х.Л., Роуботэм М., Бэрон Р. (октябрь 1998 г.). «Постгерпетическая невралгия: раздражительные ноцицепторы и деафферентация». Нейробиол. Дис . 5 (4): 209–27. doi : 10.1006/nbdi.1998.0204 . PMID 9848092 . S2CID 13217293 .
- ^ a b c d Юань, Джейсон; Брукс, Хеддвен Л.; Бармен, Сьюзан М .; Барретт, Ким Э. (2019). Обзор медицинской физиологии Ганонга . ISBN 978-1-26-012240-4.
- ^ Фейн, Алан. Ноцицепторы: клетки, которые чувствуют боль .
- ^ "Путь боли" . Проверено 2 июня 2008 г. .[ мертвая ссылка ]
- ^ Холл, Майкл Э .; Холл, Джон Э. (2021). Учебник Гайтона и Холла по медицинской физиологии (14-е изд.). Филадельфия, Пенсильвания: Saunders/Elsevier. ISBN 978-0-323-59712-8.
- ↑ Hucho T, Levine JD (август 2007 г.). «Сигнальные пути при сенсибилизации: к биологии ноцицепторных клеток» . Нейрон . 55 (3): 365–76. doi : 10.1016/j.neuron.2007.07.008 . PMID 17678851 . S2CID 815135 .
- ^ Снеддон Л.У.; Брейтуэйт В.А.; Нежный МЮ (2003). «Есть ли у рыб ноцицепторы? Доказательства эволюции сенсорной системы позвоночных» . Труды Лондонского королевского общества B: Биологические науки . 270 (1520): 1115–1121. doi : 10.1098/rspb.2003.2349 . ПВК 1691351 . PMID 12816648 .
- ^ Пастор Дж .; Сория Б.; Бельмонте К. (1996). «Свойства ноцицептивных нейронов сегментарного ганглия пиявки» . Журнал нейрофизиологии . 75 (6): 2268–2279. doi : 10.1152/jn.1996.75.6.2268 . PMID 8793740 .
- ^ Виттенбург Н.; Баумайстер Р. (1999). «Тепловое избегание у Caenorhabditis elegans : подход к изучению ноцицепции» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (18): 10477–10482. Бибкод : 1999PNAS...9610477W . doi : 10.1073/pnas.96.18.10477 . ЧВК 17914 . PMID 10468634 .
- ^ Ильич П.А.; Уолтерс ET (1997). «Механосенсорные нейроны, иннервирующие сифон Aplysia , кодируют вредные раздражители и проявляют ноцицептивную сенсибилизацию» . Журнал неврологии . 17 (1): 459–469. doi : 10.1523/JNEUROSCI.17-01-00459.1997 . ПВК 6793714 . PMID 8987770 .
- ^ Трейси Дж.; Дэниел В.; Уилсон Р.И.; Лоран Г.; Бензер С. (2003). « безболезненный , ген дрозофилы необходим для ноцицепции» . Сотовый . 113 (2): 261–273. doi : 10.1016/S0092-8674(03)00272-1 . PMID 12705873 . S2CID 1424315 .
- ^ «Странная боль: изменчивое, вводящее в заблуждение ощущение» .
- Рецепторы чувств
- ноцицепция
- Рецепторные клетки