| Поищите аллостерический язык в Викисловаре, бесплатном словаре. |
В биохимии , аллостерическая регулирование (или аллостерическое управление ) является регуляцией фермента путем связывания эффекторной молекулы на участке, кроме фермента активного сайта . [1]
Сайт, с которым связывается эффектор, называется аллостерическим сайтом или регуляторным сайтом . Аллостерические сайты позволяют эффекторам связываться с белком, что часто приводит к конформационным изменениям, связанным с динамикой белка . Эффекторы, которые усиливают активность белка, называются аллостерическими активаторами , тогда как те, которые снижают активность белка, называются аллостерическими ингибиторами .
Аллостерические регуляции являются естественным примером контуров управления, таких как обратная связь от последующих продуктов или прямая связь от исходных субстратов. Аллостерия на большие расстояния особенно важна для передачи сигналов клетками . [2] Аллостерическая регуляция также особенно важна для способности клетки регулировать активность ферментов .
Термин allostery происходит от древнегреческих Allos ( ἄλλος ), "других", и музыкальные центры ( στερεὀς ), "твердое тело (объект)". Это относится к тому факту, что регуляторный сайт аллостерического белка физически отличается от его активного сайта.
Модели [ править ]
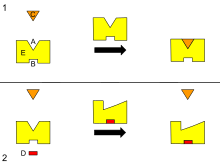
B - Аллостерический сайт
C - Субстрат
D - Ингибитор
E - Фермент
Это диаграмма аллостерической регуляции фермента.
Многие аллостерические эффекты могут быть объяснены согласованной моделью MWC выдвинутых Моно, Вайманом и Changeux , [3] или с помощью последовательной модели (также известной как модель KNF) , описанной Кошланда, Неметите и Филмер. [4] Оба постулируют, что белковые субъединицы существуют в одной из двух конформаций , напряженной (T) или расслабленной (R), и что расслабленные субъединицы связывают субстрат легче, чем субъединицы в напряженном состоянии. Две модели больше всего различаются своими предположениями о взаимодействии субъединиц и предсуществовании обоих состояний. Для белков, в которых субъединицы существуют более чем в двух конформацияхможно использовать ландшафтную модель аллостерии, описанную Куендет, Вайнштейном и ЛеВином [5] .
Согласованная модель [ править ]
Согласованная модель аллостерии, также называемая моделью симметрии или моделью MWC , постулирует, что субъединицы фермента связаны таким образом, что конформационные изменения в одной субъединице обязательно передаются всем остальным субъединицам. Таким образом, все субъединицы должны существовать в одной и той же конформации. Модель также утверждает, что в отсутствие какого-либо лиганда (субстрата или другого) равновесие благоприятствует одному из конформационных состояний, T или R. Равновесие может быть смещено в состояние R или T посредством связывания одного лиганда ( аллостерический эффектор или лиганд) на сайт, отличный от активного сайта (аллостерический сайт).
Последовательная модель [ править ]
Последовательная модель аллостерической регуляции утверждает, что субъединицы не связаны таким образом, чтобы конформационные изменения в одной вызывали аналогичные изменения в других. Таким образом, все субъединицы фермента не требуют одинаковой конформации. Более того, последовательная модель диктует, что молекулы субстрата связываются посредством протокола индуцированной подгонки . Хотя такая индуцированная подгонка переводит субъединицу из напряженного состояния в расслабленное состояние, она не распространяет конформационные изменения на соседние субъединицы. Вместо этого связывание с субстратом одной субъединицы лишь незначительно изменяет структуру других субъединиц, так что их сайты связывания становятся более восприимчивыми к субстрату. Подвести итоги:
- субъединицы не обязательно должны существовать в одной и той же конформации
- молекулы субстрата связываются по протоколу индуцированной подгонки
- конформационные изменения не распространяются на все субъединицы
Модель Морфеина [ править ]
Morpheein модель аллостерическому регулирования является диссоциативной согласованной моделью. [6]
Морфеин - это гомоолигомерная структура, которая может существовать как ансамбль физиологически значимых и функционально различных альтернативных четвертичных ансамблей. Переходы между альтернативными сборками морфеина включают диссоциацию олигомеров, конформационные изменения в диссоциированном состоянии и повторную сборку с образованием другого олигомера. Требуемый этап разборки олигомера отличает модель морфеина для аллостерической регуляции от классических моделей MWC и KNF.
Порфобилиногенсинтаза (PBGS) является прототипом морфеина.
Ансамблевые модели [ править ]
Ансамблевые модели аллостерической регуляции перечисляют статистический ансамбль аллостерической системы как функцию ее потенциальной энергетической функции , а затем связывают конкретные статистические измерения аллостерии с определенными энергетическими терминами в энергетической функции (такими как межмолекулярный солевой мост между двумя доменами). [7] Ансамблевые модели, такие как ансамблевая аллостерическая модель [8] и аллостерическая модель Изинга [9], предполагают, что каждая область системы может принимать два состояния, аналогичные модели MWC. Модель ландшафта аллостерии, представленная Куэндет, Вайнштейном и Левином [5] позволяет доменам иметь любое количество состояний, и вклад определенного молекулярного взаимодействия в данное аллостерическое взаимодействие можно оценить с помощью строгого набора правил. Моделирование молекулярной динамики может использоваться для оценки статистического ансамбля системы, чтобы его можно было проанализировать с помощью ландшафтной модели аллостерии.
Аллостерическая модуляция [ править ]
Аллостерическая модуляция используется для изменения активности молекул и ферментов в биохимии и фармакологии. Для сравнения, типичное лекарство создается для связывания с активным центром фермента, что, таким образом, запрещает связывание субстрата с этим ферментом, вызывая снижение активности фермента. Аллостерическая модуляция происходит, когда эффектор связывается с аллостерическим сайтом (также известным как регуляторный сайт) фермента и изменяет активность фермента. Аллостерические модуляторы предназначены для того, чтобы соответствовать аллостерическому сайту, чтобы вызвать конформационное изменение фермента, в частности изменение формы активного сайта, которое затем вызывает изменение его активности. В отличие от обычных лекарств модуляторы не являются конкурентными ингибиторами.. Они могут быть положительными (активирующими), вызывающими повышение активности фермента, или отрицательными (ингибирующими), вызывающими снижение активности фермента. Использование аллостерической модуляции позволяет контролировать эффекты специфической активности ферментов; в результате аллостерические модуляторы очень эффективны в фармакологии. [10] В биологической системе аллостерическую модуляцию трудно отличить от модуляции посредством представления субстрата .
Модель измерения энергии [ править ]
Примером этой модели является Mycobacterium tuberculosis , бактерия, которая идеально приспособлена к жизни в макрофагах человека. Сайты фермента служат связью между различными субстратами. В частности, между AMP и G6P . Такие сайты также служат механизмом определения эффективности фермента. [11]
Положительная модуляция [ править ]
Положительная аллостерическая модуляция (также известная как аллостерическая активация ) происходит, когда связывание одного лиганда увеличивает притяжение между молекулами субстрата и другими сайтами связывания. Примером является связывание молекул кислорода с гемоглобином , где кислород эффективно является и субстратом, и эффектором. Аллостерический или «другой» сайт является активным сайтом соседней белковой субъединицы . Связывание кислорода с одной субъединицей вызывает конформационные изменения в этой субъединице, которая взаимодействует с оставшимися активными сайтами, чтобы усилить ихкислородное сродство. Другой пример аллостерической активации наблюдается в цитозольной IMP-GMP специфической 5'-нуклеотидазе II (cN-II), где сродство к субстрату GMP увеличивается при связывании GTP на границе раздела димеров.
Отрицательная модуляция [ править ]
Отрицательная аллостерическая модуляция (также известная как аллостерическое ингибирование ) происходит, когда связывание одного лиганда снижает сродство к субстрату на других активных сайтах. Например, когда 2,3-BPG связывается с аллостерическим сайтом гемоглобина, сродство к кислороду всех субъединиц снижается. Это когда в сайте связывания отсутствует регулятор.
Прямые ингибиторы тромбина являются прекрасным примером отрицательной аллостерической модуляции. Были обнаружены аллостерические ингибиторы тромбина, которые потенциально могут использоваться в качестве антикоагулянтов.
Другой пример - стрихнин , судорожный яд, который действует как аллостерический ингибитор рецептора глицина . Глицин является основным пост- синаптической тормозящее нейротрансмиттера в млекопитающих спинного мозга и ствола головного мозга . Стрихнин действует в отдельном сайте связывания на рецепторе глицина аллостерическим образом; то есть его связывание снижает сродство рецептора глицина к глицину. Таким образом, стрихнин подавляет действие тормозящего медиатора, что приводит к судорогам.
Другой пример, в котором может наблюдаться отрицательная аллостерическая модуляция, - это между АТФ и ферментом фосфофруктокиназой внутри петли отрицательной обратной связи, которая регулирует гликолиз . Фосфофруктокиназа ( как правило , называют ФФК ) представляет собой фермент , который катализирует третий этап гликолиза: фосфорилирование из фруктозо-6-фосфата в фруктозо-1,6-дифосфат . PFK может аллостерически подавляться высокими уровнями АТФ в клетке. Когда уровни АТФ высоки, АТФ будет связываться с аллосторным участком фосфофруктокиназы., вызывая изменение трехмерной формы фермента. Это изменение приводит к снижению его сродства к субстрату ( фруктозо-6-фосфату и АТФ ) в активном центре, и фермент считается неактивным. Это вызывает прекращение гликолиза при высоком уровне АТФ, таким образом сохраняя глюкозу в организме и поддерживая сбалансированный уровень клеточного АТФ. Таким образом, АТФ служит отрицательным аллостерическим модулятором для PFK, несмотря на то, что он также является субстратом фермента.
Типы [ править ]
Гомотропный [ править ]
Гомотропный аллостерический модулятор является субстратом для своего целевого фермента , а также регулирующей молекулой активности фермента. Обычно это активатор фермента. [1] Например, O 2 и CO являются гомотропными аллостерическими модуляторами гемоглобина. Аналогично, в IMP / GMP-специфической 5'-нуклеотидазе связывание одной молекулы GMP с единственной субъединицей тетрамерного фермента приводит к увеличению сродства к GMP последующих субъединиц, как показано на графиках зависимости сигмоидального субстрата от скорости. [1]
Гетеротропный [ править ]
Гетеротропный аллостерический модулятор - это регуляторная молекула, которая не является субстратом фермента. Это может быть активатор или ингибитор фермента. Например, H + , CO 2 и 2,3-бисфосфоглицерат являются гетеротропными аллостерическими модуляторами гемоглобина. [12] И снова в IMP / GMP-специфической 5'-нуклеотидазе связывание молекулы GTP на границе димера в тетрамерном ферменте приводит к увеличению сродства к субстрату GMP в активном центре, что указывает на гетеротропную аллостерическую активацию K-типа. [1]
Как было подробно описано выше, некоторые аллостерические белки могут регулироваться как их субстратами, так и другими молекулами. Такие белки способны к гомотропным и гетеротропным взаимодействиям. [1]
Основные активаторы [ править ]
Некоторые аллостерические активаторы называют «незаменимыми» или «облигатными» активаторами в том смысле, что в их отсутствие активность их целевого фермента очень низкая или незначительная, как в случае с активностью N-ацетилглутамата в отношении карбамоилфосфата. синтетазой I, например. [13] [14]
Нерегулирующая аллостерия [ править ]
Нерегулирующий аллостерический сайт - это любой нерегулирующий компонент фермента (или любого белка), который сам по себе не является аминокислотой. Например, многие ферменты требуют связывания натрия для обеспечения правильного функционирования. Однако натрий не обязательно действует как регуляторная субъединица; натрий присутствует всегда, и нет известных биологических способов добавления / удаления натрия для регулирования активности ферментов. Нерегулирующая аллостерия может включать любые другие ионы, помимо натрия (кальция, магния, цинка), а также другие химические вещества и, возможно, витамины.
Фармакология [ править ]
Аллостерическая модуляция рецептора является результатом связывания аллостерических модуляторов в другом сайте (« регуляторный сайт »), отличном от сайта эндогенного лиганда (« активный сайт »), и усиливает или подавляет эффекты эндогенного лиганда. В нормальных условиях он действует, вызывая конформационные изменения в молекуле рецептора, что приводит к изменению аффинности связывания лиганда. Таким образом, аллостерический лиганд модулирует активацию рецептора своим первичным ортостерическим лигандом, и можно думать, что он действует как диммер в электрической цепи, регулируя интенсивность ответа.
Например, рецептор ГАМК A имеет два активных сайта, которые связывают нейромедиатор гамма-аминомасляная кислота (ГАМК), но также имеет сайты связывания, регулирующие бензодиазепин и общий анестетик . Каждый из этих регуляторных сайтов может производить положительную аллостерическую модуляцию, усиливая активность ГАМК. Диазепам является положительным аллостерическим модулятором в регуляторном сайте бензодиазепина, а его антидот флумазенил является антагонистом .
Более свежие примеры лекарств, которые аллостерически модулируют свои мишени, включают цинакальцет, имитирующий кальций, и маравирок для лечения ВИЧ .
Аллостерические сайты как мишени для лекарств [ править ]
Аллостерические сайты могут представлять собой новую мишень для лекарств . Существует ряд преимуществ использования аллостерических модуляторов в качестве предпочтительных терапевтических агентов по сравнению с классическими ортостерическими лигандами. Например, сайты аллостерического связывания рецептора, связанного с G-белком (GPCR), не столкнулись с таким же эволюционным давлением, как ортостерические сайты для размещения эндогенного лиганда, поэтому они более разнообразны. [15] Таким образом, большая селективность GPCR может быть достигнута путем нацеливания на аллостерические сайты. [15] Это особенно полезно для GPCR, где селективная ортостерическая терапия была затруднена из-за сохранения последовательности ортостерического сайта у подтипов рецепторов. [16]Кроме того, эти модуляторы обладают пониженным потенциалом токсических эффектов, поскольку модуляторы с ограниченным взаимодействием будут иметь максимальный уровень своего действия, независимо от введенной дозы. [15] Другой тип фармакологической селективности, который является уникальным для аллостерических модуляторов, основан на кооперативности. Аллостерический модулятор может проявлять нейтральную кооперативность с ортостерическим лигандом на всех подтипах данного рецептора, кроме интересующего подтипа, который называется «абсолютной селективностью подтипа». [16] Если аллостерический модулятор не обладает заметной эффективностью, он может обеспечить другое мощное терапевтическое преимущество перед ортостерическими лигандами, а именно способность селективно настраивать повышающие или понижающие тканевые ответы только при наличии эндогенного агониста. [16] Сайты связывания малых молекул, специфичные для олигомеров, являются лекарственными мишенями для имеющих медицинское значение морфеинов . [17]
Синтетические аллостерические системы [ править ]
Существует множество синтетических соединений, содержащих несколько нековалентных сайтов связывания, которые проявляют конформационные изменения при занятии одного сайта. Кооперативность между вкладом единичного связывания в таких супрамолекулярных системах является положительной, если занятие одного сайта связывания увеличивает аффинность Δ G во втором сайте, и отрицательной, если аффинность не повышена. Большинство синтетических аллостерических комплексов основаны на конформационной реорганизации при связывании одного эффекторного лиганда, что затем приводит либо к усилению, либо к ослаблению ассоциации второго лиганда с другим сайтом связывания. [18] [19] [20]Конформационное связывание между несколькими сайтами связывания в искусственных системах обычно намного больше, чем в белках с их обычно большей гибкостью. Параметр, определяющий эффективность (измеряемый соотношением констант равновесия Krel = KA (E) / KA в присутствии и отсутствии эффектора E), представляет собой конформационную энергию, необходимую для принятия закрытой или напряженной конформации для связывания лиганда. А. [21]
Во многих поливалентных супрамолекулярных системах [22] может происходить прямое взаимодействие между связанными лигандами, что может привести к большому взаимодействию. Наиболее распространено такое прямое взаимодействие между ионами в рецепторах ионных пар. [23] [24] Это сотрудничество часто также называют аллостерией, хотя конформационные изменения здесь не обязательно запускают события связывания.
Интернет-ресурсы [ править ]
Аллостерическая база данных [ править ]
Аллостерия - это прямое и эффективное средство регуляции биологической функции макромолекул, возникающее за счет связывания лиганда в аллостерическом сайте, топографически отличном от ортостерического сайта. Ожидается, что из-за часто высокой селективности рецепторов и более низкой токсичности в отношении мишеней аллостерическая регуляция будет играть все большую роль в открытии лекарств и биоинженерии. База данных AlloSteric (ASD, http://mdl.shsmu.edu.cn/ASD ) [25]предоставляет центральный ресурс для отображения, поиска и анализа структуры, функций и соответствующих аннотаций для аллостерических молекул. В настоящее время ASD содержит аллостерические белки более 100 видов и модуляторы трех категорий (активаторы, ингибиторы и регуляторы). Каждый белок снабжен аннотацией с подробным описанием аллостерии, биологического процесса и связанных заболеваний, а каждый модулятор - сродством связывания, физико-химическими свойствами и терапевтической областью. Интеграция информации об аллостерических белках в РАС должна позволить предсказывать аллостерию для неизвестных белков с последующей экспериментальной проверкой. Кроме того, модуляторы, настроенные в ASD, могут использоваться для исследования потенциальных аллостерических целей для запрашиваемого соединения,и может помочь химикам внести изменения в структуру для создания новых аллостерических лекарств.
Аллостерические остатки и их предсказание [ править ]
Не все белковые остатки играют одинаково важную роль в аллостерической регуляции. Идентификация остатков, необходимых для аллостерии (так называемых «аллостерических остатков»), была в центре внимания многих исследований, особенно в последнее десятилетие. [26] [27] [28] [29] [30] [31] [32] [33] Отчасти этот растущий интерес является результатом их общей важности в науке о белках, но также и потому, что аллостерические остатки могут использоваться в биомедицинские контексты . Фармакологически важные белки с сайтами, на которые трудно воздействовать, могут уступить место подходам, в которых один альтернативно нацелен на более легкие для доступа остатки, которые способны аллостерически регулировать первичный интересующий сайт. [34]Эти остатки в широком смысле можно классифицировать как поверхностные и внутренние аллостерические аминокислоты. Аллостерические сайты на поверхности обычно играют регулирующую роль, фундаментально отличную от таковых внутри; поверхностные остатки могут служить рецепторами или эффекторными сайтами при передаче аллостерических сигналов, тогда как те, что находятся внутри, могут действовать, чтобы передавать такие сигналы. [35]
См. Также [ править ]
- База данных ASD
- Конкурентное торможение
- Кооперативная привязка
- Кинетика ферментов
- Белковая динамика
- Теория рецепторов
Ссылки [ править ]
- ^ a b c d e Сринивасан Б., Фоухар Ф, Шукла А., Сампанги С., Кулкарни С., Абашидзе М., Ситараман Дж., Лью С., Мао Л., Актон ТБ, Сяо Р., Эверетт Дж. К., Монтелионе GT, Тонг Л., Баларам Х. (Март 2014 г.). «Аллостерическая регуляция и активация субстрата в цитозольной нуклеотидазе II из Legionella pneumophila» . Журнал FEBS . 281 (6): 1613–1628. DOI : 10.1111 / febs.12727 . PMC 3982195 . PMID 24456211 .
- ↑ Bu Z, Callaway DJ (2011). «Белки движутся! Белковая динамика и дальняя аллостерия в передаче сигналов клетки». Структура белка и заболевания . Достижения в химии белков и структурной биологии. 83 . С. 163–221. DOI : 10.1016 / B978-0-12-381262-9.00005-7 . ISBN 9780123812629. PMID 21570668 .
- ^ Моно J, Вайман J, Changeux JP (май 1965 г.). «О природе аллостерических переходов: правдоподобная модель». Журнал молекулярной биологии . 12 : 88–118. DOI : 10.1016 / s0022-2836 (65) 80285-6 . PMID 14343300 .
- ^ Кошланда DE, Némethy G, Filmer D (январь 1966). «Сравнение экспериментальных данных связывания и теоретических моделей в белках, содержащих субъединицы». Биохимия . 5 (1): 365–85. DOI : 10.1021 / bi00865a047 . PMID 5938952 .
- ^ a b Cuendet MA, Weinstein H, LeVine MV (декабрь 2016 г.). «Аллостерический пейзаж: количественная оценка термодинамических связей в биомолекулярных системах» . Журнал химической теории и вычислений . 12 (12): 5758–5767. DOI : 10.1021 / acs.jctc.6b00841 . PMC 5156960 . PMID 27766843 .
- ↑ Jaffe EK (сентябрь 2005 г.). «Морфеины - новая структурная парадигма аллостерической регуляции». Направления биохимических наук . 30 (9): 490–7. DOI : 10.1016 / j.tibs.2005.07.003 . PMID 16023348 .
- ^ Motlagh HN, Wrabl JO, Li J, Hilser VJ (апрель 2014). «Ансамблевый характер аллостерии» . Природа . 508 (7496): 331–9. Bibcode : 2014Natur.508..331M . DOI : 10,1038 / природа13001 . PMC 4224315 . PMID 24740064 .
- ^ Hilser VJ, Wrabl JO, Motlagh HN (2012). «Структурно-энергетические основы аллостерии» . Ежегодный обзор биофизики . 41 : 585–609. DOI : 10,1146 / annurev-Biophys-050511-102319 . PMC 3935618 . PMID 22577828 .
- ^ ЛеВин М.В., Weinstein H (май 2015). «AIM для аллостерии: использование модели Изинга для понимания обработки и передачи информации в аллостерических биомолекулярных системах» . Энтропия . 17 (5): 2895–2918. Bibcode : 2015Entrp..17.2895L . DOI : 10.3390 / e17052895 . PMC 4652859 . PMID 26594108 .
- ↑ Abdel-Magid AF (февраль 2015 г.). «Аллостерические модуляторы: новая концепция в открытии лекарств» . Письма по медицинской химии ACS . 6 (2): 104–7. DOI : 10.1021 / ml5005365 . PMC 4329591 . PMID 25699154 .
- ^ Аллостерическая пируваткиназа на основе «логических ворот» синергетически определяет уровни энергии и сахара у Mycobacterium tuberculosis Венхэ Чжун, Лян Цуй, Бун Чонг Го, Циксу Цай, Пейин Хо, Йок Хиан Чион, Мэн Юань, Аббас Эль Сахили, Линда А. Фотергилл -Гилмор, Малкольм Д. Уолкиншоу, Жюльен Лескар и Питер К. Дедон http://rdcu.be/A44I
- ^ Эдельштейн SJ (1975). «Кооперативные взаимодействия гемоглобина». Ежегодный обзор биохимии . 44 : 209–32. DOI : 10.1146 / annurev.bi.44.070175.001233 . PMID 237460 .
- ^ Ши D, Allewell Н.М., Tuchman M (июнь 2015). «Семейство N-ацетилглутамат-синтазы: структуры, функции и механизмы» . Международный журнал молекулярных наук . 16 (6): 13004–22. DOI : 10.3390 / ijms160613004 . PMC 4490483 . PMID 26068232 .
- ↑ de Cima S, Polo LM, Díez-Fernández C, Martínez AI, Cervera J, Fita I, Rubio V (ноябрь 2015 г.). «Структура человеческой карбамоилфосфатсинтетазы: расшифровка включения / выключения уреагенеза человека» . Научные отчеты . 5 (1): 16950. Bibcode : 2015NatSR ... 516950D . DOI : 10.1038 / srep16950 . PMC 4655335 . PMID 26592762 .
- ^ a b c A. Christopoulos, LT May, VA Avlani и PM Sexton (2004) Аллостеризм рецепторов, связанных с G-белками: перспективы и проблемы. Труды Биохимического общества, том 32, часть 5
- ^ a b c May LT, Leach K, Sexton PM, Christopoulos A (2007). «Аллостерическая модуляция рецепторов, связанных с G-белком». Ежегодный обзор фармакологии и токсикологии . 47 : 1–51. DOI : 10.1146 / annurev.pharmtox.47.120505.105159 . PMID 17009927 .
- Перейти ↑ Jaffe EK (2010). "Морфеины - новый путь к открытию аллостерических лекарств ~! ~ 12 февраля 2010! 21 мая 2010! 08 июня 2010!" . Журнал "Материалы открытой конференции" . 1 : 1–6. DOI : 10.2174 / 2210289201001010001 . PMC 3107518 . PMID 21643557 .
- ^ Такеучи М, Икеда М, Sugasaki А, Синкай S (ноябрь 2001 г.). «Молекулярный дизайн искусственных молекулярных и ионных систем распознавания с аллостерическими гостевыми ответами». Счета химических исследований . 34 (11): 865–73. DOI : 10.1021 / ar0000410 . PMID 11714258 .
- ^ Кремер C, Люцен A (май 2013). «Искусственные аллостерические рецепторы». Химия . 19 (20): 6162–96. DOI : 10.1002 / chem.201203814 . PMID 23463705 .
- ^ Ковбасюк L, Кремер R (июнь 2004). «Аллостерические супрамолекулярные рецепторы и катализаторы». Химические обзоры . 104 (6): 3161–87. DOI : 10.1021 / cr030673a . PMID 15186190 .
- ↑ Schneider HJ (сентябрь 2016 г.). «Параметры эффективности в искусственных аллостерических системах». Органическая и биомолекулярная химия . 14 (34): 7994–8001. DOI : 10.1039 / c6ob01303a . PMID 27431438 .
- ^ Badjić JD, Nelson A, Cantrill SJ, Тернбулл WB, Стоддарт JF (сентябрь 2005). «Многовалентность и кооперативность в супрамолекулярной химии». Счета химических исследований . 38 (9): 723–32. DOI : 10.1021 / ar040223k . PMID 16171315 .
- ^ Ким С.К., Сесслер JL (октябрь 2010). «Рецепторы ионной пары» . Обзоры химического общества . 39 (10): 3784–809. DOI : 10.1039 / c002694h . PMC 3016456 . PMID 20737073 .
- ↑ McConnell AJ, Beer PD (май 2012 г.). «Гетеродитопические рецепторы для распознавания ионных пар». Angewandte Chemie . 51 (21): 5052–61. DOI : 10.1002 / anie.201107244 . PMID 22419667 .
- ^ Хуанг З., Чжу Л., Цао И, Ву Г, Лю Х, Чен И, Ван Ц, Ши Т, Чжао И, Ван И, Ли В, Ли И, Чен Х, Чен Г, Чжан Дж (январь 2011 г.). «ASD: обширная база данных аллостерических белков и модуляторов» . Исследования нуклеиновых кислот . 39 (выпуск базы данных): D663–9. DOI : 10.1093 / NAR / gkq1022 . PMC 3013650 . PMID 21051350 .
- ^ Panjkovich A, Daura X (октябрь 2012). «Использование гибкости белка для прогнозирования местоположения аллостерических сайтов» . BMC Bioinformatics . 13 : 273. DOI : 10,1186 / 1471-2105-13-273 . PMC 3562710 . PMID 23095452 .
- ^ Суэл GM, беззамочные SW, Стена MA, Ranganathan R (январь 2003). «Эволюционно консервативные сети остатков опосредуют аллостерическую связь в белках». Структурная биология природы . 10 (1): 59–69. DOI : 10.1038 / nsb881 . PMID 12483203 . S2CID 67749580 .
- ^ Mitternacht S, Березовский (сентябрь 2011). «Связывание рычагов как молекулярная основа аллостерической регуляции» . PLOS Вычислительная биология . 7 (9): e1002148. Bibcode : 2011PLSCB ... 7E2148M . DOI : 10.1371 / journal.pcbi.1002148 . PMC 3174156 . PMID 21935347 .
- ^ Gasper PM, Fuglestad B, Komives Е.А., Марквик PR, McCammon JA (декабрь 2012). «Аллостерические сети в тромбине различают прокоагулянтную и антикоагулянтную активности» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (52): 21216–22. DOI : 10.1073 / pnas.1218414109 . PMC 3535651 . PMID 23197839 .
- ^ Гош A, Vishveshwara S (ноябрь 2008). «Вариации кликов и сообществ в белковых структурах во время аллостерической коммуникации: исследование динамически уравновешенных структур комплексов метионил тРНК синтетазы». Биохимия . 47 (44): 11398–407. DOI : 10.1021 / bi8007559 . PMID 18842003 .
- ^ Sethi A, Eargle J, Черный AA, Luthey-Schulten Z (апрель 2009). «Динамические сети в тРНК: белковые комплексы» . Труды Национальной академии наук Соединенных Штатов Америки . 106 (16): 6620–5. Bibcode : 2009PNAS..106.6620S . DOI : 10.1073 / pnas.0810961106 . PMC 2672494 . PMID 19351898 .
- ^ Vanwart AT, Eargle J, Luthey-Schulten Z, Amaro RE (август 2012). «Изучение вклада компонентов остатка в динамические сетевые модели аллостерии» . Журнал химической теории и вычислений . 8 (8): 2949–2961. DOI : 10.1021 / ct300377a . PMC 3489502 . PMID 23139645 .
- ^ Rivalta I, султан М., Ли С., Manley Г.А., Лория JP, Батиста VS (май 2012). «Аллостерические пути в имидазол-глицеринфосфатсинтазе» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (22): E1428–36. DOI : 10.1073 / pnas.1120536109 . PMC 3365145 . PMID 22586084 .
- ^ Кристиан Ф.А. Негре, Уриэль Н. Морзан, Хайди П. Хендриксон, Ританкар Пал, Джордж П. Лиси, Дж. Патрик Лориа, Иван Ривальта, Джунмин Хо, Виктор С. Батиста. (2018). «Центральность собственного вектора для характеристики аллостерических путей белка» . Труды Национальной академии наук . 115 (52): E12201 – E12208. DOI : 10.1073 / pnas.1810452115 . PMC 6310864 . PMID 30530700 . CS1 maint: несколько имен: список авторов ( ссылка )
- Перейти ↑ Clarke D, Sethi A, Li S, Kumar S, Chang RW, Chen J, Gerstein M (май 2016 г.). «Выявление аллостерических горячих точек с помощью динамики: применение для межвидового и внутривидового сохранения» . Структура . 24 (5): 826–837. DOI : 10.1016 / j.str.2016.03.008 . PMC 4883016 . PMID 27066750 .
Внешние ссылки [ править ]
- Мгновенное представление о системе классификации механизмов аллостерии белков от Королевского химического общества
