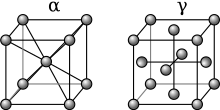
При атмосферном давлении существуют три аллотропные формы железа : альфа-железо (α-Fe), гамма-железо (γ-Fe) и дельта-железо (δ-Fe). При очень высоком давлении существует четвертая форма, называемая эпсилон-железом (ε-Fe) . Некоторые противоречивые экспериментальные данные предполагают существование пятой формы высокого давления, которая устойчива при очень высоких давлениях и температурах. [1]
Фазы железа при атмосферном давлении важны из-за различий в растворимости углерода , образующего разные типы стали . Фазы железа высокого давления важны как модели твердых частей планетарных ядер. Внутреннее ядро от Земли , как правило , предполагается , что состоит в основном из кристаллического железодефицитного никеля сплава с й структурой. [2] [3] [4] Считается, что внешнее ядро, окружающее твердое внутреннее ядро, состоит из жидкого железа, смешанного с никелем и небольшими количествами более легких элементов.
Стандартные аллотропы давления [ править ]
Альфа-железо (α-Fe) [ править ]
При температуре ниже 912 ° C (1,674 ° F) железо имеет объемно-центрированную кубическую структуру и известно как α-железо или феррит . Это термодинамически стабильный и достаточно мягкий металл. α-Fe может подвергаться давлению до прибл. 15 ГПа, прежде чем превратиться в форму под высоким давлением, называемую ε-железом , которое кристаллизуется в гексагональной плотноупакованной (ГПУ) структуре.
В магнитном отношении α-железо парамагнитно при высоких температурах. Тем не менее, как он охлаждается до 771 ° C (1044K или 1420 ° F), [5] температура Кюри (Т С или 2 ), она становится ферромагнитной . Также происходит обратное: когда α-железо нагревается выше температуры Кюри, случайное тепловое возбуждение атомов превышает ориентированный магнитный момент неспаренных электронных спинов, и оно становится парамагнитным. [6] В прошлом парамагнитная форма α-железа была известна как бета-железо (β-Fe). [7] [8] Однако эта терминология устарела.и вводит в заблуждение, поскольку, когда температура железа опускается ниже температуры Кюри, магнитные домены выравниваются, но структурных изменений не происходит. β-Fe кристаллографически идентичен α-Fe, за исключением магнитных доменов и параметра расширенной объемно-центрированной кубической решетки в зависимости от температуры, и поэтому имеет лишь незначительное значение при термообработке стали . По этой причине бета-фазу обычно не считают отдельной фазой, а просто высокотемпературным концом поля альфа-фазы. A 2 образует границу между полями бета-железа и альфа на фазовой диаграмме на Рисунке 1.
Точно так же A 2 имеет лишь второстепенное значение по сравнению с критическими температурами A 1 ( эвтектоид ), A 3 и A см . A см , где аустенит находится в равновесии с цементитом + γ-Fe, находится за правым краем на рис. 1. Фазовое поле α + γ, технически, является полем β + γ над A 2 . Обозначение бета поддерживает непрерывность последовательности фаз в чугуне и стали, состоящей из греческих букв: α-Fe, β-Fe, аустенит (γ-Fe), высокотемпературный δ-Fe и гексаферрум высокого давления (ε-Fe). .
Первичной фазой низкоуглеродистой или мягкой стали и большинства чугунов при комнатной температуре является ферромагнитное α-Fe. [9] [10] Он имеет твердость примерно 80 по Бринеллю . [11] [12] Максимальная растворимость составляет около 0,02 мас.% При 727 ° C (1341 ° F) и 0,001% углерода при 0 ° C (32 ° F). [13] Когда он растворяется в железе, атомы углерода занимают межузельные «дыры». Углерод, диаметр которого примерно в два раза больше диаметра тетраэдрического отверстия , создает сильное локальное поле деформации.
Низкоуглеродистая сталь (углеродистая сталь с содержанием углерода до 0,2 мас.%) Состоит в основном из α-Fe и увеличивающегося количества цементита (Fe 3 C, карбид железа). Смесь имеет слоистую структуру, называемую перлитом . Поскольку каждый из бейнита и перлита содержит α-Fe в качестве компонента, любой железоуглеродный сплав будет содержать некоторое количество α-Fe, если ему позволить достичь равновесия при комнатной температуре. Количество α-Fe зависит от процесса охлаждения.
А 2 критическая температура и индукционный нагрев [ править ]
β-Fe и критическая температура A 2 важны при индукционном нагреве стали, например, при термообработке с упрочнением поверхности. Сталь обычно austenitized при 900-1000 ° С перед его гасили и отпуска . Высокочастотное переменное магнитное поле индукционного нагрева нагревает сталь за счет двух механизмов ниже температуры Кюри: резистивного или джоулева (I 2 R) нагрева и ферромагнитных гистерезисных потерь. Выше A 2 механизм гистерезиса исчезает, и необходимое количество энергии на градус повышения температуры существенно больше, чем ниже A 2 . Схемы согласования нагрузки могут потребоваться для изменениясопротивление индукционного источника питания для компенсации изменения. [14]
Гамма-железо (γ-Fe) [ править ]
По мере охлаждения железа до 1394 ° C (2541 ° F) его кристаллическая структура меняется на гранецентрированную кубическую (ГЦК) кристаллическую структуру. В таком виде его называют гамма-железом (γ-Fe) или аустенитом . γ-железо может растворять значительно больше углерода (до 2,04% по массе при 1146 ° C). Эта γ-форма насыщения углеродом проявляется в нержавеющей стали .
Дельта-железо (δ-Fe) [ править ]
По мере охлаждения расплавленное железо затвердевает при температуре 1538 ° C (2800 ° F) в свой δ-аллотроп, который имеет объемно-центрированную кубическую (ОЦК) кристаллическую структуру. [15] δ-железо может растворять до 0,08% углерода по массе при 1475 ° C.
Аллотропы высокого давления [ править ]
Эпсилон-железо / гексаферрум (ε-Fe) [ править ]
При давлениях выше примерно 10 ГПа и температурах в несколько сотен кельвинов α-железо превращается в гексагональную плотноупакованную (ГПУ) структуру, также известную как ε-железо или гексаферрум; [16] более высокотемпературная γ-фаза также превращается в ε-железо, но при более высоком давлении. Обнаружен антиферромагнетизм в сплавах эпсилон-Fe с Mn, Os и Ru. [17]
Экспериментальная высокая температура и давление [ править ]
Альтернативная устойчивая форма, если она существует, может появиться при давлении не менее 50 ГПа и температуре не менее 1500 К; считалось, что он имеет ромбическую или двойную ГПУ структуру. [1] по состоянию на декабрь 2011 г., недавние и текущие эксперименты проводятся на аллотропах углерода высокого давления и сверхплотного углерода .
Фазовые переходы [ править ]
Точки плавления и кипения [ править ]
Температура плавления железа экспериментально хорошо определена для давлений менее 50 ГПа.
Для более высоких давлений опубликованные данные (по состоянию на 2007 год) помещают тройную точку γ-ε-жидкости при давлениях, которые различаются на десятки гигапаскалей, и 1000 K в точке плавления. Вообще говоря, компьютерное моделирование методом молекулярной динамики плавления железа и экспериментов с ударной волной предполагает более высокие температуры плавления и гораздо более крутой наклон кривой плавления, чем статические эксперименты, проводимые в ячейках с алмазными наковальнями . [18]
Точки плавления и кипения железа, наряду с его энтальпией атомизации , ниже, чем у более ранних элементов 3d группы от скандия до хрома , что свидетельствует об уменьшении вклада 3d-электронов в металлическую связь, поскольку они все больше и больше привлекаются в металл. инертное ядро ядром; [19] однако, они выше, чем значения для предыдущего элемента марганца, потому что этот элемент имеет наполовину заполненную трехмерную подоболочку и, следовательно, его d-электроны нелегко делокализовать. Та же тенденция проявляется для рутения, но не для осмия. [20]
Структурные фазовые переходы [ править ]
Точные температуры, при которых железо переходит из одной кристаллической структуры в другую, зависят от того, сколько и какого типа другие элементы растворены в железе. Фазовая граница между различными твердыми фазами проводится на бинарной фазовой диаграмме , которая обычно отображается как зависимость температуры от процента железа. Добавление некоторых элементов, таких как хром , сужает температурный диапазон гамма-фазы, в то время как другие увеличивают температурный диапазон гамма-фазы. В элементах, которые уменьшают диапазон гамма-фазы, фазовая граница альфа-гамма соединяется с фазовой границей гамма-дельта, образуя то, что обычно называют гамма-петлей . Добавление добавок гамма-петли сохраняет чугун в объемно-центрированной кубической структуре и предотвращает повреждение стали.фазовый переход в другие твердые состояния. [21]
См. Также [ править ]
- Закалка (металлургия)
Ссылки [ править ]
- ^ a b Boehler, Рейнхард (2000). «Эксперименты при высоком давлении и фазовая диаграмма материалов нижней мантии и ядра». Обзоры геофизики . Американский геофизический союз. 38 (2): 221–245. Bibcode : 2000RvGeo..38..221B . DOI : 10.1029 / 1998RG000053 . S2CID 33458168 .
- ^ Коэн, Рональд; Стиксруд, Ларс. «Кристалл в центре Земли» . Архивировано из оригинала 5 февраля 2007 года . Проверено 5 февраля 2007 .
- ^ Stixrude, Ларс; Коэн, Р. Э. (март 1995 г.). «Упругость железа при высоком давлении и анизотропия внутреннего ядра Земли». Наука . 267 (5206): 1972–5. Bibcode : 1995Sci ... 267.1972S . DOI : 10.1126 / science.267.5206.1972 . PMID 17770110 . S2CID 39711239 .
- ^ "Что находится в центре Земли?" . Новости BBC. 31 августа 2011 г.
- ^ a b Фазовые диаграммы сплавов . Справочник ASM. 3 . ASM International. 1992. С. 2.210, 4.9. ISBN 978-0-87170-381-1.
- ^ Cullity, BD; Грэм, компакт-диск (2009). Введение в магнитные материалы (2-е изд.). IEEE. п. 91. ISBN 978-0-471-47741-9.
- ^ DK Bullens et al ., Сталь и ее термическая обработка, Vol. I, четвертое изд. , J. Wiley & Sons Inc., 1938, стр. 86.
- ^ Авнер, SH (1974). Введение в металловедение (2-е изд.). Макгроу-Хилл. п. 225. ISBN 978-0-07-002499-1.
- ^ Мараниан, Питер (2009), Уменьшение хрупких и усталостных разрушений в стальных конструкциях , Нью-Йорк: Американское общество инженеров-строителей, ISBN 978-0-7844-1067-7.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ Структура из простой стали , извлечено 21 октября 2008 г..
- ^ Альваренг HD, Ван де Путта Т, Ван Steenberge N, Sietsma Дж, Terryn Н (январь 2015). «Влияние морфологии и микроструктуры карбидов на кинетику поверхностного обезуглероживания C-Mn сталей». Metall Mater Trans . 46 (1): 123–133. Bibcode : 2015MMTA ... 46..123A . DOI : 10.1007 / s11661-014-2600-у . S2CID 136871961 .
- ^ Смит и Хашеми 2006 , стр. 363.
- ^ Семятин, SL; Штутц, DE (1986). Индукционная термообработка стали . ASM International. С. 95–98. ISBN 978-0-87170-211-1.
- ^ Лайман, Тейлор, изд. (1973). Металлография, структуры и фазовые диаграммы . Справочник по металлам. 8 (8-е изд.). Парк Металлов, Огайо: ASM International. OCLC 490375371 .
- ^ Матон О; Baudelet F; Itié JP; Polian A; d'Astuto M; Chervin JC; Паскарелли S (14 декабря 2004 г.). «Динамика магнитного и структурного фазового перехода альфа-эпсилон в железе». Письма с физическим обзором . 93 (25): 255503. arXiv : cond-mat / 0405439 . Bibcode : 2004PhRvL..93y5503M . DOI : 10.1103 / PhysRevLett.93.255503 . PMID 15697906 . S2CID 19228886 .
- ^ GC Fletcher; Р.П. Аддис (ноябрь 1974 г.). «Магнитное состояние фазы железа» (PDF) . Журнал физики F: Физика металлов . 4 (11). п. 1954. Bibcode : 1974JPhF .... 4.1951F . DOI : 10.1088 / 0305-4608 / 4/11/020 . Проверено 30 декабря 2011 года .
- ^ Boehler, Reinhard; Росс, М. (2007). «Свойства горных пород и минералов. Плавление при высоком давлении». Минеральная физика . Трактат по геофизике. 2 . Эльзевир. С. 527–41. DOI : 10.1016 / B978-044452748-6.00047-X . ISBN 9780444527486.
- ^ Гринвуд и Эрншоу, стр. 1116
- ^ Гринвуд и Эрншоу, стр. 1074-75
- ^ Майер Курц, изд. (2002-07-22). Справочник по выбору материалов . п. 44. ISBN 9780471359241. Проверено 19 декабря 2013 года .