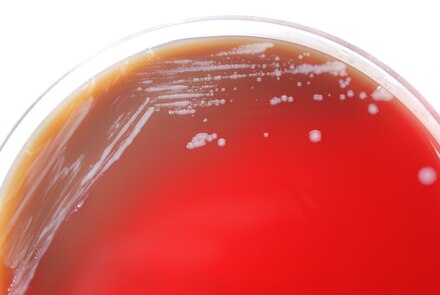
| Burkholderia mallei | |
|---|---|
 | |
| Научная классификация | |
| Домен: | |
| Тип: | |
| Учебный класс: | |
| Заказ: | |
| Семья: | |
| Род: | |
| Разновидность: | B. mallei |
| Биномиальное имя | |
| Burkholderia mallei ( Zopf 1885) Yabuuchi et al. 1993 г. | |
| Синонимы | |
Сап бациллы Леффлера 1882 | |
Burkholderia mallei - грамотрицательная биполярная аэробная бактерия , возбудитель рода Burkholderia для людей и животных, вызывающая сап ; латинское название этой болезни ( молоточек ) дало название вида вызывающее. Он тесно связан с Б. pseudomallei , и мультилокальной последовательностью вводом является подвидом Б. pseudomallei. [1] B. mallei произошла от B. pseudomallei путем избирательной редукции и делецийгенома B. pseudomallei . [2] В отличие от B. pseudomallei и других представителей рода, B. mallei неподвижен; по форме коккобациллярная, длиной около 1,5–3,0 мкм и диаметром 0,5–1,0 мкм с закругленными концами.
Открытие и ранняя история [ править ]
Вильгельм Шютц и Фридрих Лёффлер впервые выделили B. mallei в 1882 году. [3] Он был выделен из инфицированной печени и селезенки лошади. [4] Эта бактерия также является одной из первых идентифицированных бактерий, содержащих систему секреции типа VI, которая важна для ее патогенности. [5] В 1885 году немецкий ботаник и бактериолог Вильгельм Цопф (1846–1909) дал патогену его биномиальное название после анализа образцов бактерии. Далее он уточнил свои наблюдения с патогеном в 1886 г. [6]
Семья Burkholderiaceae [ править ]
Большинство организмов Burkholderiaceae живут в почве; однако B. mallei этого не делает. Поскольку B. mallei является облигатным патогеном млекопитающих , он должен инфицировать млекопитающее- хозяина, чтобы жить и передаваться от одного хозяина к другому. [7]
Род Burkholderia [ править ]
B. mallei очень близок к B. pseudomallei , будучи на 99% идентичным консервативным генам по сравнению с B. pseudomallei . Б. malllei имеет около 1,4 Мб меньше ДНК , чем Б. pseudomallei . [4] B. mallei, возможно, произошла от штамма B. pseudomallei после того, как последний заразил животное. Бактерия потеряла бы гены, которые не были необходимы для жизни в животном-хозяине. Это предположение нашло поддержку в исследованиях, которые сравнивают штаммы B. mallei с B. pseudomallei и показывают, что их два соответствующих геномаочень похожи. Гены, которые позволили бактериям выжить в почвенной среде, например гены, которые дали B. mallei способность защищать от бактерицидных, антибиотиков и противогрибковых средств, вероятно, были удалены. Таким образом, причина того, что B. mallei не обнаруживается вне хозяина, заключается в том, что у него отсутствуют гены, необходимые для выживания в почве. Сравнение геномов также, кажется, указывает на то, что B. mallei все еще развивается и адаптируется к внутриклеточному образу жизни. [8]
Геном [ править ]
Геном B. mallei был секвенирован в США Институтом геномных исследований . Размер генома меньше, чем у B. pseudomallei . Б. mallei последовательность выявила хромосому 3,5 мег пара оснований (МБ) и 2,3 Мб «megaplasmid». Многие вставки последовательности и фазовый переменные гены также были найдены. [3] геном для Б. mallei состоит из двух круговые хромосомы. На хромосоме 1 расположены гены, относящиеся к метаболизму , образованию капсул и биосинтезу липополисахаридов . B. malleiимеет полисахаридную капсулу, которая указывает на его потенциал как патогена. Хромосома 2 - это место, где находится большая часть информации о системах секреции и генах, связанных с вирулентностью . [4] Мультилокусное типирование последовательностей показало, что B. mallei, скорее всего, произошла от сокращения клона B. pseudomallei . Около 1000 генов B. pseudomellei отсутствуют или варьируют в геноме B. mallei . Геном B. mallei также имеет большое количество инсерционных последовательностей. [8]
Таксономия [ править ]
B. mallei сначала называли " Bacillus mallei " и относились к роду Pseudomonas до начала 1990-х годов. Это также упоминалось как «фарс». Сейчас это часть рода Burkholderia . [3]
Печатать [ править ]
Не существует стандартизированной системы для различения B. mallei и B. pseudomallei . Методы, которые использовались для дифференциации и идентификации одного штамма от другого, включают риботипирование , гель-электрофорез в импульсном поле , мультилокусный ферментный электрофорез, анализ случайной амплификации полиморфной ДНК и мультилокусное типирование последовательностей. [3] Однако сравнение ДНК B. mallei и B. pseudomallei необходимо проводить на уровне 23S рДНК, поскольку на уровне 16S рДНК между этими двумя видами не обнаружено различий . [9]
Рост в культуре [ править ]
И B. mallei, и B. pseudomallei можно культивировать в лаборатории; питательный агар можно использовать для выращивания бактерий. При выращивании в культуре B. mallei вырастает гладкими, серыми, полупрозрачными колониями . За 18 часов при 37 ° C колония B. mallei может вырасти примерно до 0,5–1,0 мм в диаметре. Рост культуры B. mallei на агаре МакКонки изменчив. Многие микробиологи не знакомы с B. mallei, и в результате ее часто ошибочно принимают за вид Pseudomonas или как загрязнитель в культуре. [3]
Устойчивость к антибиотикам и восприимчивость [ править ]
Бактерия восприимчива к многочисленным дезинфицирующим средствам, включая хлорид бензалкония , йод , хлорид ртути , перманганат калия , 1% гипохлорит натрия и этанол . Микроорганизм также можно уничтожить нагреванием или ультрафиолетом . Антибиотики, такие как стрептомицин , амикацин , тетрациклин , доксициклин , карбапенемы , цефтазидим , амоксициллин / клавулановая кислота , пиперациллин ,хлорамфеникол и сульфатиазол были эффективны против бактерий in vitro . B. mallei , как и B. pseudomallei , также устойчив к ряду антибиотиков, включая аминогликозиды , полимиксины и бета-лактамы . В настоящее время нет вакцины для людей или животных, защищающей от инфекции B. mallei . [3] Перед разработкой вакцины необходима модель на животных, которая будет предсказывать иммунные ответы, необходимые для создания иммунитета к бактериям. Мыши довольно близки к людям по своей восприимчивости кB. mallei и будет идеальным выбором животного для создания модели вакцины. [4]
Патогенность [ править ]
B. mallei вызывает болезнь сапа , которая исторически чаще всего поражала животных, таких как лошади , мулы и ослы , и редко людей. Лошади считаются естественными хозяевами инфекции B. mallei и очень восприимчивы к ней. [4] B. mallei заражает и получает доступ к клетке своего хозяина посредством лизиса входной вакуоли . B. mallei, попав внутрь клетки, обладает бактериальной белково-зависимой, актиновой подвижностью. Он также может инициировать слияние клеток-хозяев, в результате которого образуются многоядерные гигантские клетки.(MNGC). Последствия MNGC еще предстоит определить, но они могут позволить бактериям распространяться на другие клетки, уклоняться от ответов иммунной системы инфицированного хозяина или позволить бактериям оставаться в хозяине дольше. B. mallei способен выживать внутри клеток-хозяев благодаря своим способностям нарушать бактерицидные функции клетки. Он рано покидает вакуоли, что позволяет эффективно размножаться бактериям внутри клетки. Ранний выход из клетки также предотвращает разрушение бактерий лизосомальными дефензинами и другими агентами, убивающими патогены. MNGC могут помочь защитить бактерии от иммунных реакций. [10] B. malleiспособность жить в клетке-хозяине делает разработку вакцины против нее трудной и сложной. Вакцина должна вызывать клеточно-опосредованный иммунный ответ, а также гуморальный ответ на бактерии, чтобы быть эффективной в защите от B. mallei . Что касается вакцины против B. mallei , то близость B. mallei к B. pseudomallei может сделать возможным, что вакцина, разработанная для одного типа, будет эффективна против другого. [7]
Симптомы инфекции B. mallei [ править ]
У лошадей, хронически инфицированных B. mallei с болезнью сапа, обычно наблюдаются выделения из носа, содержащие слизь , поражения легких и узелки вокруг печени или селезенки. Острая инфекция у лошадей приводит к сильной лихорадке, потере жира или мышц, эрозии поверхности носовой перегородки , кровотечению или выделению слизи. Бактерия в основном поражает легкие и дыхательные пути. [4] Человеческое заражение B. mallei встречается редко, хотя иногда встречается среди лабораторных работников, работающих с бактериями, или среди тех, кто часто находится рядом с инфицированными животными. [3]Бактерии обычно заражают человека через глаза, нос, рот или порезы на коже. После того, как люди заражаются, они развивают лихорадку и суровость . В конце концов, они заболевают пневмонией , гнойничками и абсцессами , которые, если их не лечить антибиотиками, приводят к летальному исходу в течение недели или 10 дней. То, как кто-то заражается бактериями, также влияет на тип симптомов, которые могут возникнуть. Если бактерии проникают через кожу, это может вызвать местную кожную инфекцию, а вдыхание B. mallei может вызвать сепсис, легочные, мышечные, печеночные или селезеночные инфекции. B. malleiУровень смертности от инфекции составляет 95%, если ее не лечить, и уровень смертности 50% среди лиц, получавших антибиотики. [4]
Клеточный ответ на инфекцию [ править ]
В первые дни заражения B. mallei нейтрофилы , макрофаги и Т-клетки в большом количестве попадают в селезенку. Ранний клеточный ответ на инфекцию B. mallei включает клетки Gr-1 + ( антиген ) и подразумевает их важность для иммунитета против этой бактериальной инфекции. Т-клетки ( оксид азота ) на самом деле более активно борются с B. mallei на более поздних стадиях инфицирования хозяина. [11]
Липополисахарид, выделенный из B. mallei, продемонстрировал значительно более низкую биологическую активность по сравнению с ЛПС из Escherichia coli , что согласуется с более низкой степенью ацилирования его липида A : основные формы липида A B. mallei были пента- и тетраацилированными, тогда как классические липид А из E. coli гексаацилировали. Кроме того, липид А из B. mallei почти в половине молекул содержит остаток 4-амино-4-дезоксиарабинозы, который частично нейтрализует отрицательный заряд фосфатных групп, необходимый для взаимодействия с положительно заряженнымиаминокислот из TLR4 . В то же время, липид А ацильных цепей в B. mallei были в среднем более длинные (14-16 атомов углерода ) , чем в E.coli , (14 атомов углерода), но ЛПС из Б. mallei оказался более слабым активатором. Б. mallei может использовать LPS с низкой биологической активностью , чтобы избежать надлежащего признания со стороной TLR4 / МД-2 комплексов врожденной иммунной системы , смачивая ответ хозяина иммунного и увеличивая риск бактериального распространения. [12]
Глобальное присутствие [ править ]
B. mallei уничтожен в Соединенных Штатах и большинстве западных стран, но все еще поражает животных в Африке, Азии, на Ближнем Востоке, в Центральной и Южной Америке. [4] Многие западные страны смогли ликвидировать болезнь с помощью программ борьбы с сапом и законов, требующих уведомления департаментов здравоохранения о случаях заражения и уничтожения любого животного, пораженного B. mallei . [13]
Возможен как биологическое оружие [ править ]
B. mallei и B. pseudomallei в прошлом были в списке потенциальных боевых биологических агентов. В Центрах по контролю и профилактике заболеваний классифицируют B. mallei как категория B критический биологический агент. [7] В результате исследования в отношении B. mallei могут проводиться только в учреждениях с уровнем биобезопасности 3 в США и за рубежом. Хотя он очень заразен и является потенциальным биологическим оружием, мало исследований было проведено в отношении этой бактерии. [4] B. mallei и B. pseudomalleiв соответствии с политикой институционального надзора за исследованиями двойного использования в биологических науках, вызывающие озабоченность, будут подлежать надзору для обеспечения ответственного расследования этих агентов. [14]
Заболеваемость в США [ править ]
В марте 2000 года один из первых случаев сапа с 1940-х годов в США произошел у молодого микробиолога, работавшего в Медицинском научно-исследовательском институте инфекционных заболеваний армии США . У исследователя был диабет 1 типа, и он работал с B. mallei около двух лет, но он не всегда носил перчатки при проведении исследования. Исследователь испытал увеличение лимфатических узлов и лихорадку, которая длилась 10 дней даже после лечения антибиотиками. В следующие недели исследователь испытал усталость , озноб, ночную потливость и потерю веса. В следующем месяце его симптомы, казалось, исчезли после лечения кларитромицином., но после прекращения приема лекарства симптомы снова появились. После проведения нескольких тестов на культурах из крови исследователя и биопсии абсцесса печени, бактерия была идентифицирована как B. mallei . После того, как было установлено, что заразило исследователя, был назначен еще один курс антибиотиков ( имипенем и доксициклин ) с 6- месячным курсом лечения. Через год исследователь полностью выздоровел.
Этот инцидент также показал, что порез или ссадина кожи не являются абсолютно необходимыми для заражения болезнью, поскольку исследователь не помнил ни одного пореза или несчастного случая во время работы в лаборатории. Случай был значительным, поскольку он продемонстрировал трудности, с которыми сталкиваются микробиологические лаборатории при идентификации агентов биологического оружия, и возможные последствия, если не будут приняты меры для подготовки к реальной биологической атаке. [13]
История как оружие биологической войны [ править ]
B. mallei преднамеренно использовались для заражения животных и людей во время Первой мировой войны. Немцы использовали B. mallei для заражения с сапом животных, которых отправляли из нейтральных стран к союзникам. [3] Планы немцев по биологической войне начались в 1915 году на восточном побережье США; они намеревались заразить и убить домашний скот, который был отправлен союзникам, и облегчить передачу болезни людям. На Восточном побережье собирали множество животных для отправки союзникам, сражавшимся в Европе. Немцы также нанесли удар по животноводству Румынии , Норвегии и Испании, выращивая культуру сапа. Немецкий биологический саботажв конечном итоге распространился на Аргентину , где агенты использовали бактериальные культуры из Испании для заражения крупного рогатого скота, лошадей и мулов, которых Аргентина поставляла союзникам. Использование Германией микробов в качестве оружия - одна из немногих задокументированных атак намеренного применения биологического оружия против нейтральных стран. [15]
Японцы использовали B. mallei в своих исследовательских подразделениях по биологическому оружию. Наиболее известное и известное подразделение, Unit 731 , использовало эту бактерию для проведения экспериментов на живых людях. Однако японцы не создали биологическое оружие из B. mallei . Они действительно использовали B. mallei для проверки его эффективности в загрязнении источников воды, и результаты этих тестов были успешными.
Российская программа создания биологического оружия также заинтересовалась B. mallei и провела с ней полевые испытания. Некоторые исследователи из программы были фактически инфицированы и убиты ею в ходе своих исследований. Было высказано предположение, что русские в конечном итоге использовали B. mallei во время войны в Афганистане против моджахедов . [3]
См. Также [ править ]
- Тест Маллейна
Ссылки [ править ]
- ^ Года D, G Рэндл, Симпсон AJ, Aanensen DM, Pitt TL, Киношита R, Спратт BG (2003). «Мультилокусное типирование последовательностей и эволюционные отношения между возбудителями мелиоидоза и сапа, Burkholderia pseudomallei и Burkholderia mallei » . J. Clin. Microbiol . 41 (5): 2068–79. DOI : 10.1128 / JCM.41.5.2068-2079.2003 . PMC 154742 . PMID 12734250 .
- ^ Сонг Х, Хван Дж, Йи Х, Ульрих Р.Л., Ю Й, Нирман В.К., Ким Х.С. (2010). Охман Х (ред.). «Ранняя стадия бактериальной редуктивной эволюции генома в хозяине» . PLOS Патогены . 6 (5): e1000922. DOI : 10.1371 / journal.ppat.1000922 . PMC 2877748 . PMID 20523904 .
- ^ Б с д е е г ч я Dance, ДАБ (2010). «4. Мелиоидоз и сап как возможное биологическое оружие» . В Фонге, И. В.; Алибек, Кеннет (ред.). Биотерроризм и инфекционные агенты: новая дилемма 21 века . Springer. С. 99–145. ISBN 978-1-4419-1266-4.
- ^ a b c d e f g h i Whitlock GC, Estes DM, Torres AG (2007). «Сап: вперед на скачки с Burkholderia mallei » . FEMS Microbiol. Lett . 277 (2): 115–22. DOI : 10.1111 / j.1574-6968.2007.00949.x . PMID 18031330 .
- ^ Шелл М.А., Рики Л., Ульрих и др. (2007). «Секреция типа VI является основным фактором вирулентности Burkholderia mallei ». Mol Microbiol . 64 (6): 1466–1485. DOI : 10.1111 / j.1365-2958.2007.05734.x . PMID 17555434 . S2CID 25690886 .
- ^ DePaolo, Чарльз (15 сентября 2016). Уильям Уотсон Чейн и развитие бактериологии . Макфарланд. ISBN 9781476666518. Проверено 12 апреля 2018 г. - через Google Книги.
- ^ a b c Бонди С.К., Голдберг Дж. Б. (2008). «Стратегии создания вакцин против Burkholderia mallei и Burkholderia pseudomallei » . Экспертные ревакцины . 7 (9): 1357–65. DOI : 10.1586 / 14760584.7.9.1357 . PMC 2680498 . PMID 18980539 .
- ^ а б Лосада Л., Роннинг С.М., ДеШазер Д., Вудс Д., Федорова Н., Ким Х.С., Шабалина С.А., Пирсон Т.Р., Бринкач Л., Тан П., Нанди Т., Крабтри Дж., Барсук Дж., Бекстром-Штернберг С., Сакиб М., Шутцер С.Е., Кейм П., Нирман В.К. (2010). «Продолжающаяся эволюция Burkholderia mallei через сокращение генома и крупномасштабные перестройки» . Genome Biol Evol . 2 : 102–16. DOI : 10.1093 / GbE / evq003 . PMC 2839346 . PMID 20333227 .
- ^ Bauernfeind A, роликовый C, D Meyer, Jungwirth R, Schneider I (1998). «Молекулярная процедура для быстрого обнаружения Burkholderia mallei и Burkholderia pseudomallei » . J. Clin. Microbiol . 36 (9): 2737–41. DOI : 10.1128 / JCM.36.9.2737-2741.1998 . PMC 105196 . PMID 9705426 .
- ^ Galyov EE, Бретт PJ, DeShazer D (2010). "Молекулярное понимание патогенеза Burkholderia pseudomallei и Burkholderia mallei ". Анну. Rev. Microbiol . 64 : 495–517. DOI : 10.1146 / annurev.micro.112408.134030 . PMID 20528691 .
- Перейти ↑ Rowland CA, Lever MS, Griffin KF, Bancroft GJ, Lukaszewski RA (2010). «Защитные клеточные ответы на инфекцию Burkholderia mallei ». Микробы заражают . 12 (11): 846–53. DOI : 10.1016 / j.micinf.2010.05.012 . PMID 20542133 .
- ^ Корнеев, К; Арбатский, Н; Молинаро, А; Palmigiano, A; Шайхутдинова, Р; Шнейдер, М; Пирс, G; Кондакова А; Свиряева, Э; Sturiale, L; Гароццо, Д; Круглов, А; Недоспасов, С; Друцкая, М; Knirel, Y; Купраш, Д (2015). «Структурная связь ацильных групп липида А с активацией мышиного толл-подобного рецептора 4 липополисахаридами из патогенных штаммов Burkholderia mallei, Acinetobacter baumannii и Pseudomonas aeruginosa» . Границы иммунологии . 6 : 595. DOI : 10.3389 / fimmu.2015.00595 . PMC 4655328 . PMID 26635809 .
- ^ a b Сринивасан А., Краус К.Н., ДеШазер Д., Беккер П.М., Дик Дж. Д., Спейсек Л., Бартлетт Дж. Г., Бирн В. Р., Томас Д. Л. (2001). «Сап у военного микробиолога-исследователя». N. Engl. J. Med . 345 (4): 256–8. DOI : 10.1056 / NEJM200107263450404 . PMID 11474663 .
- ^ "Политика правительства Соединенных Штатов по институциональному надзору за вызывающими озабоченность исследованиями двойного использования наук о жизни" (PDF) . Помощник секретаря по вопросам готовности и реагирования (ASPR) Министерства здравоохранения и социальных служб США.
- ^ Уилис M (1998). «Первые выстрелы в биологической войне». Природа . 395 (6699): 213. DOI : 10.1038 / 26089 . PMID 9751039 . S2CID 5478674 .
Внешние ссылки [ править ]
- « Геномы Burkholderia mallei и соответствующая информация» . ПАТРИК Биоинформатический ресурсный центр . НИАИД. Архивировано из оригинала на 2011-08-24 . Проверено 24 июня 2010 .
- Патема- Буркхолдерия Ресурс
- "Сап ( Burkholderia mallei ) Общие сведения" . Центры по контролю и профилактике заболеваний.
- «Агенты / болезни биотерроризма» . Центры по контролю и профилактике заболеваний. Архивировано из оригинала на 2014-07-22.:]
- «Сап» . Центр биозащищенности. Архивировано из оригинала на 2009-05-31.
- " Burkholderia mallei " . Браузер таксономии NCBI . 13373.