| Коннексин | ||||||||
|---|---|---|---|---|---|---|---|---|
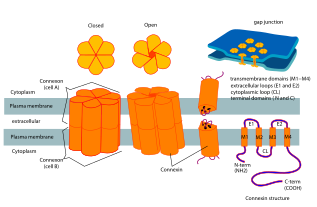
 Додекамер коннексина-26. Щелевое соединение, состоящее из двенадцати идентичных белков коннексина, по шесть в мембране каждой клетки. Каждая из этих шести единиц представляет собой отдельный полипептид, который четыре раза проходит через мембрану (называемые четырехпроходными трансмембранными белками). | ||||||||
| Идентификаторы | ||||||||
| Символ | Коннексин | |||||||
| Pfam | PF00029 | |||||||
| ИнтерПро | IPR013092 | |||||||
| PROSITE | PDOC00341 | |||||||
| TCDB | 1.A.24 | |||||||
| OPM суперсемейство | 194 | |||||||
| Белок OPM | 2zw3 | |||||||
| ||||||||
Коннексины ( Сх ) ( TC # 1.A.24 ), или белки щелевых соединений , являются структурно родственными трансмембранными белками, которые собираются с образованием щелевых соединений позвоночных. Совершенно другое семейство белков, иннексины , образуют щелевые контакты у беспозвоночных . [1] Каждый щелевой переход состоит из двух полуканалов или коннексонов., которые состоят из гомо- или гетерогексамерных массивов коннексинов, и коннексон в одной плазматической мембране стыкуется конец к концу с коннексоном в мембране близко противоположной клетки. Гемиканал состоит из шести субъединиц коннексина, каждая из которых состоит из четырех трансмембранных сегментов. Щелевые соединения важны для многих физиологических процессов, таких как скоординированная деполяризация сердечной мышцы , правильное эмбриональное развитие и проводимая реакция в микрососудистой сети. По этой причине мутации в генах, кодирующих коннексин, могут приводить к функциональным нарушениям и аномалиям развития.
Номенклатура [ править ]
Коннексины обычно называют в соответствии с их молекулярной массой, например, Cx26 - это белок коннексина 26 кДа. Конкурирующая номенклатура - это белковая система щелевых соединений , в которой коннексины сортируются по их α (GJA) и β (GJB) формам, а дополнительные коннексины сгруппированы в группы C, D и E, за которыми следует идентификационный номер, например, GJA1 соответствует Сх43. После голосования на конференции Gap Junction Conference (2007) в Эльсиноре сообщество согласилось использовать систему номенклатуры GJ для генов, кодирующих коннексины, но пожелало сохранить номенклатуру коннексинов для кодируемых белков с использованием веса человеческого белка для нумерации. ортологичных белков.
Структура [ править ]
Коннексины содержат четыре высокоупорядоченных трансмембранных сегмента (TMS), в первую очередь неструктурированные цитоплазматические концы C и N, цитоплазматическую петлю (CL) и две внеклеточные петли (EL-1) и (EL-2). Коннексины собираются в группы по шесть, чтобы сформировать полуканалы или коннексоны, а затем два полуканала объединяются, образуя щелевое соединение.
Доступна кристаллическая структура канала щелевого соединения, образованного Cx26 человека (также известного как GJB2) с разрешением 3,5 Å. [2] Карта плотности показала два межмембранных полуканала и расположение четырех TMS шести протомеров, образующих каждый полуканал. Полуканалы имеют положительно заряженный вход в цитоплазму, воронку, отрицательно заряженный трансмембранный путь и внеклеточную полость. Пора сужается у воронки, которая образована шестью аминоконцевыми спиралями, выстилающими стенку канала, что, таким образом, определяет ограничение размера молекулы на входе в канал.
Семейство генов коннексина разнообразно: двадцать один идентифицированный член в секвенированном геноме человека и двадцать у мыши (девятнадцать из которых являются ортологичными парами). Обычно они весят от 25 до 60 кДа и имеют среднюю длину 380 аминокислот. Было обнаружено, что различные коннексины объединяются как в гомомерные, так и в гетеромерные щелевые переходы, каждый из которых может проявлять различные функциональные свойства, включая проводимость пор, избирательность по размеру, селективность заряда, стробирование напряжения и химическое стробирование. [3]
Биосинтез и интернализация [ править ]
Замечательный аспект коннексинов заключается в том, что у них относительно короткий период полураспада, составляющий всего несколько часов. [4] Результатом является наличие динамического цикла, в котором синтезируются и заменяются коннексины. Было высказано предположение, что такая короткая продолжительность жизни позволяет более точно регулировать физиологические процессы, например, в миометрии .
От ядра к мембране [ править ]
Поскольку они транслируются рибосомами, коннексины встраиваются в мембрану эндоплазматического ретикулума (ER). [5] Именно в ER коннексины правильно складываются, образуя две внеклеточные петли, EL-1 и EL-2. Также в ER начинается олигомеризация молекул коннексина в полуканалы, процесс, который может продолжаться и в промежуточном компартменте UR-Golgi. [4] Расположение этих полуканалов может быть гомотипическим, гетеротипическим и комбинированным гетеротипическим / гетеромерным. После выхода из ER и прохождения через ERGIC свернутые коннексины обычно попадают в цис- сеть Гольджи. [6]Однако некоторые коннексины, такие как Cx26, могут транспортироваться независимо от Гольджи. [7] [8] [9] [10] [11]
Сборка щелевого соединения [ править ]
После внедрения в плазматическую мембрану клетки полуканалы свободно диффундируют в липидном бислое. [12] С помощью специфических белков, в основном кадгеринов , полуканалы могут стыковаться с полуканалами соседних клеток, образуя щелевые соединения. [13] Недавние исследования показали существование связи между адгезивными соединениями и щелевыми соединениями, [14] предполагая более высокий уровень координации, чем считалось ранее.
Функция [ править ]
Щелевые соединения коннексина обнаруживаются только у позвоночных , тогда как функционально аналогичная (но генетически неродственная) группа белков, innexins , ответственна за щелевые соединения у беспозвоночных . Ортологи Innexin также были идентифицированы у Chordates , но они больше не способны образовывать щелевые соединения. Вместо этого каналы, образованные этими белками (называемыми паннексинами ), действуют как очень большие трансмембранные поры, которые соединяют внутри- и внеклеточные компартменты.
Внутри ЦНС щелевые контакты обеспечивают электрическую связь между клетками-предшественниками, нейронами и глиальными клетками. Исследования показали, что с использованием мышей с нокаутом специфического коннексина , связывание клеток важно для передачи визуальных сигналов. В сетчатке окружающий свет влияет на сцепление клеток, обеспечиваемое каналами щелевого соединения, адаптируя зрительную функцию к различным условиям освещения. Сцепление клеток регулируется несколькими механизмами, включая экспрессию коннексина. [16]
Decrock et al. . обсудили многоуровневую платформу, через которую коннексины и паннексины могут влиять на следующие клеточные функции в ткани: (1) щелевые соединительные каналы коннексина (GJC) обеспечивают прямую межклеточную коммуникацию малых молекул, (2) гемиканалы коннексина и каналы паннексина могут способствовать к аутокринным / паракринным сигнальным путям, и (3) различные структурные домены этих белков обеспечивают независимые от каналов функции, такие как межклеточная адгезия , взаимодействия с цитоскелетом и активация внутриклеточных сигнальных путей. [17]Таким образом, коннексины и паннексины вносят многогранный вклад в развитие мозга и специфические процессы в нейроглио-сосудистой единице, включая синаптическую передачу и пластичность, передачу глиальных сигналов, вазомоторный контроль и целостность гематоэнцефалического барьера в зрелой ЦНС. [17]
Специфичность субстрата [ править ]
Различные коннексины могут проявлять разные специфичности в отношении растворенных веществ. Например, аденозин примерно в 12 раз лучше проходил через каналы, образованные Cx32, тогда как AMP и ADP проходили примерно в 8 раз лучше, а АТФ более чем в 300 раз лучше через каналы, образованные Cx43. Таким образом, добавление фосфата к аденозину, по-видимому, смещает его относительную проницаемость с каналов, образованных Cx32, на каналы, образованные Cx43. Это может иметь функциональные последствия, поскольку энергетический статус клетки может контролироваться посредством экспрессии коннексина и образования каналов. [18]
Транспортная реакция [ править ]
Транспортная реакция, катализируемая щелевыми контактами коннексина:
- Малые молекулы (цитоплазма клетки 1) ⇌ малые молекулы (цитоплазма клетки 2)
Коннексины человека и их влияние на болезнь [ править ]
| Коннексин | Ген | Расположение и функции |
|---|---|---|
| Сх43 | GJA1 | Экспрессируется на поверхности сосудистой сети атеросклеротической бляшкой и активируется во время атеросклероза у мышей. Может иметь патологические эффекты. Также экспрессируется между клетками гранулезы , что необходимо для пролиферации. Обычно экспрессируется в астроцитах, также обнаруживается в большинстве астроцитом человека и в астроглиальном компоненте глионейрональных опухолей. [19] Это также главный кардиальный коннексин, обнаруживаемый в основном в миокарде желудочков. [20] Связано с окулодентодигитальной дисплазией . |
| Сх46 | GJA3 | |
| Сх37 | GJA4 | Индуцируется в гладких мышцах сосудов во время коронарного артериогенеза. Мутации Сх37 не смертельны. Образует щелевые контакты между ооцитами и клетками гранулезы и необходимы для выживания ооцитов. |
| Сх40 | GJA5 | Избирательно экспрессируется в миоцитах предсердий. Отвечает за скоординированную электрическую активацию предсердий. [21] |
| Сх33 | GJA6 (GJA6P) | Псевдоген у человека |
| Сх50 | GJA8 | Щелевые соединения между горизонтальными клетками А-типа в сетчатке мыши и кролика [22] |
| Сх59 | GJA10 | |
| Сх62 | GJA10 | Cx62 человека соответствует Cx57 (мышь). Расположение в несущей аксон горизонтальной клетке B-типа в сетчатке кролика [23] |
| Сх32 | GJB1 | Основной компонент периферического миелина. Мутации в человеческом гене вызывают Х-сцепленную болезнь Шарко-Мари-Тута , наследственную невропатию. В нормальном мозге человека CX32 экспрессируется в нейронах и олигодендроцитах. [19] |
| Сх26 | GJB2 | Мутировал по синдрому Фохвинкеля, а также по синдрому кератита-иктиоза-глухоты (KID) . |
| Сх31 | GJB3 | Может быть связан с вариабельной эритрокератодермией . |
| Сх30.3 | GJB4 | Fonseca et al. подтвердил экспрессию Cx30.3 в тимоцитах . [24] Может быть связан с вариабельной эритрокератодермией. |
| Сх31.1 | GJB5 | |
| Сх30 | GJB6 | Мутировал по синдрому Клустона (гидротическая эктодермальная дисплазия) |
| Сх25 | GJB7 | |
| Сх45 | GJC1 / GJA7 | Эпителиальные клетки протоков поджелудочной железы человека. [25] Атриовентрикулярный узел. |
| Сх47 | GJC2 / GJA12 | Экспрессируется в щелевых соединениях олигодентроцитов [26] |
| Сх31.3 | GJC3 | Человеческий ортолог мышиного Сх29. Не известно об образовании щелевых контактов. [27] |
| Cx36 | GJD2 / GJA9 | Функция бета-клеток поджелудочной железы, опосредующая высвобождение инсулина. Нейроны во всей центральной нервной системе, где они синхронизируют нервную активность. [28] |
| Сх31.9 | GJD3 / GJC1 | |
| Сх39 | GJD4 | |
| Сх40.1 | GJD4 | |
| Сх23 | GJE1 |
Щелевые соединения важны для многих физиологических процессов, таких как скоординированная деполяризация сердечной мышцы , правильное эмбриональное развитие и проводимая реакция в микрососудистой сети. По этой причине делеция или мутация различных изоформ коннексина вызывает отличительные фенотипы и патологии. [29] В то время как мутации в Сх43 в основном связаны с окулодентодигитальной дисплазией, мутации Сх47 связаны с болезнью Пелизея-Мерцбахера и лимфедемой. Мутации Сх40 в основном связаны с фибрилляцией предсердий. Мутации в Cx37 еще не описаны, но полиморфизмы в гене Cx37 участвуют в развитии артериальных заболеваний. [30]
Ссылки [ править ]
- ^ Лодиш, Харви Ф .; Арнольд Берк; Пол Мацудаира; Крис А. Кайзер; Монти Кригер; Мэтью П. Скотт; С. Лоуренс Зипурски; Джеймс Дарнелл (2004). Молекулярная клеточная биология (5-е изд.). Нью-Йорк: WH Freeman and Company. С. 230–1 . ISBN 0-7167-4366-3.
- Перейти ↑ Maeda S, Nakagawa S, Suga M, Yamashita E, Oshima A, Fujiyoshi Y, Tsukihara T (апрель 2009 г.). «Структура канала щелевого соединения коннексина 26 при разрешении 3,5 А». Природа . 458 (7238): 597–602. DOI : 10,1038 / природа07869 . ISSN 1476-4687 . PMID 19340074 . S2CID 4431769 .
- ^ Ayad WA, Локк D, Корин IV, Harris AL (июнь 2006). «Гетеромерные, но не гомомерные каналы коннексина избирательно проницаемы для инозитолфосфатов» . J. Biol. Chem . 281 (24): 16727–39. DOI : 10.1074 / jbc.M600136200 . ISSN 0021-9258 . PMID 16601118 .
- ^ a b Laird DW (март 2006 г.). «Жизненный цикл коннексинов в здоровье и болезни» . Биохим. Дж . 394 (Pt 3): 527–43. DOI : 10.1042 / BJ20051922 . PMC 1383703 . PMID 16492141 .
- ↑ Беннетт М.В., Зукин Р.С. (февраль 2004 г.). «Электрическая связь и нейрональная синхронизация в мозге млекопитающих». Нейрон . 41 (4): 495–511. DOI : 10.1016 / s0896-6273 (04) 00043-1 . PMID 14980200 . S2CID 18566176 .
- ^ Musil, LS; Гуденаф Д.А. (1993). «Сборка множества субъединиц интегрального белка канала плазматической мембраны, коннексина 43 щелевого соединения, происходит после выхода из ER». Cell . 74 (6): 1065–77. DOI : 10.1016 / 0092-8674 (93) 90728-9 . PMID 7691412 . S2CID 12169415 .
- ↑ Evans WH, Ahmad S, Diez J, George CH, Kendall JM, Martin PE (1999). «Пути торговли людьми, ведущие к образованию щелевых контактов». Новартис найден. Symp . Симпозиумы Фонда Новартис. 219 : 44–54, обсуждение 54–9. DOI : 10.1002 / 9780470515587.ch4 . ISBN 9780470515587. PMID 10207897 .
- ^ Джордж CH, Кендалл JM, Эванс WH (март 1999). «Пути внутриклеточного трафика в сборке коннексинов в щелевые соединения» . J. Biol. Chem . 274 (13): 8678–85. DOI : 10.1074 / jbc.274.13.8678 . PMID 10085106 .
- ^ Джордж CH, Кендалл JM, Кэмпбелл AK, Эванс WH (ноябрь 1998). «Химеры коннексина-акворина сообщают о цитоплазматической кальциевой среде вдоль путей транспортировки, ведущих к биогенезу щелевых соединений в живых клетках COS-7» . J. Biol. Chem . 273 (45): 29822–9. DOI : 10.1074 / jbc.273.45.29822 . PMID 9792698 .
- ^ Мартин PE, Джордж CH, Кастро C, Кендалл JM, Капель J, Кэмпбелл AK, Revilla A, Barrio LC, Evans WH (январь 1998 г.). «Сборка химерных белков коннексина-экворина в функциональные каналы щелевых соединений. Отчетность о кальциевой среде внутриклеточной и плазматической мембраны» . J. Biol. Chem . 273 (3): 1719–26. DOI : 10.1074 / jbc.273.3.1719 . PMID 9430718 .
- ^ Martin PE, Errington RJ Эванс WH (2001). «Сборка щелевого соединения: множественные флуорофоры коннексина идентифицируют сложные пути трафика». Cell Commun. Клеи . 8 (4–6): 243–8. DOI : 10.3109 / 15419060109080731 . PMID 12064596 . S2CID 3029281 .
- ^ Томас Т, Джордан К, Симек Дж, Шао Q, Jedeszko С, Р Уолтон, лэрд DW (октябрь 2005 г.). «Механизмы транспорта Сх43 и Сх26 к плазматической мембране и регенерации щелевого соединения» . J. Cell Sci . 118 (Pt 19): 4451–62. DOI : 10,1242 / jcs.02569 . PMID 16159960 .
- ^ Jongen WM, Fitzgerald DJ, Asamoto M, Пикколи C, Slaga TJ, Gros D, Takeichi M, Ямасаки H (август 1991). «Регулирование опосредованной коннексином 43 межклеточной коммуникации щелевого соединения посредством Ca2 + в эпидермальных клетках мышей контролируется E-кадгерином» . J. Cell Biol . 114 (3): 545–55. DOI : 10,1083 / jcb.114.3.545 . PMC 2289094 . PMID 1650371 .
- ↑ Wei CJ, Francis R, Xu X, Lo CW (май 2005 г.). «Connexin43, связанный с N-кадгерин-содержащим мультибелковым комплексом, необходим для образования щелевых соединений в клетках NIH3T3» (PDF) . J. Biol. Chem . 280 (20): 19925–36. DOI : 10.1074 / jbc.M412921200 . PMID 15741167 . S2CID 770387 .
- ^ Dbouk HA, Mroue RM, Эль-Саббан ME, Talhouk RS (март 2009). «Коннексины: множество функций, выходящих за рамки сборки каналов щелевых соединений» . Сигнал сотовой связи . 7 : 4. DOI : 10,1186 / 1478-811X-7-4 . PMC 2660342 . PMID 19284610 .
- ^ Кихара AH, де Кастро Л.М., Moriscot А.С., Hamassaki DE (май 2006). «Длительная адаптация к темноте изменяет экспрессию коннексина в сетчатке мышей». J Neurosci Res . 83 (7): 1331–41. DOI : 10.1002 / jnr.20815 . PMID 16496335 . S2CID 2919282 .
- ^ a b Decrock E, De Bock M, Wang N, Bultynck G, Giaume C, Naus CC, Green CR, Leybaert L (август 2015 г.). «Пути передачи сигналов коннексина и паннексина, архитектурный план физиологии и патологии ЦНС?». Клетка. Мол. Life Sci . 72 (15): 2823–51. DOI : 10.1007 / s00018-015-1962-7 . ISSN 1420-9071 . PMID 26118660 . S2CID 17170098 .
- Перейти ↑ Goldberg GS, Moreno AP, Lampe PD (сентябрь 2002 г.). «Щелевые соединения между клетками, экспрессирующими коннексин 43 или 32, демонстрируют обратную селективность по отношению к аденозину и АТФ» . J. Biol. Chem . 277 (39): 36725–30. DOI : 10.1074 / jbc.M109797200 . ISSN 0021-9258 . PMID 12119284 .
- ^ а б Ароника Е., Гортер Дж. А., Янсен Г. Х., Леенстра С., Янкая Б., Трост Д. (май 2001 г.). «Экспрессия белков щелевых соединений коннексина 43 и коннексина 32 в опухолях головного мозга, связанных с эпилепсией, и в перилезионной эпилептической коре головного мозга». Acta Neuropathol . 101 (5): 449–59. DOI : 10.1007 / s004010000305 . PMID 11484816 . S2CID 6738913 .
- ^ Verheule S, ван Kempen MJ, т.е Welscher PH, Квак BR, Jongsma HJ (май 1997). «Характеристика каналов щелевого соединения в миокарде предсердий и желудочков взрослых кроликов». Circ. Res . 80 (5): 673–81. DOI : 10.1161 / 01.res.80.5.673 . PMID 9130448 .
- ^ Голлоб М.Х., Джонс Д.Л., Кран А.Д., Данис Л., Гонг XQ, Шао К. и др. (Июнь 2006 г.). «Соматические мутации в гене коннексина 40 (GJA5) при фибрилляции предсердий». N. Engl. J. Med . 354 (25): 2677–88. DOI : 10.1056 / NEJMoa052800 . PMID 16790700 .
- ↑ Мэсси, Стивен (16 января 2009 г.). Коннексины: Руководство (1-е изд.). Springer-Verlag Gmbh. С. 3– ?. ISBN 978-1-934115-46-6.
- ^ Бейер, Эрик С .; Причал, Вивиана М. (16 января 2009 г.). Коннексины: Руководство (1-е изд.). Springer-Verlag Gmbh. С. 387–417. ISBN 978-1-934115-46-6.
- ↑ Fonseca PC, Nihei OK, Urban-Maldonado M, Abreu S, de Carvalho AC, Spray DC, Savino W, Alves LA (июнь 2004 г.). «Характеристика коннексина 30.3 и 43 в тимоцитах». Иммунол. Lett . 94 (1–2): 65–75. DOI : 10.1016 / j.imlet.2004.03.019 . PMID 15234537 .
- ↑ Tai MH, Olson LK, Madhukar BV, Linning KD, Van Camp L, Tsao MS, Trosko JE (январь 2003 г.). «Характеристика межклеточной коммуникации щелевого соединения в иммортализованных эпителиальных клетках протока поджелудочной железы человека с характеристиками стволовых клеток». Поджелудочная железа . 26 (1): e18–26. DOI : 10.1097 / 00006676-200301000-00025 . PMID 12499933 . S2CID 34571252 .
- ^ Kamasawa Н, Шик А, Морита М, Yasumura Т, Дэвидсон КГ, Nagy СО, кожная JE (2005). «Коннексин-47 и коннексин-32 в щелевых соединениях соматов олигодендроцитов, миелиновых оболочек, паранодальных петлях и резцах Шмидта-Лантермана: последствия для ионного гомеостаза и сифонирования калия» . Неврология . 136 (1): 65–86. DOI : 10.1016 / j.neuroscience.2005.08.027 . PMC 1550704 . PMID 16203097 .
- ^ Sargiannidou I, Ahn M, Энрикес AD, Peinado A, Рейнольдс R, Abrams C, Шерер SS, Клеопа KA (май 2008). «Человеческие олигодендроциты экспрессируют Cx31.3: функция и взаимодействия с мутантами Cx32» . Neurobiol. Дис . 30 (2): 221–33. DOI : 10.1016 / j.nbd.2008.01.009 . PMC 2704064 . PMID 18353664 .
- ^ Коннорс BW, Long MA (2004). «Электрические синапсы в мозге млекопитающих» . Анну. Rev. Neurosci . 27 : 393–418. DOI : 10.1146 / annurev.neuro.26.041002.131128 . PMID 15217338 .
- ^ Pfenniger A, Вольвенд A, Квак BR (январь 2011). «Мутации в генах коннексинов и болезни» . Евро. J. Clin. Инвестируйте . 41 (1): 103–16. DOI : 10.1111 / j.1365-2362.2010.02378.x . ISSN 1365-2362 . PMID 20840374 . S2CID 24404442 .
- ^ Molica F, Меенса MJ, Morel S, Квак BR (сентябрь 2014). «Мутации в генах сердечно-сосудистых коннексинов». Биол. Cell . 106 (9): 269–93. DOI : 10.1111 / boc.201400038 . PMID 24966059 . S2CID 10070999 .
Внешние ссылки [ править ]
- СМИ, связанные с коннексинами, на Викискладе?
- Коннексины в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
На момент редактирования в этой статье используется контент из "1.A.24 Семейство коннексинов, образующих разрывное соединение (Connexin)" , которое лицензировано таким образом, чтобы разрешить повторное использование в соответствии с непортированной лицензией Creative Commons Attribution-ShareAlike 3.0 , но не под GFDL . Все соответствующие условия должны быть соблюдены.