Эта статья требует дополнительных ссылок для проверки . ( октябрь 2008 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
Трихотецены представляют собой очень большое семейство химически родственных микотоксинов, продуцируемых различными видами Fusarium , Myrothecium , Trichoderma , Trichothecium , Cephalosporium , Verticimonosporium и Stachybotrys . Трихотецены - это класс сесквитерпенов . Наиболее важными структурными особенностями, обуславливающими биологическую активность трихотеценов, являются 12,13-эпоксидное кольцо, присутствие гидроксильных или ацетильных групп в соответствующих положениях в ядре трихотецена, а также структура и положение боковой цепи. Они производятся на различных зерновых, таких как пшеница, овес или кукуруза, различнымиВиды Fusarium, такие как F. graminearum , F. sporotrichioides , F. poae и F. equiseti .
Некоторые плесневые грибки, вырабатывающие трихотеценовые микотоксины, такие как Stachybotrys chartarum , могут расти во влажных помещениях. Было обнаружено, что макроциклические трихотецены, продуцируемые S. chartarum, могут переноситься по воздуху и, таким образом, способствовать возникновению проблем со здоровьем у людей, находящихся в зданиях. [1] [2] ядовитый гриб в Японии и Китае , Podostroma CORNU-Дама , содержит шесть трихотецены, в том числе satratoxin H , роридин Е и verrucarin .
Классификация [ править ]
Общая классификация [ править ]
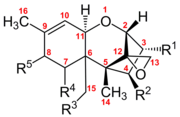
Трихотецены представляют собой группу из более чем 150 химически родственных микотоксинов . [3] Каждый трихотецен показывает структуру ядра, состоящую из одного шестичленного кольца, содержащего один атом кислорода, окруженного двумя углеродными кольцами. [4] Эта сердцевинная кольцевая структура содержит эпоксид или трициклический эфир в 12,13 углеродных положениях, а также двойную связь в 9,10 углеродных положениях. [5] Эти две функциональные группы в первую очередь отвечают за способность трихотецена подавлять синтез белка и вызывать общие цитотоксические эффекты. [6] Примечательно, что эта основная структура является амфипатической , содержащей как полярные, так и неполярные части. [7]Все трихотецены связаны этой общей структурой, но каждый трихотецен также имеет уникальный образец замещения кислородсодержащих функциональных групп в возможных местах на атомах углерода 3, 4, 7, 8 и 15. [5] Эти функциональные группы определяют свойства отдельные трихотецены, а также служат основой для наиболее часто используемой системы классификации для этого семейства токсинов. Эта система классификации разбивает семейство трихотеценов на четыре группы: типы A, B, C и D.
Трикотецены типа А имеют замещения гидроксильных , сложноэфирных или функциональных групп вокруг центральной кольцевой структуры. [4] Обычными примерами из них являются неозоланиол с гидроксильным замещением у углерода 8 и токсин Т-2 с замещением сложным эфиром у углерода 8.
Трикотецены типа B классифицируются по наличию карбонильных функциональных групп, замещенных вокруг основной кольцевой структуры. [4] Обычные примеры из них включают ниваленол и трихотецин, оба из которых имеют кетонную функциональную группу при атоме углерода 8.
Трихотецены типа C имеют дополнительную углеродную 7, эпоксидную группу углерод 8. [4] Типичным примером этого является кротоцин. который также имеет сложноэфирную функциональную группу при атоме углерода 4.
Трихотецены типа D имеют дополнительное кольцо между углеродом 4 и углеродом 15. [4] Эти кольца могут иметь различные дополнительные функциональные группы. Распространенными примерами из них являются роридин А и сатратоксин Н.
Хотя отдельные функциональные группы этих типов классификации придают каждому трихотецену уникальные химические свойства, их тип классификации явно не указывает на их относительную токсичность. [4] В то время как трихотецены типа D считаются наиболее токсичными, типы A и B обладают относительно смешанной токсичностью. [4]
Альтернативные классификации [ править ]
Описанная выше система классификации чаще всего используется для группировки молекул семейства трихотеценов. Однако для этих сложных молекул также существует множество альтернативных систем классификации. Трихотецены также в целом можно охарактеризовать как простые или макроциклические. [6] Простые трихотецены включают типы A, B и C, тогда как макроциклические трихотецены включают тип D и характеризуются наличием мостика углерод 4 - углерод 15. Кроме того, Дж. Ф. Гроув предложил классификацию трикотеценов на три группы, которая также была основана на функциональных паттернах замещения кольцевого скелета. [8] Трикотецены группы 1 имеют только функциональные группы, замещенные в третьем, полностью насыщенном углеродном кольце. [8]Трикотецены группы 2 содержат дополнительные функциональные группы на центральном кольце, содержащем 9,10-углеродную двойную связь. [8] Наконец, трихотецены группы 3 содержат кетонную функциональную группу при атоме углерода 8; это тот же критерий для трихотеценов типа B. [8]
Достижения в области эволюционной генетики также привели к предложению систем классификации трихотеценов, основанных на пути их биосинтеза. Гены, ответственные за биосинтез микотоксина, обычно расположены в кластерах; у Fusariumi они известны как гены TRI. [9] Каждый из генов TRI отвечает за выработку фермента, который выполняет определенный этап биосинтеза трихотеценов. Мутации в этих генах могут приводить к продукции вариантных трихотеценов, и поэтому эти молекулы могут быть сгруппированы на основе общих стадий биосинтеза. Например, общая стадия биосинтеза трихотеценов контролируется геном TRI4 . [10]Этот ферментный продукт контролирует добавление трех или четырех атомов кислорода к триходиену с образованием изотриходиола или изотрихотриола соответственно. [10] Затем из любого из этих промежуточных продуктов можно синтезировать различные трихотецены, и, следовательно, их можно было бы классифицировать как t-тип, если они синтезированы из изотрихотриола, так и d-тип, если они синтезированы из изотриходиола. [4]
Механизм действия [ править ]
Токсичность трикотеценов в первую очередь является результатом их широко цитируемого действия в качестве ингибиторов синтеза белка. Это ингибирование происходит в рибосомах на всех трех стадиях синтеза белка: инициации, удлинении и прекращении. [11] Во время инициации трихотецены могут либо ингибировать ассоциацию двух рибосомных субъединиц, либо ингибировать функцию зрелой рибосомы, предотвращая ассоциацию первой тРНК со стартовым кодоном. [11] Ингибирование при удлинении, скорее всего, происходит из-за того, что трихотецены препятствуют функции пептидилтрансферазы , фермента, который катализирует образование новых пептидных связей на 60-й субъединице рибосомы. [12]Ингибирование во время терминации также может быть результатом ингибирования пептидилтрансферазы или способности трихотеценов предотвращать гидролиз, необходимый на этой конечной стадии. [11] Интересно отметить, что паттерн замещения кольцевого ядра трихотеценов влияет на действие токсина либо как ингибитор инициации, либо как ингибитор удлинения / окончания. [11] Трихотецены также обладают способностью влиять на общую функцию клеточных ферментов из-за тенденции тиоловых групп активного центра атаковать 12,13-углеродное эпоксидное кольцо. [13] Эти ингибирующие эффекты наиболее ярко проявляются в активно пролиферирующих клетках, например, в желудочно-кишечном тракте или костном мозге..
Синтез белка происходит как в цитоплазме клетки, так и в просвете митохондрий , цитоплазматической органелле, ответственной за выработку энергии клетки. Это осуществляется посредством ферментативного пути, который генерирует сильно окисленные молекулы, называемые активными формами кислорода , например перекисью водорода . [14] Активные формы кислорода могут реагировать и вызывать повреждение многих критических частей клетки, включая мембраны, белки и ДНК . [15]Торможение трихотеценом синтеза белка в митохондриях позволяет активным формам кислорода накапливаться в клетке, что неизбежно приводит к окислительному стрессу и индукции запрограммированного пути гибели клеток, апоптоза . [15]
Индукция апоптоза в клетках с высоким уровнем активных форм кислорода происходит из-за множества клеточных сигнальных путей. Первый - это путь р53, который, как показано, активируется токсином Т-2. p53 - это белок, отвечающий за контроль клеточного цикла, но увеличение активности этого белка также приводит к повышенной активации белков BAX в клетке. [16] Эти белки BAX в первую очередь ответственны за увеличение проницаемости митохондриальной мембраны и приводят к высвобождению цитохрома с и активных форм кислорода. [16] Высвобождение цитохрома с из митохондрий вызывает апоптоз, инициируя сборку каспаз., или белки, ответственные за разрушение клетки изнутри. Кроме того, было показано, что трихотецены, такие как Т-2, усиливают сигнальный путь N-концевой киназы c-Jun в клетках. [17] Здесь N-концевая киназа c-Jun способна повышать фосфорилирование своей мишени, c-Jun, в свою активную форму. Активированный c-jun действует как фактор транскрипции в ядре клетки для белков, важных для облегчения последующего пути апоптоза. [17]
Симптомология [ править ]
Микотоксины трихотецена токсичны для людей, других млекопитающих, птиц, рыб, различных беспозвоночных, растений и эукариотических клеток. [18] Специфическая токсичность варьируется в зависимости от конкретного токсина и вида животных, однако способ введения играет значительно более важную роль в определении летальности. Последствия отравления будут зависеть от концентрации воздействия, продолжительности времени и способа воздействия на человека. Высококонцентрированный раствор или большое количество газа с большей вероятностью могут вызвать серьезные последствия, включая смерть. При потреблении токсин подавляет синтез рибосомных белков, ДНК и РНК, [19] [18] [20] митохондриальные функции [21] [22] [23] деление клеток [24][25] при одновременной активации клеточного стрессового ответа, называемого риботоксическим стрессовым ответом [26]
Микотоксины трихотецена могут всасываться местным , пероральным и ингаляционным путями и очень токсичны на субклеточном, клеточном и органическом уровне. [18] Трихотецены отличаются от большинства других потенциальных оружейных токсинов, поскольку они могут действовать через кожу, что объясняется их амфипатическими и липофильными характеристиками. Небольшая амфипатическая природа трихотеценов позволяет им легко пересекать клеточные мембраны [7] и взаимодействовать с различными органеллами, такими как митохондрии, [27] [28] эндоплазматический ретикулум (ER). [29] и хлоропласт [30]Липофильная природа трихотеценов позволяет им легко всасываться через кожу [31], слизистую оболочку легких и кишечник. Прямое нанесение на кожу или пероральный прием трихотецена вызывает быстрое раздражение кожи или слизистой оболочки кишечника. [19] [18] В качестве раздражителя кожи и образования пузырей он, как утверждается, в 400 раз более опьяняющий, чем серный иприт .
Реакция организма на микотоксин, пищеварительную токсичную алейкию, происходит через несколько дней после употребления в четыре этапа. Первая стадия включает воспаление слизистой оболочки желудка и кишечника . Вторая стадия характеризуется лейкопенией , гранулопенией и прогрессирующим лимфоцитозом . Третья стадия характеризуется появлением красной сыпи на коже тела, а также кровоизлиянием кожи и слизистых. В тяжелых случаях может развиться афония и смерть от удушения. К четвертой стадии клетки лимфоидных органов и эритропоэзав костном мозге и селезенке истощаются, а иммунный ответ снижается. Заражение может быть вызвано такой незначительной травмой, как порез, царапина или ссадина. [32]
Выявляются следующие симптомы:
- Сильный зуд и покраснение кожи, язвочки, шелушение кожи
- Искажение любого из органов чувств, потеря способности координировать движения мышц
- Тошнота, рвота и диарея
- Боль в носу и горле, выделения из носа, зуд и чихание
- Кашель, затрудненное дыхание, хрипы, боль в груди и срыгивание крови
- Временные нарушения свертываемости крови
- Повышенная температура тела [33] [34]
Нормативные вопросы [ править ]
Когда речь идет о животных и человека пищи, типа А трихотецены (например , Т-2 токсин , НТ-2 токсин , diacetoxyscirpenol ) представляют особый интерес , поскольку они являются более токсичными , чем другой пищевого происхождения Трихотецены т.е. B группы типа (например , деоксиниваленол , ниваленол , 3- и 15- ацетилдезоксиниваленол ). Однако дезоксиниваленол вызывает беспокойство, поскольку он является наиболее распространенным трихотеценом в Европе. [35] Основные эффекты трихотеценов - связанные с их концентрацией в продукте - это снижение потребления корма, рвота и подавление иммунитета. Относительно немного стран, в первую очередь в Европейском Союзе, рекомендовали максимальные пределы содержания этих микотоксинов в продуктах питания и кормах для животных. Тем не менее, трихотецены часто проверяются на предмет наличия в других местах, чтобы предотвратить их попадание в пищевую цепочку и предотвратить потери в животноводстве.
История [ править ]
Считается, что трихотецены были обнаружены Советским Союзом в 1932 году в Оренбурге, Россия, во время Второй мировой войны . Около 100 000 человек (60% смертность) начали страдать и умирать от пищевой токсической алевкии , смертельного заболевания с симптомами, напоминающими радиацию. Считается, что советские мирные жители заболели от употребления зараженного хлеба и вдыхания плесени через загрязненное сено, пыль и вентиляционные системы. Считается, что виновными являются токсины Fusarium sporotrichioides и Fusarium poae, которые являются высокими продуцентами токсина Т-2 . [36] Фузариозвиды, вероятно, являются наиболее часто цитируемыми и одними из самых многочисленных грибов, продуцирующих трихотецен. [37]
Трихотецены представляют собой идеальный боевой биологический агент, поскольку они смертоносны и недороги в производстве в больших количествах, стабильны в виде аэрозолей для диспергирования и не требуют эффективной вакцинации / лечения. [12] Данные свидетельствуют о том, что микотоксины уже использовались в качестве биологического оружия.
- 1964 г. Есть неподтвержденные сообщения, что египетские или российские войска использовали Т-2 с ипритом.
- 1974-1981 инциденты с « желтым дождем » в Юго-Восточной Азии (Лаос, Камбоджа) и Афганистане [38] [39] [40] [41]
- В 1975 и 1981 годах во время войны во Вьетнаме Советский Союз якобы поставлял микотоксины армиям Вьетнама и Лаоса для использования против сил сопротивления в Лаосе и Камбодже [42] [43]
- 1985–1989 гг. Ирано-иракская война, сообщения о поставках микотоксинов в Ирак (в виде порошка и дыма) [44]
С тех пор о трихотеценах сообщалось во всем мире. [45] Они оказали значительное экономическое влияние на мир из-за таких причин, как: гибель людей и животных, увеличение расходов на здравоохранение и ветеринарное обслуживание, сокращение животноводства, утилизация зараженных пищевых продуктов и кормов, а также инвестиции в исследования. и приложения для уменьшения серьезности проблемы микотоксинов. Эти микотоксины ежегодно приводят к потерям в миллионы долларов из-за факторов, которые часто не поддаются контролю человека (экологические, экологические или способ хранения). [46]
Загрязнение пищевых продуктов [ править ]
Опасные концентрации трихотеценов были обнаружены в кукурузе, пшенице, ячмене, овсе, рисе, ржи, овощах и других культурах. Болезни, вызванные инфекцией, включают гниль семян, гниль всходов, корневую гниль , гниль стеблей и гниль початков. [47] Трихотецены также являются обычными загрязнителями кормов для домашней птицы, и их неблагоприятное воздействие на здоровье и продуктивность птицы было тщательно изучено. [48]
Несколько исследований показали, что оптимальные условия для роста грибов не обязательно являются оптимальными для производства токсинов. [49] Производство токсинов больше всего при высокой влажности и температуре 6-24 ° C. Размножение и производство грибов улучшается в тропических условиях с высокими температурами и влажностью; муссоны , ливневые паводки и несезонные дожди во время сбора урожая. [50] Трихотецены были обнаружены в пробах воздуха, что позволяет предположить, что они могут распыляться на споры или мелкие частицы [51] [52]
О естественном возникновении TCT сообщалось в Азии , Африке , Южной Америке , Европе и Северной Америке [53]
- Акакабибио, болезнь аналогичной этиологии, также была связана с зерном, загрязненным трихотеценом, в Японии. [54]
- В Китае злаки или продукты из них, загрязненные трихотеценами, включая ДОН, токсин Т-2 и НИВ, также были связаны со вспышками желудочно-кишечных расстройств. [55]
- В Югославии исследования микотоксигенных грибов в сыром молоке показали, что 91% протестированных образцов были заражены [56]
- В США в 1988–1989 годах в семи штатах Среднего Запада было проведено исследование, в ходе которого были обнаружены микотоксины в 19,5–24,7% образцов кукурузы. [57] С начала 1900-х годов были описаны случаи рвоты у животных и людей после употребления в пищу злаков, инфицированных видами Fusarium. [58] [59]
- В исследовании, проведенном в районе Бихара с 1985 по 1987 год, 51% протестированных образцов были загрязнены плесенью. [60]
- В другом исследовании, проведенном в регионе Бихар [61], высокие уровни были зарегистрированы в арахисовой муке, используемой для молочного скота.
- В Лудхиане и Пенджабе исследователи обнаружили 75% образцов с молочных ферм зараженными. [62]
- В Индии из-за заражения арахиса микотоксинами было потеряно около 10 миллионов долларов. [63]
Безопасность [ править ]
Прямых противоядий от воздействия трихотецена нет. Следовательно, управление рисками на загрязненных территориях в первую очередь определяется лечением симптомов воздействия, а также предотвращением воздействия в будущем.
Лечение [ править ]
Типичные пути воздействия трихотеценовых токсинов включают местное всасывание, прием внутрь и вдыхание. Тяжесть симптомов зависит от дозы и типа воздействия, но лечение в первую очередь направлено на поддержку систем организма, поврежденных микотоксином. Первым шагом в большинстве случаев заражения является снятие потенциально загрязненной одежды и тщательная промывка участков воздействия водой. [64] Это предохраняет жертву от повторного воздействия. Жидкости и электролиты можно давать жертвам с высоким уровнем поражения желудочно-кишечного тракта, чтобы смягчить последствия снижения всасывания в желудочно-кишечном тракте. Свежий воздух и вспомогательное дыхание также могут применяться при развитии легкого респираторного расстройства. [64]Обострение тяжелых симптомов может потребовать применения передовой медицинской помощи. Начало лейкопении или снижение количества лейкоцитов можно лечить с помощью переливания плазмы или тромбоцитов . [64] Гипотензию можно лечить с помощью норадреналина или дофамина . [64] Развитие тяжелой сердечно-легочной недостаточности может потребовать интубации и дополнительных медикаментов для стабилизации сердечной и легочной деятельности.
Кроме того, существует множество химических веществ, которые могут косвенно уменьшить повреждающее действие трихотеценов на клетки и ткани. Растворы активированного угля часто назначают при проглатывании в качестве адсорбента . [65] Здесь древесный уголь действует как пористое вещество для связывания токсина, предотвращая его абсорбцию через желудочно-кишечный тракт и увеличивая его удаление из организма через кишечник. Подобные детоксифицирующие адсорбенты также могут быть добавлены в корм для животных после заражения, чтобы снизить биодоступность токсина при употреблении. Антиоксидантытакже полезны для смягчения повреждающих эффектов трихотеценов в ответ на увеличение количества активных форм кислорода, которые они производят в клетках. Как правило, считается, что хорошая диета, богатая пробиотиками, витаминами и питательными веществами, белками и липидами, эффективна для уменьшения симптомов отравления трихотеценом. [16] Например, было обнаружено , что витамин Е противодействует образованию перекиси липидов, вызванной токсином Т-2 у кур. [66] Точно так же совместный прием модифицированных глюкоманн и селенав рационе цыплят, потребляющих также токсин Т-2, снижается вредное воздействие токсинов, связанных с истощением антиоксидантов в печени. Несмотря на то, что эти антиоксиданты не являются прямым антидотом, они могут иметь решающее значение для снижения тяжести воздействия трихотецена.
Профилактика [ править ]
Трихотецены - это микотоксины, вырабатываемые плесневыми грибами, которые часто загрязняют запасы зерновых продуктов. Это делает загрязнение трихотеценом серьезной проблемой для общественного здравоохранения, и во многих районах действуют строгие ограничения на допустимое содержание трихотецена. Например, в Европейском Союзе допускается содержание только 0,025 промилле токсина Т-2 в хлебобулочных изделиях, предназначенных для употребления в пищу человеком. [67] Плесневые грибки, способные производить трихотецены, хорошо растут в темных местах с умеренным климатом и высоким содержанием влаги. Следовательно, один из лучших способов предотвратить загрязнение пищевых продуктов трихотеценом - это хранить ресурсы в надлежащих условиях, чтобы предотвратить рост плесени. [16]Например, обычно рекомендуется хранить зерно только в помещениях с влажностью менее 15%. [68] Однако, если территория уже была загрязнена трихотеценовыми токсинами, существует множество возможных стратегий дезактивации для предотвращения дальнейшего воздействия. Было показано, что обработка 1% гипохлоритом натрия (NaOCl) в 0,1 М гидроксиде натрия (NaOH) в течение 4–5 часов подавляет биологическую активность токсина Т-2. [16] Инкубация с водным озоном в концентрации приблизительно 25 частей на миллион также приводит к разложению различных трихотеценов посредством механизма, включающего окисление двойной углеродной связи 9,10. [69] УФВоздействие также оказалось эффективным при правильных условиях. [16]
Помимо стратегий физического и химического обеззараживания, прогрессивные исследования в области молекулярной генетики также привели к появлению потенциала биологического обеззараживания. Многие микробы, включая бактерии, дрожжи и грибы, развили продукты ферментативных генов, которые способствуют специфической и эффективной деградации трихотеценовых микотоксинов. [68] Многие из этих ферментов специфически разрушают 12,13-углеродное эпоксидное кольцо, что важно для токсичности трихотеценов. Например, штамм Eubacteria BBSH 797 продуцирует ферменты деэпоксидазы, которые восстанавливают 12,13-углеродное эпоксидное кольцо до группы с двойной связью. [68]Они, наряду с другими микробами, проявляющими детоксицирующие свойства трихотецена, могут использоваться в магазинах кормов для предотвращения токсического действия загрязненного корма при употреблении. [16] Кроме того, молекулярное клонирование генов, ответственных за производство этих детоксифицирующих ферментов, может быть полезно для получения штаммов сельскохозяйственных продуктов, устойчивых к отравлению трихотеценом. [16]
Эпокситрихотецены [ править ]
Эпокситрихотецены являются разновидностью вышеупомянутого и когда-то были исследованы для военного использования в Восточной Германии и, возможно, во всем советском блоке. [70] После появления симптомов отравления эпокситихотеценом лечение невозможно, хотя последствия могут исчезнуть, не оставив при этом необратимых повреждений.
Планы использования в качестве крупномасштабного биологического оружия были отброшены, поскольку соответствующие эпокситрихотецены очень быстро разлагаются под воздействием ультрафиолетового излучения и тепла, а также под воздействием хлора, что делает их бесполезными для открытых атак и отравления источников воды. [ необходима цитата ]
Ссылки [ править ]
- ^ Обнаружение переносимых по воздуху Stachybotrys chartarum макроциклических трихотеценовых микотоксинов в помещении
- Перейти ↑ Etzel RA (2002). «Микотоксины». ДЖАМА . 287 (4): 425–7. DOI : 10,1001 / jama.287.4.425 . PMID 11798344 .
- ^ "Американское фитопатологическое общество" . Американское фитопатологическое общество . Проверено 7 мая 2018 .
- ^ a b c d e f g h McCormick SP, Stanley AM, Stover NA, Alexander NJ (июль 2011 г.). «Трихотецены: от простых микотоксинов к сложным» . Токсины . 3 (7): 802–14. DOI : 10,3390 / toxins3070802 . PMC 3202860 . PMID 22069741 .
- ^ a b Защита от трихотеценовых микотоксинов . Национальные академии. 1983-01-01. ISBN 9780309034302.
- ^ а б Беннетт Дж. В., Клих М. (июль 2003 г.). «Микотоксины» . Обзоры клинической микробиологии . 16 (3): 497–516. DOI : 10.1128 / CMR.16.3.497-516.2003 . PMC 164220 . PMID 12857779 .
- ^ a b Миддлбрук JL, Leatherman DL (сентябрь 1989 г.). «Специфическая ассоциация токсина Т-2 с клетками млекопитающих». Биохимическая фармакология . 38 (18): 3093–102. DOI : 10.1016 / 0006-2952 (89) 90020-8 . PMID 2783163 .
- ^ a b c d Grove JF (1988). «Немакроциклические трихотецены». Отчеты о натуральных продуктах . 5 (2): 187–209. DOI : 10.1039 / NP9880500187 . ISSN 0265-0568 . PMID 3062504 .
- ^ Кимура, Макото; Токай, Такеши; о'Доннелл, Керри; Уорд, Тодд Дж .; Фудзимура, Макото; Хамамото, Хироши; Шибата, Такехико; Ямагути, Исаму (27 марта 2003 г.). «Кластер генов биосинтеза трихотецена Fusarium graminearum F15 содержит ограниченное количество генов основных путей и экспрессию несущественных генов» . Письма FEBS . 539 (1–3): 105–110. DOI : 10.1016 / S0014-5793 (03) 00208-4 . PMID 12650935 . S2CID 19787988 .
- ^ a b McCormick SP, Александр NJ, Проктор RH (июль 2006 г.). «Fusarium Tri4 кодирует многофункциональную оксигеназу, необходимую для биосинтеза трихотецена». Канадский журнал микробиологии . 52 (7): 636–42. DOI : 10.1139 / w06-011 . PMID 16917519 .
- ^ а б в г Кисслинг К. (1986). «Биохимический механизм действия микотоксинов» (PDF) . Чистая и прикладная химия . 58 (2): 327–338. DOI : 10,1351 / pac198658020327 . S2CID 94777285 .
- ^ a b Henghold WB (июль 2004 г.). «Другие биологические токсины биологического оружия: рицин, стафилококковый энтеротоксин B и трихотеценовые микотоксины». Дерматологические клиники . 22 (3): 257-62, v. DOI : 10.1016 / j.det.2004.03.004 . PMID 15207307 .
- Перейти ↑ Ueno Y, Matsumoto H (октябрь 1975 г.). «Инактивация некоторых тиол-ферментов трихотеценовыми микотоксинами из видов Fusarium» . Химико-фармацевтический бюллетень . 23 (10): 2439–42. DOI : 10,1248 / cpb.23.2439 . PMID 1212759 .
- ^ Зоров БД, Juhaszova М, Sollott SJ (июль 2014). «Митохондриальные активные формы кислорода (ROS) и ROS-индуцированное высвобождение ROS» . Физиологические обзоры . 94 (3): 909–50. DOI : 10.1152 / Physrev.00026.2013 . PMC 4101632 . PMID 24987008 .
- ^ a b Фанг Х, Ву И, Го Дж, Жун Дж, Ма Л, Чжао З, Цзо Д., Пэн С. (август 2012 г.). «Токсин Т-2 вызывает апоптоз в дифференцированных мышиных эмбриональных стволовых клетках посредством митохондриального пути, опосредованного активными формами кислорода». Апоптоз . 17 (8): 895–907. DOI : 10.1007 / s10495-012-0724-3 . PMID 22614820 . S2CID 17446994 .
- ^ a b c d e f g h Адхикари М., Неги Б., Кошик Н., Адхикари А., Аль-Хедхайри А.А., Кошик Н.К., Чой Э.Х. (май 2017 г.). «Микотоксин Т-2: токсикологические эффекты и стратегии дезактивации» . Oncotarget . 8 (20): 33933–33952. DOI : 10.18632 / oncotarget.15422 . PMC 5464924 . PMID 28430618 .
- ^ a b Li M, Pestka JJ (сентябрь 2008 г.). «Сравнительная индукция расщепления 28S рибосомной РНК рицином и трихотеценами дезоксиниваленолом и Т-2 токсином в макрофагах» . Токсикологические науки . 105 (1): 67–78. DOI : 10.1093 / toxsci / kfn111 . PMC 2734305 . PMID 18535001 .
- ^ a b c d Ваннемахер Р., Винер С. Л., Сиделл Ф. Р., Такафуджи Э. Т., Франц Д. Р. (1997). Микотоксины трихотеценового происхождения . Медицинские аспекты химической и биологической войны . 6 (1-е изд.). = Государственная печать США. С. 655–76. ISBN 978-9997320919.
- ^ a b Маклафлин C, Воган M, Кэмпбелл I, Вей CM, Стаффорд M, Хансен B (1977). «Подавление синтеза белка трихотеценами». Микотоксины в здоровье человека и животных . Парк Форест Юг, Иллинойс: Издатели Pathotox. С. 263–75.
- ^ Дежардин А.Е., Хон Т.М., McCormick SP (сентябрь 1993). «Биосинтез трихотецена у видов Fusarium: химия, генетика и значение» . Микробиологические обзоры . 57 (3): 595–604. DOI : 10.1128 / MMBR.57.3.595-604.1993 . PMC 372927 . PMID 8246841 .
- ↑ Fried HM, Warner JR (январь 1981 г.). «Клонирование дрожжевого гена устойчивости к триходермину и рибосомного белка L3» . Труды Национальной академии наук Соединенных Штатов Америки . 78 (1): 238–42. Полномочный код : 1981PNAS ... 78..238F . DOI : 10.1073 / pnas.78.1.238 . PMC 319027 . PMID 7017711 .
- ^ Буазиз С, Martel С, Шэрэф эль Dein О, Абид-Essefi S, Бреннер С, Лемер С, Н Бача (август 2009 г.). «Вызванная фузариозным токсином токсичность в культивируемых клетках и в изолированных митохондриях включает PTPC-зависимую активацию митохондриального пути апоптоза» . Токсикологические науки . 110 (2): 363–75. DOI : 10.1093 / toxsci / kfp117 . PMID 19541794 .
- Перейти ↑ Bin-Umer MA, McLaughlin JE, Basu D, McCormick S, Tumer NE (декабрь 2011 г.). «Трихотеценовые микотоксины ингибируют митохондриальную трансляцию - значение механизма токсичности» . Токсины . 3 (12): 1484–501. DOI : 10,3390 / toxins3121484 . PMC 3268453 . PMID 22295173 .
- ^ Аскона-Olivera СО, Оуян Y, Мерта Дж, Чу Ф., Pestka JJ (июль 1995 года). «Индукция цитокиновых мРНК у мышей после перорального воздействия трихотеценового вомитоксина (дезоксиниваленола): связь с распределением токсина и ингибированием синтеза белка». Токсикология и прикладная фармакология . 133 (1): 109–20. DOI : 10,1006 / taap.1995.1132 . PMID 7597700 .
- ^ Thompson WL, Ваннемахер RW (1986). «Структурно-функциональные отношения 12,13-эпокситрихотеценовых микотоксинов в культуре клеток: сравнение с летальностью всего животного». Токсикон . 24 (10): 985–94. DOI : 10.1016 / 0041-0101 (86) 90004-8 . PMID 3824405 .
- ↑ Шифрин В.И., Андерсон П. (май 1999 г.). «Трихотеценовые микотоксины вызывают риботоксический стрессовый ответ, который активирует N-концевую киназу c-Jun и митоген-активируемую протеинкиназу p38 и вызывает апоптоз» . Журнал биологической химии . 274 (20): 13985–92. DOI : 10.1074 / jbc.274.20.13985 . PMID 10318810 .
- ^ Cundliffe Е, пушка М, Дэвис Дж (январь 1974). «Механизм подавления синтеза белка эукариот токсинами трихотеценовых грибов» . Труды Национальной академии наук Соединенных Штатов Америки . 71 (1): 30–4. DOI : 10.1073 / pnas.71.1.30 . PMC 387925 . PMID 4521056 .
- ^ Cundliffe E, Davies JE (март 1977). «Ингибирование инициации, удлинения и прекращения синтеза эукариотических белков трихотеценовыми грибковыми токсинами» . Противомикробные препараты и химиотерапия . 11 (3): 491–9. DOI : 10.1128 / AAC.11.3.491 . PMC 352012 . PMID 856003 .
- Перейти ↑ Ueno Y (1985). «Токсикология микотоксинов». Критические обзоры в токсикологии . 14 (2): 99–132. DOI : 10.3109 / 10408448509089851 . PMID 3158480 .
- ^ Пейс Ю.Г., Вт МР, Кентерберийский WJ (1988). «Микотоксин Т-2 подавляет синтез митохондриального белка». Токсикон . 26 (1): 77–85. DOI : 10.1016 / 0041-0101 (88) 90139-0 . PMID 3347933 .
- ^ Coulombe RA (март 1993). «Биологическое действие микотоксинов» . Журнал молочной науки . 76 (3): 880–91. DOI : 10.3168 / jds.S0022-0302 (93) 77414-7 . PMID 8463495 .
- Перейти ↑ Schwarzer K (2009). «Вредное действие микотоксинов на физиологию животных». 17-й Ежегодный семинар по кормовой технологии и питанию ASAIM SEA . Хюэ, Вьетнам.
- ^ «Трихотеценовый микотоксин | IDPH» . www.dph.illinois.gov . Проверено 7 мая 2018 .
- ^ Уэно Y (апрель 1984). «Токсикологические особенности токсина Т-2 и родственных трихотеценов». Фундаментальная и прикладная токсикология . 4 (2 Pt 2): S124–32. DOI : 10.1016 / 0272-0590 (84) 90144-1 . PMID 6609858 .
- ^ Миллер JD (2003). «Аспекты экологии токсинов фузариоза в злаках». In de Vries JW, Trucksess MW, Jakson LS (ред.). Микотоксины и безопасность пищевых продуктов . Нью-Йорк: Kluwer Academic / Plenum Publishers. С. 19–27.
- ^ Йоффе AZ (1950). Токсичность грибов на зерновых, перезимовавших в поле: по этиологии пищевой токсической алевкии (канд. Экон. ). Ленинград: Ин-т. Бот. Акад. Sci. п. 205.
- Перейти ↑ Rocha O, Ansari K, Doohan FM (апрель 2005 г.). «Влияние трихотеценовых микотоксинов на эукариотические клетки: обзор». Пищевые добавки и загрязнители . 22 (4): 369–78. DOI : 10.1080 / 02652030500058403 . PMID 16019807 . S2CID 1534222 .
- ^ Heyndrickx А, Sookvanichsilp Н, ван ден Heede М (1984). «Обнаружение трихотеценовых микотоксинов (желтый дождь) в крови, моче и фекалиях иранских солдат, пострадавших от газовой атаки». Archives Belges = Бельгийский архив . Дополнение: 143–6. PMID 6535464 .
- ^ Mirocha CJ, Pawlosky RA, Чаттерджи K, Уотсон S, Hayes W (ноябрь 1983). «Анализ токсинов Fusarium в различных образцах, используемых в биологической войне в Юго-Восточной Азии». Журнал - Ассоциация официальных химиков-аналитиков . 66 (6): 1485–99. PMID 6643363 .
- ↑ Spyker MS, Spyker DA (октябрь 1983 г.). «Желтый дождь: химическая война в Юго-Восточной Азии и Афганистане». Ветеринария и токсикология человека . 25 (5): 335–40. PMID 6636506 .
- ^ Ваннемахер JR, Wiener SL. "Глава 34: Трихотеценовые микотоксины". В Sidell FR, Takafuji ET, Franz DR (ред.). Медицинские аспекты химической и биологической войны . Учебник военной медицины серии. Офис главного хирурга, Департамент армии, Соединенные Штаты Америки.
- ↑ Хейг AM (22 марта 1982 г.). Специальный отчет 98: Химическая война в Юго-Восточной Азии и Афганистане: отчет для Конгресса от государственного секретаря Хейга (отчет). Вашингтон, округ Колумбия: Типография правительства США.
- ^ Такер JB (2001). « Противоречие « желтый дождь » : уроки соблюдения контроля над вооружениями». Нераспространение Ред . 8 : 25–39. DOI : 10.1080 / 10736700108436836 . S2CID 22473397 .
- ^ «ЦНС - получить микробный посевной материал для стандартного или нового агента» . webarchive.loc.gov . Архивировано из оригинала на 2001-11-27 . Проверено 6 мая 2018 .
- ^ Dohnal В, Ежковой А, июнь Д, Kuca К (январь 2008). «Метаболические пути токсина Т-2». Текущий метаболизм лекарств . 9 (1): 77–82. DOI : 10.2174 / 138920008783331176 . PMID 18220574 .
- Перейти ↑ Zain, Mohamed E. (2011-04-01). «Воздействие микотоксинов на человека и животных» . Журнал Саудовского химического общества . 15 (2): 129–144. DOI : 10.1016 / j.jscs.2010.06.006 . ISSN 1319-6103 .
- ^ Schollenberger М Мюллер HM, Эрнст K, Sondermann S, M Либшер, Schlecker C, Wischer G, Дрохнер W, Гартунг K, Piepho HP (октябрь 2012). «Возникновение и распространение 13 трихотеценовых токсинов в естественно загрязненных растениях кукурузы в Германии» . Токсины . 4 (10): 778–87. DOI : 10,3390 / toxins4100778 . PMC 3496988 . PMID 23162697 .
- Перейти ↑ Leeson S, Dias GJ, Summers JD (1995). «Трихотецены». Нарушения обмена веществ у птицы . Гуэлф, Онтарио, Канада. С. 190–226.
- ^ Hesseltine CW, Шотуэлл OL, Смит M, Ellis JJ, Vandegraft E, G Shannon (1970). «Продукция различных афлатоксинов штаммами серии Aspergillis flavus ». Proc. первая американо-японская конф. Токсичный микроорг . Вашингтон.
- ^ Dudeja Р, Гупта Р. К., Минхас А.С. (ред.). Безопасность пищевых продуктов в 21 веке: перспективы общественного здравоохранения .
- ^ Brasel TL, Douglas DR, Wilson SC, Straus DC (январь 2005). «Обнаружение переносимых по воздуху макроциклических трихотеценовых микотоксинов Stachybotrys chartarum на частицах меньшего размера, чем конидии» . Прикладная и экологическая микробиология . 71 (1): 114–22. DOI : 10,1128 / AEM.71.1.114-122.2005 . PMC 544211 . PMID 15640178 .
- ^ Cho S, Seo S, Schmechel D, Гриншпун SA, Репонен T (сентябрь 2005). «Аэродинамические характеристики и респираторное отложение фрагментов грибов». Атмосферная среда . 39 (30): 5454–5465. Bibcode : 2005AtmEn..39.5454C . DOI : 10.1016 / j.atmosenv.2005.05.042 .
- Перейти ↑ Beasley VR, ed. (1989). Трихотеценовый микотоксикоз: патофизиологические эффекты . 1 . Бока-Ратон: CRC Press. С. 1–26.
- ^ Уэно У, Ишии К, Сакаи К, Kanaeda S, Tsunoda Н (1972). «Токсикологические подходы к метаболитам Fusaria. IV. Микробиологическое исследование« отравления бобовой скорлупой лошадей »с выделением токсичных трихотеценов, неозоланиола и Т-2 токсина Fusarium solani M-1-1». Японский J. Exp. Med . 42 (3): 187–203. PMID 4538152 .
- ↑ Лу XY (1988). «Загрязнение зерновых культур фузариозом в Китае». Proc. Японский доц. Микотоксикология . Дополнение 1: 97–98.
- ^ Skrinjar M, Данев M, Dimic G (1995). «Исследование на наличие токсигенных грибов и афлатоксинов в сыром молоке». Acta Aliment . 24 : 395–402.
- ^ Russell L, Cox DF, Ларсен G, Bodwell K, Нельсон CE (январь 1991). «Заболеваемость плесенью и микотоксинами на заводах по производству кормов для животных в семи штатах Среднего Запада, 1988-1989 годы» . Журнал зоотехники . 69 (1): 5–12. DOI : 10.2527 / 1991.6915 . PMID 1825995 .
- ↑ Наумов Н.А. (1916). «Дурманящий хлеб». Мин. Емл. (Россия), Trudy Ruiri Miwel. I. Фитопатол. Учен, Ком. : 216.
- ^ Дунин М (1930). «Фузариоз зерновых культур в Европейской России в 1923 году». Фитопатол . 16 : 305–308.
- ^ Ranjan KS, Синха AK (1991). «Встречаемость микотоксигенных грибов и микотоксинов в кормах для животных из Бихара, Индия». Журнал продовольственной науки и сельского хозяйства . 56 (1): 39–47. DOI : 10.1002 / jsfa.2740560105 .
- ^ Филлипс С. И., Wareing PW, Датт А, Паниграхи S, Медлки В (1996-01-01). «Микофлора и заболеваемость афлатоксином, зеараленоном и стеригматоцистином в молочных кормах и образцах кормов из Восточной Индии и Бангладеш». Микопатология . 133 (1): 15–21. DOI : 10.1007 / BF00437094 . ISSN 0301-486X . S2CID 32084324 .
- ^ Dhand NK, Joshi DB, Jand SK (1998). «Афлатоксины в молочных кормах / ингредиентах». Ind. J. Anim. Nutr . 15 : 285–286.
- ^ Васанти S, Бхат RV (ноябрь 1998). «Микотоксины в пищевых продуктах - наличие, здоровье, экономическое значение и меры контроля пищевых продуктов». Индийский журнал медицинских исследований . 108 : 212–24. PMID 9863277 .
- ^ a b c d "T-2 TOXIN - База данных HSDB Национальной медицинской библиотеки" . toxnet.nlm.nih.gov . Проверено 7 мая 2018 .
- ^ Эдрингтон TS, Kubena LF, Харви RB, Rottinghaus GE (сентябрь 1997). «Влияние суперактивированного угля на токсическое действие афлатоксина или токсина Т-2 на выращивание бройлеров» . Птицеводство . 76 (9): 1205–11. DOI : 10,1093 / пс / 76.9.1205 . PMID 9276881 .
- ^ Hoehler D, Марквардт RR (декабрь 1996). «Влияние витаминов Е и С на токсическое действие охратоксина А и токсина Т-2 у цыплят» . Птицеводство . 75 (12): 1508–15. DOI : 10.3382 / ps.0751508 . PMID 9000276 .
- ^ Stoev SD (март 2015). «Пищевые микотоксикозы, оценка риска и недооцененная опасность замаскированных микотоксинов, а также совместные эффекты или взаимодействие микотоксинов». Экологическая токсикология и фармакология . 39 (2): 794–809. DOI : 10.1016 / j.etap.2015.01.022 . PMID 25734690 .
- ^ a b c Девриз М., Де Бакер П., Кроубелс С. (2013). «Различные методы противодействия выработке микотоксинов и их влиянию на здоровье животных» . Vlaams Diergen Tijds . 82 (4): 181–190. DOI : 10.21825 / vdt.v82i4.16695 .
- ↑ Young JC, Zhu H, Zhou T (март 2006 г.). «Разложение микотоксинов трихотецена водным озоном». Пищевая и химическая токсикология . 44 (3): 417–24. DOI : 10.1016 / j.fct.2005.08.015 . PMID 16185803 .
- ↑ Die Chemie der Kampfstoffe, Государственное издание ГДР, 1988
Внешние ссылки [ править ]
- Структуры некоторых микотоксинов трихотеценового происхождения.
- Роберт В. Ваннемахер и Стэнли Л. Вайнер: трихотеценовые микотоксины, глава 34, Медицинские аспекты химической и биологической войны