Анти-перипланарный
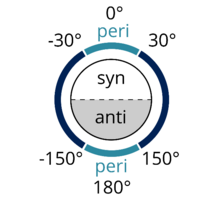
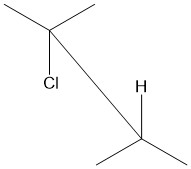
В органической химии антиперипланарный или антиперипланарный описывает валентный угол A-B-C-D в молекуле. В этом конформере двугранный угол связи A-B и связи C-D больше +150° или меньше -150° [1] (рис. 1 и 2 ). Антиперипланарность часто используется в учебниках для обозначения строго антикомпланарности [2] с двугранным углом AB CD, равным 180° (рис. 3). В проекции Ньюмена, молекула будет располагаться в шахматном порядке с антиперипланарными функциональными группами, направленными вверх и вниз, на 180 ° друг от друга (см. Рисунок 4). На рис. 5 показан 2-хлор-2,3-диметилбутан в козловой проекции с хлором и водородом антиперипланарно друг к другу.
Синперипланарный или синперипланарный похож на антиперипланарный. В син-перипланарном конформере A и D находятся по одну сторону от плоскости связи, с двугранным углом A-B и C-D между +30° и -30° (см. Рисунок 2).
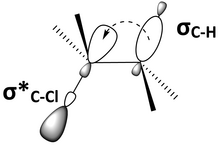
Важным фактором в антиперипланарном конформере является взаимодействие между молекулярными орбиталями. Антиперипланарная геометрия помещает связывающую орбиталь и антисвязывающую орбиталь примерно параллельно друг другу или син-перипланарно. Рисунок 6 представляет собой другое изображение 2-хлор-2,3-диметилбутана (рисунок 5), показывающее связывающую C-H орбиталь, σ C-H , и разрыхляющую C-Cl орбиталь, σ* C-Cl , syn -перипланарный. Параллельные орбитали могут перекрываться и участвовать в гиперконъюгации .. Если связывающая орбиталь является донором электронов, а антисвязывающая орбиталь является акцептором электронов, то связывающая орбиталь сможет передать электроотрицательность антисвязывающей орбитали. Это донорно-акцепторное взаимодействие заполненных и незаполненных молекул оказывает общий стабилизирующий эффект на молекулу. Однако переход со связывающей орбитали на антисвязывающую орбиталь также приведет к ослаблению обеих этих связей. На рисунке 6 2-хлор-2,3-диметилбутан стабилизирован за счет гиперконъюгации за счет донорства электронов от σ CH в σ * C-Cl , но связи C–H и C–Cl ослаблены. Диаграмма молекулярных орбиталей показывает, что смешивание σ C–H и σ* C–Clв 2-хлор-2,3-диметилбутане снижает энергию обеих орбиталей (рис. 7).
Реакция бимолекулярного отщепления будет происходить в молекуле, где разрыв связи углерод-водород и уходящая группа являются антиперипланарными [4] [5] [6] [7] (рис. 8). Эта геометрия предпочтительна, потому что она выравнивает орбитали σ C-H и σ * CX . [8] [9] На рисунке 9 показаны орбиталь σ C-H и орбиталь σ* CX , параллельные друг другу, что позволяет орбитали σ C-H передаваться на антисвязывающую орбиталь σ* CX посредством гиперконъюгации. Это служит для ослабления связи CH и CX, обе из которых разрываются в E 2реакция. Это также заставляет молекулу легче перемещать свои электроны σC -H на орбиталь πC -C (рис. 10).
В перегруппировке пинакола метильная группа оказывается антиперипланарной по отношению к функциональной группе активированного спирта. [10] [11] Это помещает орбиталь σ C–C метильной группы параллельно орбитали σ* C–O активированного спирта. Перед тем, как активированный спирт уйдет в виде H 2 O, метильная связывающая орбиталь переходит на разрыхляющую С-О орбиталь, ослабляя обе связи. Эта гиперконъюгация облегчает 1,2-метиловый сдвиг, который происходит для удаления воды. См. рисунок 11 для механизма.
Термин «анти-перипланарный» был впервые использован Кляйном и Прелогом в их работе под названием «Описание стерических отношений между одинарными связями», опубликованной в 1960 г. [12] «Анти» относится к двум функциональным группам, лежащим на противоположных сторонах плоскости связь. «Пери» происходит от греческого слова «близкий», поэтому перипланар означает «приблизительно плоский». [13] В своей статье «Перипланарно или копланарно?» Кейн и Херш отмечают, что во многих учебниках по органике термин «антиперипланарный» означает полностью антипланарный или антикомпланарный, что технически неверно. [14]