Dioxygenyl ионов , О+
2, Это редко встречается oxycation , в которых оба атома кислорода имеют формальную степень окисления от +1/2. Формально он получается из кислорода удалением электрона :
- О 2 → О+
2+ е -
Изменение энергии для этого процесса называется энергией ионизации молекулы кислорода. По сравнению с большинством молекул эта энергия ионизации очень высока и составляет 1175 кДж / моль. [1] В результате объем химии O+
2довольно ограничен, действуя в основном как одноэлектронный окислитель. [2]
Структура и молекулярные свойства [ править ]
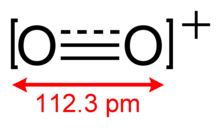
О+
2имеет порядок связи 2,5 и длину связи 112,3 пм в твердом O 2 [AsF 6 ]. [3] Это изоэлектронное с монооксидом азота и парамагнитно. [4] энергия связи составляет 625,1 кДж моль -1 и растяжения частоты 1858 см -1 , [5] оба из которых являются высокими по сравнению с большинством молекул.
Синтез [ править ]
Нил Бартлетт продемонстрировал, что диоксигенилгексафтороплатинат (O 2 PtF 6 ), содержащий диоксигенильный катион, может быть получен при комнатной температуре путем прямой реакции газообразного кислорода (O 2 ) с гексафторидом платины (PtF 6 ): [6]
- O 2 + PtF 6 → [O
2]+
[PtF
6]-
Соединение также может быть получено из смеси газов фтора и кислорода в присутствии платиновой губки при 450 ° C и из дифторида кислорода ( OF
2) выше 400 ° C: [6]
- 6 ИЗ
2 + 2 Pt → 2 [O
2] [PtF
6] + O
2
При более низких температурах (около 350 ° C) вместо диоксигенилгексафтороплатината образуется тетрафторид платины . [6] Диоксигенилгексафтороплатинат сыграл ключевую роль в открытии соединений благородных газов . Наблюдение за тем, что PtF 6 является достаточно мощным окислителем для окисления O 2 (который имеет первый потенциал ионизации 12,2 эВ ), привело Бартлетта к выводу, что он также должен быть способен окислять ксенон (первый потенциал ионизации 12,13 эВ). Его последующее исследование дало первое соединение благородного газа , гексафтороплатината ксенона . [7]
О+
2также встречается в подобных соединениях формы O 2 MF 6 , где M - мышьяк (As), сурьма (Sb), [8] золото (Au), [9] ниобий (Nb), рутений (Ru), рений ( Re), родий (Rh), [10] ванадий (V), [11] или фосфор (P). [12] Другие формы также засвидетельствованы, включая O 2 GeF 5 и (O 2 ) 2 SnF 6 . [11]
Тетрафторборатные и гексафторфосфатные соли могут быть получены реакцией дифторида кислорода с трифторидом бора или пентафторидом фосфора при -126 ° C: [12]
- 2 O 2 F 2 + 2 BF 3 → 2 O 2 BF 4 + F 2
- 2 O 2 F 2 + 2 PF 5 → 2 O 2 PF 6 + F 2
Эти соединения быстро разлагаются при комнатной температуре:
- 2 O 2 BF 4 → 2 O 2 + F 2 + 2 BF 3
- 2 O 2 PF 6 → 2 O 2 + F 2 + 2 PF 5
Некоторые соединения, включая O 2 Sn 2 F 9 , O 2 Sn 2 F 9 · 0,9HF, O 2 GeF 5 · HF и O 2 [Hg (HF)] 4 (SbF 6 ) 9, могут быть получены с помощью ультрафиолетового облучения кислорода. и фтор, растворенный в безводном фтористом водороде с оксидом металла. [13]
Реакции [ править ]
Реакция O 2 BF 4 с ксеноном при 173 K (-100 ° C) дает белое твердое вещество, которое, как полагают, является F – Xe – BF 2 , содержащим необычную связь ксенон-бор: [14]
- 2 O 2 BF 4 + 2 Xe → 2 O 2 + F 2 + 2 FXeBF 2
Диоксигенильные соли O 2 BF 4 и O 2 AsF 6 реагируют с монооксидом углерода с образованием оксалилфторида C 2 O 2 F 2 с высоким выходом. [15]
Ссылки [ править ]
- ^ Майкл Клагстон; Розалинд Флемминг (2000). Продвинутая химия , Oxford University Press, ISBN 0-19-914633-0 , ISBN 978-0-19-914633-8 , стр. 355.
- ^ Фут, Кристофер С .; Валентин, Джоан С. (1995). Активный кислород в химии . Джоэл Ф. Либман, А. Гринберг. Springer. ISBN 0-412-03441-7.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.п. 616
- ^ Коттон, Ф. Альберт ; Уилкинсон, Джеффри ; Мурильо, Карлос А .; Бохманн, Манфред (1999), Advanced Inorganic Chemistry (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Дж. Шамир; Дж. Биненбойм; Его Превосходительство Клаассен (1968). «Частота колебаний катиона O 2 + ». Варенье. Chem. Soc. 90 (22): 6223–6224. DOI : 10.1021 / ja01024a054 .
- ^ a b c Бартлетт, Нил ; Ломанн, Д.Х. (1962). "Фториды благородных металлов. Часть II. Диоксигенилгексафтороплатинат (V), [O
2]+
[PtF
6]-
.» . , J. Chem Soc. , 115 :. 5253-5261 DOI : 10.1039 / jr9620005253 . - ^ Бартлетт, Нил (1962). "Гексафтороплатинат ксенона (V), Xe+
[PtF
6]-
». Proc Chem Soc. , .. :. 197-236 DOI : 10.1039 / PS9620000197 . - ^ Янг, AR; Хирата, Т .; Морроу, С.И. (1964). «Получение диоксигенильных солей из дифторида кислорода». Варенье. Chem. Soc. 86 (1): 20–22. DOI : 10.1021 / ja01055a006 .
- Перейти ↑ Nakajima, Tsuyoshi (1995). Фтор-углеродные и фторид-углеродные материалы: химия, физика, приложения . CRC Press. ISBN 0-8247-9286-6.
- ^ Василе, Майкл Дж .; Фалконер, Уоррен Э. (1975). «Пароперенос диоксигенильных солей». J. Chem. Soc., Dalton Trans. 1975 (4): 316–318. DOI : 10.1039 / DT9750000316 .
- ^ a b Холлеман, Арнольд Ф .; Виберг, Эгон (2001). Неорганическая химия . Академическая пресса. п. 475. ISBN 0-12-352651-5.
- ^ a b Соломон, Ирвин Дж .; Брабец, Роберт I .; Уениши, Рой К .; Кейт, Джеймс Н .; Макдонаф, Джон М. (1964). «Новые диоксигенильные соединения». Неорг. Chem. 3 (3): 457. DOI : 10.1021 / ic50013a036 .
- ^ Мазей, Зоран; Горешник, Евгений (03.02.2020). «Синтез диоксигенильных солей фотохимическими реакциями в жидком безводном фтористом водороде: рентгеновские кристаллические структуры α- и β-O 2 Sn 2 F 9, O 2 Sn 2 F 9 · 0,9HF, O 2 GeF 5 · HF и O 2 [Hg (HF)] 4 (SbF 6) 9 дюймов . Неорганическая химия . 59 (3): 2092–2103. DOI : 10.1021 / acs.inorgchem.9b03518 . ISSN 0020-1669 .
- ^ Goetschel, CT; Лоос, KR (1972). «Реакция ксенона с диоксигенилтетрафторборатом. Получение FXe-BF 2 ». Журнал Американского химического общества . 94 (9): 3018–3021. DOI : 10.1021 / ja00764a022 .
- ^ Pernice, H .; Willner, H .; Eujen, R. (2001). «Реакция диоксигенильных солей с13
CO Образование F13
С (О)13
C (O) F». Журнал химии фтора . 112 (2):. 277-590 DOI : 10.1016 / S0022-1139 (01) 00512-7 .