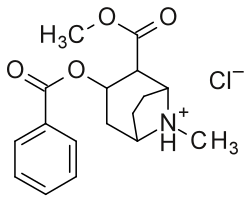
Это список аналогов кокаина . Аналог кокаина является (обычно) искусственная конструкция из нового химического соединения из (часто отправной точкой естественно) молекулярной структуры кокаина, в результате продукт достаточно похож на кокаин , чтобы показатель сходства, но переделки к, его химической функции. В рамках аналогичных соединений, созданных из структуры кокаина, так называемые «аналоги кокаина» сохраняют 3 β -бензоилокси или аналогичную функциональность (специально используемый термин обычно отличается от фенилтропанов, но в широком смысле, как категория, включает их) на тропановом скелете по сравнению с другими стимуляторами такого рода. Многие из полусинтетического кокаина аналогов собственно , которые были сделаны и изучено состояли из девяти среди следующих классов соединений: [а]
- стереоизомеры кокаина
- 3 -замещенные в β- фенильном кольце аналоги
- 2 β -замещенных аналога
- N- модифицированные аналоги кокаина
- 3 β- карбамоиловые аналоги
- 3 β -алкил-3-бензилтропаны
- 6/7-замещенные кокаины
- 6-алкил-3-бензилтропаны
- пиперидиновые гомологи кокаина
Ниже: альтернативная двумерная молекулярная диаграмма кокаина; показан конкретно как протонированный , NH +, гидрохлорид , и без учета трехмерной стереохимии
Однако строгие аналоги кокаина также могут включать такие другие потенциальные комбинации, как фенацилтропаны и другие углеродные разветвленные заместители, не перечисленные выше. Этот термин может также свободно использоваться для обозначения наркотиков, изготовленных из кокаина или имеющих в своей основе полный синтез кокаина, но модифицированных для изменения их действия и QSAR . К ним относятся как анестетики-блокаторы внутриклеточных натриевых каналов, так и лиганды, стимулирующие обратный захват дофамина (такие как некоторые, а именно, пиперидины , связанные с тропановым мостиком и вырезанные из них.). Кроме того, исследователи поддержали комбинаторные подходы к взятию наиболее многообещающих аналогов, выясненных в настоящее время, и их смешиванию с целью открытия новых и эффективных соединений для оптимизации их использования для различных конкретных целей. [b]

Хотя карбметокси обозначен в его функции как водородная связь на этом изображении, было обнаружено, что в первую очередь электростатические факторы доминируют над связыванием в этом пространстве площади молекулярной поверхности над действующим принципом водородной связи. [c]
Аналоги sensu stricto [ править ]
Стереоизомеры кокаина [ править ]
| Стереоизомер | Буквенно-цифровое присвоение С. Сингха | IC 50 ( нМ ) [ 3 H] WIN 3542 ингибирование мембран полосатого тела крысы Средняя стандартная ошибка ≤5% во всех случаях | Номенклатура ИЮПАК |
|---|---|---|---|
| R- кокаин ( эритроксилин ) | - | 102 | метил (1R, 2R, 3S, 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| R -псевдокаин (Делькаин, Депсокаин, Декстрокаин, Изококаин, Псикаин. [2] ) | 172 | 15800 | метил (1R, 2S , 3S, 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| R -аллококаин | 173 | 6160 | метил (1R, 2R, 3R , 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| R -аллопсевдокаин | 174 | 28500 | метил (1R, 2S , 3R , 5S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксилат |
| S- кокаин | 175 | 15800 | метил (1S, 3R, 4R, 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан- 4- карбоксилат |
| S- псевдокаин | 176 | 22500 | метил (1S, 3R, 4S , 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан- 4- карбоксилат |
| S -аллококаин | 177 | 9820 | метил (1S, 3S , 4R, 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан- 4- карбоксилат |
| S -аллопсевдокаин | 178 | 67700 | метил (1S, 3S , 4S , 5R) -3- (бензоил) окси-8-метил-8-азабицикло [3.2.1] октан- 4- карбоксилат |
Если 2D-диаграммы, приведенные для структурных аналогов ниже, не указывают на стереохимию, следует предполагать, что они имеют общую конформацию R- кокаина, если не указано иное.
Естественная изомерия кокаина нестабильна по нескольким причинам, помимо высокой степени лабильности ; например: C2-карбометокси в своем конечном продукте биосинтеза сохраняет аксиальное положение, которое может подвергаться эпимеризации через омыление, чтобы получить первый в экваториальном положении.
Для создания следующих аналогов кокаина традиционно требовалась стадия, на которой 2-CMT использовался в качестве промежуточного молекулярного продукта.
Замещения при расщеплении бензоильной ветви (за исключением исчерпывающей фенильной группы) [ править ]
| Салицилметилэкгонин [3] | Метильваниллилекгонин [4] |
NB Fries продукт перегруппировки аспирина, используемый для получения сальбутамола . Однако в данном случае это относится к предшественнику, поскольку мигрированная ацетильная группа может быть предметом галоформной реакции . Однако более прямой путь к ванилиновой кислоте - это просто окисление ванилина до функционализированной бензойной кислоты .
Замены бензольного кольца арена во 2 ', 3', 4 '(5' и 6 ') положениях ( арил ) [ править ]
пара- замещенные бензоилметилэкгонины [ править ]
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | 4 ′ = R | DAT [ 3 H] ВЫИГРАТЬ 35428 | 5-HTT [ 3 H] Пароксетин | СЕТЬ [ 3 H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
| (кокаин) | ЧАС | 249 ± 37 | 615 ± 120 | 2500 ± 70 | 2,5 | 10.0 | |
| не-бензоилокси аналог сравнительных лиганды не-тропан аналог сравнительных лиганды | 11b (WIN 35428) (низоксетин) (флуоксетин) | F - - | 24 ± 4 775 ± 20 5200 ± 1270 | 690 ± 14 762 ± 90 15 ± 3 | 258 ± 40 135 ± 21 963 ± 158 | 28,7 1,0 0,003 | 10,7 0,2 0,2 |
| 183a | я | 2522 ± 4 | 1052 ± 23 | 18458 ± 1073 | 0,4 | 7.3 | |
| 183b | Ph | 486 ± 63 | - | - | - | - | |
| 183c | OAc | 144 ± 2 | - | - | - | - | |
| 183d | ОЙ | 158 ± 8 | 3104 ± 148 | 601 ± 11 | 19,6 | 3.8 | |
| ( 4'-Фторокаин ) [5] | F | - | - | - | - | - | |
| ( метиловый эфир пара- изотиоцианатобензоилэкгонина ) [6] ( пара- Isococ) | NCS | - | - | - | - | - |
МАТ кармана связывания , аналогичной липофильного место на кокаин-подобных соединений, включая бензольного кольца, приблизительна до 9 Å в длину. Что лишь немного больше, чем само по себе фенильное кольцо. [f]
мета- замещенные бензоилметилэкгонины [ править ]
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | 3 ′ = R | DAT [ 3 H] ВЫИГРАТЬ 35428 | 5-HTT [ 3 H] Пароксетин | СЕТЬ [ 3 H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
| 184a | я | 325 ɑ | - | - | - | - | |
| 184b | ОЙ | 1183 ± 115 | 793 ± 33 | 3760 ± 589 | 0,7 | 3.2 | |
| 191 | O Bn | - | - | - | - | - | |
| ( м -Изокок) | NCS | - | - | - | - | - |
- ɑ Значение IC 50 для вытеснения [ 3 H] кокаина
орто- замещенные бензоилметилэкгонины [ править ]
Гидроксилированный аналог 2'-ОН продемонстрировал десятикратное увеличение эффективности по сравнению с кокаином. [час]
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | 2 ′ = R | DAT [ 3 H] ВЫИГРАТЬ 35428 | 5-HTT [ 3 H] Пароксетин | СЕТЬ [ 3 H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
| 185a | я | 350 ɑ | - | - | - | - | |
| 185b | F | 604 ± 67 | 1770 ± 309 | 1392 ± 173 | 2,9 | 2.3 | |
| 185c ( 2'-ацетоксикокаин ) [7] | OAc | 70 ± 1 | 219 ± 20 | 72 ± 9 | 3.1 | 1.0 | |
| 185d ( 2'-гидроксикокаин ) [3] | ОЙ | 25 ± 4 | 143 ± 21 | 48 ± 2 | 5,7 | 1.9 |
- ɑ Значение IC 50 для вытеснения [ 3 H] кокаина
многообразные бензоилоксифенильные замещения [ править ]
Множественные замены (замены замен; например, мета - и пара -) или многократно ("многократно") замещенные аналоги являются аналогами, в которых имеет место более одной модификации исходной молекулы (имеющей многочисленные промежуточные составляющие). Они создаются путем экстраполяции результатов взаимосвязи между структурой и деятельностью, которые часто удивляют. Это даже обычный случай, когда две отдельные замены могут каждая давать более слабое, более низкое сродство или даже полностью неэффективное соединение соответственно; но из-за открытий, которые часто при совместном использовании такие два взаимно неполноценных изменения, добавляемые в тандеме к одному аналогу, могут привести к тому, что полученное производное будет проявлять гораздо большую эффективность, сродство, селективность и / или силу, чем даже исходное соединение; что в противном случае было бы скомпрометировано любым из этих двух изменений, сделанных отдельно.
Для описания и ссылки на этот механизм обратите внимание на то, что опиоид оксикодон, полученный из кодеина, в 1,5-1,7 раза больше обезболивающего действия морфина (опиоид, по отношению к которому кодеин, по сравнению с ним, только на 8-12%, или 0,17 его сила у крыс); однако промежуточными продуктами оксикодона в его синтезе из кодеина являются: - эффективность кодеина ( т.е. кодеинона); 0,13 морфина ( т.е. 14-гидроксикодеина) у крыс и меньше у мышей (для иллюстрации: первое даже меньше 0,17 морфина, как у кодеина); причем конечное возможное отдельное промежуточное соединение между кодеином и оксикодоном ( то есть 7,8-дигидрокодеин) составляет не более 150-200% от количества кодеина. [8]
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | орто -2 ′ = R | мета -3 ′ = R | пара -4 ′ = R | DAT [ 3 H] ВЫИГРАТЬ 35428 | 5-HTT [ 3 H] Пароксетин | СЕТЬ [ 3 H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|---|---|
| 186 | HO | ЧАС | я | 215 ± 19 | 195 ± 10 | 1021 ± 75 | 0,9 | 4,7 | |
| ( Ваниллилметилэкгонин ) [4] | ЧАС | ОСН 3 | ОЙ | - | - | - | - | - |
бензоил фенил-альтерации [ править ]
Аналоги нафталина позволяют для дальнейших числовых замен, в том числе восьми позиций пери замещенных структур. Возможны многие другие изменения, создающие различные ароматические кольца .
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | C = R | DAT [ 3 H] Кокаин (IC 50 ) | 5-HTT [ 3 H] Пароксетин | СЕТЬ [ 3 H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
| 187 | 1-нафталин | 742 ± 48 | - | - | - | - | |
| 188 | 2-нафталин | 327 ± 63 | - | - | - | - |
Модификации бензоильной ветви [ править ]
- Бензоилтиометилэкгонин [10]
Сера вместо кислорода в простой связи бензоилового эфира приводит к более низкой электроотрицательности, чем у кокаина.
Водород с C1-тропановым кольцом - замещения [ править ]
ср. гидрокситропакокаин для природного алкалоида (без карбметокси в положении 2), который является заместителем C1 с гидроксигруппой .
| Структура | Банальное имя | R (фрагмент C1) | K i ( нМ ) @ DAT | K i ( нМ ) @ SERT | K i ( нМ ) @ NET | σ 1 сродство K i | σ 2 сродство K i | IC 50 (мкМ) ингибирование Na + ( приток натриевых каналов в нейронах неокортекса, стимулированный вертридином) c | LogP (алгоритм XLogP3, Ченг и др., 2007) |
|---|---|---|---|---|---|---|---|---|---|
| (-)-Кокаин | ЧАС | 326 ± 106 | 513 ± 143 | 358 ± 69 | 6,7 ± 0,3 мкМ d [13] | "значительный" [14] | 6,99 ± 2,43 | 2.30 | |
| (-) - 1-метил-кокаин | Мне | 163 ± 23 | 435 ± 77 | 488 ± 101 | "неоценимый" | 1,13 мкМ | 16,01 ± 1,90 | 2,67 | |
| (-) - 1-этил-кокаин | Et | 95,1 ± 17,0 ɑ | 1,106 ± 112 | 598 ± 179 | - | - | - | 3.20 | |
| (-) - 1-н-пропил-кокаин | n -Pr | 871 ± 205 ɑ | 2 949 ± 462 б | 796 ± 195 | - | - | - | 3,56 | |
| (-) - 1-н-пентил-кокаин | н -С 5 Н 11 | 1,272 ± 199 млрд | 1,866 ± 400 ɑ | 1,596 ± 21 б | - | - | - | 4,64 | |
| (-) - 1-фенил-кокаин | Ph | 32,3 ± 5,7 б | 974 ± 308 | 1,980 ± 99 б | 524 нМ | 198 нМ | 0,29 ± 0,07 | 3,77 |
- ɑ , P <0,05 по сравнению с (-) - кокаином (односторонний ANOVA с последующим тестом множественных сравнений Даннета)
- b , P <0,01 по сравнению с (-) - кокаином (односторонний ANOVA с последующим тестом множественных сравнений Даннета)
- c Было обнаружено, что лидокаин имеет значение 39,6 ± 2,4, самое слабое из всех протестированных.
- d В той же ссылке указано 25,9 ± 2,4 мкМ для (+) - кокаина и 13,6 ± 1,3 мкМ для норкокаина. Для сравнения он дает 12,7 ± 1,5 мкМ для сигмаергического сродства (+) - амфетамина. Другая ссылка дает 1,7-6,7 мкМ для (-) - кокаина. Все значения K i . [15]
- Используя тот же набор данных, что и в таблице выше, было обнаружено, что следующие соединения сравниваются как:
- ЦФТ @ DAT = 39,2 ± 7,1 (n = 5)
- флуоксетин @ SERT = 27,3 ± 9,2 (n = 3)
- дезипрамин @ NET = 2,74 ± 0,59 (n = 3)
Аналоги кокаина, замещающие положение C1-тропанового кольца, требующие сульфиниминовой ( N -сульфинилиминовой) химии (до внедрения которой были несостоятельны), которые связываются в отличие от типичной конфигурации в DAT (открытое для наружного) как кокаин (с его концом D79- Y156 с расстоянием 6,03 Å), или в атипичной (закрытой для выхода) конформации бензтропинов (3,29 Å). Хотя они ближе к открытому к наружному: (-) - 1-метил-кокаин = 4,40 Å и (-) - 1-фенил-кокаин = 4,89 Å и демонстрируют предпочтительное взаимодействие с обращенной наружу конформацией DAT, они, по-видимому, не имеют поведенческой стимуляции как закрытого типа. Несмотря на нестимулирующие поведенческие профили, у них все же есть антидепрессивный поведенческий профиль. [12]
С1-фенильный аналог в десять раз сильнее кокаина в качестве лиганда обратного захвата дофамина и в двадцать четыре раза сильнее в качестве местного анестетика (потенциал-зависимый блокатор Na + -каналов), тогда как метильный аналог C1 в 2,3 раза менее эффективен в качестве местного анестетика. [12]
2 β -замены (включая замену метаболита переэтерификации кокаэтиленом) [ править ]
Учет того, что большие и громоздкие заместители C2 будут изменять тропан, искажая пиперидиновую кольцевую часть его скелета в достаточной степени, чтобы ухудшить его функциональность, или что в указанном случае это будет препятствовать связыванию, в частности на 8-аза-конце, чтобы ослабить стерическое напряжение переходя к своему месту из положения 2, [l] во многих случаях кажется необоснованным. [м] (примеры показаны в таблице изображений ниже)
Соединение 197b показало увеличенную в 1131 раз селективность по аффинности по сравнению с переносчиком серотонина с лишь незначительным снижением активности переносчиков дофамина и норэпинефрина. [n] В то время как 197c имел 469- кратное увеличение SERT , с большей аффинностью к DAT, чем кокаин, и был приблизительно равным NET . [o] 197b был в 137 раз, а 196c - в 27 раз менее активным при связывании с переносчиком серотонина, но оба имели отношение NET / DAT, которое давало лучший дофаминергический препарат, чем кокаин. [п]
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | р | DAT [ 3 H] ВЫИГРАТЬ 35428 | 5-HTT [ 3 H] Пароксетин | СЕТЬ [ 3 H] Низоксетин | Селективность 5-HTT / DAT | Селективность NET / DAT |
|---|---|---|---|---|---|---|---|
| (Кокаин) | Мне | 89 ± 4,8 | 1045 ± 89 | 3298 ± 293 | 11,7 | 37,0 | |
| 196a ( кокаэтилен ) | Et | 195 ± 45 | 5801 ± 493 | 10000 ± 751 | 29,7 | 51,3 | |
| 196b | n -Pr | 196 ± 46 | 4517 ± 430 | 6124 ± 262 | 23,3 | 31,2 | |
| 196c | i -Pr | 219 ± 48 | 25224 ± 1498 | 30384 ± 1685 | 115 | 139 | |
| 196d | Ph | 112 ± 31 | 33666 ± 3330 | 31024 ± 1909 | 300 | 277 | |
| 196e | Млрд | 257 ± 14 | 302 ± 23 | 20794 ± 950 | 1.2 | 80,9 | |
| 196f | β-фенэтил | 181 ± 10 | 615 ± 52 | 19944 ± 1026 | 3,4 | 110 | |
| 196 г | γ-фенилпропил | 147 ± 19 | 374 ± 15 | 4893 ± 344 | 2,5 | 33,3 | |
| 196ч | циннамил | 371 ± 15 | 368 ± 6,3 | 68931 ± 3476 | 1.0 | 186 | |
| 196i | п- NO 2 -β-фенэтил | 601 ± 28 | - | - | - | - | |
| 196j | п- Cl-β-фенэтил | 271 ± 12 | - | - | - | - | |
| 196 тыс. | п- NH 2 -β-фенэтил | 72 ± 7 | - | - | - | - | |
| 196л | р - NCS- β-фенэтил | 196 ± 14 | - | - | - | - | |
| 196 кв.м. | п - азидо- β-фенэтил | 227 ± 19 | - | - | - | - | |
| 196н | ( p -NHCOCH 2 Br) β-фенэтил | 61 ± 6 | - | - | - | - | |
| 196o | ( п- NHCO (CH 2 ) 2 CO 2 Et) β-фенэтил | 86 ± 4 | - | - | - | - | |
| 197a | NH 2 | 753 ± 41,3 | 13725 ± 1256 | 3981 ± 229 | 18,2 | 5,3 | |
| 197b | -NMe 2 | 127 ± 6,36 | 143713 ± 8854 | 7329 ± 158 | 1131 | 57,7 | |
| 197c | -N (OMe) мне | 60 ± 6,4 | 28162 ± 2565 | 3935 ± 266 | 469 | 65,6 | |
| 197d | -NHMe | 2424 ± 118 | 44798 ± 2105 | 4213 ± 206 | 18,5 | 1,7 | |
| 197e ( бензоилэкгонин ) | -ОЙ | 195000 | - | - | - | - | |
| 197f | HOCH 2 - | 561 ± 149 | - | - | - | - | |
| 197 г ( тропакокаин ) | ЧАС | 5180 ± 1160 | - | - | - | - |
Функциональные замены карбметоксиэфира в 2 положениях Bioisostere [ править ]
Бензоилэкгонин, то есть соединение 197e , (отличается от своего кокаинового родителя только деметилированием C2-карбметокси до карбокси) имеет крайнюю потерю активности (его приблизительное сродство составляет 195000 нМ), как показывают методики определения связывания in vitro. эффективность (при которой проникновение ГЭБ не влияет на этот вопрос, как это делают исследования in vivo ) и, как предполагается, возможно, связано с образованием цвиттериона . [р]
| Структура | Буквенно-цифровое присвоение С. Сингха (имя) | р | [ 3 H] Мазиндол | [ 3 H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | (ЧАС) | 580 ± 70 | 570 ± 180 | 1.0 | |
| 198a | ЧАС | 520 ± 40 | 260 ± 70 | 0,5 | |
| 198b | CO 2 Et (5'-карбоэтокси) | 120 ± 10 | 290 ± 40 | 2,4 | |
| 198c | BOC | 2230 ± 220 | 1820 ± 810 | 0,8 | |
| 198d | Ph | 2000 ± 640 | 2920 ± 1620 | 1.5 | |
| 198e | CH = CHCO 2 Me | 3600 ± 400 | 3590 ± 1180 | 1.0 |
| Структура | Буквенно-цифровое присвоение С. Сингха | р | [ 3 H] Мазиндол | [ 3 H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 199a | β (или R ) CO 2 Et | 710 ± 150 | 1060 ± 340 | 1.5 | |
| 199b | α (или S ) CO 2 Et | 5830 ± 630 | 8460 ± 620 | 1.4 |
| Структура | Буквенно-цифровое присвоение С. Сингха | р | [ 3 H] Мазиндол | [ 3 H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 200 | 880 ± 350 | 400 ± 140 | 0,4 |
Функциональные замещения карбметоксиэфира Vinylogous 2 в β- положениях [ править ]
201b и 201c демонстрируют значительно повышенную эффективность по сравнению с кокаином; тогда как 201a , 201d и 201e значительно меньше. Это предполагает, что акцептор водородной связи в положении 2 β не обязательно имеет исключительное значение для создания аналогов кокаина с более высоким связыванием.
| Структура | Буквенно-цифровое присвоение С. Сингха | р | [ 3 H] Мазиндол | [ 3 H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 201a | ЧАС | 1730 ± 550 | 1120 ± 390 | 0,6 | |
| 201b | Cl | 222 ± 49 | 368 ± 190 | 1.6 | |
| 201c | CO 2 Et | 50 ± 10 | 130 ± 10 | 2,6 | |
| 201d | CH = CHCO 2 Et | 1220 ± 100 | 870 ± 50 | 0,7 | |
| 201e | PO (OEt) 2 | 4850 ± 470 | 5500 ± 70 | 1.1 |
N- модификации [ править ]
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | № 8- R | [ 3 H] Связывание мазиндола | [ 3 H] Поглощение DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 217 (метиодид кокаина) | - | 10700 ± 1530 ɑ | - | - | |
| (Кокаин) | CH 3 | 280 ± 60 102 ɑ | 320 ± 10 | 1.1 | |
| 218 ( норкокаин ) | ЧАС | 303 ± 59 ɑ | - | - | |
| 219a | Млрд | 668 ± 67 ɑ | - | - | |
| 219b | Ac | 3370 ± 1080 ɑ | - | - | |
| 219c | СН 2 СН 2 ОН | 700 ± 100 | 1600 ± 200 | 2.3 | |
| 219d | СН 2 СО 2 СН 3 | 480 ± 40 | 1600 ± 100 | 3.3 | |
| 219e | CH 2 CO 2 H | 380 ± 20 | 2100 ± 400 | 5.5 | |
| 220а | SO 2 CH 3 ( Ms ) | 1290 ± 80 | 1970 ± 70 | 1.5 | |
| 220b | SO 2 CF 3 ( Tf ) | 330 ± 30 | 760 ± 20 | 2.3 | |
| 220c | SO 2 NCO | 120 ± 10 | 160 ± 10 | 1.3 | |
| 220d | SO 2 Ph | 20 800 ± 3500 | 61000 | 2,9 | |
| 220e | SO 2 С 6 Н 4 -4-NO 2 ( нозил ) | 5720 ± 1140 | 18 800 ± 90 | 3.3 | |
| 220f | SO 2 C 6 H 4 -4-OCH 3 | 6820 ± 580 | 16400 ± 1400 | 2,4 | |
| 221a | НЕТ | 99500 ± 12300 | 23 1700 ± 39 500 | 2.3 | |
| 221b | НЕТ 2 | 7500 ± 900 | 21200 ± 600 | 2,8 | |
| 221c | NHCOCH 3 | > 1000000 | > 1000000 | - | |
| 221d | NH 2 | - | - | - |
- ɑ IC 50 (нМ) для перемещения [ 3 H] WIN 35428
Мостиковые ( N- ограниченные / связанные) слитые с тропаном аналоги кокаина [ править ]
Тропановый мост с 8 на 2 позиции [ править ]
См. N -мостиковые фенилтропаны с передней и задней частью .
| Сложный | Буквенно-цифровое присвоение С. Сингха | р | [ 3 H] Мазиндол | [ 3 H] DA | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| 222 | 44900 ± 6200 | 115000 ± 15700 | 2,6 |
Аналоги кокаина с обратным мостиком считаются более близкими к непривязанным аналогам кокаина и производным фенилтропана (где неподеленная пара азота не является фиксированной или ограниченной ) и лучше имитирует их сродство. Это происходит из-за того, что когда восьмое положение углеродного тропана свободно вращается и не связано, оно предпочтительно занимает осевое положение, определяющее его наименьшее энергетическое и наиболее свободное состояние. В аналогах с передним мостиком жесткая фиксация неподеленных азотных пар заставляет их находиться в экваториальном положении для пиперидиновой кольцевой части тропанового ядра, указывая на мостик с двумя углеродными и тремя метиленовыми звеньями; отдавая засвидетельствованным передним мостом аналогам кокаина предпочтение SERT перед DAT. [y]
Аналоги трициклического кокаина [ править ]
Связывание азотного 8-тропанового положения на одну позицию дальше (за пределами 2 β и пересечение его / оставляя его открытым в виде водорода и, таким образом, возможно наличие дополнительных неограниченных замещений там) и полностью связывая 3 β арил, заменяя его; дает обширную структуру с передним мостиком для создания структурно трициклического ряда аналогов кокаина.
С 8 по 3 позицию [ править ]
первая структура (ди- хлор бензол, 2 & beta ; -CH 2 OCOMe) SERT = 1,6, DAT = 1870, NET = 638
вторая структуры ( п - Бром, мета - хлор, 2 β -CO 2 Me) SERT = 2.3, DAT = 5420, NET = 459
3-я структура ( пара- йод, мета- хлор, 2 β -CH 2 OCOPh) SERT = 0,06, DAT / NET оба => 10K
| Сложный | Икс | Y | р | SERT K i (нМ) | DAT K i (нМ) | NET K i (нМ) |
| 1 | Cl | Cl | CH 2 OCOMe | 1.6 | 1870 г. | 638 |
| 2 | Br | Cl | CO 2 Me | 2.3 | 5420 | 459 |
| 3 | я | Cl | CH 2 OCOPh | 0,06 | > 10 тыс. | > 10 тыс. |
Азаборнане сужение тропанового кольца [ править ]
Были внесены изменения, укорачивающие тропановую кольцевую систему с включением длины бензоилокси в C3, в отличие от азаборнановых фенилтропанов ; [17], вероятно, исправляет неглубокое проникновение (для хорошей эффективности) последнего.
5-бензоат (слева, внизу) и 6-бензоат (справа, внизу)
Сравнение тропанового кольца и норборнана в наложении, с контрастом бензоильной ветви в ее конфигурации в том, как она располагается вытянутой из тела любого основного типа кольца (показано дважды в разных цветах, для наглядности выше)
Метоксикокаин и аналоги метоксипсевдокаина в тропановом положении 6/7 [ править ]
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | Икс | K i (нМ) [ 3 H] Связывание мазиндола | K i (нМ) [ 3 H] DA поглощение | Селективность Поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | 280 ± 60 | 320 ± 10 | 1.1 | ||
| (Псевдокаин) | 10400 ± 300 | 13 800 ± 1500 | 1.3 | ||
| 225a | 2β, 6β-ОСН 3 | 98000 ± 12000 | 68000 ± 5000 | 0,7 | |
| 225b | 2α, 6β-ОСН 3 | 190000 ± 11000 | 510000 ± 110000 | 2,7 | |
| 225c | 2β, 7β-ОСН 3 | 4200 ± 100 | 6100 ± 200 | 1.4 | |
| 225d | 2α, 7β-ОСН 3 | 45000 ± 5000 | 110000 ± 4000 | 2,4 | |
| 225e | 2α, 7α-ОСН 3 | 54000 ± 3000 | 200000 ± 70000 | 3,7 |
3 β -положение 2 '- (6') и 2 аналога комбинации β- замещения [ править ]
| Сложный | Буквенно-цифровое присвоение С. Сингха | 2 β - R | C2′- R | IC 50 (нМ) (смещение [ 3 H] WIN 35428) |
|---|---|---|---|---|
| 211a | CO 2 OH | ЧАС | 6214 ± 1269 | |
| 211b | CH 2 OCOCH 3 | ЧАС | 2995 ± 223 | |
| 211c | КОНХЧ 3 | ЧАС | > 100000 | |
| 211d | CO 2 Et | ЧАС | 2031 ± 190 | |
| 211e | CO 2 - i -Pr | ЧАС | 1377 ± 10 | |
| 211f | CO 2 Ph | ЧАС | 2019 ± 253 | |
| 211 г | CO 2 CH 2 Ph | ЧАС | 4602 ± 325 | |
| 211ч | 3-фенил-1,2,4-оксадиазол | ЧАС | 3459 ± 60 | |
| 211i | CH = CH 2 | ЧАС | 2165 ± 253 | |
| 211j | Канал 2 Кан 3 | ЧАС | 2692 ± 486 | |
| 212 | CO 2 - i -Pr | HO | 663 ± 70 4507 ± 13 ɑ 34838 ± 796 б |
- ɑ Для замещения [ 3 H] пароксетина (5-HTT и NET)
- b Для замещения [ 3 H] низоксетина (5-HTT и NET)
3 β- карбамоиловые аналоги [ править ]
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | Икс | IC 50 (нМ) ингибирование связывания [ 3 H] кокаина (полосатая ткань крысы) | IC 50 (нМ) ингибирование поглощения [ 3 H] DA (полосатая ткань крысы) | Селективность поглощения / связывания |
|---|---|---|---|---|---|
| (Кокаин) | (ЧАС) | 70 ± 10 | 210 ± 70 | 3.0 | |
| 223a | ЧАС | 5600 ± 700 | 52600 ± 3000 | 9,4 | |
| 223b | 4-НЕТ 2 | 1090 ± 250 | 5700 ± 1200 | 5.2 | |
| 223c | 4-NH 2 | 63300 ± 12200 | > 100000 | - | |
| 223d | 4-N 3 | 1000 ± 240 | 1180 ± 360 | 1.2 | |
| 223e | 4-NCS | 260 ± 60 | 490 ± 80 | 1.9 | |
| 223f | 3-НЕТ 2 | 37 ± 10 | 178 ± 23 | 4.8 | |
| 223 г | 3-NH 2 | 2070 ± 340 | 23100 ± 900 | 11.1 | |
| 223ч | 3-N 3 | 630 ± 150 | 3900 ± 1590 | 6.2 | |
| 223i | 3-NCS | 960 ± 210 | 4900 ± 420 | 5.1 |
Замены фенильных 3-позиционных связей [ править ]
См .: Список фенилтропанов (многие фенилтропаны получают из метаболитов кокаина, таких как метилэкгонидин , в качестве предшественников . В то время как полностью синтетические методы были разработаны из исходного материала винилкарбеноидов и пирролов) [22]
Разница в длине бензоилокси и фенильной связи, в отличие от кокаина и фенилтропана, приводит к более короткому расстоянию между центроидом ароматического бензола и мостиковым азотом тропана в последних PT. Это расстояние составляет 5,6 Å для фенилтропанов и 7,7 Å для кокаина или аналогов с интактным бензоилокси. [ac] Это может объяснить повышенный профиль поведенческой стимуляции PT по сравнению с кокаином. [ad] Различия в связывающей способности также объяснялись с учетом сольватационных эффектов; кокаин, содержащий 2 β , 3 β-эфирные группы считаются более сольватированными, чем соединения типа WIN (например, тропарил). Более высокий p K ɑ азота тропана (8,65 для кокаина, 9,55 для тропарила и 11,95 для винилового аналога 43a ), пониженная водная сольватация и пониженная конформационная гибкость добавлены к увеличению сродства связывания. [ae]
Несмотря на наблюдаемое усиление стимуляции, у фенилтропанов отсутствует местный анестезирующий эффект блокирования натриевых каналов, который бензоилокси придает кокаину. Помимо местного воздействия, это придает кокаину сродство к связыванию с сайтами на натрийзависимых транспортных участках допамина и серотонина, которые отличаются и специфичны для MAT в отличие от общих натриевых каналов; создание отдельного механизма реляционной аффинности к переносчикам в дополнение к его ингибированию обратного захвата для этих переносчиков; это уникально для местного анестетика в кокаине и его аналогах с аналогичным заменителем бензоилокси, который оставляет нетронутой способность блокировать натриевые каналы.Преодоление таких соединений функционально по отношению к МАТ по сравнению с аналогами фенилтропана, у которых удален мостик местного анестетика.[23] (Требуется перекачка части ионов натрия из аксона через Na + / K + -АТФазу ). Кроме того, было даже постулировано, что решающая роль в отношении энергии электронов, передаваемых через сенсибилизацию напряжением (и, следовательно,блокирование потенциала действия с помощью молекулы, способной пересекать ее специфический канал, в случае кокаина - натриевый канал , который потенциально служит для восстановления -количественное определение его заряда) на сайте связывания рецептора может ослабить опосредующее влияние ингибирующей регуляции, которую играют ауторецепторы, замедляя высвобождение нейротрансмиттера при оттокесоздается в результате агонизма соединения; позволяя этому оттоку продолжаться без попытки организма поддерживать гомеостаз, действуя так же быстро, как реагирующее на его конформационные изменения. [24]
3 β -алкилфенилтропан и 3 β -алкенильные аналоги [ править ]
Соединение 224e , аналог 3 β- стирола, имело самую высокую эффективность в своей группе. В то время как 224b и 224c показали наибольшую селективность, при этом 224b имел в десять раз большую эффективность в отношении переносчика дофамина, чем кокаин. [аф]
( т.е. соединение " 224e ")
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | п | IC 50 (нМ) [ 3 H] Связывание кокаина | IC 50 (нМ) [ 3 H] DA поглощение | Селективность поглощения / связывания |
|---|---|---|---|---|---|
| (Кокаин) | 101 ± 26 | 209 ± 20 | 2.1 | ||
| 224a | 1 | 885 ± 18 | 1020 ± 52 | 1.1 | |
| 224b | 2 | 9,9 ± 0,33 | 70,5 ± 1,0 | 7.1 | |
| 224c | 3 | 344 ± 12 | 2680 ± 190 | 7,8 | |
| 224d | 71,6 ± 0,7 | 138 ± 9 | 1.9 | ||
| 224e | 2,10 ± 0,04 | 5,88 ± 0,09 | 2,8 |
Аналоги 6-алкил-3-бензилтропана [ править ]
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя / номер WIN ) | р | K i (нМ) [ 3 H] WIN 35428 связывание | IC 50 (нМ) [ 3 H] DA поглощение | Селективность поглощение / связывание |
|---|---|---|---|---|---|
| (Кокаин) | 32 ± 5 338 ± 221 | 405 ± 91 405 ± 91 | 12,6 1,2 | ||
| 11a (WIN 35065-2) | 33 ± 17 314 ± 222 | 373 ± 10 | 11,3 | ||
| (-) - 229a | ЧАС | 33 ± 5 | 161 ± 100 | 4.9 | |
| 229a | ЧАС | 91 ± 10 | 94 ± 26 | 1.0 | |
| 229b | Мне | 211 ± 23 | - | - | |
| 229c | Et | 307 ± 28 | - | - | |
| 229d | n -Pr | 4180 ± 418 | - | - | |
| 229e | n -Bu | 8580 ± 249 | - | - | |
| 229f | Млрд | 3080 ± 277 | - | - | |
| (+) - 230а | ЧАС | 60 ± 6 | 208 ± 63 | 3.5 | |
| 230а | ЧАС | 108 ± 14 | 457 ± 104 | 4.2 | |
| 230b | Мне | 561 ± 64 | - | - | |
| 230c | Et | 1150 ± 135 | - | - | |
| 230d | n -Pr | 7240 ± 376 | - | - | |
| 230e | n -Bu | 19700 ± 350 | - | - | |
| 230f | Млрд | 7590 ± 53 | - | - | |
| 231b | Мне | 57 ± 5 | 107 ± 36 | 1.9 | |
| 231c | Et | 3110 ± 187 | - | - | |
| 231d | n -Pr | 5850 ± 702 | - | - | |
| 231f | Млрд | 1560 ± 63 | - | - | |
| 232b | Мне | 294 ± 29 | 532 ± 136 | 1,8 | |
| 232c | Et | 6210 ± 435 | - | - | |
| 232d | n -Pr | 57 300 ± 3440 | - | - | |
| 232f | Млрд | 3080 ± 277 | - | - | |
| 241 | Млрд | 4830 ± 434 | - | - |
| Подкатегория ( соединение № С. Сингха ) | а R = H | б R = Me | c R = Et | d R = n -Pr | е R = n -Bu | f R = Bn |
|---|---|---|---|---|---|---|
| 6α-изомеры: 237a — f | ||||||
| 6β-изомеры (экзо): 238a — f | ||||||
| Производные 3β-бензила: 239a — f | ||||||
| промежуточные сложные эфиры алкилидена: 240a-f | ||||||
NB , что 237A и 238а имеют такое же соединениекак оба родителя либо для серии с водородом насыщенного в их соответствующей замены места.
Прямой 2,3-пиримидино плавленый [ править ]
ниже: халькостробамин.
ср. стробамин (справа) для более эффективного соединения, как показано ниже.
| Структура | буквенно-цифровое присвоение | R 1 | R 2 | hDAT IC 50 (нМ) | hSERT IC 50 (нМ) | hNET IC 50 (нМ) |
|---|---|---|---|---|---|---|
| (-) - 3а | ЧАС | С 6 Н 5 | 58 300 (20 200) | 6140 (3350) | NA | |
| (+) - 3а | ЧАС | С 6 Н 5 | 48 700 (20 100) | 6030 (3400) | NA | |
| (-) - 3b | ЧАС | NH 2 | NA | NA | NA | |
| (+) - 3b | ЧАС | NH 2 | NA | NA | NA | |
| (-) - 3c | ЧАС | CH 3 | NA | NA | NA | |
| (+) - 3c | ЧАС | CH 3 | NA | NA | NA | |
| (-) - 3д | ЧАС | ЧАС | NA | NA | NA | |
| (+) - 3д | ЧАС | ЧАС | NA | NA | NA | |
| (+/—) - 3e | С 6 Н 5 | С 6 Н 5 | 30 000 (11 200) | 3650 (1700) | NA |
- « NA » = «нет сходства», например, не поддается количественному определению.
Прямые дигетеробензол (пиримидино) 2,3-конденсированные и, таким образом, жесткие аналоги кокаина. [27]
Кокаин-гомологи пиперидина [ править ]
ср. фенилтропан-пиперидин-гомологи для соединений с более оптимизированной конформацией, которые дают более высокое сродство при связывании с MAT.
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | 2 β -R | IC 50 (нМ) |
|---|---|---|---|
| (Кокаин) | CO 2 CH 3 ( т.е. CO 2 Me) | 249 ± 37 | |
| 183a | CO 2 CH 3 | 2522 ± 4 | |
| 242 | ЧАС | 11589 ± 4 | |
| 243 | CO 2 CH 3 | 8064 ± 4 |
Аналоги гаптена кокаина [ править ]
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | 2 β -R |
|---|---|---|
| 394 (GNC) ɑ | CO 2 (CH 2 ) 5 CO 2 H | |
| 395 (сукцинил норкокаин) [29] | CO 2 CH 3 | |
| GNE b [30], включая белки -носители : GNE-FLiC GNE-KLH GNE-BSA | ||
| 396 | CONH (CH 2 ) 5 CO 2 H |
- ɑ 6- (2R, 3S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбонилоксигексановая кислота
- b 6- (2R, 3S) -3- (бензоилокси) -8-метил-8-азабицикло [3.2.1] октан-2-карбоксамидогексановая кислота
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | р |
|---|---|---|
| 401a | CH 3 | |
| 401b | (CH 2 ) 5 CO 2 H | |
| 401c | CH 2 CO 2 H | |
| 401d | COCH 2 CH 2 CO 2 H | |
| 401e | ЧАС | |
| 401f | CH 2 CH 2 Br | |
| 385 г | (CH 2 ) 2 NHCO (CH 2 ) 2 CONH 2 | |
| 402a | O (CH 2 ) 4 NHCO (CH 2 ) 2 CO 2 ... 2,3-дигидро-1H-изоиндол-1,3-дион | |
| 402b | ОЙ | |
| 402c | O (CH 2 ) 2 ... 1,4-ксилол ... NH 2 | |
| 402d | NH (CH 2 ) 5 CO 2 H | |
| 402e | O (CH 2 ) 4 NHCO (CH 2 ) 2 CONH 2 | |
| 403a | NH 2 | |
| 403b | NHCOCH 2 Br | |
| 403c | NHCO (CH 2 ) 3 CO 2 H | |
| 403d | (CH 2 ) 3 NHCO (CH 2 ) 2 CONH 2 |
Кокаиновые гаптены, которые создают каталитические антитела, требуют переходных состояний, как это происходит в естественных условиях . [31] [32]
| Сложный | Имя |
|---|---|
| K1-KLH / BSA [34] | |
| K2-KLH / BSA |
Структурные / функциональные промежуточные аналоги [ править ]
Аналоги пиперидина [ править ]
- JZ-IV-10 (« гибрид модафинила » с нокаином. [35] см. Список аналогов модафинила )
- Нокаин
Отчасти недавний случай в предварительном современном фольклоре, который прошел через круговорот слухов, в основном связанных с университетами и мелочами популярной культуры, заключался в том, что кокаин - это один элемент, или увеличение веса молекулы, или увеличение заряда и т. Д., От молекулярной структуры сахар. [36] Хотя такое утверждение является ложным , как общее предлогом, есть декстрозы на основе супер-структура , которая имеет неопределенно подобную накладку с кокаином , который является «бензоил- бета - D -гликозид.»
- Бензоил- бета - D- глюкозид
Аналоги бензтропина (3α-дифенилметокситропан) [ править ]
- Бензатропин (БЗТ) [37]
- Дифторпин (O-620), более селективный как DARI, чем кокаин. Также антихолинергическое и антигистаминное средство.
- AHN 1-055 Структура такая же, как у бензтропина, но с 4 ', 4'-бисфторированием.
- GA 103 N-фенилпропилбис-4-фторбензтропин.
- JHW 007 [38] N- (н-бутил) -3α- [бис (4′-фторфенил) метокси] -тропан.
В отличие от кокаина и фенилтропанов, бензтропины и соединения GBR (и, как исключение для самого кокаинового фармакофора, аллотропакокаин ) среди прочих считаются «атипичными» лигандами насоса обратного захвата DAT, поскольку они стабилизируют переносчик дофамина в обращенном внутрь или закрытом - внешняя конформация, это контрастирует с тем, что считается «кокаиноподобным» сродством к DAT; что вместо этого сохранит DAT стабильным в конформации open-to-out. Это означает, что связывание многих ингибиторов обратного захвата дофамина нетипично для метода связывания кокаина с DAT и значительно отличается от него. [39]
«Дифторпин» не является фенилтропаном, но фактически принадлежит к семейству бензатропина DRI. Не путать с «диарил» -фенилтропанами .
В некоторых отношениях они важны, потому что они разделяют SAR, совпадающие с GBR 12909 и родственными аналогами.
SAR показали, что 4 ', 4'-дифторирование - отличный способ повысить DAT-активность бензтропина и дает отличную селективность по SERT и NET. [40] [41]
Кроме того, замена N-Me, например, на н-фенилпропил помогает снизить мускариновую активность до уровня, аналогичного сродству DRI. [40]
Это замечательно, учитывая, что немодифицированный (нативный) бензтропин в 60 раз более активен как холинолитик, чем как допаминергическое средство. [40]
Помимо рассмотрения рецептора M1, аналоги этого класса бензтропина по-прежнему не заменяют кокаин и не имеют склонности к повышению двигательной активности.
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | р | Р' | K i (нМ) [ 3 H] WIN 35428 связывание | IC 50 (нМ) [ 3 H] DA поглощение | Селективность поглощение / связывание |
|---|---|---|---|---|---|---|
| (Кокаин) | 388 ± 47 | - | - | |||
| (12909 ГБР) | 11,6 ± 31 | - | - | |||
| (Бензтропин) | ЧАС | ЧАС | 118 ± 9 | 403 ± 115 | 3,4 | |
| 249a | 4′-F | ЧАС | 32,2 ± 10 | 48 | 1.5 | |
| 249b (AHN 1-055) | 4′-F | 4′-F | 11,8 ± 1 | 71 | 6.0 | |
| 249c | 3 ', 4'-ди-F | ЧАС | 27,9 ± 11 | 181 ± 45,7 | 6.5 | |
| 249d | 4′-Cl | ЧАС | 30,0 ± 12 | 115 | 3.8 | |
| 249e | 4′-Cl | 4′-Cl | 20,0 ± 14 | 75 | 3.8 | |
| 249f | 3 ', 4'-ди-Cl | ЧАС | 21,1 ± 19 | 47 | 2.2 | |
| 249 г | 3 ', 4'-ди-Cl | F | 18,9 ± 14 | 24 | 1.3 | |
| 249ч | 4′-Br | ЧАС | 37,9 ± 7 | 29 | 0,8 | |
| 249i | 4′-Br | 4′-Br | 91,6 | 34 | 0,4 | |
| 249j | 4'-NO 2 | ЧАС | 197 ± 8 | 219 | 1.1 | |
| 249 тыс. | 4'-CN | ЧАС | 196 ± 9 | 222 | 1.1 | |
| 249л | 4′-CF 3 | ЧАС | 635 ± 10 | 2155 | 3,4 | |
| 249 кв.м. | 4'-ОН | ЧАС | 297 ± 13 | 677 | 2.3 | |
| 249n | 4'-OMe | ЧАС | 78,4 ± 8 | 468 | 6.0 | |
| 249o | 4'-OMe | 4'-OMe | 2000 ± 7 | 2876 | 1.4 | |
| 249p | 4'-я | ЧАС | 187 ± 5 | 512 | 2,7 | |
| 249q | 4'-я | 4'-я | 420 ± 7 | 2536 | 6.0 | |
| 249р | 4′-Et | ЧАС | 520 ± 8 | 984 | 1.9 | |
| 249с | 4′- т- Бу | ЧАС | 1918 г. | 4456 | 2.3 | |
| 250a | 3′-F | ЧАС | 68,5 ± 12 | 250 ± 64,7 | 3,6 | |
| 250b | 3′-F | 3′-F | 47,4 ± 1 | 407 ± 63,9 | 8,6 | |
| 250c | 3′-Cl | ЧАС | 21,6 ± 7 | 228 ± 77,1 | 10,5 | |
| 250d | 3′-CF 3 | ЧАС | 187 ± 5 | 457 ± 72,0 | 2,4 | |
| 251a | 2′-F | ЧАС | 50,0 ± 12 | 140 ± 17,2 | 2,8 | |
| 251b | 2′-Cl | ЧАС | 228 ± 9 | 997 ± 109 | 4.4 | |
| 251c | 2'-я | ЧАС | 309 ± 6 | 1200 ± 1,64 | 3.9 | |
| 251d | 2'-NH 2 | ЧАС | 840 ± 8 | 373 ± 117 | 0,4 |
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | р | Р' | IC 50 (нМ) DAT (связывание [ 3 H] WIN 35428) | IC 50 (нМ) 5-HTT (связывание [ 3 H] циталопрама) | Селективность 5-HTT / DAT |
|---|---|---|---|---|---|---|
| (бензтропин) | 312 ± 1,1 | 24100 ± 14800 | 77,2 | |||
| (ВЫИГРАТЬ 35428) | 12,9 ± 1,1 | 160 ± 20 | 12,4 | |||
| R- 256 | 2040 ± 283 | 1460 ± 255 | 0,7 | |||
| S- 257a | ЧАС | ЧАС | 33,5 ± 4,5 | 10100 ± 1740 | 301 | |
| С- 257b | ЧАС | F | 13,2 ± 1,9 | 4930 ± 1200 | 373 | |
| S- 257c (дифторпин) | F | F | 10,9 ± 1,2 | 3530 ± 1480 | 324 | |
| S -257d | ЧАС | Cl | 15,8 ± 0,95 | 5960 ± 467 | 377 | |
| S -257e | Cl | Cl | 91,4 ± 0,85 | 3360 ± 1480 | 36,8 | |
| S -257f | ЧАС | Br | 24,0 ± 4,6 | 5770 ± 493 | 240 | |
| S -257 г | Br | Br | 72,0 ± 3,65 | 2430 ± 339 | 33,7 | |
| S -257ч | ЧАС | я | 55,9 ± 10,3 | 9280 ± 1640 | 166 | |
| S -257i | Br | я | 389 ± 29,4 | 4930 ± 82 | 12,7 | |
| S -257j | я | я | 909 ± 79 | 8550 ± 442 | 9,4 | |
| S -257 тыс. | ЧАС | Мне | 49,5 ± 6,0 | 13200 | 266 | |
| S -257л | Мне | Мне | 240 ± 18,4 | 9800 ± 2680 | 40,8 |
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | р | п | IC 50 (нМ) DAT (связывание [ 3 H] WIN 35428) | IC 50 (нМ) 5-HTT (связывание [ 3 H] циталопрама) | Селективность 5-HTT / DAT |
|---|---|---|---|---|---|---|
| 258a | 20,3 ± 3,5 | - | - | |||
| 258b | ЧАС | 1 | 223 ± 53 | 4970 ± 700 | 22,3 | |
| 258c | ЧАС | 3 | 22,0 ± 11,9 | 19,7 ± 3 | 0,9 | |
| 258d | Br | 3 | 80,2 ± 8,8 | 234 ± 0,5 | 2,9 | |
| 258e | я | 3 | 119 ± 11 | 2200 ± 1250 | 18,5 | |
| 258f | ЧАС | 5 | 99,0 ± 28 | 550 ± 63 | 5.5 | |
| 259 | 616 ± 88 | 55200 ± 20000 | 89,3 |
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | р | K i (нМ) DAT (связывание [ 3 H] WIN 35428) | IC 50 (нМ) 5-HTT (поглощение [ 3 H] DA) | Селективность поглощения / связывания |
|---|---|---|---|---|---|
| 260 (AHN 2-003) | ЧАС | 11,2 ± 11 | 9,7 | 0,9 | |
| 261a | 3-фенилпропил | 41,9 ± 11 | 230 | 5.5 | |
| 261b | индол-3-этил | 44,6 ± 11 | 1200 | 26,9 | |
| 261c | 4-фенилбутил | 8,51 ± 14 | 39 | 4.6 | |
| 261d | 4- (4'-нитрофенил) бутил | 20,2 ± 11 | 650 | 32,2 | |
| 261e | 3- (4'-фторфенил) пропил | 60,7 ± 12 | - | - | |
| 262a | н- бутил | 24,6 ± 8 | 370 | 15.0 | |
| 262b | циклопропилметил | 32,4 ± 9 | 180 | 5.5 | |
| 262c | аллил | 29,9 ± 10 | 14 | 0,5 | |
| 262d | бензил | 82,2 ± 15 | 290 | 3.5 | |
| 262e | 4-фторбензил | 95,6 ± 10 | 200 | 2.1 | |
| 262f | циннанил | 86,4 ± 12 | 180 | 2.1 | |
| 262 г | [бис (4-фторфенил) метокси] этил | 634 ± 23 | - | - | |
| 262ч | [(4-нитрофенил) фенилметокси] этил | 57,0 ± 17 | - | - | |
| 263 | ацетил | 2340 | 4600 | 2.0 | |
| 264 | формил | 2020 ± 13 | 5400 | 2,7 | |
| 265a | Ц | 0% ɑ | - | - | |
| 265b | РС | 18% ɑ | - | - | |
| (AHN 2-005) [42] | СН 2 СН = СН 2 | - | - | - | |
| (JHW 007) [42] | CH 2 CH 2 CH 2 CH 3 | - | - | - | |
| (GA 2-99) [42] | СН 2 СН 2 NH 2 | - | - | - | |
| (GA 103) [42] | CH 2 CH 2 CH 2 CH 2 Ph | - | - | - | |
| 266 | 108 ± 12 | 130 | 1.2 |
ɑ Ингибирование при 10 мкМ
| Сложный | Буквенно-цифровое присвоение С. Сингха (имя) | IC 50 (нМ) DAT (связывание [ 3 H] WIN 35428) | IC 50 (нМ) 5-HTT (связывание [ 3 H] циталопрама) | |
|---|---|---|---|---|
| R / S -268 | 2β, 3β | > 10000 | > 1660 | |
| R / S -269 | 2α, 3β | 20300 | > 1660 | |
| R / S -270 | 2α, 3α | 22300 | > 1660 | |
| R / S -271 | 2β, 3α | 520 | > 1660 |
Аналоги изоксазолина тропанила [ править ]
Это единственное известное соединение, которое аллостерически модулирует SERT таким образом в условиях in vitro ( тианептинбыло показано, что он делает то же самое, но продемонстрировал свою эффективность только в образцах живых тканей in vivo ). Принимая во внимание его неконкурентное ингибирование переносчиков 5-HT, снижающих V max с небольшим изменением K m для серотонина, предположительно стабилизируя обращенную к цитоплазме конформацию SERT: в этом отношении считается, что он имеет профиль, противоположный профилю действия препарата против зависимости. ибогаин (за исключением функции, с помощью которой, как считается, опосредуются его антиаддиктивные свойства, т. е. блокировка никотиновых каналов α 3 β 4. см. 18-Метоксикорнаридиндля такой никотинергической активности без аналогичной аффинности SERT). [43]
Точно так же такие периферические соображения DAT (когда, как это часто бывает, считается конформационным, а не объясняется иным образом как электростатическое), могут составлять различие в сродстве через аллосертическую оккульсию между фенилтропаном циклопентилрутения в его отличии от трикарбонилхрома.
| Сложный | Имя | |||
|---|---|---|---|---|
| - | ||||
| 4а | 4c | 5а | 5c | |
| - | ||||
| 6а | 6b | 6c | 7а | |
| - | ||||
| 7b | 7c | 8а | 8b | |
| - | ||||
| 8c | 9а | 9b | 9c | |
| - | ||||
| 9c | 10а | 10b | 10c | |
| - | ||||
| 11а | 11b | 12а | 12b |
8-Аминопентацикло (лиганд σ-рецептора) Аналоги тришомокубана [ править ]
ср. другие тришомокубаны, такие как бистан .
Было показано, что агонисты сигма-рецепторов с наномолярным сродством, такие как CM156 , противодействуют пагубным эффектам кокаина при совместном введении с ним. Показательно, что, например, местный анестезирующий эффект на сигма-сайте, опосредующий токсичность, или иным образом перекрещивание или связывание отдельных функций кокаина снижает порог до его профиля безопасности. [45] Полициклические каркасные молекулы: N- замещенные 8-аминопентацикло [5.4.0.0 2,6 .0 3,10 .0 5,9 ] ундеканы (AHD) и родственные им. 3-FPh, 14b , имеет 1,2 ± 0,1 K i (нМ ± SEM) @ DAT. [46]
[[Файл: (1R, 2S, 3S, 5S, 6S, 7R, 8R, 9S, 10S) -N - ((3-фторфенил) метил) -N-метилпентацикло (5.4.0.0 2,6 .0 3,10 .0 5,9 ) ундекан-8-амин.png]]
Аналоги бициклических аминов [ править ]
- EXP-561
Аналоги хинуклидина [ править ]
- Бутилтолилхинуклидин
Дигидроимидазолы [ править ]
См .: Список аналогов Мазиндола
Мазиндол обычно считают непривычным (у людей и некоторых других млекопитающих, но он привыкает, например, к гончим [ar] ) тетрациклическим ингибитором обратного захвата дофамина (несколько ошибочная классификация в первом случае).
Это слабофункциональный аналог, используемый в исследованиях кокаина; в значительной степени из-за того, что N- этилмалеимид способен ингибировать приблизительно 95% специфического связывания [ 3 H] мазиндола с остатками сайта (-ов) связывания MAT, однако указанный эффект 10 мМ N- этилмалеимида был предотвращен в его Совокупность всего на 10 мкм М кокаина. В то время как ни 300 мкм M допамина или D -amphetamine получали достаточную защиту , чтобы противопоставить эффективности кокаина. [as] Вышеупомянутые шаги в его синтезе показывают сходство его предшественников с ингибитором обратного захвата MAT пипрадролом и родственными соединениями.
Местные анестетики (обычно не стимуляторы ЦНС) [ править ]
В исследованиях на животных некоторые из местных анестетиков показали остаточные свойства ингибитора обратного захвата дофамина [48], хотя обычно не так легко доступны. Ожидается, что они будут более кардиотоксичными, чем фенилтропаны. Например, диметокаин оказывает стимулирующее действие на поведение (и поэтому не перечислен ниже), если его доза в 10 раз превышает количество кокаина. Диметокаин эквивалентен кокаину с точки зрения его анестетической эквивалентности. [48] Было показано, что «спасение» интралипида обращает вспять кардиотоксические эффекты блокаторов натриевых каналов и, предположительно, те эффекты, которые возникают при внутривенном введении кокаина.
| Имя | Другие распространенные имена |
|---|---|
| Амилокаин | Stovaine |
| Артикаин | Астракаин, Септанест, Септокаин, Ультракаин, Зоркаин |
| Бензокаин | |
| Бупивакаин | Marcaine, Sensorcaine, Vivacaine |
| Бутакаин | |
| Картикаин | |
| Хлоропрокаин | Несакаин |
| Цинхокаин / Дибукаин | Цинкаин, Цинчокаин, Нуперкаинал, Нуперкаин, Совкаин |
| Циклометикаин | Сурфакаин, Топокаин |
| Этидокаин | |
| Eucaine | α-эвкаин, β-эвкаин |
| Фомокаин [49] | |
| Фотокаин [49] | |
| Гексилкаин | Циклаин, Осмокаин |
| Левобупивакаин | Чирокаин |
| Лидокаин / Лигнокаин | Ксилокаин, Бетакаин е |
| Мепивакаин | Карбокаин, Полокаин |
| Меприлкаин / Оракаин | Эпирокаин |
| Метабутоксикаин | Примакаин |
| Фенакаин / Холокаин | |
| Пиперокаин | Метикаин |
| Прамокаин / Прамоксин | |
| Прилокаин | Citanest |
| Пропоксикаин / Равокаин | |
| Прокаин / Новокаин | Борокаин (прокаин борат), этокаин |
| Пропаракаин / Алкаин | |
| Хинизокаин | Диметизохин |
| Ризокаин | |
| Ропивакаин | Наропин |
| Тетракаин / Аметокаин | Понтокаин, Дикаин |
| Тримекаин | Месдикаин, Мезокаин, Месокаин |
См. Также [ править ]
Кокаин- N- оксид : гидрокситропакокаин : м- гидроксибензоилэкгонин :
- Алкалоиды коки, связанные с биосинтезом кокаина, включают: бензоилэкгонин, экгонидин, экгонин, гидрокситропакокаин, метилэкгонина циннамат, тропакокаин и труксиллин.
- Метаболиты кокаина (человека) , которые включают: бензоилэкгонин (BE), метиловый эфир экгонина (EME), экгонин, норкокаин, п- гидроксикокаин, м- гидроксикокаин, п- гидроксибензоилэкгонин ( p OHBE) и м- гидроксибензоилэкгонин.
- Допаминергические препараты
- Федеральный закон об аналогах
- Фармакофор
- Фармакопея
- Фармакокинетика
- Фармакодинамика
Общие аналоги прототипов D - RA :
- Замещенные амфетамины
- Замещенные катиноны
- Замещенные фенэтиламины
- Замещенные фенилморфолины
- Замещенные метилендиоксифенэтиламины
Примечания (включая конкретные места цитат из использованных ссылок) [ править ]
- ^ [1] ← Страница № 969 (45-я страница статьи) §III. ¶1. Финальная линия. Последнее предложение.
- ^ [1] ← Страница № 1,018 (94-я страница статьи) 2-й столбец, 2-й абзац.
- ^ [1] ← Страница № 940 (16-я страница статьи) под таблицей 8., выше §4
- ^ [1] ← Страница № 970 (46-я страница статьи) Таблица 27. Рисунок 29.
- ^ [1] ← Страница № 971 (47-я страница статьи) Рисунок 30. & Страница № 973 (49-я страница статьи) Таблица 28.
- ^ [1] ← Страница № 982 (58-я страница статьи)
- ^ [1] ← Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 973 (49-я страница статьи) Таблица 28
- ^ [1] ← Страница № 972 (48-я страница статьи) №2, строка 10.
- ^ [1] ← Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 973 (49-я страница статьи) Таблица 28
- ^ [1] ← Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 973 (49-я страница статьи) Таблица 28
- ^ [1] ← Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 971 (47-я страница статьи) Рисунок 30 & Страница № 973 (49-я страница статьи) Таблица 28
- ^ [1] ← Страница № 974 (50-я страница статьи) Первая (левая) колонка, третья ¶
- ^ [1] ← Страница № 937 (13-я страница статьи) Вторая (правая) колонка, первая ¶. Выше / перед §2
- ^ [1] ← Страница № 974 (50-я страница статьи) Финал ¶ (5-я), Вторая строка.
- ^ [1] ← Страница № 975 (51-я страница статьи) Первый ¶, первая строка.
- ^ [1] ← Страница № 975 (51-я страница статьи) Первая ¶, 4-я строка.
- ^ [1] ← Страница № 973 (49-я страница статьи) §C. & Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 976 (52-я страница статьи) Таблица 29.
- ^ [1] ← Страница № 974 (50-я страница статьи) Первая (левая) колонка, четвертая ¶
- ^ [1] ← Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ← Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ← Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ← Страница № 974 (50-я страница статьи) Рисунок 31 & Страница № 977 (53-я страница статьи) Таблица 30.
- ^ [1] ← Страница № 978 (54-я страница статьи) §D & Страница № 980 (56-я страница статьи) Рисунок 33 & Страница № 981 (57-я страница статьи) Таблица 32.
- ^ [1] ← Страница № 980 (56-я страница статьи) Схема 52.
- ^ [1] ← Страница № 963 (39-я страница статьи) 2-я (правая) колонка, 2-й абзац.
- ^ [1] ← Страница № 982 (58-я страница статьи) §G & Страница № 983 (59-я страница статьи) Рисунок 36 & Страница № 984 (60-я страница статьи) Таблица 35.
- ^ [1] ← Страница № 979 (55-я страница статьи) Таблица 31.
- ^ [1] ← Страница № 981 (57-я страница статьи) §E & Page № 982 (58-я страница статьи) Таблица 33.
- ^ [1] ← Страница № 970 (46-я страница статьи) §B, 10-я строка
- ^ [1] ← Страница № 971 (47-я страница статьи) 1-я, 10-я строка
- ^ [1] ← Страница № 949 (25-я страница статьи) 3-я, 20-я строка
- ^ [1] ← Страница № 982 (58-я страница статьи) 3-й, строки 2, 5 и 6.
- ^ [1] ← Страница № 982 (58-я страница статьи) §F, Таблица 34 и Рисунок 35.
- ^ [1] ← Страница № 984 (60-я страница статьи) §H, Рисунок 37 & Страница № 985 (61-я страница статьи) Таблица 36.
- ^ [1] ← Страница № 984 (60-я страница статьи) Схема 56.
- ^ [1] ← Страница № 986 (62-я страница статьи) §I, Таблица 37 и Схема 58
- ^ [1] ← Страница № 1,014 (90-я страница статьи) §VIII, A. Рисунок 59.
- ^ [1] ← Страница № 1,016 (92-я страница статьи) Рисунок 60.
- ^ [1] ← Страница № 987 (63-я страница статьи) §IV, Рисунок 39 & Страница № 988 (64-я страница статьи) Таблица 38.
- ^ [1] ← Страница № 987 (63-я страница статьи) Рисунок 40, Страница № 988 (64-я страница статьи) §B & Страница № 989 (65-я страница статьи) Таблица 39.
- ^ [1] ← Страница № 987 (63-я страница статьи) Рисунок 41, Страница № 989 (65-я страница статьи) §C & Страница № 990 (66-я страница статьи) Таблица 40.
- ^ [1] ← Страница № 988 (64-я страница статьи) Рисунок 42, Страница № 990 (66-я страница статьи) § 2 & Страница № 992 (68-я страница статьи) Таблица 41.
- ^ [1] ← Страница № 988 (64-я страница статьи) Рисунок 43, Страница № 992 (68-я страница статьи) § 3 и Таблица 42.
- ^ [1] ← Страница № 1,011 (87-я страница статьи) §VII (7) 1-й ¶.
- ^ [1] ← Страница № 969 (45 страница статьи) вторая (правая сторона) столбец второго ¶ .
Ссылки [ править ]
- ^ Б с д е е г ч я J к л м п о р Q R сек т у V ш х у г аа аЬ ас объявлением ае аф аг ах аи а ^ ак ал ам ао ап водн ар , как Singh, Satendra; и другие. (2000). «Химия, дизайн и взаимосвязь структура-активность антагонистов кокаина» (PDF) . Chem. Rev. 100 (3): 925–1024. DOI : 10.1021 / cr9700538 . PMID 11749256 .
- Перейти ↑ Watson-Williams, E (1925). «Псикаин: искусственный кокаин» . Br , J Med . 1 (3340): 11. DOI : 10.1136 / bmj.1.3340.11 . PMC 2196615 . PMID 20771843 .
- ^ а б Сингх, S; Басмаджян, ВП; Avor, К; Pouw, B; Сил, TW (1997). «Удобный синтез 2? - или 4? -Гидроксикокаина» . Синтетические коммуникации . 27 (22): 4003–4012. DOI : 10.1080 / 00397919708005923 .
et. эль-Мозельхи, TF; Avor, KS; Басмаджян, врач-терапевт (сентябрь 2001 г.). «2? -Замещенные аналоги кокаина: синтез и потенциал связывания переносчика дофамина». Archiv der Pharmazie (Weinheim) . 334 (8–9): 275–8. DOI : 10.1002 / 1521-4184 (200109) 334: 8/9 <275 :: АИД-ardp275> 3.0.co; 2-Б . PMID 11688137 .
et. Сил, TW; Avor, К; Сингх, S; Холл, N; Чан, HM; Басмаджян, Г.П. (1997). «2? -Замещение кокаина избирательно усиливает связывание переносчиков допамина и норэпинефрина». NeuroReport . 8 (16): 3571–5. DOI : 10.1097 / 00001756-199711100-00030 . PMID 9427328 . - ^ а б Смит, РМ; Покетт, Массачусетс; Смит, П.Дж. (1984). «Гидроксиметоксибензоилметилэкгонины: новые метаболиты кокаина из мочи человека». Журнал аналитической токсикологии . 8 (1): 29–34. DOI : 10.1093 / JAT / 8.1.29 . PMID 6708474 .
- ^ Gatley SJ, Ю. DW, Fowler JS, Макгрегор RR, Schlyer DJ, Dewey SL, Вольф П., Мартин T, Shea CE, Volkow ND (март 1994). «Исследования с дифференциально меченым [11C] кокаином, [11C] норкокаином, [11C] бензоилэкгонином и [11C] - и 4 '- [18F] фторококаином, чтобы выяснить, в какой степени метаболиты [11C] кокаина вносят вклад в ПЭТ-изображения мозг бабуина ". Журнал нейрохимии . 62 (3): 1154–62. DOI : 10.1046 / j.1471-4159.1994.62031154.x . PMID 8113802 .
- ^ Кэрролл, FI; Левин, AH; Boja, JW; Кухар, MJ (1992). «Рецептор кокаина: биохимическая характеристика и взаимосвязь между структурой и активностью аналогов кокаина на транспортере допамина». Журнал медицинской химии . 35 (6): 969–981. DOI : 10.1021 / jm00084a001 . PMID 1552510 .
- ^ Сил, TW; Avor, К; Сингх, S; Холл, N; Чан, HM; Басмаджян, Г.П. (1997). «2'-Замена кокаина избирательно усиливает связывание переносчиков дофамина и норэпинефрина». NeuroReport . 8 (16): 3571–5. DOI : 10.1097 / 00001756-199711100-00030 . PMID 9427328 .
- ^ Баккет, WR; Фаркухарсон, Мюриэль Э .; Хайнинг, CG (1964). «Обезболивающие свойства некоторых 14-замещенных производных кодеина и кодеинона». J. Pharm. Pharmacol . 16 (3): 174–182. DOI : 10.1111 / j.2042-7158.1964.tb07440.x . PMID 14163981 .
- ^ Сакамури, Сукумар; и другие. (2000). «Синтез новых аналогов спироциклического кокаина с использованием сочетания Сузуки». Буквы тетраэдра . 41 (13): 2055–2058. DOI : 10.1016 / S0040-4039 (00) 00113-1 .
- ^ Исомура, Шигеки; Хоффман, Тимоти З .; Виршинг, Питер; Джанда, Ким Д. (2002). «Бензоилтио-. Кокаин, замена аналога. Синтез, свойства и реакционная способность бензоилтиоэфира кокаина, обладающего абсолютной конфигурацией кокаина». Варенье. Chem. Soc . 124 (14): 3661–3668. DOI : 10.1021 / ja012376y . PMID 11929256 .
- ^ Дэвис, Франклин А .; Gaddiraju, Narendra V .; Тедду, Нареш; Hummel, Joshua R .; Kondaveeti, Sandeep K .; Здилла, Майкл Дж. (2012). «Энантиоселективный синтез аналогов кокаина C-1 с использованием сульфиниминов (N-сульфинилиминов)» . Журнал органической химии . 77 (5): 2345–2359. DOI : 10.1021 / jo202652f . ISSN 0022-3263 . PMID 22300308 .
- ^ a b c Рейт, MEA; Али, С .; Хашим, А .; Шейх, IS; Theddu, N .; Gaddiraju, NV; Mehrotra, S .; Schmitt, KC; Мюррей, TF; Sershen, H .; Унтервальд, EM; Дэвис, Ф.А. (2012). «Новые замещенные аналоги кокаина C-1 в отличие от кокаина или бензтропина» . Журнал фармакологии и экспериментальной терапии . 343 (2): 413–425. DOI : 10,1124 / jpet.112.193771 . ISSN 1521-0103 . PMC 3477221 . PMID 22895898 . Полная статья
- ^ Шарки, J; Глен, штат Калифорния; Вулф, S; Кухар, MJ (1988). «Связывание кокаина на сигма-рецепторах». Eur J Pharmacol . 149 (1–2): 171–4. DOI : 10.1016 / 0014-2999 (88) 90058-1 . PMID 2840298 .
- ^ Nuwayhid, Самер J .; Верлинг, Линда Л. (2006). «Рецепторы сигма2 (σ2) как мишень для действия кокаина в полосатом теле крысы». Европейский журнал фармакологии . 535 (1–3): 98–103. DOI : 10.1016 / j.ejphar.2005.12.077 . ISSN 0014-2999 . PMID 16480713 .
- ^ Участие рецептора сигма 1 в обусловленном кокаином предпочтении места: возможная зависимость от блокады захвата допамина Паскаль Ромье и др. Нейропсихофармакология (2002) 26 444-455.10.1038 / S0893-133X (01) 00391-8
- ^ Yoshihiro Hamaya, Hesham Abdelrazek, Гари Р. Стрихарца (2002). «A-854: Сравнительная эффективность в отношении импульсной блокады и кожной анальгезии традиционных и новых местных анестетиков» . Тезисы ежегодного собрания Американского общества анестезиологов .
... гидроксипропилбензоилэкгонин (HPBE) - единственное эффективное анальгетическое соединение в [Esterom].
CS1 maint: несколько имен: список авторов ( ссылка )[ постоянная мертвая ссылка ] - ^ a b c d e f g Патент США 6,479,509
- ^ Козиковский, AP; Simoni, D .; Роберти, М .; Ронданин, Р .; Wang, S .; Du, P .; Джонсон, К.М. (1999). «Синтез 8-окса аналогов норкокаина, обладающих интересной кокаиноподобной активностью». Письма по биоорганической и медицинской химии . 9 (13): 1831–1836. DOI : 10.1016 / S0960-894X (99) 00273-5 . PMID 10406650 .
- ^ Хоппинг, Александр (2000). «Новые конформационно ограниченные аналоги тропана за счет 6-эндо-триггерной радикальной циклизации и стилле-сцепления - переключение активности в отношении переносчика серотонина и / или норэпинефрина». Журнал медицинской химии . 43 (10): 2064–2071. DOI : 10.1021 / jm0001121 . PMID 10821718 .
- Перейти ↑ Zhang, Ao (2002). «Производные тиофена: новая серия мощных ингибиторов обратного захвата норэпинефрина и серотонина». Биоорганический . 12 (7): 993–995. DOI : 10.1016 / S0960-894X (02) 00103-8 . PMID 11909701 .
- Перейти ↑ Zhang, Ao (2002). "Дальнейшие исследования конформационно ограниченных аналогов трициклического тропана и их ингибирования поглощения на сайтах переносчиков моноаминов: синтез (Z) -9- (замещенный арилметилен) -7-азатрицикло [4.3.1.0 3,7] деканов как новый класс переносчиков серотонина Ингибиторы ». Журнал медицинской химии . 45 (9): 1930–1941. DOI : 10.1021 / jm0105373 . PMID 11960503 .
- ^ Дэвис, HM; Saikali, E; Секстон, Т; Чайлдерс, SR (1993). «Новые 2-замещенные аналоги кокаина: связывающие свойства на сайтах транспорта дофамина в полосатом теле крысы». Евро. J. Pharmacol . 244 (1): 93–7. DOI : 10.1016 / 0922-4106 (93) 90063-F . PMID 8420793 .
- ^ "Карта лекарств" веб-сайта Drugbank "," (DB00907) "для кокаина: определение десяти целей молекулы in vivo, включая сродство дофаминового / серотонинового натриевых каналов и сродство K-опиоидов" . Drugbank.ca . Проверено 9 марта 2010 года .
- ^ Сахлхольм, Кристоффер; Нильссон, Йоханна; Марчеллино, Даниэль; Fuxe, Kjell; Орхем, Питер (2012). «Чувствительность к напряжению и кинетика дезактивации гистаминовых H 3 и H 4 рецепторов» . Biochimica et Biophysica Acta (BBA) - Биомембраны . 1818 (12): 3081–3089. DOI : 10.1016 / j.bbamem.2012.07.027 . PMID 22885137 . ... Было показано, что активность агонистов в отношении некоторых рецепторов нейромедиаторов регулируется напряжением, механизм, который, как предполагалось, играет решающую роль в регуляции высвобождения нейромедиаторов ингибирующими ауторецепторами ...
- ^ Энантиоселективный синтез стробамина и его аналогов Xing Zhang et al. Центр органической и медицинской химии, Институт Исследовательского Треугольника. Выпуск в честь профессора Джеймса Кука ARKIVOC 2010 (iv) 96-103
- ^ Алкалоиды; Vol. 44, Джеффри Корделл
- ^ a b Аппель, Майкл; Данн, Уильям Дж .; Reith, Maarten EA; Миллер, Ларри; Флиппен-Андерсон, Джудит Л. (2002). «Анализ связывания аналогов кокаина с переносчиками моноаминов с использованием трехмерного QSAR разложения тензор». Биоорганическая и медицинская химия . 10 (5): 1197–1206. DOI : 10.1016 / S0968-0896 (01) 00389-3 . ISSN 0968-0896 . PMID 11886784 .
- ^ Хикс, MJ; Де, ВР; Розенберг, JB; Дэвидсон, JT; Морено, AY; Janda, KD; Wee, S; Кооб Г.Ф .; Hackett, NR; Каминский С.М.; Worgall, S; Тот, М; Mezey, JG; Кристалл, Р.Г. (2011). «Аналог кокаина в сочетании с разрушенным аденовирусом: вакцинационная стратегия для вызова иммунитета с высоким титром против лекарств, вызывающих зависимость» . Mol Ther . 19 (3): 612–9. DOI : 10.1038 / mt.2010.280 . PMC 3048190 . PMID 21206484 .
- ^ Кинси, BM; Kosten, TR; Орсон, FM (2010). «Активная иммунотерапия для лечения кокаиновой зависимости» . Наркотики будущего . 35 (4): 301–306. DOI : 10,1358 / dof.2010.035.04.1474292 . PMC 3142961 . PMID 21796226 .
- ^ Wee, S; Хикс, MJ; Де, ВР; Розенберг, JB; Морено, AY; Каминский С.М.; Janda, KD; Кристалл, RG; Кооб, GF (2011). «Новая кокаиновая вакцина, связанная с разрушенным вектором переноса гена аденовируса, блокирует психостимулирующий и усиливающий эффекты кокаина» . Нейропсихофармакология . 37 (5): 1083–91. DOI : 10.1038 / npp.2011.200 . PMC 3306868 . PMID 21918504 .
- ^ Каталитические антитела против кокаина и методы использования и производства те же патенты Google US 6566084 B1
- ^ Дэн, Шисянь; Бхарат, Наринэ; де Прада, Палома; Ландри, Дональд В. (2004). «Субстратный катализ антителами». Органическая и биомолекулярная химия . 2 (3): 288–90. DOI : 10.1039 / b314264g . ISSN 1477-0520 . PMID 14747854 .
- ^ Хо, М; Сегре, М. (2003). «Ингибирование связывания кокаина с переносчиком дофамина человека одноцепочечным антиидиотипическим антителом: его клонирование, экспрессия и функциональные свойства» . Biochim Biophys Acta . 1638 (3): 257–66. DOI : 10.1016 / s0925-4439 (03) 00091-7 . PMC 3295240 . PMID 12878327 .
- ^ Шабакер, DS; Киршбаум, KS; Сегре, М. (2000). «Изучение возможности создания антиидиотипической кокаиновой вакцины: анализ специфичности антикокаиновых антител (Ab1), способных индуцировать антиидиотипические антитела Ab2beta» . Иммунология . 100 (1): 48–56. DOI : 10.1046 / j.1365-2567.2000.00004.x . PMC 2326984 . PMID 10809958 .
- ^ Чжоу, Цзя; Он, Ронг; Джонсон, Кеннет М .; Е, Яньпин; Козиковски, Алан П. (2004). "Основанные на пиперидине гибридные лиганды нокаина / модафинила как сильнодействующие ингибиторы переносчиков моноаминов: эффективное открытие лекарств путем рациональной гибридизации свинца" . Журнал медицинской химии . 47 (24): 5821–5824. DOI : 10.1021 / jm040117o . ISSN 0022-2623 . PMC 1395211 . PMID 15537337 .
- ^ Обмен мнениями скептиков: сахар является одним элементом от кокаина (или любого другого наркотика?)
- ^ Веласкес-Санчес, Клара; Гарсия-Вердуго, Хосе М .; Мурга, Хуан; Каналес, Хуан Дж. (2013). «Атипичный ингибитор транспорта дофамина, JHW 007, предотвращает вызванную амфетамином сенсибилизацию и синаптическую реорганизацию в прилежащем ядре». Прогресс нейропсихофармакологии и биологической психиатрии . 44 : 73–80. DOI : 10.1016 / j.pnpbp.2013.01.016 . ISSN 0278-5846 . PMID 23385166 .
- ^ Танда, G; Ньюман, А; Ebbs, AL; Tronci, V; Зеленый, Дж; Tallarida, RJ; Кац, JL (2009). «Комбинации кокаина с другими ингибиторами захвата дофамина: оценка аддитивности» . J Pharmacol Exp Ther . 330 (3): 802–9. DOI : 10,1124 / jpet.109.154302 . PMC 2729796 . PMID 19483071 .
- ^ Шмитт, KC; Ротман, РБ; Рейт, Мэн (2013). «Неклассическая фармакология переносчика дофамина: атипичные ингибиторы, аллостерические модуляторы и частичные субстраты» . J. Pharmacol. Exp. Ther . 346 (1): 2–10. DOI : 10,1124 / jpet.111.191056 . PMC 3684841 . PMID 23568856 .
- ^ a b c Ротман, РБ; Baumann, MH; Prisinzano, TE; Ньюман, АХ (2008). «Ингибиторы транспорта дофамина на основе GBR12909 и бензтропина в качестве потенциальных лекарств для лечения кокаиновой зависимости» . Biochem Pharmacol . 75 (1): 2–16. DOI : 10.1016 / j.bcp.2007.08.007 . PMC 2225585 . PMID 17897630 .
- ^ Runyon, SP; Кэрролл, FI (2006). «Лиганды переносчика дофамина: последние разработки и терапевтический потенциал». Curr Top Med Chem . 6 (17): 1825–43. DOI : 10.2174 / 156802606778249775 . PMID 17017960 .
- ^ а б в г Лоланд, CJ; Desai, RI; Zou, M.-F .; Cao, J .; Grundt, P .; Герстбрейн, К .; Ситте, HH; Ньюман, AH; Кац, JL; Гетер, У. (2007). «Взаимосвязь между конформационными изменениями в переносчике допамина и кокаиноподобными субъективными эффектами ингибиторов поглощения» . Молекулярная фармакология . 73 (3): 813–823. DOI : 10,1124 / mol.107.039800 . ISSN 0026-895X . PMID 17978168 .
- ^ Далланоче, Клелия; Канови, Мара; Матера, Карло; Меннини, Тициана; Де Амичи, Марко; Гобби, Марко; Де Микели, Карло (2012). «Новое спироциклическое производное тропанил-Δ2-изоксазолина усиливает связывание циталопрама и пароксетина с переносчиками серотонина, а также захват серотонина». Биоорганическая и медицинская химия . 20 (21): 6344–6355. DOI : 10.1016 / j.bmc.2012.09.004 . ISSN 0968-0896 . PMID 23022052 .
- ^ C. Dallanoce et al. - Биоорг. Med. Chem. 20 (2012) 6344-6355
- ^ Сюй, YT; Kaushal, N .; Shaikh, J .; Уилсон, LL; Mesangeau, C .; Маккарди, CR; Мацумото, Р.Р. (2010). «Новый замещенный пиперазин, CM156, ослабляет стимулирующие и токсические эффекты кокаина у мышей» . Журнал фармакологии и экспериментальной терапии . 333 (2): 491–500. DOI : 10,1124 / jpet.109.161398 . ISSN 0022-3565 . PMC 2872963 . PMID 20100904 .
- ^ Банистер, Сэмюэл Д .; Маноли, Мирал; Barron, Melissa L .; Werry, Eryn L .; Кассиу, Майкл (2013). «N-замещенные 8-аминопентацикло [5.4.0.02,6.03,10.05,9] ундеканы в качестве лигандов σ-рецепторов с потенциальным нейрозащитным действием». Биоорганическая и медицинская химия . 21 (19): 6038–6052. DOI : 10.1016 / j.bmc.2013.07.045 . ISSN 0968-0896 . PMID 23981939 .
- ^ Ruetsch, YA; Böni, T; Боргеат, А (август 2001 г.). «От кокаина до ропивакаина: история местных анестетиков». Curr Top Med Chem . 1 (3): 175–82. DOI : 10.2174 / 1568026013395335 . PMID 11895133 .
- ^ a b Wilcox, KM; Kimmel, HL; Линдси, КП; Вотав, младший; Гудман, ММ; Хауэлл, LL (2005). «Сравнение in vivo усиливающих эффектов и переносчиков дофамина местных анестетиков у макак-резусов» (PDF) . Синапс . 58 (4): 220–228. CiteSeerX 10.1.1.327.1264 . DOI : 10.1002 / syn.20199 . PMID 16206183 . Архивировано из оригинального (PDF) 11 июня 2010 года.
- ^ a b Шенбергер, Матиас; Дамийонайтис, Арунас; Чжан, Цзинань; Нагель, Даниэль; Траунер, Дирк (2014). «Разработка нового блокатора фотохромных ионных каналов путем азологизации фомокаина» . ACS Chemical Neuroscience . 5 (7): 514–518. DOI : 10.1021 / cn500070w . ISSN 1948-7193 . PMC 4102962 . PMID 24856540 . статья nih.gov
- ^ Патент США 6,479,509 Патент изобретателя Фрэнка Айви Кэрролла, правопреемник: Институт исследовательского треугольника
- ^ Патент США US6479509 Структуры B1, представленные на рассмотрение, 5-е соединение внизу на изображении.
Внешние ссылки [ править ]
| Викискладе есть медиафайлы, связанные с аналогами кокаина . |
- В предварительной заявке на патент США перечислены примеры соединений, являющихся тропанами, для перспективного использования в исследованиях.
- Статья об исследовании аналога кокаина
- Список молекул типа тропанила и их регистрационные номера CAS