Эта статья требует дополнительных ссылок для проверки . ( декабрь 2010 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
| Миофибробласт | |
|---|---|
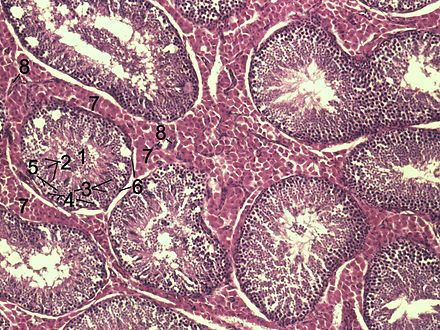 Гистологический срез паренхимы яичка кабана . 1 просвет Tubulus semiferus contortus , 2 сперматиды , 3 сперматоцита , 4 сперматогонии , 5 клеток Сертоли , 6 миофибробластов , 7 клеток Лейдига , 8 капилляров | |
| Подробности | |
| Идентификаторы | |
| латинский | миофибробласт |
| MeSH | D058628 |
| TH | H2.00.03.0.01013 |
| Анатомические термины микроанатомии | |
Миофибробластов представляет собой клетку , которая находится в между фибробластом и гладкой мышечной клеткой в фенотипе .
Структура [ править ]
Миофибробласты обнаруживаются субэпителиально на многих поверхностях слизистых оболочек, например, почти по всем желудочно-кишечным и мочеполовым трактам. Здесь они не только действуют как регулятор формы крипт и ворсинок, но также действуют как клетки стволовых ниш в криптах кишечника и как части атипичных антигенпрезентирующих клеток. У них есть как поддержка, так и паракринная функция в большинстве мест.
Местоположение [ править ]
Обычно они обнаруживаются в грануляционной ткани и строме опухолей. Обычно они выстилают желудочно-кишечный тракт, регулируя форму крипт и ворсинок.
Маркеры [ править ]
Миофибробласты обычно окрашивают виментин промежуточных филаментов, который является общим мезенхимальным маркером и «альфа- актин гладких мышц » (человеческий ген = ACTA2 ), а также на палладин , который представляет собой белок каркаса актина цитоскелета . Они положительны для других гладких маркеров, таких как десмин промежуточного филаментного типа, в некоторых тканях, но могут быть отрицательными для десмина в некоторых других. Подобная гетерогенная положительность может существовать почти для всех маркеров гладких мышц, за исключением, вероятно, нескольких, которые положительны только для сократительных гладких мышц, таких как метавинкулин и смоотелин.
Некоторые миофибробласты (особенно если они имеют звездчатую форму) также могут быть положительными на GFAP .
Развитие [ править ]
Есть много возможных путей развития миофибробластов:
- Частичная гладкомышечная дифференцировка фибробластической клетки
- Активация звездчатых клеток (например, печеночных клеток Ито или звездчатых клеток поджелудочной железы ).
- Утрата сократительного фенотипа (или приобретение «синтетического фенотипа») гладкомышечной клетки.
- Прямая миофибробластическая дифференцировка клеток-предшественников, находящихся в стромальной ткани.
- Направление и рекрутирование циркулирующего мезенхимального предшественника, который может напрямую дифференцироваться, как указано выше, или косвенно дифференцироваться через другие типы клеток в качестве промежуточных.
- Эпителиально-мезенхимальная трансдифференцировка ( EMT ) эпителиальной клетки .
Возможно, наиболее хорошо изученный путь образования миофибробластов - это дифференцировка, зависимая от TGF-beta1, из клеток фибробластов . Активация TGF-бета - рецептора 1 и TGF-бета - рецептора 2 приводит к индукции канонического SMAD2 / SMAD3 пути. [1] Вместе с совместной активацией неканонического пути EGFR эти события приводят к усилению регуляции гена ACTA2 и последующей продукции альфа-белка гладких мышц актина. Описано несколько регуляторов пути дифференцировки миофибробластов, включая гиалуронан и CD44.корецепторная активация EGFR. [2]
Функция [ править ]
Во многих органах, таких как печень, легкие и почки, они в первую очередь вовлечены в фиброз. В ткани раны они участвуют в укреплении раны за счет отложения внеклеточных волокон коллагена, а затем в сокращении раны за счет внутриклеточного сокращения и сопутствующего выравнивания волокон коллагена путем опосредованного интегрином натяжения пучков коллагена. Перициты и мезангиальные клетки почек являются некоторыми примерами модифицированных миофибробластоподобных клеток.
Миофибробласты могут мешать распространению электрических сигналов [3], контролирующих сердечный ритм [4], что приводит к аритмии как у пациентов, перенесших сердечный приступ, так и у плода. Урсодиол - многообещающий препарат от этого состояния. [5]
Заживление ран [ править ]
Миофибробласты могут сокращаться за счет использования комплекса актин-миозин гладкомышечного типа, богатого формой актина, называемой альфа-актином гладких мышц. Эти клетки затем способны ускорить заживление раны, сжимая края раны.
Ранние работы по заживлению ран показали, что грануляционная ткань, взятая из раны, может сокращаться in vitro (или в ванне для органов) так же, как и гладкие мышцы, при воздействии веществ, вызывающих сокращение гладких мышц, таких как адреналин или ангиотензин .
Совсем недавно было показано, что фибробласты могут превращаться в миофибробласты с фотобиомодуляцией .
После завершения заживления эти клетки теряются в результате апоптоза, и было высказано предположение, что при некоторых фиброзных заболеваниях (например, циррозе печени , фиброзе почек, забрюшинном фиброзе) этот механизм не работает, что приводит к сохранению миофибробластов и, как следствие, к их расширению. из внеклеточного матрикса (фиброза) с сокращением.
Точно так же в ранах, которые не рассасываются и становятся келоидами или гипертрофическими рубцами , миофибробласты могут сохраняться, а не исчезать в результате апоптоза. [6]
См. Также [ править ]
- Список типов клеток человека, полученных из зародышевых листков
Ссылки [ править ]
- ↑ Evans RA, Tian YC, Steadman R, Phillips AO (январь 2003 г.). «Опосредованная TGF-beta1 терминальная дифференцировка фибробластов и миофибробластов - роль белков Smad». Экспериментальные исследования клеток . 282 (2): 90–100. DOI : 10.1016 / S0014-4827 (02) 00015-0 . PMID 12531695 .
- ^ Midgley AC, Rogers M, Холлет MB, Clayton A, Bowen T, Phillips AO, Steadman R (май 2013). «Трансформация стимулированного фактором роста-β1 (TGF-β1) фибробласта в дифференцировку миофибробластов опосредуется рецептором эпидермального фактора роста (EGFR), поддерживаемым гиалуронаном (HA), и совместной локализацией CD44 в липидных рафтах» . Журнал биологической химии . 288 (21): 14824–38. DOI : 10.1074 / jbc.M113.451336 . PMC 3663506 . PMID 23589287 .
- ^ Quinn TA, Camelliti P, Rog-Zielinska Е.А., Siedlecka U, Поггиоли T, Тул ET, Knöpfel T, Kohl P (декабрь 2016). «Электротонная связь возбудимых и невозбудимых клеток сердца, выявленная оптогенетикой» . Труды Национальной академии наук Соединенных Штатов Америки . 113 (51): 14852–14857. DOI : 10.1073 / pnas.1611184114 . PMC 5187735 . PMID 27930302 .
- ^ Gourdie RG, Dimmeler S, Kohl P (сентябрь 2016). «Новые терапевтические стратегии, направленные на фибробласты и фиброз при сердечных заболеваниях» . Обзоры природы. Открытие наркотиков . 15 (9): 620–38. DOI : 10.1038 / nrd.2016.89 . PMC 5152911 . PMID 27339799 .
- ^ Новости BBC
- ^ Frangogiannis NG (2017). «Внеклеточный матрикс при повреждении, ремонте и ремоделировании миокарда» . J Clin Invest . 127 (5): 1600–1612. DOI : 10.1172 / JCI87491 . PMC 5409799 . PMID 28459429 .
Внешние ссылки [ править ]
- СМИ, связанные с миофибробластом, на Викискладе?