Эта статья требует дополнительных ссылок для проверки . ( август 2012 г. ) ( Узнайте, как и когда удалить этот шаблон сообщения ) |
В химии , А одинарная связь является химической связью между двумя атомами с участием двух валентных электронов . То есть атомы разделяют одну пару электронов, в которой образуется связь. [1] Таким образом, одинарная связь является разновидностью ковалентной связи . При совместном использовании каждый из двух вовлеченных электронов больше не находится в единоличном владении орбитали, на которой он возник. Скорее, оба электрона проводят время на любой из орбиталей, которые перекрываются в процессе связывания. Как структура Льюисаодинарная связь обозначается как AːA или AA, для которой A представляет собой элемент (Moore, Stanitski и Jurs 329). В первом варианте каждая точка представляет собой общий электрон, а во втором варианте полоса представляет собой оба электрона, общих в одинарной связи.
Ковалентная связь также может быть двойной или тройной связью . Одинарная связь слабее двойной или тройной связи. Эту разницу в силе можно объяснить, исследуя компонентные связи, из которых состоит каждый из этих типов ковалентных связей (Мур, Станицкий и Юрс, 393).
Обычно одинарная облигация является сигма-облигацией . Исключением является связь в дибороне , которая является пи-связью . Напротив, двойная связь состоит из одной сигма-связи и одной пи-связи, а тройная связь состоит из одной сигма-связи и двух пи-связей (Мур, Станицкий и Юрс 396). Количество соединений компонентов - вот что определяет несоответствие прочности. Само собой разумеется, что одинарная связь является самой слабой из трех, потому что она состоит только из сигма-связи, а двойная или тройная связь состоит не только из этого типа компонентной связи, но также по крайней мере из одной дополнительной связи.
Одинарная связь обладает способностью к вращению - свойством, которым не обладают двойная или тройная связь. Структура пи-связей не допускает вращения (по крайней мере, не при 298 К), поэтому двойная связь и тройная связь, которые содержат пи-связи, сохраняются благодаря этому свойству. Сигма-связь не столь ограничительна, и одинарная связь может вращаться, используя сигма-связь в качестве оси вращения (Мур, Станицкий и Юрс 396-397).
Другое сравнение свойств может быть выполнено по длине связи. Одинарные связи являются самыми длинными из трех типов ковалентных связей, поскольку межатомное притяжение больше в двух других типах, двойных и тройных. Увеличение количества компонентных связей является причиной увеличения притяжения по мере того, как больше электронов распределяется между связанными атомами (Мур, Станицкий и Юрс 343).
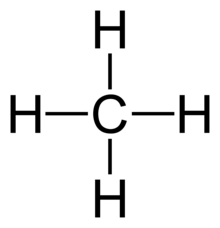
Одинарные связи часто наблюдаются в двухатомных молекулах . Примеры такого использования одинарных связей включают H 2 , F 2 и HCl .
Одинарные связи также наблюдаются в молекулах, состоящих из более чем двух атомов. Примеры такого использования одинарных связей включают:
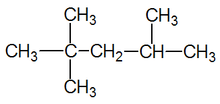
Одиночная связь проявляется даже в таких сложных молекулах, как углеводороды крупнее метана. Тип ковалентной связи в углеводородах чрезвычайно важен для номенклатуры этих молекул. Углеводороды, содержащие только одинарные связи, называются алканами (Moore, Stanitski и Jurs 334). Названия конкретных молекул, принадлежащих к этой группе, заканчиваются суффиксом -ан . Примеры включают этан , 2-метилбутан и циклопентан (Moore, Stanitski и Jurs 335).
Ссылки [ править ]
- ^ «ковалентная связь - одинарные связи» . Chemguide.co.uk . Проверено 12 августа 2012 .
Мур, Джон У., Конрад Л. Станицки и Питер К. Юрс. Химия: молекулярная наука, Университет Индианы. Австралия: Cengage Learning, 2012. Печать.
См. Также [ править ]
- Заказ облигаций
