| Стрептококк | |
|---|---|
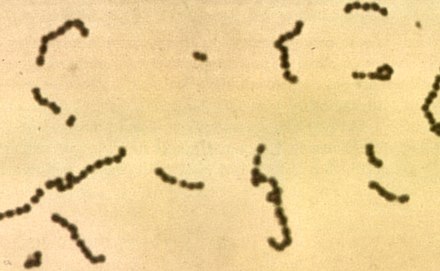 | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Фирмикуты |
| Учебный класс: | Бациллы |
| Заказ: | Лактобациллы |
| Семья: | Streptococcaceae |
| Род: | Streptococcus Rosenbach , 1884 г. |
| Виды [1] | |
| |
Стрептококк является родом из грамположительного кокка (множественных числе кокков ) или сферических бактерийкоторый принадлежит к семейству Streptococcaceae ,пределах порядка Lactobacillales (молочнокислые бактерий), в филюме Firmicutes . [2] Деление клеток у стрептококков происходит по одной оси , поэтому по мере роста они имеют тенденцию образовывать пары или цепочки, которые могут казаться изогнутыми или скрученными. Это отличается от стафилококков , которые делятся по нескольким осям, образуя неправильные, похожие на виноград кластеры клеток . Большинство стрептококков отрицательны к оксидазеи каталаза-отрицательные , и многие из них являются факультативными анаэробами (способны расти как в аэробных, так и в анаэробных условиях).
Термин был придуман в 1877 году венским хирургом Альбертом Теодором Бильротом (1829–1894) [3] путем объединения приставки «strepto-» (от древнегреческого : στρεπτός , латинизировано : streptós , букв. «Легко скручивается, податливый» [4]. ] ) вместе с суффиксом «-coccus» (от современной латыни : coccus , от древнегреческого: κόκκος , латинизировано: kókkos , букв. «зерно, семя, ягода». [5] ) В 1984 году многие бактерии, ранее сгруппированные в род Streptococcus были выделены вродов Enterococcus и Lactococcus . [6] В настоящее время насчитывается более 50 видов этого рода. Было обнаружено, что этот род является частью микробиома слюны . [7]
Патогенез и классификация [ править ]
Помимо стрептококкового фарингита (стрептококковой ангины), некоторые виды Streptococcus являются причиной многих случаев розового глаза , [8] менингита , бактериальной пневмонии , эндокардита , рожи и некротического фасциита (бактериальные инфекции, поедающие плоть). Однако многие виды стрептококков не являются патогенными и составляют часть комменсальной микробиоты человека рта, кожи, кишечника и верхних дыхательных путей. Стрептококки также являются необходимым ингредиентом при производстве сыра Эмменталер («Швейцарский») . [цитата необходима ]
Виды Streptococcus классифицируются на основе их гемолитических свойств. [9] Альфа-гемолитики вызывают окисление железа в молекулах гемоглобина в красных кровяных тельцах, придавая ему зеленоватый цвет на кровяном агаре. Бета-гемолитические виды вызывают полный разрыв красных кровяных телец. На кровяном агаре это выглядит как обширные области, свободные от клеток крови, окружающие колонии бактерий. Гамма-гемолитические виды не вызывают гемолиза. [ необходима цитата ]
Бета-гемолитические стрептококки далее классифицируются по группировке Лансфилда , классификации серотипов (то есть, описывающей конкретные углеводы, присутствующие на стенке бактериальной клетки). [6] 21 описанный серотип назван группами Lancefield от A до W (за исключением I и J). Эта система классификации была разработана Ребеккой Лэнсфилд , ученым из Университета Рокфеллера . [ необходима цитата ]
В медицине наиболее важными группами являются альфа-гемолитические стрептококки S. pneumoniae и Streptococcus viridans , а также бета-гемолитические стрептококки группы A и B Лансфилда (также известные как «стрептококки группы A» и «стрептококки группы B»). ).
Таблица: Стрептококки, имеющие отношение к медицине (не все альфа-гемолитики) [9]
| Разновидность | Хозяин | Болезнь |
| S. pyogenes | человек | фарингит , целлюлит , рожа |
| S. agalactiae | человек, крупный рогатый скот | неонатальный менингит и сепсис |
| С. dysgalactiae | человек, животные | эндокардит , бактериемия , пневмония , менингит , респираторные инфекции |
| S. gallolyticus | человек, животные | инфекции желчных или мочевыводящих путей , эндокардит |
| S. anginosus | человек, животные | подкожные / органные абсцессы , менингит , респираторные инфекции |
| S. sanguinis | человек | эндокардит, кариес зубов |
| S. suis | свинья | менингит |
| S. mitis | человек | эндокардит |
| S. mutans | человек | кариес |
| S. pneumoniae | человек | пневмония |
Альфа-гемолитический [ править ]
Когда присутствует альфа-гемолиз (альфа-гемолиз), агар под колонией будет казаться темным и зеленоватым из-за преобразования гемоглобина в зеленый биливердин . Streptococcus pneumoniae и группа оральных стрептококков ( Streptococcus viridans или viridans streptococci) проявляют альфа-гемолиз. Альфа-гемолиз также называют неполным гемолизом или частичным гемолизом, поскольку клеточные мембраны эритроцитов остаются нетронутыми. Это также иногда называют зеленым гемолизом из-за изменения цвета агара.
Пневмококки [ править ]
- S. pneumoniae (иногда называемый пневмококком) является основной причиной бактериальной пневмонии и нерегулярной этиологии среднего отита , синусита , менингита и перитонита . Воспаление считается основной причиной того, как пневмококки вызывают заболевание, отсюда и тенденция диагнозов, связанных с ними, включать воспаление.
Группа viridans: альфа-гемолитики [ править ]
- В viridans стрептококков являются большой группой синантропных бактерий , которые являются либо альфа-гемолитическим , производя зеленую окраску на крови агара пластин (отсюда и название «viridans», от латинского Viridis , зеленый), или nonhemolytic. У них нет антигенов Лэнсфилда. [2]
Бета-гемолитический [ править ]
Бета-гемолиз (β-гемолиз), иногда называемый полным гемолизом, представляет собой полный лизис эритроцитов в среде вокруг и под колониями: область становится светлой (желтой) и прозрачной. Стрептолизин, экзотоксин, представляет собой фермент, вырабатываемый бактериями, который вызывает полный лизис красных кровяных телец. Существует два типа стрептолизина: стрептолизин O (SLO) и стрептолизин S (SLS). Стрептолизин О - чувствительный к кислороду цитотоксин, секретируемый большинством стрептококков группы А.(ГАЗ) и взаимодействует с холестерином в мембране эукариотических клеток (в основном красных и белых кровяных телец, макрофагов и тромбоцитов) и обычно приводит к бета-гемолизу под поверхностью кровяного агара. Стрептолизин S представляет собой устойчивый к кислороду цитотоксин, который также продуцируется большинством штаммов ГАЗ, что приводит к очищению поверхности кровяного агара. SLS влияет на иммунные клетки, включая полиморфноядерные лейкоциты и лимфоциты, и считается, что он предотвращает избавление иммунной системы хозяина от инфекции. Streptococcus pyogenes , или ГАЗ, демонстрирует бета-гемолиз.
Некоторые виды со слабой бета-гемолитикой вызывают интенсивный гемолиз при совместном выращивании со штаммом Staphylococcus . Это называется тестом CAMP. Streptococcus agalactiae демонстрирует это свойство. С помощью этого теста можно предположительно идентифицировать Clostridium perfringens . Listeria monocytogenes также является положительной на агаре с овечьей кровью.
Группа А [ править ]
S. pyogenes группы А является возбудителем широкого спектра стрептококковых инфекций группы А (ГАЗ). Эти инфекции могут быть неинвазивными или инвазивными. Неинвазивные инфекции обычно встречаются чаще и менее серьезны. Наиболее распространенными из этих инфекций являются стрептококковый фарингит (ангина) и импетиго . [10] Скарлатина также является неинвазивной инфекцией, но в последние годы не так распространена.
Инвазивные инфекции, вызываемые бета-гемолитическими стрептококками группы А, имеют тенденцию быть более тяжелыми и менее распространенными. Это происходит, когда бактерия может инфицировать участки, где она обычно не встречается, например кровь и органы . [11] Заболевания, которые могут быть вызваны, включают синдром стрептококкового токсического шока , некротический фасциит , пневмонию и бактериемию . [10] По оценкам, во всем мире ГАЗ является причиной более 500 000 смертей ежегодно, что делает его одним из ведущих патогенов в мире . [10]
Дополнительные осложнения могут быть вызваны ГАЗ, а именно острая ревматическая лихорадка и острый гломерулонефрит . Ревматическая лихорадка , заболевание, поражающее суставы , почки и сердечные клапаны , является следствием невылеченной инфекции стрептококка А, вызванной не самой бактерией. Ревматическая лихорадка вызывается антителами, вырабатываемыми иммунной системой для борьбы с инфекцией, перекрестно реагирующими с другими белками в организме. Эта «перекрестная реакция» заставляет тело атаковать себя и приводит к вышеуказанным повреждениям. Предполагается, что аналогичный аутоиммунный механизм, инициированный инфекцией бета-гемолитическим стрептококком группы А (БГСА), вызываетпедиатрические аутоиммунные нейропсихиатрические расстройства, связанные со стрептококковыми инфекциями (PANDAS) , при которых аутоиммунные антитела влияют на базальные ганглии, вызывая быстрое проявление психических, моторных, сонных и других симптомов у педиатрических пациентов.
Инфекция GAS обычно диагностируется с помощью экспресс-теста на стрептококк или посева.
Группа B [ править ]
S. agalactiae , или стрептококк группы B, GBS , вызывает пневмонию и менингит у новорожденных и пожилых людей , иногда с системной бактериемией . Важно отметить, что Streptococcus agalactiae - наиболее частая причина менингита у детей в возрасте от одного до трех месяцев. Они также могут колонизировать кишечник и женские половые пути, увеличивая риск преждевременного разрыва плодных оболочек во время беременности и передачи микроорганизма младенцу. Американский колледж акушеров и гинекологов , Американская академия педиатрии, И Центры по контролю и профилактике заболеваний рекомендуют всем беременным женщинам в возрасте от 35 до 37 недель беременности , чтобы пройти тестирование на СГБ. Женщинам с положительным результатом теста следует назначать профилактические антибиотики во время родов, которые обычно предотвращают передачу инфекции младенцу. [12]
Соединенное Королевство решило принять протокол, основанный на факторах риска, а не протокол, основанный на культуре, как в США. [13] В текущих рекомендациях указано, что при наличии одного или нескольких из следующих факторов риска женщину следует лечить антибиотиками во время родов :
- Преждевременные роды (<37 недель)
- Длительный разрыв плодных оболочек (> 18 часов)
- Внутриродовая лихорадка (≥38 ° C)
- История болезни СГБ у предыдущего ребенка
- GBS бактериурии во время этой беременности
Этот протокол позволяет назначать антибиотики во время родов 15–20% беременных женщин и предотвращать 65–70% случаев раннего сепсиса СГБ. [14]
Группа C [ править ]
Эта группа включает в себя S. следе , который вызывает душит у лошадей, [15] и С. zooepidemicus - С. оборы являются клональным потомком или биоваром наследственного S. zooepidemicus -Каких вызывает инфекции у некоторых видов млекопитающих, в том числе крупного рогатого скота и лошадей . С. dysgalactiae [ противоречивы ] также является членом группы С, бета-гемолитические стрептококки , которые могут вызвать фарингит и другие Pyogenic инфекции , аналогичные стрептококков группы А .
Группа D (энтерококки) [ править ]
Многие бывшие стрептококки группы D были переклассифицированы и помещены в род Enterococcus (включая E. faecalis , E. faecium , E. durans и E. avium ). [16] Например, Streptococcus faecalis теперь называется Enterococcus faecalis . E. faecalis иногда является альфа-гемолитическим, а E. faecium иногда является бета-гемолитическим. [17]
Остальные неэнтерококковые штаммы группы D включают Streptococcus gallolyticus , Streptococcus bovis и Streptococcus equinus .
Негемолитические стрептококки вызывают заболевание редко. Однако слабогемолитические бета-гемолитические стрептококки группы D и Listeria monocytogenes (которая на самом деле является грамположительной палочкой) не следует путать с негемолитическими стрептококками.
Стрептококки группы F [ править ]
Стрептококки группы F были впервые описаны в 1934 году Лонгом и Блиссом среди «мелких гемолитических стрептококков». [18] Кроме того, они известны как Streptococcus anginosus ( в соответствии с системой классификации Lancefield) или в качестве членов milleri S. группы ( в соответствии с европейской системой).
Стрептококки группы G [ править ]
Эти стрептококки обычно, но не исключительно, являются бета-гемолитиками. Streptococcus dysgalactiae [ противоречивый ] - преобладающий вид, с которым встречаются, особенно при заболеваниях человека. S. canis является примером GGS, который обычно встречается у животных, но может вызывать инфекцию у людей. S. phocae - это подвид GGS, который был обнаружен у морских млекопитающих и морских рыб. У морских млекопитающих он в основном связан с менингоэнцефалитом , сепсисом и эндокардитом , но также связан со многими другими патологиями. Его экологический резервуар и способы передачи у морских млекопитающих недостаточно изучены.
Стрептококки группы H [ править ]
Стрептококки группы H вызывают инфекции у собак среднего размера. Стрептококки группы H редко вызывают заболевание человека, если человек не имеет прямого контакта со ртом собаки. Один из наиболее распространенных способов распространения - это контакт человека с собакой изо рта в рот. Однако собака может лизать руку человека, и инфекция также может распространяться. [19]
Молекулярная таксономия и филогенетика [ править ]
Стрептококки были разделены на шесть групп на основе их последовательностей 16S рДНК: S. anginosus, S. gallolyticus, S. mitis, S. mutans, S. pyogenes и S. salivarius . [21] Группы 16S были подтверждены секвенированием всего генома (см. Рисунок). Важные возбудители S.pneumoniae , и S. Пирролидонилпептидаза принадлежат S. тШзу и С. Пирролидонилпептидаза группе, соответственно, [22] в то время как возбудитель зубного кариеса , стрептококки , является базальным к Streptococcus группе.
Геномика [ править ]
Секвенированы геномы сотен видов. [24] Большинство геномов Streptococcus имеют размер от 1,8 до 2,3 МБ и кодируют от 1700 до 2300 белков. Некоторые важные геномы перечислены в таблице. [25] Четыре вида, представленные в таблице ( S. pyogenes, S. agalactiae, S. pneumoniae и S. mutans ), имеют в среднем около 70% идентичности попарной белковой последовательности. [25]
| особенность | S. pyogenes | S. agalactiae | S. pneumoniae | S. mutans |
|---|---|---|---|---|
| пар оснований | 1,852,442 | 2 211 488 | 2 160 837 | 2 030 921 |
| ORF | 1792 | 2118 | 2236 | 1963 г. |
| профаги | да | нет | нет | нет |
Бактериофаг [ править ]
Бактериофаги описаны для многих видов Streptococcus . У S. pneumoniae описано 18 профагов размером от 38 до 41 т.п.н., каждый из которых кодирует от 42 до 66 генов. [ необходима цитата ] Некоторые из первых обнаруженных фагов Streptococcus были Dp-1 [26] [27] и ω1 (псевдоним ω-1). [28] [29] [30] В 1981 году было обнаружено семейство Cp (фаг Complutense 1, официально Streptococcus virus Cp1 , Picovirinae ) с Cp-1 в качестве первого члена. [31] Dp-1 и Cp-1 заражают обаS. pneumoniae и S. mitis . [32] Однако ряды хозяев большинства фагов Streptococcus систематически не исследовались.
Естественная генетическая трансформация [ править ]
Естественная генетическая трансформация включает передачу ДНК от одной бактерии к другой через окружающую среду. Трансформация - это сложный процесс, зависящий от экспрессии множества генов. Чтобы быть способной к трансформации, бактерия должна войти в особое физиологическое состояние, называемое компетентностью . S. pneumoniae , S. mitis и S. oralis могут стать компетентными и в результате активно приобретать гомологичную ДНК для трансформации по хищническому братоубийственному механизму [33]. Этот братоубийственный механизм в основном использует некомпетентных братьев и сестер, находящихся в той же нише [34] Среди высококомпетентных изолятов S. pneumoniae Li et al.[35] показали, что приспособленность к назальной колонизации и вирулентность (инфекционность легких) зависят от целостной системы компетентности. Компетенция может позволить стрептококковому патогену использовать внешнюю гомологичную ДНК для рекомбинационной репарации повреждений ДНК, вызванных окислительной атакой хозяина. [36]
См. Также [ править ]
- Quellung реакция
- Стрептококковая инфекция у домашней птицы
- Стрептокиназа
- Стрептококковый фарингит
Ссылки [ править ]
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw топор ay az ba bb bc bd be bf bg bh bi bj bk bl bm bn bo bp bq br bs bt Parte, AC«Streptococcus». LPSN .
- ^ a b Райан KJ, Рэй CG, ред. (2004). Шеррис Медицинская микробиология (4-е изд.). Макгроу Хилл. С. 293 –4. ISBN 978-0-8385-8529-0.
- ^ «стрептококк» . Интернет-словарь этимологии . Проверено 25 июля 2018 года .
- ^ στρεπτός в Лидделле , Генри Джордж ; Скотт, Роберт (1940) Греко-английский лексикон , полностью пересмотренный и дополненный Джонсом, сэром Генри Стюартом , с помощью Маккензи, Родерика. Оксфорд: Clarendon Press. В цифровой библиотеке Персея Университета Тафтса.
- ^ κόκκος у Лидделла и Скотта
- ^ a b Facklam R (октябрь 2002 г.). «Что случилось со стрептококками: обзор таксономических и номенклатурных изменений» . Clin. Microbiol. Ред . 15 (4): 613–30. DOI : 10.1128 / CMR.15.4.613-630.2002 . PMC 126867 . PMID 12364372 .
- ^ Ван, Кун; Лу, Вэньсинь; Ту, Цичао; Ге, Ичэнь; Он, Цзиньчжи; Чжоу, Ю; Гоу, Япин; Ностранд, Джой Д Ван; Цинь, Юйцзя; Ли, Цзяо; Чжоу, Цзичжун; Ли, Ян; Сяо, Лиин; Чжоу Сюэдун (10 марта 2016 г.). «Предварительный анализ микробиома слюны и их потенциальной роли в красном плоском лишае полости рта» . Научные отчеты . 6 (1): 22943. Bibcode : 2016NatSR ... 622943W . DOI : 10.1038 / srep22943 . PMC 4785528 . PMID 26961389 .
- ^ «Как избавиться от конъюнктивита, симптомы, лечение, причины и изображения» .
- ^ a b Паттерсон MJ (1996). Барон С; и другие. (ред.). Стрептококк. В: Медицинская микробиология Барона (4-е изд.). Univ Техасского медицинского отделения. ISBN 978-0-9631172-1-2. (через книжную полку NCBI) .
- ^ a b c Коэн-Порадосу Р., Каспер Д.Л. (2007). «Эпидемиология стрептококка группы А и последствия вакцины» . Clin. Заразить. Dis . 45 (7): 863–5. DOI : 10.1086 / 521263 . PMID 17806050 .
- ^ «Стрептококковые инфекции (инвазивные стрептококки группы А)» . Департамент здравоохранения и психической гигиены г. Нью-Йорка . Проверено 21 ноября 2012 года .
- ^ Schrag S, Gorwitz R, Фульц-Обломки К, Schuchat А (2002). «Профилактика перинатального стрептококкового заболевания группы B. Пересмотренное руководство CDC». MMWR Recomm Rep . 51 (RR-11): 1–22. PMID 12211284 .
- ^ Хьюз, RG; Brocklehurst, P; Стир, ПиДжей; Хит, П; Стенсон, Б.М. (ноябрь 2017 г.). «Профилактика стрептококковой инфекции группы B у новорожденных с ранним началом. Руководство № 36» . BJOG . 124 (12): e280 – e305. DOI : 10.1111 / 1471-0528.14821 . PMID 28901693 .
- ^ Норвиц, ER; Шорге, JO (2013). Краткий обзор акушерства и гинекологии (4-е изд.). Чичестер: ISBN компании John Wiley & Sons, Ltd. 978-1118341735.
- Перейти ↑ Harrington DJ, Sutcliffe IC, Chanter N (2002). «Молекулярные основы инфекции и болезни Streptococcus equi». Микробы заражают . 4 (4): 501–10. DOI : 10.1016 / S1286-4579 (02) 01565-4 . PMID 11932201 .
- ↑ Köhler W (июнь 2007 г.). «Современное состояние видов в пределах родов Streptococcus и Enterococcus». Международный журнал медицинской микробиологии . 297 (3): 133–50. DOI : 10.1016 / j.ijmm.2006.11.008 . PMID 17400023 .
- ^ Holt et al. (1994). Руководство Берджи по детерминантной бактериологии (9-е изд.). Липпинкотт Уильямс и Уилкинс. ISBN 0-683-00603-7
- ↑ Whitworth JM (ноябрь 1990 г.). «Группа F Lancefield и родственные стрептококки» (PDF) . J. Med. Microbiol . 33 (3): 135–51. DOI : 10.1099 / 00222615-33-3-135 . PMID 2250284 .
- ^ «Бактериальная инфекция (стрептококк) у собак» . petmd.com . Проверено 12 декабря 2014 .
- ^ «Бактерии-Firmicutes-Bacilli-Lactobacillales-Streptococcaceae-Streptococcus» . ПАТРИК, Чикагский университет . Проверено 12 декабря 2014 .
- Перейти ↑ Kawamura Y, Hou XG, Sultana F, Miura H, Ezaki T (1995). «Определение последовательностей 16S рРНК Streptococcus mitis и Streptococcus gordonii и филогенетических отношений между членами рода Streptococcus » . Int J Syst Bacteriol . 45 (2): 406–408. DOI : 10.1099 / 00207713-45-2-406 . PMID 7537076 .
- ^ Лю Д., Молекулярное обнаружение бактериальных патогенов человека ( Бока-Ратон : CRC Press , 2011), стр. 324 .
- ^ Сюй, П; Алвес, JM; Котенок, Т; Браун, А; Чен, Z; Одзаки, LS; Manque, P; Ge, X; Серрано, MG; Puiu, D; Хендрикс, S; Ван, Y; Чаплин, доктор медицины; Акан, Д; Paik, S; Петерсон, Д.Л .; Макрина, Флорида; Бак, Джорджия (2007). «Геном условно-патогенного микроорганизма Streptococcus sanguinis» . Журнал бактериологии . 189 (8): 3166–75. DOI : 10.1128 / JB.01808-06 . PMC 1855836 . PMID 17277061 .
- ^ Геномы Streptococcus и соответствующая информация в PATRIC
- ^ a b Ферретти Дж. Дж., Аждик Д., МакШан В. М. (2004). «Сравнительная геномика видов стрептококков». Индийский журнал медицинских исследований . 119 Дополнение: 1–6. PMID 15232152 .
- ↑ McDonnell M, Ronda C, Tomasz A (1975) «Диплофаг»: бактериофаг Diplococcus pneumoniae. Вирусология 63: 577–582
- ^ NCBI: Streptococcus фаг Dp-1 (виды)
- ^ Tiraby JG, Tiraby E, Fox MS (декабрь 1975) Пневмококковые бактериофаги. Вирусология 68: 566–569. DOI: 10.1016 / 0042-6822 (75) 90300-1 . PMID 844
- Перейти ↑ López R (2004). «Streptococcus pneumoniae и его бактериофаги: один длинный аргумент». Int. Microbiol . 7 (3): 163–71. PMID 15492930 . PDF из веб-архива (9 августа 2017 г.)
- ^ Рубенс Лопес, Эрнесто Гарсия: Последние тенденции в молекулярной биологии пневмококковых капсул, литических ферментов и бактериофагов , Oxford Academic FEMS Microbiology Reviews. Том 28, выпуск 5. 1 ноября 2004 г., стр. 554–580, doi: 10.1016 / j.femsre.2004.05.002 ( полный текст)
- Перейти ↑ Ronda C, López R, García E (1981). «Выделение и характеристика нового бактериофага Cp-1, заражающего Streptococcus pneumoniae» . J. Virol . 40 (2): 551–9. DOI : 10,1128 / JVI.40.2.551-559.1981 . PMC 256658 . PMID 6275103 .
- ^ Ouennane S, Leprohon Р, Муано S (2015). «Различные вирулентные пневмофаги заражают Streptococcus mitis» . PLOS ONE . 10 (2): e0118807. Bibcode : 2015PLoSO..1018807O . DOI : 10.1371 / journal.pone.0118807 . PMC 4334900 . PMID 25692983 .
- ^ Johnsborg О, Eldholm В, Bjørnstad М. Л., Håvarstein Л. (2008). «Хищный механизм резко увеличивает эффективность латерального переноса генов у Streptococcus pneumoniae и родственных комменсальных видов». Мол. Microbiol . 69 (1): 245–53. DOI : 10.1111 / j.1365-2958.2008.06288.x . PMID 18485065 . S2CID 30923996 .
- ^ Claverys JP, Håvarstein LS (2007). «Каннибализм и братоубийство: механизмы и причины существования». Nat. Rev. Microbiol . 5 (3): 219–29. DOI : 10.1038 / nrmicro1613 . PMID 17277796 . S2CID 35433490 .
- ^ Ли Г, Лян З, Ван X, Ян Y, Шао З, Ли М, Ма Y, Цюй Ф, Моррисон Д. А., Чжан Дж. Р. (2016). «Зависимость гипертрансформируемых пневмококковых изолятов к естественной трансформации для пригодности и вирулентности in vivo» . Заразить. Иммун . 84 (6): 1887–901. DOI : 10.1128 / IAI.00097-16 . PMC 4907133 . PMID 27068094 .
- ^ Michod RE Бернштейн H, Nedelcu AM (2008). «Адаптивное значение секса у микробных патогенов». Заразить. Genet. Evol . 8 (3): 267–85. DOI : 10.1016 / j.meegid.2008.01.002 . PMID 18295550 .
Внешние ссылки [ править ]
- Геномы стрептококков и соответствующая информация в PATRIC , центре ресурсов по биоинформатике, финансируемом NIAID
- Центры по профилактике заболеваний (CDC) (март 2000 г.). «Принятие рекомендаций по профилактике перинатальных стрептококковых заболеваний группы B поставщиками дородовой помощи - Коннектикут и Миннесота, 1998» . MMWR Morb. Смертный. Wkly. Rep . 49 (11): 228–32. PMID 10763673 .
- Канадский фонд Strep B
- Великобритания [[ благотворительная организация по поддержке стрептококковых инфекций группы B ]
- Вдохновленные природой открытия ферментов CRISPR значительно расширяют возможности редактирования генома . На сайте: SciTechDaily. 16 июня 2020 г. Источник: Media Lab, Массачусетский технологический институт.