В физической химии , то уравнение Аррениуса формула для температурной зависимости скоростей реакции . Уравнение было предложено Сванте Аррениусом в 1889 году на основе работы голландского химика Якоба Хенрикуса ван 'т Хоффа, который в 1884 году заметил, что уравнение Ван' т Гоффа для температурной зависимости констант равновесия предлагает такую формулу для скоростей как прямые, так и обратные реакции. Это уравнение имеет широкое и важное применение при определении скорости химических реакций и для расчета энергии активации. Аррениус дал физическое обоснование и интерпретацию формулы. [1] [2][3] В настоящее время этосоотношениелучше всего рассматривать как эмпирическое . [4] : 188 Его можно использовать для моделирования температурных изменений коэффициентов диффузии, заполнения кристаллических вакансий, скорости ползучести и многих других термически индуцированных процессов / реакций. Уравнение Эйринга , разработанное в 1935 году, также выражает взаимосвязь между скоростью и энергией.
Уравнение [ править ]
Уравнение Аррениуса дает зависимость константы скорости химической реакции от абсолютной температуры как
где
- k - константа скорости (частота столкновений, приводящих к реакции),
- T - абсолютная температура (в градусах Кельвина ),
- A - предэкспоненциальный множитель , постоянный для каждой химической реакции,
- E a - энергия активации реакции (в тех же единицах, что и RT ),
- R - универсальная газовая постоянная . [1] [2] [3]
В качестве альтернативы уравнение может быть выражено как
где
- E a - энергия активации реакции (в тех же единицах, что и k B T ),
- k B - постоянная Больцмана .
Единственное различие заключается в единицах измерения энергии E a : в первой форме используется энергия на моль , что является обычным в химии, а во второй форме напрямую используется энергия на молекулу , что является обычным явлением в физике. Различные блоки учитываются при помощи либо газовая постоянная , R , или постоянная Больцмана , к B , как множитель температуры Т .
Единицы предэкспоненциального множителя A идентичны единицам константы скорости и будут варьироваться в зависимости от порядка реакции. Если реакция первого порядка, она имеет единицы: с -1 , и по этой причине ее часто называют частотным фактором или частотой попыток реакции. Проще говоря, k - это количество столкновений, которые приводят к реакции в секунду, A - количество столкновений (ведущих к реакции или нет) в секунду, происходящих при правильной ориентации для реакции [5] иэто вероятность того, что любое данное столкновение приведет к реакции. Можно видеть, что либо повышение температуры, либо уменьшение энергии активации (например, за счет использования катализаторов ) приведет к увеличению скорости реакции.
Учитывая небольшой температурный диапазон кинетических исследований, разумно аппроксимировать энергию активации как не зависящую от температуры. Точно так же в широком диапазоне практических условий слабой температурной зависимостью предэкспоненциального фактора можно пренебречь по сравнению с температурной зависимостью фактора; за исключением случая "безбарьерных" реакций с ограниченной диффузией, когда преэкспоненциальный фактор является доминирующим и непосредственно наблюдаемым.
С помощью этого уравнения можно грубо оценить, что скорость реакции увеличивается примерно в 2 или 3 раза на каждые 10 ° C повышения температуры.
Заговор Аррениуса [ править ]
Принимая натуральный логарифм урожайности уравнения Аррениуса:
Переставляем урожайность:
Это имеет ту же форму, что и уравнение для прямой линии:
где х является обратным по Т .
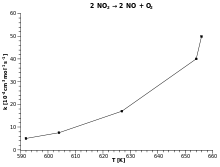
Таким образом, когда реакция имеет константу скорости , которая удовлетворяет уравнению Аррениуса, участок Ln к по сравнению с Т -1 дает прямую линию, градиент которого и перехвата может быть использована для определения E и A . Эта процедура стала настолько распространенной в экспериментальной химической кинетике, что практики стали использовать ее для определения энергии активации реакции. То есть энергия активации определяется как (- R ), умноженное на наклон графика зависимости ln k от (1 / T ):
Модифицированное уравнение Аррениуса [ править ]
Модифицированное уравнение Аррениуса [6] делает явной температурную зависимость предэкспоненциального множителя. Модифицированное уравнение обычно имеет вид
Исходное выражение Аррениуса, приведенное выше, соответствует n = 0. Подходящие константы скорости обычно лежат в диапазоне -1 < n <1 . Теоретический анализ дает различные прогнозы для n . Было указано, что «на основе температурных исследований константы скорости невозможно установить, наблюдается ли экспериментально предсказанная зависимость предэкспоненциального множителя от T 1/2 ». [4] : 190 Однако, если доступны дополнительные доказательства из теории и / или эксперимента (например, зависимость от плотности), нет никаких препятствий для точных проверок закона Аррениуса.
Другой распространенной модификацией является растянутая экспоненциальная форма [ необходима ссылка ]
где β - безразмерное число порядка 1. Это обычно рассматривается как чисто эмпирическая поправка или ложный фактор, чтобы модель соответствовала данным, но может иметь теоретическое значение, например, показывая наличие диапазона энергий активации или в особом случаи, такие как скачкообразное изменение диапазона Мотта .
Теоретическая интерпретация уравнения [ править ]
Концепция Аррениуса об энергии активации [ править ]
Аррениус утверждал, что для превращения реагентов в продукты они должны сначала получить минимальное количество энергии, называемое энергией активации E a . При абсолютной температуре T долю молекул, кинетическая энергия которых превышает E a, можно рассчитать с помощью статистической механики . Концепция энергии активации объясняет экспоненциальный характер отношений, и так или иначе она присутствует во всех кинетических теориях.
Расчеты констант скорости реакции включают усреднение энергии по распределению Максвелла – Больцмана с нижней границей и поэтому часто относятся к типу неполных гамма-функций , которые оказываются пропорциональными .
Теория столкновений [ править ]
Один из подходов - это теория столкновений химических реакций, разработанная Максом Траутцем и Уильямом Льюисом в 1916–18 годах. В этой теории предполагается, что молекулы реагируют, если они сталкиваются с относительной кинетической энергией вдоль линии их центров, превышающей E a . Число бинарных столкновений между двумя разнородными молекулами в секунду на единицу объема составляет [7]
где n A и n B - плотность молекул A и B , d AB - средний диаметр A и B , T - температура, умноженная на постоянную Больцмана k B для преобразования в единицы энергии, а μ AB это приведенная масса .
Затем вычисляется константа скорости, чтобы теория столкновений предсказывала, что предэкспоненциальный множитель равен числу столкновений Z AB . Однако для многих реакций это плохо согласуется с экспериментом, поэтому константа скорости записывается как . Здесь P - эмпирический стерический фактор , часто намного меньший, чем 1, который интерпретируется как доля достаточно энергичных столкновений, в которых две молекулы имеют правильную взаимную ориентацию для реакции. [7]
Теория переходного состояния [ править ]
Уравнение Эйринга , еще одно выражение, подобное Аррениусу, появляется в « теории переходного состояния » химических реакций, сформулированной Вигнером , Эйрингом , Поланьи и Эвансом в 1930-х годах. Уравнение Эйринга можно записать:
где = энергия Гиббса активации, - энтропия активации , - энтальпия активации, - постоянная Больцмана и - постоянная Планка . [8]
На первый взгляд это выглядит как экспонента, умноженная на линейный по температуре множитель . Однако свободная энергия сама по себе является величиной, зависящей от температуры. Свободная энергия активации - это разница члена энтальпии и члена энтропии, умноженная на абсолютную температуру. Предэкспоненциальный множитель зависит в первую очередь от энтропии активации. Общее выражение снова принимает форму экспоненты Аррениуса (энтальпии , а не энергии) , умноженной на медленно меняющейся функции Т . Точная форма температурной зависимости зависит от реакции и может быть рассчитана с использованием формул статистической механики, включающей статистические суммы реагентов и активированного комплекса.
Ограничения идеи энергии активации Аррениуса [ править ]
И энергия активации Аррениуса, и константа скорости k определяются экспериментально и представляют собой макроскопические параметры реакции, которые не просто связаны с пороговыми энергиями и успехом отдельных столкновений на молекулярном уровне. Рассмотрим конкретное столкновение (элементарную реакцию) между молекулами A и B. Угол столкновения, относительная поступательная энергия, внутренняя (особенно колебательная) энергия - все это будет определять вероятность того, что столкновение приведет к образованию молекулы продукта AB. Макроскопические измерения E и kявляются результатом множества индивидуальных столкновений с разными параметрами столкновения. Чтобы исследовать скорость реакции на молекулярном уровне, эксперименты проводятся в условиях, близких к столкновению, и этот предмет часто называют динамикой молекулярных реакций. [9]
Другая ситуация, когда объяснение параметров уравнения Аррениуса не оправдано, - это гетерогенный катализ , особенно для реакций, которые демонстрируют кинетику Ленгмюра-Хиншелвуда . Ясно, что молекулы на поверхности не «сталкиваются» напрямую, и простое молекулярное поперечное сечение здесь неприменимо. Вместо этого предэкспоненциальный множитель отражает перемещение по поверхности к активному участку. [10]
Отклонения от закона Аррениуса при стекловании наблюдаются во всех классах стеклообразующих веществ. [11] Закон Аррениуса предсказывает, что движение структурных единиц (атомов, молекул, ионов и т. Д.) Должно замедляться в процессе стеклования с меньшей скоростью, чем наблюдается экспериментально. Другими словами, структурные единицы замедляются быстрее, чем предсказывает закон Аррениуса. Это наблюдение является разумным, если предположить, что блоки должны преодолевать энергетический барьер с помощью энергии тепловой активации. Тепловая энергия должна быть достаточно высокой, чтобы допускать поступательное движение единиц, которое приводит к вязкому течению материала.
См. Также [ править ]
- Ускоренное старение
- Уравнение Эйринга
- Q10 (температурный коэффициент)
- Уравнение Ван 'т Гоффа
- Соотношение Клаузиуса – Клапейрона
- Уравнение Гиббса – Гельмгольца.
- Фронт цветения сакуры - прогноз по уравнению Аррениуса
Ссылки [ править ]
- ^ а б Аррениус, С.А. (1889). "Über die Dissociationswärme und den Einfluß der Temperatur auf den Dissociationsgrad der Elektrolyte" . Z. Phys. Chem. 4 : 96–116. DOI : 10.1515 / ZPCH-1889-0408 . S2CID 202553486 .
- ^ а б Аррениус, С.А. (1889). "Über die Reaktionsgeschwindigkeit bei der Inversion von Rohrzucker durch Säuren" . Z. Phys. Chem. 4 : 226–48. DOI : 10.1515 / ZPCH-1889-0116 .
- ^ a b Laidler, KJ (1987) Химическая кинетика , третье издание, Harper & Row, стр. 42
- ^ a b Кеннет Коннорс, Химическая кинетика, 1990, VCH Publishers Chemical Kinetics: Исследование скорости реакции в растворе в Google Книгах
- ^ Зильберберг, Мартин С. (2006). Химия (четвертое изд.). Нью-Йорк: Макгроу-Хилл. п. 696 . ISBN 0-07-111658-3.
- ^ Определение ИЮПАК Goldbook модифицированного уравнения Аррениуса .
- ^ a b Laidler, Keith J .; Мейзер, Джон Х. (1982). Физическая химия (1-е изд.). Бенджамин / Каммингс. С. 376–78. ISBN 0-8053-5682-7.
- ^ Laidler, Кейт Дж .; Мейзер, Джон Х. (1982). Физическая химия (1-е изд.). Бенджамин / Каммингс. С. 378–83. ISBN 0-8053-5682-7.
- Перейти ↑ Levine, RD (2005) Molecular Reaction Dynamics , Cambridge University Press
- ^ Слот, Тьерри К .; Райли, Натан; Шиджу, Н. Равендран; Медлин, Дж. Уилл; Ротенберг, Гади (2020). «Экспериментальный подход для управления эффектами ограничения на границах раздела катализатора» . Химическая наука . 11 (40): 11024–11029. DOI : 10.1039 / D0SC04118A . ISSN 2041-6520 .
- ^ Bauer, Th .; Lunkenheimer, P .; Лоидл, А. (2013). «Кооперативность и замораживание молекулярного движения при стекловании». Письма с физическим обзором . 111 (22): 225702. arXiv : 1306.4630 . Bibcode : 2013PhRvL.111v5702B . DOI : 10.1103 / PhysRevLett.111.225702 . PMID 24329455 . S2CID 13720989 .
Библиография [ править ]
- Полинг, LC (1988). Общая химия . Dover Publications.
- Лайдлер, KJ (1987). Химическая кинетика (3-е изд.). Харпер и Роу.
- Лайдлер, KJ (1993). Мир физической химии . Издательство Оксфордского университета.
Внешние ссылки [ править ]
- Растворимость углекислого газа в полиэтилене - Использование уравнения Аррениуса для расчета растворимости частиц в полимерах









![{\ Displaystyle E _ {\ rm {a}} \ Equiv -R \ left [{\ frac {\ partial \ ln k} {\ partial (1 / T)}} \ right] _ {P}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d79cf5cbb3009fb526eb1c5fa2a719f5432f6748)

![{\ Displaystyle к = А \ ехр \ влево [- \ влево ({\ гидроразрыва {E_ {а}} {RT}} \ вправо) ^ {\ бета} \ вправо],}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89847c364b7f6ebd0bbd35c26fb4e0d66b5fd679)











