| CFU-GEMM | |
|---|---|
 Эритроциты, лейкоциты и тромбоциты являются производными клеток CFU-GEMM. | |
| Подробности | |
| Дает начало | Миелоидные клетки |
| Место расположения | Костный мозг |
| Функция | колониеобразующая единица |
| Идентификаторы | |
| TH | H2.00.04.3.02008 |
| Анатомические термины микроанатомии | |
CFU-GEMM - это колониеобразующая единица, которая генерирует миелоидные клетки. Клетки CFU-GEMM являются олигопотенциальными клетками-предшественниками [1] [2] миелоидных клеток; поэтому их также называют обычными миелоидными клетками- предшественниками или миелоидными стволовыми клетками . «GEMM» означает гранулоцит , эритроцит , моноцит , мегакариоцит . [3]
Общий миелоидный предшественник (CMP) и общий лимфоидный предшественник (CLP) являются первой ветвью дифференцировки клеток в кроветворении после гемоцитобласта ( гемопоэтических стволовых клеток ).
Структура [ править ]
В современной терминологии CFU-S относится к плюрипотентным стволовым клеткам, которые могут дифференцироваться во все типы клеток крови. CFU-S делится на две линии: лимфоидный предшественник (CFU-LSC) и миелоидный предшественник (CFU-GEMM). Клетка CFU-GEMM способна дифференцироваться в лейкоциты, эритроциты и тромбоциты, которые обычно находятся в циркулирующей крови. [4]
Было высказано предположение, что эозинофилы не происходят от общего миелоидного предшественника у людей. [5]
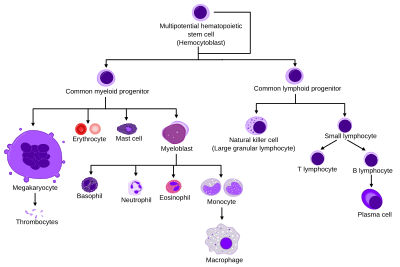
На соседнем изображении CFU-GEMM - это научное название «общего миелоидного предшественника», который отвечает за формирование всех клеток миелоидных клонов. Как видно на изображении, CFU-GEMM способен производить разнообразный набор клеток. Он созревает в мегакариоцит, эритроцит, тучную клетку или миелобласт в зависимости от наличия определенных факторов, которые побуждают клетку выбирать клон, которому следует следовать.
Маркеры поверхности [ править ]
Клетки характеризуются экспрессией маркеров клеточной поверхности CD 33, CD 34 и HLA-DR . [6] Эти поверхностные маркеры представляют собой белки на поверхности, которые уникальны для определенных клеток и определенных периодов созревания, что позволяет исследователям различать две разные клетки, а также то, на какой стадии клетка находится в своем развитии.
Развитие [ править ]
Факторы роста [ править ]
Дифференцировке и пролиферации CFU-GEMM способствуют факторы роста, такие как интерлейкины и цитокины. ИЛ-3 и GM-CSF, как отдельные факторы, одинаково активны в стимуляции CFU-GEMM, но комбинация обоих факторов производит дополнительные стимулирующие эффекты на CFU-GEMM. Рост CFU-GEMM стимулируется фактором стволовых клеток или SCF . Было обнаружено, что SCF также взаимодействует с GM-CSF, IL-6 , IL-3 , IL-11 или эритропоэтином, увеличивая количество CFU-GEMM. [6]
CFU-GEMM дает начало CFU-GM (ведущему к монобластам и миелобластам ), CFU-Meg (ведущему к мегакариобластам ) и CFU-E (ведущему к проэритробластам ). Стволовая клетка будет следовать определенной линии в зависимости от наличия определенных факторов роста и цитокинов . GM-CSF и IL-3 работают вместе, чтобы стимулировать производство всех линий. Когда присутствует эритропоэтин (ЭПО), производство красных кровяных телец из CFU-GEMM будет активировано. G-CSF, M-CSF, IL-5, IL-4 и IL-3 стимулируют выработку нейтрофилов, моноцитов, эозинофилов, базофилов и тромбоцитов соответственно. [4]
Исследования [ править ]
Поскольку клетка CFU-GEMM является очень ранним предком зрелых клеток крови, в норме она не обнаруживается в крови. Хотя CFU-GEMM присутствует в костном мозге , наиболее часто встречается в пуповине между матерью и ребенком. Было обнаружено, что эти клетки обладают высокой эффективностью повторного посева , а это означает, что при взятии из пуповины и выращивании в культуре высокий процент этих клеток способен образовывать колонии. Результаты исследований, проведенных Carow, Hangoc и Broxmeyer в 1993 году, показывают, что CFU-GEMM можно классифицировать как стволовые клетки из-за его высокой эффективности репликации в присутствии определенных факторов роста и цитокинов. [1]
Рост и продукция CFU-GEMM и BFU-E зависят от стимулирующих факторов от источника импульсной активности (BPA), такого как высвобождение интерлейкина-1 (IL-1) моноцитами , a было изучено в 1987 году. Также было показано, что фибробласты способны секретировать эти BPA, однако отвечают только на регуляторные молекулы, такие как интерлейкин-1. Результаты показали, что IL-1 увеличивает стимулирующие эффекты CFU-GEMM в зависимости от дозы с максимальной эффективностью около 140 нг / мл. Это исследование показало, что IL-1 играет важную роль в регуляции выработки стимулирующих факторов, которые влияют на клетки-предшественники кроветворения . [7]
В другом исследовании, проведенном в 2014 году, исследователи искали молекулы для стимуляции пролиферации долговременных гемопоэтических стволовых клеток (LT-HSC). Они протестировали библиотеку из более чем 5000 небольших молекул, все, кроме одной (UM729), подавляли рост. Был создан более мощный аналог, получивший название UM171. По сравнению с другими подобными химическими веществами, UM171 допускал большую пролиферацию HSC и меньшее количество апоптотических клеток по сравнению с контролем, а также большее количество мультипотенциальных предшественников, таких как CFU-GEMM. Кроме того, UM171 не повлиял на скорость деления. При использовании вместе с SR1 известный фактор транскрипции, UM171 позволил подавить дифференцировку и привел к увеличению роста CFU-GEMM. Эти результаты предполагают, что UM171 + SR1 вместе усиливают пролиферацию клеток-предшественников и подавляют дифференцировку. [8]
См. Также [ править ]
- Список типов клеток человека, полученных из зародышевых листков
Ссылки [ править ]
- ^ a b Carow CE, Hangoc G, Broxmeyer HE (февраль 1993 г.). «Человеческие мультипотенциальные клетки-предшественники (CFU-GEMM) обладают обширной способностью воспроизводить вторичные CFU-GEMM: эффект усиливается плазмой пуповинной крови» . Кровь . 81 (4): 942–9. DOI : 10.1182 / blood.V81.4.942.942 . PMID 7679010 .
- ^ Roodman GD, LeMaistre CF, Clark GM, Page CP, Ньюкомб TF, Knight WA (август 1987). «КОЕ-GEMM коррелируют с восстановлением нейтрофилов и тромбоцитов у пациентов, получавших аутологическую трансплантацию костного мозга после химиотерапии с высокими дозами мелфалана». Пересадка костного мозга . 2 (2): 165–73. PMID 3332164 .
- ^ "Подол I WBC Морфология и физиология" . Архивировано из оригинала 25 декабря 2008 года . Проверено 30 декабря 2008 .
- ^ a b Ciesla, Бетти (2007). Гематология на практике . Филадельфия, Пенсильвания: Компания FA Davis. ISBN 978-0-8036-1526-7.
- ^ Мори Y, Ивасаки Х, Коно К. и др. (Январь 2009 г.). «Идентификация предшественника человеческого эозинофильного предшественника: пересмотр фенотипического определения человеческого общего миелоидного предка» . J. Exp. Med . 206 (1): 183–93. DOI : 10,1084 / jem.20081756 . PMC 2626675 . PMID 19114669 .
- ^ a b "CFU-GEMM (Энциклопедия цитокинов и клеток - COPE)" . www.copewithcytokines.de . Проверено 19 ноября 2015 .
- ^ Зукали, младший; Броксмейер, HE; Динарелло, Калифорния; Гросс, М.А. и Вайнер, Р.С. (1987). «Регулирование ранних человеческих гемопоэтических (CFU-GEMM и BFU-E) клеток-предшественников in vitro с помощью среды, обусловленной фибробластами, индуцированной интерлейкином 1» (PDF) . Кровь . 69 (1): 33–37. DOI : 10.1182 / blood.V69.1.33.33 .
- ^ Фарес, I .; Chagaroui, J .; Гаро, Ю. (6 декабря 2014 г.). «Производные пиримидо-индола являются новыми агонистами самовосстановления гемопоэтических стволовых клеток пуповинной крови» . Кровь . 124 (21): 650. DOI : 10,1182 / blood.V124.21.650.650 .