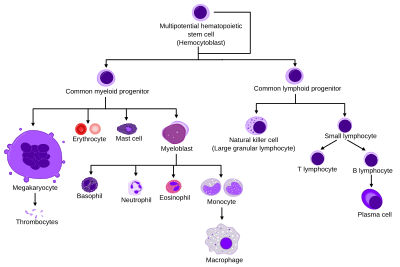
Гемопоэз ( / ч ɪ ˌ м æ т oʊ р ɔɪ я с ɪ ы , ч я м ə т oʊ -, ˌ ч ɛ м ə - / , [1] из греческого αἷμα , 'крови' и ποιεῖν « , чтобы сделать '; также hematopoiesis в американском английском; иногда также h (a) emopoiesis ) - образование кровиклеточные компоненты. Все клеточные компоненты крови происходят из гемопоэтических стволовых клеток . [2] У здорового взрослого человека ежедневно вырабатывается примерно 10 11 –10 12 новых клеток крови для поддержания стабильного уровня в периферическом кровообращении. [3] [4] [ необходима страница ]
Процесс [ править ]
Гематопоэтические стволовые клетки (HSC) [ править ]
Гематопоэтические стволовые клетки (HSC) находятся в мозговом веществе кости ( костном мозге ) и обладают уникальной способностью давать начало всем различным типам зрелых клеток крови и тканям. [2] HSC являются самообновляющимися клетками: когда они дифференцируются, по крайней мере, некоторые из их дочерних клеток остаются в виде HSC, поэтому пул стволовых клеток не истощается. Это явление называется асимметричным делением. [5] Другие дочерние клетки HSC ( миелоидные и лимфоидные клетки-предшественники) могут следовать любым другим путям дифференцировки, которые приводят к производству одного или нескольких конкретных типов клеток крови, но не могут обновляться. Пул предшественников неоднороден.и можно разделить на две группы; длительные самообновляющиеся HSC и только временно самообновляющиеся HSC, также называемые краткосрочными. [6] Это один из основных жизненно важных процессов в организме.
Типы ячеек [ править ]
Все клетки крови делятся на три линии. [7]
- Красные кровяные тельца , также называемые эритроцитами, являются клетками, переносящими кислород . Эритроциты функционируют и попадают в кровь. Количество ретикулоцитов, незрелых эритроцитов, дает оценку скорости эритропоэза .
- Лимфоциты - это краеугольный камень адаптивной иммунной системы. Они происходят от обычных лимфоидных предшественников. Лимфоидная линия состоит из Т-клеток , В-клеток и естественных клеток-киллеров . Это лимфопоэз .
- Клетки миелоидной линии, которые включают гранулоциты , мегакариоциты и макрофаги , происходят от общих миелоидных предшественников и участвуют в таких разнообразных ролях, как врожденный иммунитет и свертывание крови . Это миелопоэз .
Гранулопоэз (или гранулоцитопоэз) - это кроветворение гранулоцитов, за исключением тучных клеток, которые являются гранулоцитами, но с экстрамедуллярным созреванием. [8]
Мегакариоцитопоэз - это кроветворение мегакариоцитов.
Терминология [ править ]
Между 1948 и 1950 годами Комитет по уточнению номенклатуры клеток и болезней крови и кроветворных органов опубликовал отчеты о номенклатуре клеток крови. [9] [10] Обзор терминологии показан ниже, от самой ранней до последней стадии разработки:
- [корень] взрыв
- про [корень] цита
- [корень] цита
- мета [корневая] цита
- имя зрелой клетки
Корень для колониеобразующих единиц эритроцитов (КОЕ-Е) - «rubri», для колониеобразующих единиц гранулоцит-моноцит (КОЕ-ГМ) - «грануло» или «миело» и «моно», для колониеобразующих единиц лимфоцитов. (КОЕ-Л) - это «лимфо», а для колониеобразующих единиц мегакариоцитов (КОЕ-мег) - «мегакарио». Согласно этой терминологии, этапами образования эритроцитов являются: рубрибласт, прорубрицит, рубрицит, метарубрицит и эритроцит. Однако в настоящее время наиболее распространенной является следующая номенклатура:
| Комитет | "лимфо" | "рубри" | «грануло» или «миело» | "мононуклеоз" | «мегакарио» |
|---|---|---|---|---|---|
| Происхождение | Лимфоидный | Миелоидный | Миелоидный | Миелоидный | Миелоидный |
| КОЕ | КОЕ-Л | КОЕ-ГЕММ → КОЕ-Э | КОЕ-ГЕММ → КОЕ-ГМ → КОЕ-G | КОЕ-ГЕММ → КОЕ-ГМ → КОЕ-М | КОЕ-ГЭММ → КОЕ-мег |
| Процесс | лимфоцитопоэз | эритропоэз | гранулоцитопоэз | моноцитопоэз | тромбоцитопоэз |
| [корень] взрыв | Лимфобласт | Проэритробласт | Миелобласт | Монобласт | Мегакариобласт |
| про [корень] цита | Пролимфоцит | Полихроматофильный эритроцит | Промиелоцит | Промоноцит | Промегакариоцит |
| [корень] цита | - | Нормобласт | Эозино / нейтро / базофильный миелоцит | Мегакариоцит | |
| мета [корневая] цита | Большой лимфоцит | Ретикулоцит | Эозинофильный / нейтрофильный / базофильный метамиелоцит , эозинофильная / нейтрофильная / базофильная группа клеток | Ранний моноцит | - |
| имя зрелой клетки | Малый лимфоцит | Эритроцит | гранулоциты ( эозино / нейтро / базофилы ) | Моноцит | тромбоциты ( тромбоциты ) |
Остеокласты также возникают из гемопоэтических клеток линии моноцитов / нейтрофилов, в частности CFU-GM.
Местоположение [ править ]
У развивающихся эмбрионов кроветворение происходит в скоплениях клеток крови в желточном мешке, называемых островками крови . По мере развития происходит кроветворение в селезенке , печени и лимфатических узлах . Когда костный мозг развивается, он в конечном итоге берет на себя задачу формирования большей части клеток крови для всего организма. [2] Однако созревание, активация и некоторая пролиферация лимфоидных клеток происходит в селезенке, тимусе и лимфатических узлах. У детей кроветворение происходит в костном мозге длинных костей, таких как бедренная и большеберцовая кость. У взрослых это происходит в основном в области таза, черепа, позвонков и грудины. [11]
Экстрамедуллярный [ править ]
В некоторых случаях при необходимости может возобновиться кроветворная функция печени, тимуса и селезенки. Это называется экстрамедуллярным кроветворением . Это может привести к значительному увеличению размеров этих органов. Во время внутриутробного развития, поскольку кости и, следовательно, костный мозг развиваются позже, печень функционирует как главный кроветворный орган. Следовательно, в процессе развития печень увеличивается. [12] Экстрамедуллярный гемопоэз и миелопоэз могут поставлять лейкоциты при сердечно-сосудистых заболеваниях и воспалениях в зрелом возрасте. [13] [14] селезенка макрофаги и молекула адгезии могут быть вовлечены в регулировании экстрамедуллярного поколения миелоидных клеток всердечно-сосудистые заболевания . [15] [16]
Созревание [ править ]
- Морфологические характеристики гемопоэтических клеток показаны при окраске по Райту, окраске по Май-Гимзе или окраске по Маю-Грюнвальду-Гимза. В скобках указаны альтернативные названия определенных ячеек.
- Некоторые клетки могут иметь несколько характерных черт. В этих случаях было включено более одного представления одной и той же ячейки.
- Вместе моноциты и лимфоциты составляют агранулоциты, в отличие от гранулоцитов (базофилов, нейрофилов и эозинофилов), которые образуются во время гранулопоэза.
- B., N. и E. обозначают базофильный, нейтрофильный и эозинофильный соответственно - как в случае базофильного промиелоцита. Для лимфоцитов фактическими обозначениями являются Т и В.
- Полихромный эритроцит (ретикулоцит) справа показывает свой характерный внешний вид при окрашивании метиленовым синим или лазурью B.
- Эритроцит справа является более точным представлением его реального внешнего вида при просмотре через микроскоп.
- Другие клетки, возникающие из моноцита: остеокласт, микроглия (центральная нервная система), клетка Лангерганса (эпидермис), клетка Купфера (печень).
- Для ясности, T- и B-лимфоциты разделены, чтобы лучше указать, что плазматическая клетка возникает из B-клетки. Обратите внимание, что нет никакой разницы во внешнем виде B- и T-клеток, если не применяется специфическое окрашивание.
По мере созревания стволовая клетка претерпевает изменения в экспрессии генов, которые ограничивают типы клеток, которыми она может стать, и приближают ее к определенному типу клеток ( клеточная дифференцировка ). Эти изменения часто можно отследить, отслеживая присутствие белков на поверхности клетки. Каждое последующее изменение приближает ячейку к окончательному типу ячейки и дополнительно ограничивает ее потенциал, чтобы стать ячейкой другого типа.
Определение клеточной судьбы [ править ]
Были предложены две модели кроветворения: детерминизм и стохастическая теория. [17] Для стволовых клеток и других недифференцированных клеток крови в костном мозге определение обычно объясняется теорией детерминизма гематопоэза, согласно которой колониестимулирующие факторы и другие факторы гемопоэтического микроокружения определяют, что клетки следуют определенному пути развития. дифференцировка клеток. [2] Это классический способ описания кроветворения. В стохастической теориинедифференцированные клетки крови случайным образом дифференцируются в определенные типы клеток. Эта теория была подтверждена экспериментами, показывающими, что в популяции гематопоэтических клеток-предшественников мыши лежащая в основе стохастическая изменчивость в распределении Sca-1 , фактора стволовых клеток , подразделяет популяцию на группы, демонстрирующие переменную скорость клеточной дифференцировки . Например, под влиянием эритропоэтина (фактора дифференцировки эритроцитов) субпопуляция клеток (определяемая уровнями Sca-1) дифференцировалась в эритроциты в семь раз быстрее, чем остальная популяция. [18] Кроме того, было показано, что если дать возможность расти, эта субпопуляция восстановит исходную субпопуляцию клеток, подтверждая теорию о том, что это стохастический обратимый процесс. Еще один уровень, на котором может иметь значение стохастичность, - это процесс апоптоза и самообновления. В этом случае гемопоэтическое микроокружение преобладает над тем, чтобы некоторые клетки выжили, а некоторые, с другой стороны, совершили апоптоз и умирали. [2] Регулируя этот баланс между различными типами клеток, костный мозг может изменять количество различных клеток, которые в конечном итоге будут производиться. [19]
Факторы роста [ править ]
Производство красных и белых кровяных телец регулируется с большой точностью у здоровых людей, а производство лейкоцитов быстро увеличивается во время инфекции. Размножение и самообновление этих клеток зависят от факторов роста. Одним из ключевых участников самообновления и развития гемопоэтических клеток является фактор стволовых клеток (SCF) [22], который связывается с рецептором c-kit на HSC. Отсутствие SCF смертельно. Существуют и другие важные факторы роста гликопротеинов, которые регулируют пролиферацию и созревание, такие как интерлейкины IL-2 , IL-3 , IL-6 , IL-7 . Другие факторы, называемые колониестимулирующими факторами(CSF), специфически стимулируют продукцию коммитированных клеток. Три CSF представляют собой CSF гранулоцитов-макрофагов (GM-CSF), CSF гранулоцитов (G-CSF) и CSF макрофагов (M-CSF). [23] Они стимулируют образование гранулоцитов и действуют либо на клетки-предшественники, либо на клетки конечного продукта.
Эритропоэтин необходим для того, чтобы миелоидная клетка-предшественник стала эритроцитом. [20] С другой стороны, тромбопоэтин заставляет миелоидные клетки-предшественники дифференцироваться в мегакариоциты ( тромбоцит- образующие клетки). [20] На диаграмме справа представлены примеры цитокинов и дифференцированных клеток крови, которые они вызывают. [24]
Факторы транскрипции [ править ]
Факторы роста инициируют пути передачи сигналов, которые приводят к активации факторов транскрипции . Факторы роста вызывают разные результаты в зависимости от комбинации факторов и стадии дифференцировки клетки. Например, длительная экспрессия PU.1 приводит к миелоидному обязательству, а кратковременная индукция активности PU.1 приводит к образованию незрелых эозинофилов. [25] Недавно было сообщено, что факторы транскрипции, такие как NF-κB, могут регулироваться микроРНК (например, miR-125b) в гематопоэзе. [26]
Первым ключевым участником дифференцировки от HSC до мультипотентного предшественника (MPP) является фактор транскрипции CCAAT-энхансер, связывающий белок α ( C / EBP α). Мутации в C / EBPα связаны с острым миелоидным лейкозом . [27] С этого момента клетки могут дифференцироваться либо по линии эритроид-мегакариоцитов, либо по лимфоидной и миелоидной клонам, у которых есть общий предшественник, называемый мультипотентным предшественником с лимфоидным примированием. Есть два основных фактора транскрипции. PU.1 для линии эритроид-мегакариоцитов и GATA-1 , который приводит к лимфоидно-примированному мультипотентному предшественнику. [ необходима цитата ]
Другие факторы транскрипции включают Ikaros [28] ( развитие В-клеток ) и Gfi1 [29] (способствует развитию Th2 и ингибирует Th1) или IRF8 [30] ( базофилы и тучные клетки ). Примечательно, что определенные факторы вызывают разные ответы на разных стадиях гематопоэза. Например, CEBPα в развитии нейтрофилов или PU.1 в развитии моноцитов и дендритных клеток. Важно отметить, что процессы не являются однонаправленными: дифференцированные клетки могут восстанавливать атрибуты клеток-предшественников.
Примером является фактор PAX5 , который важен для развития В-клеток и связан с лимфомами. [31] Неожиданно оказалось, что мыши с условным нокаутом pax5 позволили периферическим зрелым В-клеткам дедифференцироваться до ранних предшественников костного мозга. Эти находки показывают, что факторы транскрипции действуют как хранители уровня дифференцировки, а не только как инициаторы. [32]
Мутации факторов транскрипции тесно связаны с раком крови, таким как острый миелоидный лейкоз (ОМЛ) или острый лимфобластный лейкоз (ОЛЛ). Например, известно, что Икарос является регулятором множества биологических событий. Мышам без Ikaros не хватает В-клеток , естественных киллеров и Т-клеток . [33] Икарос имеет шесть доменов с цинковыми пальцами , четыре из которых являются консервативными ДНК-связывающими доменами и два предназначены для димеризации . [34]Очень важным открытием является то, что разные цинковые пальцы участвуют в связывании с разными участками ДНК, и это является причиной плейотропного эффекта Икароса и различного вовлечения в рак, но в основном это мутации, связанные с пациентами с BCR-Abl, и это плохой прогностический маркер. . [35]
Другие животные [ править ]
У некоторых позвоночных гематопоэз может возникать там, где есть рыхлая строма соединительной ткани и замедленное кровоснабжение, например, в кишечнике , селезенке или почках . [36]
См. Также [ править ]
- Клональный гемопоэз
- Средства, стимулирующие эритропоэз
- Гематон
- Стимуляторы кроветворения:
- Гранулоцитарный колониестимулирующий фактор
- Гранулоцитарный макрофагальный колониестимулирующий фактор
- Экстравазация лейкоцитов
Ссылки [ править ]
- ^ «кроветворение» . Dictionary.com Полный . Случайный дом . Дата обращения 16 октября 2019 .
- ^ a b c d e Бирбрайр, Александр; Френетт, Пол С. (1 марта 2016 г.). «Неоднородность ниши в костном мозге» . Летопись Нью-Йоркской академии наук . 1370 (1): 82–96. Bibcode : 2016NYASA1370 ... 82B . DOI : 10.1111 / nyas.13016 . ISSN 1749-6632 . PMC 4938003 . PMID 27015419 .
- ^ Семестр 4 медицинские лекции в Университете Упсалы 2008 Лейфом Янссоном
- ^ Парслоу TG, Stites DP, Terr AI, Imboden JB. Медицинская иммунология (1-е изд.). ISBN 978-0-8385-6278-9.
- ^ Моррисон, Дж .; Джудит Кимбл (2006). «Асимметричные и симметричные деления стволовых клеток в развитии и раке» (PDF) . Природа . 441 (7097): 1068–74. Bibcode : 2006Natur.441.1068M . DOI : 10,1038 / природа04956 . ЛВП : 2027,42 / 62868 . PMID 16810241 . S2CID 715049 .
- ^ Morrison SJ, Вайсман IL (ноябрь 1994). «Подмножество долгосрочных репопуляций гемопоэтических стволовых клеток детерминировано и может быть выделено по фенотипу». Иммунитет . 1 (8): 661–73. DOI : 10.1016 / 1074-7613 (94) 90037-X . PMID 7541305 .
- ^ «Кроветворение из плюрипотентных стволовых клеток» . Библиотека ресурсов антител . ThermoFisher Scientific . Проверено 25 апреля 2020 года .
- Перейти ↑ Mahler (2013). Хашек, Ванда; Руссо, Колин Дж .; Валлиг, Мэтью А. (ред.). Справочник Хашека и Руссо по токсикологической патологии . младшие редакторы Брэд Болон и Рикардо Очоа; редактор иллюстраций, Бет В. (Третье изд.). [Sl]: Academic Press. п. 1863. ISBN. 978-0-12-415759-0.
- ^ «ПЕРВЫЙ отчет комиссии по уточнению номенклатуры клеток и болезней крови и кроветворных органов» . Американский журнал клинической патологии . 18 (5): 443–50. Май 1948 г. doi : 10.1093 / ajcp / 18.5_ts.443 . PMID 18913573 .
- ^ «ТРЕТИЙ, четвертый и пятый доклады комиссии по уточнению номенклатуры клеток и болезней крови и кроветворных органов» . Американский журнал клинической патологии . 20 (6): 562–79. Июнь 1950 г. doi : 10.1093 / ajcp / 20.6.562 . PMID 15432355 .
- Перейти ↑ Fernández KS, de Alarcón PA (декабрь 2013 г.). «Развитие системы кроветворения и нарушения кроветворения, которые проявляются в младенчестве и раннем детстве» . Детские клиники Северной Америки . 60 (6): 1273–89. DOI : 10.1016 / j.pcl.2013.08.002 . PMID 24237971 .
- ^ Georgiades CS, Нейман EG, Фрэнсис ИК, Sneider MB, Fishman EK (ноябрь 2002). «Типичные и атипичные проявления экстрамедуллярного кроветворения» . AJR. Американский журнал рентгенологии . 179 (5): 1239–43. DOI : 10,2214 / ajr.179.5.1791239 . PMID 12388506 .
- ^ Свирски, Филип К .; Либби, Питер; Айкава, Елена; Алькаид, Пилар; Лусцинскас, Ф. Уильям; Вайследер, Ральф; Питте, Микаэль Дж. (2 января 2007 г.). «Моноциты Ly-6Chi доминируют над моноцитозом, связанным с гиперхолестеринемией, и дают начало макрофагам в атеромах» . Журнал клинических исследований . 117 (1): 195–205. DOI : 10.1172 / JCI29950 . PMC 1716211 . PMID 17200719 .
- ^ Свирски ФК, Нарендорф М, Etzrodt М, Wildgruber М, Кортес-Retamozo В, Паницци Р, Фигуэйреду ДЛ, Колер RH, Чудновский А, Waterman , Р, Аикава Е, Mempel TR, Либби Р, Weissleder R, Pittet МДж (30 июля 2009 г.). «Идентификация моноцитов селезеночного резервуара и их развертывание в очагах воспаления» . Наука . 325 (5940): 612–616. Bibcode : 2009Sci ... 325..612S . DOI : 10.1126 / science.1175202 . PMC 2803111 . PMID 19644120 .
- ^ Датта, P; Хойер, Ф. Ф.; Григорьева Л.С.; Sager, HB; Leuschner, F; Courties, G; Бородовский, А; Новобранцева, Т; Руда, ВМ; Фитцджеральд, К; Ивамото, Y; Войткевич, G; Солнце, Y; Да Силва, N; Либби, П; Андерсон, Д.Г.; Свирски, Ф. К.; Weissleder, R; Нахрендорф, М. (6 апреля 2015 г.). «Макрофаги удерживают гемопоэтические стволовые клетки в селезенке через VCAM-1» . Журнал экспериментальной медицины . 212 (4): 497–512. DOI : 10,1084 / jem.20141642 . PMC 4387283 . PMID 25800955 .
- ^ Датта, P; Хойер, Ф. Ф.; Солнце, Y; Ивамото, Y; Трико, B; Weissleder, R; Magnani, JL; Свирски, Ф. К.; Нахрендорф, М. (сентябрь 2016 г.). «Ингибирование E-селектина снижает активацию HSC селезенки и миелопоэз у мышей с гиперхолестеринемией и инфарктом миокарда» . Артериосклероз, тромбоз и биология сосудов . 36 (9): 1802–8. DOI : 10.1161 / ATVBAHA.116.307519 . PMC 5001901 . PMID 27470513 .
- Перейти ↑ Kimmel, Marek (1 января 2014 г.). «Стохастичность и детерминизм в моделях кроветворения». Подход системной биологии к крови . Успехи экспериментальной медицины и биологии . 844 . С. 119–152. DOI : 10.1007 / 978-1-4939-2095-2_7 . ISBN 978-1-4939-2094-5. ISSN 0065-2598 . PMID 25480640 .
- ^ Чанг, Ханна Х .; Хемберг, Мартин; Бараона, Маурисио; Ingber, Donald E .; Хуанг, Суй (2008). «Шум транскриптома контролирует выбор клонов в клетках-предшественниках млекопитающих» . Природа . 453 (7194): 544–547. Bibcode : 2008Natur.453..544C . DOI : 10,1038 / природа06965 . PMC 5546414 . PMID 18497826 .
- ^ Аленци, FQ; Alenazi, BQ; Ахмад, SY; Салем, ML; Аль-Джабри, AA; Вайс, РК (март 2009 г.). «Гемопоэтические стволовые клетки: между апоптозом и самообновлением» . Йельский журнал биологии и медицины . 82 (1): 7–18. PMC 2660591 . PMID 19325941 .
- ^ a b c d Молекулярная клеточная биология. Лодиш, Харви Ф. 5. изд. : - Нью-Йорк: WH Freeman and Co., 2003, 973 с. законопроект. ISBN 0-7167-4366-3
Лодиш Х, Берк А, Зипурски С.Л., Мацудаира П., Балтимор Д., Дарнелл Дж. (2000). «Рак возникает в пролиферирующих клетках». Молекулярная клеточная биология (4-е изд.). Нью-Йорк: WH Freeman. Рисунок 24-8: Формирование дифференцированных клеток крови из гемопоэтических стволовых клеток в костном мозге. ISBN 0-7167-3136-3 - через NCBI Bookshelf. - ^ Цветок жезла; Хамфри П. Ранг; Морин М. Дейл; Риттер, Джеймс М. (2007). Фармакология Рэнга и Дейла . Эдинбург: Черчилль Ливингстон. ISBN 978-0-443-06911-6.
- ^ Broudy, VC (15 августа 1997). «Фактор стволовых клеток и кроветворение» . Кровь . 90 (4): 1345–64. DOI : 10.1182 / blood.V90.4.1345 . PMID 9269751 .
- ^ Кетли, Нью-Джерси; AC Newland (1997). «Гемопоэтические факторы роста» . Исследование уровня J Med . 73 (858): 215–221. DOI : 10.1136 / pgmj.73.858.215 . PMC 2431295 . PMID 9156123 .
- ^ Хауке, Ральф; Стефано Р. Тарантоло (ноябрь 2000 г.). «Гемопоэтические факторы роста» . Лабораторная медицина . 31 (11): 613–5. DOI : 10,1309 / HNTM-ELUV-AV9G-MA1P .
- ^ Энгель, я; Мюрр, К. (октябрь 1999 г.). «Факторы транскрипции в кроветворении» . Текущее мнение в области генетики и развития . 9 (5): 575–9. DOI : 10.1016 / s0959-437x (99) 00008-8 . PMID 10508690 .
- ^ О'Коннелл, R; Rao, D .; Балтимор, Д. (2012). «Регуляция воспалительных реакций микроРНК» . Ежегодный обзор иммунологии . 30 : 295–312. DOI : 10,1146 / annurev-Immunol-020711-075013 . PMID 22224773 .
- ^ Хо, Пенсильвания; Алонзо, Т.А.; Гербинг, РБ; Поллард, Дж; Стируолт, DL; Гурвиц, К; Heerema, NA; Хирш, Б. Раймонди, Южная Каролина; Lange, B; Франклин, JL; Радич, JP; Мешинчи, С (25 июня 2009 г.). «Распространенность и прогностические последствия мутации CEBPA при остром миелоидном лейкозе у детей (ОМЛ): отчет Детской онкологической группы» . Кровь . 113 (26): 6558–66. DOI : 10.1182 / кровь-2008-10-184747 . PMC 2943755 . PMID 19304957 .
- ^ Томпсон, Элизабет С .; Cobb, Bradley S .; Саббаттини, Пиерангела; Мейкслспергер, Соня; Парельо, Ваня; Либерг, Дэвид; Тейлор, Бенджамин; Диллон, Найл; Георгопулос, Катя (1 марта 2007 г.). «ДНК-связывающие белки Ikaros как неотъемлемые компоненты регуляторных цепей, специфичных для стадии развития В-клеток» . Иммунитет . 26 (3): 335–344. DOI : 10.1016 / j.immuni.2007.02.010 . ISSN 1074-7613 . PMID 17363301 .
- ↑ Судзуки, Дзюнпей; Маруяма, Сахо; Тамаути, Хидекадзу; Кувахара, Макото; Хориучи, Мика; Мизуки, Масуми; Очи, Мизуки; Савасаки, Тацуя; Чжу, Цзиньфан (1 апреля 2016 г.). «Gfi1, репрессор транскрипции, ингибирует индукцию программы Т-хелперов типа 1 в активированных Т-лимфоцитах CD4» . Иммунология . 147 (4): 476–487. DOI : 10.1111 / imm.12580 . ISSN 1365-2567 . PMC 4799889 . PMID 26749286 .
- ^ Сасаки, Харука; Куротаки, Дайсуке; Тамура, Томохико (1 апреля 2016 г.). «Регуляция развития базофилов и тучных клеток с помощью факторов транскрипции» . Международная аллергология . 65 (2): 127–134. DOI : 10.1016 / j.alit.2016.01.006 . ISSN 1440-1592 . PMID 26972050 .
- ^ О'Брайен, P; Морин, П., младший; Ouellette, RJ; Робишо, Джорджия (15 декабря 2011 г.). «Ген Pax-5: плюрипотентный регулятор дифференцировки В-клеток и раковых заболеваний» . Исследования рака . 71 (24): 7345–50. DOI : 10.1158 / 0008-5472.CAN-11-1874 . PMID 22127921 .
- ^ Cobaleda, C; Jochum, W; Busslinger, M (27 сентября 2007 г.). «Превращение зрелых В-клеток в Т-клетки путем дедифференцировки в незарегистрированные предшественники» . Природа . 449 (7161): 473–7. Bibcode : 2007Natur.449..473C . DOI : 10,1038 / природа06159 . PMID 17851532 . S2CID 4414856 .
- ^ Ван, JH; Nichogiannopoulou, A; Wu, L; Вс, л; Шарп, AH; Бигби, М; Георгопулос, К. (декабрь 1996 г.). «Избирательные дефекты в развитии лимфоидной системы плода и взрослого у мышей с нулевой мутацией Ikaros» . Иммунитет . 5 (6): 537–49. DOI : 10.1016 / s1074-7613 (00) 80269-1 . PMID 8986714 .
- ^ Солнце, L; Лю, А; Георгопулос, К. (1 октября 1996 г.). «Белковые взаимодействия, опосредованные цинковыми пальцами, модулируют активность Ikaros, молекулярный контроль развития лимфоцитов» . Журнал EMBO . 15 (19): 5358–69. DOI : 10.1002 / j.1460-2075.1996.tb00920.x . PMC 452279 . PMID 8895580 .
- ^ Schjerven, H; Маклафлин, Дж; Arenzana, TL; Frietze, S; Cheng, D; Wadsworth, SE; Лоусон, GW; Бенсингер, SJ; Фарнхэм, П.Дж.; Витте, О.Н. Смейл, СТ (октябрь 2013 г.). «Избирательная регуляция лимфопоэза и лейкемогенеза отдельными цинковыми пальцами Икароса» . Иммунология природы . 14 (10): 1073–83. DOI : 10.1038 / ni.2707 . PMC 3800053 . PMID 24013668 .
- ↑ Zon, LI (15 октября 1995 г.). «Биология развития кроветворения» . Кровь (Обзор). 86 (8): 2876–91. DOI : 10.1182 / blood.V86.8.2876.2876 . PMID 7579378 .
Дальнейшее чтение [ править ]
- Годин, Изабель; Кумано, Ана, ред. (2006). Развитие гемопоэтических стволовых клеток . Springer. ISBN 978-0-306-47872-7.
Внешние ссылки [ править ]
| У Схолии есть тематический профиль « Гематопоэз» . |
- Клоны гемопоэтических клеток в KEGG
- Кроветворение и гистология костного мозга