В химии , гомолиз (от греческого ὅμοιος, homoios, «равно» и λύσις, Лусиса, «разрыхление») или гомолитического деление является химической связью диссоциация молекулярной связи с помощью способа , в котором каждый из фрагментов (атом или молекула) сохраняет один из изначально связанных электронов. При гомолитическом делении нейтральной молекулы с четным числом электронов будут образовываться два свободных радикала . [1] То есть два электрона, участвующие в исходной связи, распределяются между двумя видами фрагментов. Энергия, участвующая в этом процессе, называется энергией диссоциации связи (BDE). [2]Расщепление связи также возможно с помощью процесса, называемого гетеролизом .
Бонд энергия диссоциации определяются как «энтальпия (на моль) , необходимой для разорвать данную связь какого - то конкретный молекулярного субъекта путем гомолизом,» символизирует , как D . [3] Энергия диссоциации связи зависит от прочности связи, которая определяется факторами, связанными со стабильностью образующихся радикалов.
Из-за относительно высокой энергии, необходимой для такого разрыва связей, гомолиз происходит в первую очередь при определенных обстоятельствах:
- Свет (например, ультрафиолетовое излучение)
- Высокая температура
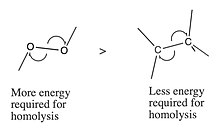
- Некоторые внутримолекулярные связи, такие как связь O – O пероксида , достаточно слабы, чтобы спонтанно гомолитически диссоциировать с небольшим количеством тепла.
- Высокие температуры в отсутствие кислорода ( пиролиз ) могут вызвать гомолитическое удаление углеродных соединений . [4]
- Большинство связующих гомолизуются при температурах выше 200 ° C. [5]
Кроме того, в некоторых случаях давление может вызвать образование радикалов. [6]
Эти условия перемещают электроны на следующую по высоте молекулярную орбиталь, создавая, таким образом, одиночную молекулярную орбиталь (или SOMO).
Факторы, вызывающие гомолиз [ править ]
Гомолитическое расщепление обусловлено способностью молекулы поглощать энергию света или тепла и энергией диссоциации связи ( энтальпией ). Если радикалы лучше способны стабилизировать свободный радикал, энергия одиночно занятой молекулярной орбитали будет снижена, как и энергия диссоциации связи. Энергия диссоциации связи определяется несколькими факторами: [5]
- Электроотрицательность
- Менее электроотрицательные атомы являются лучшими стабилизаторами радикалов, а это означает, что связь между двумя электроотрицательными атомами будет иметь более высокий BDE, чем аналогичная молекула с двумя менее электроотрицательными атомами. [5]
- Поляризуемость
- Чем больше электронное облако, тем лучше атом может стабилизировать радикал (т.е. йод очень поляризуем и является радикальным стабилизатором). [5]
- Орбитальная гибридизация
- S-характер орбитали связан с тем, насколько близко электроны находятся к ядру. В случае радикала s-характер более конкретно относится к тому, насколько близко одиночный электрон находится к ядру. Стабильность радикалов уменьшается по мере приближения к ядру, потому что сродство орбитали к электрону увеличивается. Как правило, гибридизация, сводящая к минимуму s-характер, увеличивает стабильность радикалов и снижает энергию диссоциации связи (т.е. sp3-гибридизация является наиболее стабилизирующей). [7]
- Резонанс
- Радикалы могут быть стабилизированы путем передачи отрицательного заряда из резонанса, или, другими словами, [делокализация электронов].
- Гиперконъюгация
- Углеродные радикалы стабилизируются сверхсопряжением, что означает, что более замещенные атомы углерода более стабильны и, следовательно, имеют более низкие БДЭ.
- В 2005 году Гронерт предложил альтернативную гипотезу, включающую облегчение стерического напряжения группы заместителей (в отличие от ранее принятой парадигмы, которая предполагает, что углеродные радикалы стабилизируются через алкильные группы). [9]
- Captodative Эффект
- Радикалы могут быть стабилизированы за счет синергетического эффекта заместителей как электроноакцепторной группы, так и электронодонорной группы .
- Уводящие электроны группы часто содержат пустые π * -орбитали с низкой энергией и перекрываются с SOMO, создавая две новые орбитали: одну с меньшей энергией, стабилизирующуюся относительно радикала, и пустую орбиталь с более высокой энергией. Точно так же электронодонорные орбитали объединяются с радикалом SOMO, позволяя неподеленной паре терять энергию, а радикалу переходить на новую орбиталь с более высокой энергией. Это взаимодействие является чистой стабилизацией. [5]
См. Также [ править ]
Ссылки [ править ]
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) « гомолиз (гомолитический) ». DOI : 10,1351 / goldbook.H02851
- Перейти ↑ St. John, PC, Guan, Y., Kim, Y. et al. Прогнозирование энтальпий диссоциации органических гомолитических связей с точностью, близкой к химической, с вычислительными затратами менее секунды. Нац Коммуна 11, 2328 (2020). https://doi.org/10.1038/s41467-020-16201-z
- ^ ИЮПАК. Сборник химической терминологии, 2-е изд. («Золотая книга»). Составлено AD McNaught и A. Wilkinson. Научные публикации Блэквелла, Оксфорд (1997). Онлайн-версия (2019-), созданная SJ Chalk. ISBN 0-9678550-9-8 . https://doi.org/10.1351/goldbook .
- ^ I. Пасторова, "Структура полукокса целлюлозы: комбинированное аналитическое исследование Py-GC-MS, FTIR и ЯМР", Carbohydrate Research, 262 (1994) 27-47.
- ^ a b c d e Клейден, Джонатан, Гривз, Ник, Уоррен, Стюарт. (2012). Органическая химия (второе изд.). Оксфорд: ОУП. ISBN 978-0-19-927029-3
- ^ Кристина LEKIN, Хоа Phan, Стивен М. Винтер, Joanne WL Wong, Alicea А. Leitch, Доминик Laniel, Wenjun Юн, Ричард А. Secco, Джон С. Ца, Serge Desgreniers, Пол А. Дуб, Майкл Шатрук, и Ричард T. Oakley "Взаимное превращение бисдитиазолиловых радикалов и димеров под действием тепла, давления и света", журнал Американского химического общества, 2014 г., 136 (22), 8050-8062 DOI: 10.1021 / ja502753t.
- ^ Менденхалл, G. (1978). Долгоживущие свободные радикалы. Science Progress (1933-), 65 (257), 1-18. Получено 5 декабря 2020 г. с http://www.jstor.org/stable/43420441.
- ^ Хольгер, С.П. Мюллер и др., J. Chem. Phys. 107, 8292 (1997); https://doi.org/10.1063/1.475030
- ^ J. Org. Chem. 2006, 71, 3, 1209–1219 Дата публикации: 4 января 2006 г. https://doi.org/10.1021/jo052363t