| Nanophyetus salmincola | |
|---|---|
| Научная классификация | |
| Королевство: | |
| Тип: | |
| Учебный класс: | |
| Род: | |
| Разновидность: | N. salmincola |
| Биномиальное имя | |
| Nanophyetus salmincola ( Чапин ) | |
| Синонимы | |
Troglotrema salmincola | |
Nanophyetus salmincola является пищевым происхождением кишечной трематоды паразита распространен на Тихоокеанском северо - западе побережья. Этот вид может быть наиболее распространенным эндемиком трематод в Соединенных Штатах. [1]
Жизненный цикл N. salmincola требует трех хозяев . Первый промежуточный хозяин представляет собой Juga plicifera поток улитки . Вторым промежуточным хозяином является лососевая рыба, хотя некоторые нелососевые рыбы также играют роль. Наконец, окончательным хозяином чаще всего является псовых, хотя многие другие млекопитающие также являются окончательными хозяевами, включая человека. Передача N. salmincola окончательному хозяину происходит при поедании зараженной паразитами рыбы.
Паразит наиболее известен своей связью с « болезнью отравления лососем », которая, если ее не лечить, смертельна для собак и других собак. Однако псовых поражают бактерии Neorickettsia helminthoeca , переносчиками которых является N. salmincola , а не сам паразит.
В литературе обнаружено очень мало известных случаев естественного заражения человека N. salmincola , хотя вполне вероятно, что о многих случаях не сообщается, поскольку у большинства людей симптомы отсутствуют или проявляются неспецифическими симптомами, такими как дискомфорт в желудочно-кишечном тракте. [2] Заболевание, вызванное N. salmincola , или нанофитеаз , легко предотвратить, тщательно приготовив рыбу перед употреблением. Случаев заражения человека бактериями Rickettsia, переносимыми N. salmincola, не известно .
Подвидовой паразит, Nanophyetus schikhobalowi , является эндемиком Сибири , где случаи нанофитеоза у людей описаны в научной литературе с 1931 года [3].
Открытие [ править ]
Первое сообщение об отравлении лососем (SPD) было зарегистрировано на северо-западе Орегона в 1814 году, когда автор журнала Henry's Astoria Journal отметил смерть собак после употребления в пищу сырого лосося . [4] [5] Сначала исследователи полагали, что SPD был вызван ядовитой кровью в съеденной рыбе. [6] В 1911 году маленькие белые кисты наблюдались в почках болезнетворных лососей и форели, но они были ошибочно идентифицированы как амебы. [5] Маленькие трематоды в кишечнике собак, умерших после поедания инфицированного лосося, были наконец обнаружены в 1925 году, и цисты, присутствующие в лососе, были правильно идентифицированы как промежуточные стадии трематод. [7]В ходе последующего экспериментального исследования исследователи показали, что паразиты тонкого кишечника действительно вызывают ШРЛ у собак и что цисты действительно развиваются во взрослого червя, обнаруженного в кишечнике. [8]
Впервые трематода была названа Чапином как Nanophyes salmincola в 1926 году как член семейства Heterophyidae. [9] После дальнейшего изучения морфологии Чапин назначил трематоду семейству Troglotrematidae и переименовал паразита в Nanophyetus salmincola , поскольку Nanophyes уже был захвачен. [10] Дискуссии относительно правильности классификации паразита продолжались, поскольку трематода получила дальнейшее научное внимание, а ее морфология и поведение подверглись дальнейшему изучению. В конечном итоге было принято решение о Nanophyetus salmincola , хотя Troglotrema salmincola остается синонимом.
В 1931 году Скрябин и Подяпольская описали похожего паразита, Nanophyetus schikhobalowi , который был эндемиком Восточной Сибири. Аргумент относительно того, были ли N. schikhobalowi и N. salmincola одними и теми же или разными видами, повторялся до 1966 года, когда им был предоставлен статус подвидов, чтобы отразить их биологические и географические различия, но незначительные морфологические различия. [11] [12] [13] С момента своего открытия N. schikhobalowi , как известно, естественным образом заражает людей, и исследования показывают, что уровень инфицирования в эндемичных сибирских деревнях достигает 98%. [2]
Напротив, N. salmincola не была признана источником инфекции до тех пор, пока исследователь целенаправленно не заразил себя в научном эксперименте в 1958 году. [14] Помимо экспериментального заражения Филипа североамериканской N. salmincola , первым человеком, приобретенным естественным путем. Случаи кишечной инфекции наблюдались в период с сентября 1974 г. по октябрь 1985 г. [2] В ходе исследования было выявлено 10 пациентов с положительным результатом на N. salmincolaобразцы стула и либо желудочно-кишечные жалобы, либо иным образом необъяснимая эозинофилия периферической крови. 7 пациентов вспомнили, что употребляли недоваренную или сырую рыбу. У тех, кому не было назначено эффективное лечение, симптомы и / или яйца в стуле сохранялись в течение 2 или более месяцев, прежде чем они спонтанно исчезли. Было высказано предположение, что движение, прикрепление и раздражение взрослых червей на слизистой оболочке тонкой кишки было вероятной причиной желудочно-кишечных симптомов и периферической эозинофилии. [2]
Через два года после того, как в 1987 г. были зарегистрированы первые 10 случаев заражения человека N. salmincola , Fritsche et al. сообщили о десяти дополнительных случаях нанофитеоза человека. [15] У пяти из них были жалобы со стороны желудочно-кишечного тракта, а у других пяти была необъяснимая периферическая эозинофилия. Девять из десяти вспомнили, что ели неправильно приготовленную рыбу. На этот раз эффективным методом выбора был празиквантел.
В 1990 г. был зарегистрирован первый случай заражения человека N. salmincola без употребления в пищу сырой или недоваренной зараженной рыбы. [1] Мужчина заразился в результате заражения рук при обращении с сильно зараженным свежезабитым кижуча. Диагноз нанофитеаз был поставлен на основании желудочно-кишечного дискомфорта, эзоинофилии периферической крови и положительного анализа стула. Лечение празиквантелом оказалось эффективным.
Ни в одном из случаев заражения людей североамериканскими или сибирскими подвидами не было обнаружено заражение Neorickettsia helminthoeca, переносимое трематодой, которое было обнаружено в 1950 году. Заражение риккетсией помогает объяснить более смертельный исход, поражающий псовых.
Клинические проявления у людей [ править ]
При заражении N. salmincola у людей обычно нет симптомов . Если симптомы присутствуют, они обычно неспецифичны и ошибочно принимаются за указание на другие желудочно-кишечные проблемы. Симптомы включают «диарею, необъяснимую эозинофилию периферической крови, дискомфорт в животе, тошноту и рвоту, потерю веса и усталость». [2] Яйца N. salmincola появляются в стуле примерно через неделю после употребления зараженной рыбы. [14]
Патология у собак [ править ]
Нанофизиаз у собак намного серьезнее, чем у людей. Ученые почти 200 лет назад заметили, что собаки, которые ели сырую рыбу, иногда довольно быстро умирали. Это «отравление лососем», связанное с трематодой Nanophyetus salmincola , не вызвано червем. Болезнь вызывается Neorickettsia helminthoeca , риккетсиозной бактерией, которая использует N. salmincola в качестве хозяина. Хотя к заболеванию восприимчивы только собаки, у енотов после заражения риккетсией повышается температура и наблюдается лимфатическая инфекция, но оба вскоре проходят. [16]Инкубационный период у собак составляет 5–7 дней, хотя может длиться до 33 дней. После начала болезни наблюдается резкая лихорадка в сочетании с анорексией, рвотой и дизентерией. Риккетсия поражает лимфатическую систему собаки, вызывая увеличение и, в конечном итоге, кровоизлияние во многие лимфатические узлы. Заболевание может распространяться на другие ткани, например, на лейкоциты. Смерть наступает через 10–14 дней после появления первых признаков.
Передача [ править ]
Nanophyetus salmincola чаще всего передается при употреблении в пищу сырого, недоваренного или копченого лосося или стальной форели. Обычно это означает проглатывание мышц рыбы, но были сообщения о случаях, когда предполагаемым возбудителем передачи была икра стальной головы. Исследователи предполагают, что у рыб с особенно высоким содержанием гельминтов N. salmincola может мигрировать во многие ткани рыб, а не только в мышечную ткань. В 1990 году в одном случае нанофитеаз был диагностирован у человека, который, как считается, заразился этим заболеванием в результате простого обращения со свежеубитым лососем. По иронии судьбы, инфицированный человек был исследователем, изучавшим N.salmincola у молоди кижуча, который непреднамеренно инициировал инфекцию при контакте руки в рот во время трехмесячного исследования. [17]
Резервуар [ править ]
Резервуаром N. salmincola являются еноты, норка и скунсы. [4] [5] [12] Резервуары - это организмы, которые несут в себе паразитов без каких-либо признаков патологии и распространяют паразитов благодаря своему естественному поведению. Например, еноты естественным образом распространяют N. salmincola, потому что они часто едят рыбу и испражняют яйца паразитов в воде или рядом с водой, где последующие личиночные стадии могут продолжать свой жизненный цикл. [12]
Вектор [ править ]
Переносчики - это организмы, которые передают паразитов от одного хозяина к другому. Улитки ручья Juga plicifera являются биологическими переносчиками личиночной стадии N. salmincola . Лососевые и некоторые нелососевые рыбы являются переносчиками метацеркарий N. salmincola. Переносчиками паразита могут быть как пресноводные, так и морские рыбы. Вторыми промежуточными хозяевами являются рыбы, принадлежащие к разным видам семейств Salmonidae, Cottidae и Cyprinidae. Среди тридцати четырех естественных и экспериментальных вторичных хозяев, обнаруженных в научной литературе, являются прибрежная форель-головорез, радужная форель, кижуча, кета и лосось кокани. [5]Больше заражения встречается у лососевых рыб, чем у нелососевых. В частности, лососевые рыбы родов Salmo, Oncorhynchus и Salvelinus играют значительную роль в жизненном цикле N. salmincola . [12] [18] Сам паразит также является переносчиком Neorickettsia helminthoeca .
Окончательные хосты [ править ]
Окончательные хозяева включают рыбоядных птиц и млекопитающих. Наиболее частыми окончательными хозяевами являются домашняя собака, кошка и рыжая лисица. [5] Люди также являются окончательными хозяевами N. salmincola . Длинный список экспериментальных окончательных хозяев включает хомяка и древесную крысу. В ходе экспериментального исследования не удалось заразить двух белых крыс и двух белых мышей. Трематоды существуют по всей длине тонкой кишки у более мелких животных, таких как хомяки, в то время как они существуют только в верхнем конце тонкой кишки у более крупных животных, таких как собаки. [12]
Инкубационный период [ править ]
После употребления в пищу рыбы, зараженной N. salmincola , симптомы проявляются примерно через 1 неделю, а именно в стуле обнаруживаются икры.
Морфология [ править ]
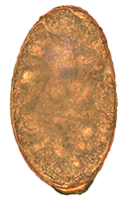
Яйца N. salmincola светло-коричневые, яйцевидные, с крышечками на одном конце и с небольшим тупым выступом на другом конце. Они измеряют от 0,087 мм до 0,097 мм от 0,038 мм до 0,055 мм. [12] Обычно в матке находится от 5 до 16 яиц, и их тяжесть позволяет им быстро тонуть в воде. [12]
N. salmincola - дигенная трематода, что означает, что это несегментированный червь, сплющенный дорсовентрально. Взрослые черви меняют форму от «шара до длинного тупого стержня». [12] Черви от 0,8 до 1,1 мм в длину и от 0,3 до 0,5 мм в ширину являются гермафродитами, так как мужские и женские репродуктивные органы находятся в одном организме. Два больших овальных семенника имеют длину от 0,2 до 0,3 мм, а круглый яичник - от 0,07 до 0,11 мм в диаметре. [11] N. salmincola имеет выступающий мешок цирруса или полый орган, окружающий копулятивный орган самца, но не имеет семенных пузырьков. Сохраняя свой характер трематоды, он имеет оральную присоску диаметром от 0,15 до 0,18 мм и вентральную присоску диаметром от 0,12 до 0,13 мм. [11]Ротовые и вентральные присоски используются для того, чтобы активно хвататься за кишечную ткань своего хозяина и активно ползать по ним, хотя червь не оставляет серьезных механических повреждений. [12]
Жизненный цикл [ править ]
Взрослый особь откладывает яйца внутри позвоночного-хозяина. Позвоночное животное выделяет яйца с фекалиями. Первая личиночная стадия, мирацидии, развиваются внутри яиц, вылупляются и уплывают. Затем мирацидии проникают в первого промежуточного хозяина - ручейную улитку Juga plicifera . После дальнейшего развития в ручье улитка N. salmincolaличинки развиваются в редии, которые дают начало церкариям. Церкарии выходят из улитки и проникают через второго промежуточного хозяина, лососевых (некоторые не лососевые) рыбы. Паразиты развиваются в метацеркарии и энцистируют в почках, мышцах и плавниках лососевых рыб. Паразиты проникают в своего последнего хозяина, включая псовых и людей, после проглатывания инфицированной рыбы и развиваются во взрослых червей, которые производят яйца, которые передаются с фекалиями хозяина. [19]
Подробная информация об этапах жизненного цикла [ править ]
Яйца и мирацидии: яйца, выходящие с фекалиями, не являются эмбриональными . Экспериментальные исследования показывают, что для вылупления яиц, собранных при комнатной температуре, требуется от 75 до 200 дней. [12] [20] Скорость вылупления мирацидий из яиц увеличивается с понижением температуры, а смертность яиц увеличивается с повышением температуры. [12] Полностью развитые мирацидии внутри яиц многократно сжимаются и удлиняются, а недавно появившиеся мирацидии плавают «характерными длинными изящными изгибами». [12] Мирацидии, похоже, не привлекают улиток, натыкаясь на них, не пытаясь проникнуть в них и заразить их. [12]
Редии: Редии - это вторая личиночная стадия жизненного цикла трематод, которая развивается из мирацидума и содержит половые клетки, которые развиваются в церкарии. Редии находятся у второго промежуточного хозяина - улитки. Редии могут составлять от 0,45 мм до 3 мм, а более крупные редии могут содержать до 76 церкарий. [12] Редии и церкарии обнаруживаются во всех тканях улитки-хозяина, но в первую очередь в гонадах и пищеварительной железе., [5] [12] Редии разрушают гонады, вторгаются в гепатопанкреас, повреждают ее 1) повышенным давлением из-за быстрый рост, 2) активное потребление паразитами, и 3) удаление паразитарных отходов. Кроме того, паразиты поглощают гликоген и липиды из гепатопанкреаса. [5]
Церкарии: церкарии имеют размеры от 0,31 до 0,47 мм, от 0,03 до 0,15 мм и живут в воде до 48 часов. Они имеют тенденцию заражать улиток длиной не менее 2,5 см, хотя наблюдались и более мелкие улитки, которые выделяют церкарии. [12] Церкарии периодически сбрасываются тысячами, попадая в полость мантии улитки и дрейфуя с «выдыхаемым потоком воды с правой стороны головы улитки». [5] [12] Церкарии из улиток в солоноватой воде с низкой соленостью выживают дольше, чем улитки в пресной воде.
После того, как церкарии отделяются от улитки, она многократно сжимается, пока не коснется рыбы и не проникает под ее кожу в течение от 30 секунд до 2 минут. Церкарии проникают дальше в почечную систему воротной крови, в почки и более глубокие ткани в основание хвоста. Места проникновения хорошо видны, так как кожа, плавники и хвосты рыбы выглядят сильно эродированными и поврежденными. [12] Церкарии также могут косвенно инфицировать рыбу, если рыба поедает церкарии орально. [5]
Метацеркарии: церкарии теряют хвост в акте проникновения и инцистируются как метацеркарии почти в любой ткани лососевых рыб. Стенка новой кисты тонкая, прозрачная и легко разрывается. Если стенка кисты разрывается, метацеркарии выползают и через несколько часов повторно образуются в более жесткой стенке кисты большего размера. [12] В то время как цисты можно найти во всех тканях рыбы, большая часть энцистментации происходит в почках и мышцах тела лососевых рыб, а также в жабрах и плавниках нелососевых рыб. У нелососевых рыб церкарии проникают меньше, чем у лососевых. [5] Инфицированные рыбы испытывают снижение плавательной активности и потерю равновесия, и у рыб нередко бывает от 1000 до 2000 метацеркарий в тканях.,[12] [21]
Важно отметить, что метацеркарии можно уничтожить путем приготовления или замораживания инфицированной рыбы. [2]
Улитка: Ju plicifera хозяин улитка распространена в прибрежных потоках и предпочитает крупные камни, мосты, старые доски и мусор на дне ручья днищ. Редко мигрирует на мелководье. Зараженность улиток высока по сравнению с количеством сбрасываемых ими церкарий, поскольку развитие личинок продолжается медленно в течение длительного периода времени. [12] Доказательства смешанной инфекции варьировались между исследованиями, но улитки с большим количеством N. salmincola не были паразитированы другими трематодами. [22]Также было обнаружено, что ежемесячная частота инфицирования улиток колеблется от 9 до 52% после обследования более 3000 улиток каждый месяц в течение 10 месяцев, и что половозрелые церкарии заражали улиток сезонным образом. Зрелые церкарии чаще заражали улиток в конце апреля - ноябре. [22]
Neorickettsia helmintheoca Neorickettsia helmintheoca является этиологическим агентом отравления лососем, который, как установлено, присутствует на всех стадиях трематод. Его размер составляет 0,3 микрометра, а пурпурное пятно Гимзы указывает на грамотрицательный результат. До сих пор только собаки восприимчивы к риккетсии, и все еще неясно, как риккетсия покидает трематодный переносчик и достигает тканей хозяина. Эксперименты действительно показывают, что бактерии вызывают некроз лимфатических фолликулов, изъязвление и сильное кровотечение у хозяина. [5]
Диагностические тесты [ править ]
- История употребления в пищу сырой рыбы
- Исследование кала на яйца N. salmincola
- Поскольку в каждом взрослом черве содержится всего несколько яиц, у пациентов с легкими инфекциями, вероятно, будут отрицательные анализы стула. Использование препаратов, окрашенных трихромом, а не концентратов формалин-этилацетат было более чувствительным для выявления случаев. [2]
Управление и терапия [ править ]
Празиквантел, 20 мг / кг массы тела, 3 раза в день. Празиквантел вызывает иммобилизованное сокращение червя, так что он больше не может захватывать стенки кишечника и может выводиться из организма. Три дозы никлозамида по 2 г или две дозы битионола по 50 мг / кг также были эффективны, когда празиквантел был недоступен или в лечении было отказано. [2] Однако однократная доза никлозамина 2 г оказалась неэффективной, как и 100 мг мебендазола перорально два раза в день в течение трех дней. Если диарея рецидивирует, также могут потребоваться общие добавки для поддержания электролитного баланса и удовлетворения потребностей в питании.
Эпидемиология [ править ]
Nanophyetus salmincola ограничен географическим диапазоном своих промежуточных хозяев, в первую очередь Тихоокеанским Северо-Западом США. Улитки водятся к западу от Каскадных гор в Орегоне, к северу от полуострова Олимпик в Вашингтоне и в некоторых частях северной Калифорнии. [2] Это «самая распространенная системная трематода в США». [23]
Стратегии общественного здравоохранения и профилактики [ править ]
- Тщательно готовьте рыбу
- Заморозить рыбу минимум на 24 часа.
- Ловите рыбу вдали от известных мест, где обитают улитки (в противном случае, особенно тщательно готовьте рыбу).
- Соблюдайте меры предосторожности при обращении с рыбой (предотвращайте передачу метацеркарий из рук в рот и остерегайтесь заражения рук сильно инфицированной рыбой)
- Периодически проверяйте рыбу на наличие признаков инфекции, таких как кисты или участки раздражения от проникновения церкарарий (актуально для рыболовных компаний, рыбных рынков и ресторанов).
- Сообщите об источниках зараженной рыбы (водоемы, рыбные предприятия, рестораны)
- Ешьте сырую рыбу только из проверенных источников, например из авторитетных ресторанов.
- Используйте моллюскициды, если их можно практически использовать в небольших водоемах.
- Держите собак подальше от ручьев, убедившись, что они испражняются вдали от мест обитания улиток.
Ссылки [ править ]
- ^ а б Харрелл, LW; Дирдорф, Т.Л. (1990). «Нанофитеаз человека: передача при контакте с естественно инфицированным кижучем (Oncorhynchus kisutch)». Журнал инфекционных болезней . 161 (1): 146–148. DOI : 10.1093 / infdis / 161.1.146 . PMID 2295848 .
- ^ Б с д е е г ч я Eastburn, RL; Fritsche, TR; Терхьюн, Калифорния младший (1987). «Кишечная инфекция человека, вызванная Nanophyetus salmincola из лососевых рыб». Am J Trop Med Hyg . 36 (3): 586–91. PMID 3578655 .
- ^ Скрябин, KJ, и Podjapolskaja, WP, (1931). Nanophyetus schikhobalowi, n. sp., em neuer Trematode aus Darm des Menschen. Zlb. Ba / ct. I. Ориг., 119: 294–297.
- ^ а б Мин, Элайджа. Нанофитеиоз . 2003. Стэнфордский университет. 12 февраля 2009 г.
- ^ a b c d e f g h i j k Millemann, RE; Knapp, SE. (1970). «Биология Nanophyetus salmincola и болезнь« отравление лососем ». Adv. Паразитология . Успехи паразитологии. 8 : 1–41. DOI : 10.1016 / S0065-308X (08) 60250-X . ISBN 978-0-12-031708-0.
- ^ Торнтон, JQ (1849). «Орегон и Калифорния в 1848 году». Том 1, Harper & Bros.
- ^ Donham, CR (1925a). Наука 61: 341.
- ^ Donham, CR, Симмс, BT и Миллер, FW (1926). Варенье. Вет. Med. Жопа. 68: 701–715
- ^ Чапин, EA (1926). N. Am. Вет. 7: 36–37.
- ^ Чапин, EA (1928) J. Parasitol. 14: 60.
- ^ a b c Витенбург, Г. (1932). «Об анатомии и систематическом положении возбудителя так называемого отравления лососем». J. Parasitol . 18 (4): 258–263. DOI : 10.2307 / 3271558 . JSTOR 3271558 .
- ^ a b c d e f g h i j k l m n o p q r s t u Bennington, E .; И. Пратт (1960). "История жизни двуустки, отравленной лососем, Nanophyetus salmincola (Chapin)". Журнал паразитологии (46): 91–100.
- ↑ Филимонова, Л.В. (1966). Пер. Гельминт. Лаборатория. Акад. Sci. СССР 17, 240–244.
- ^ а б Филипп, CB (1958). Proc. 10-й Int. Congr. Ent., Монреаль , 1956, 3: 651–653.
- ^ Fritsche TR, Eastburn RL, Wiggins LH, Terhune CA Jr. (1989) Празиквантел для лечения инфекции человека Nanophyetus salmincola (Troglotrema salmincola). 160 (5): 896-9.
- ^ RE Milleman и SE Knapp, "Биология Nanopheyus Salmincola и" болезнь отравления лососем "Advanced Parasitology, 8 (1970): 33
- ^ Ли В. Харрелл и Томас Дирдорф "Человеческий нанофитеаз: передача путем обработки естественно инфицированного лосося кижуча" Журнал инфекционных заболеваний, 161-1 (1990): 146
- ^ Витенбург, Г. (1932) Об анатомии и систематическом положении возбудителя так называемого отравления лососем. J. Parasitol. 18: 258–263.
- ^ Джон, Дэвид Т. и Уильям А. Петри, младший Маркелл и медицинская паразитология Воге. Сент-Луис: Elsevier Inc., 2006.
- ^ Simms, BT; Donham, CR; Шоу, Дж. Н. (1931). «Отравление лососем». Являюсь. J. Hyg . 13 : 363–391.
- ^ Baldwin, NL, Millemann, RE и Кнапп, SE (1967). J. Parasitol. 53: 556–564.
- ^ a b Гебхардт, Г.А., Миллеман, Р.Е., Кнапп, С.Е., и Ниберг, штат Пенсильвания (1966). J. Parasitol. 52: 54–59.
- ^ ГИДЕОН. www.gideononline.com