Флуоресцентная спектроскопия
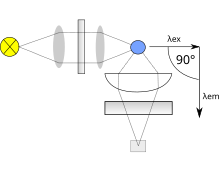
Флуоресцентная спектроскопия (также известная как флуориметрия или спектрофлуориметрия ) представляет собой тип электромагнитной спектроскопии , который анализирует флуоресценцию образца. Он включает использование луча света, обычно ультрафиолетового света , который возбуждает электроны в молекулах определенных соединений и заставляет их излучать свет; обычно, но не обязательно, видимый свет . Дополнительным методом является абсорбционная спектроскопия . В частном случае флуоресцентной спектроскопии одиночных молекул колебания интенсивности испускаемого света измеряются либо отдельными флуорофорами, либо парами флуорофоров.
Молекулы имеют различные состояния, называемые энергетическими уровнями . Флуоресцентная спектроскопия в первую очередь связана с электронными и колебательными состояниями. Как правило, исследуемые виды имеют интересующее основное электронное состояние (состояние с низкой энергией) и возбужденное электронное состояние с более высокой энергией. Внутри каждого из этих электронных состояний существуют различные колебательные состояния. [1]
При флуоресценции вещество сначала возбуждается, поглощая фотон , из основного электронного состояния в одно из различных колебательных состояний в возбужденном электронном состоянии. Столкновения с другими молекулами заставляют возбужденную молекулу терять колебательную энергию до тех пор, пока она не достигнет самого низкого колебательного состояния из возбужденного электронного состояния. Этот процесс часто визуализируют диаграммой Яблонского . [1]
Затем молекула снова падает на один из различных колебательных уровней основного электронного состояния, испуская при этом фотон. [1] Поскольку молекулы могут опускаться на любой из нескольких колебательных уровней в основном состоянии, излучаемые фотоны будут иметь разные энергии и, следовательно, частоты. Следовательно, анализируя различные частоты света, излучаемого при флуоресцентной спектроскопии, наряду с их относительной интенсивностью, можно определить структуру различных колебательных уровней.
Для атомарных видов процесс аналогичен; однако, поскольку атомы не имеют уровней колебательной энергии, испускаемые фотоны часто имеют ту же длину волны, что и падающее излучение. Этот процесс повторного излучения поглощенного фотона называется «резонансной флуоресценцией», и, хотя он характерен для атомной флуоресценции, он также наблюдается и для молекулярной флуоресценции. [2]
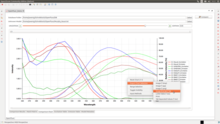
В типичном измерении флуоресценции (эмиссии) длина волны возбуждения фиксирована, а длина волны обнаружения варьируется, в то время как при измерении возбуждения флуоресценции длина волны обнаружения фиксирована, а длина волны возбуждения варьируется в интересующей области. Карта излучения измеряется путем записи спектров излучения, полученных в результате диапазона длин волн возбуждения, и их объединения вместе. Это трехмерный набор данных о поверхности: интенсивность излучения как функция длин волн возбуждения и излучения, и обычно он изображается в виде контурной карты.