Виртуальный скрининг ( VS ) - это вычислительная техника, используемая при открытии лекарств для поиска в библиотеках малых молекул с целью выявления тех структур, которые с наибольшей вероятностью будут связываться с мишенью для лекарства , обычно с белковым рецептором или ферментом . [2] [3]
Виртуальный скрининг определяется как «автоматическая оценка очень больших библиотек соединений» с использованием компьютерных программ. [4] Как следует из этого определения, VS в основном представляла собой числовую игру, в которой основное внимание уделялось огромному химическому пространству, содержащему более 10 60 возможных соединений [5]можно отфильтровать до управляемого числа, которое можно синтезировать, купить и протестировать. Хотя поиск по всей химической вселенной может быть теоретически интересной проблемой, более практичные сценарии VS сосредоточены на разработке и оптимизации целевых комбинаторных библиотек и обогащении библиотек доступных соединений из собственных репозиториев соединений или предложений поставщиков. По мере того как точность метода возросла, виртуальный скрининг стал неотъемлемой частью процесса открытия лекарств . [6] [1] Виртуальный скрининг можно использовать для выбора соединений из внутренней базы данных для скрининга, выбора соединений, которые могут быть приобретены за пределами США, и выбора соединения, которое должно быть синтезировано следующим.
Методы [ править ]
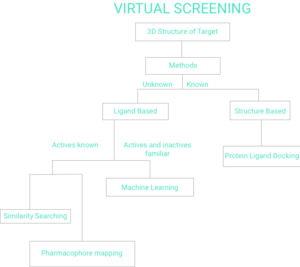
Существует две широкие категории методов скрининга: на основе лиганда и на основе структуры. [7] Остальная часть этой страницы будет отражать блок-схему виртуального скрининга на Рисунке 1.
На основе лиганда [ править ]
Учитывая набор структурно разнообразных лигандов, которые связываются с рецептором , модель рецептора может быть построена путем использования коллективной информации, содержащейся в таком наборе лигандов. Они известны как фармакофорные модели. Затем кандидатный лиганд можно сравнить с моделью фармакофора, чтобы определить, совместим ли он с ним и, следовательно, может ли он связываться. [8]
Другой подход к виртуальному скринингу на основе лигандов заключается в использовании методов двумерного анализа химического сходства [9] для сканирования базы данных молекул по одной или нескольким активным структурам лиганда.
Популярный подход к виртуальному скринингу на основе лигандов основан на поиске молекул, форма которых аналогична форме известных активных веществ, поскольку такие молекулы будут соответствовать сайту связывания мишени и, следовательно, будут связываться с мишенью. В литературе имеется ряд перспективных приложений этого класса методов. [10] [11] [12] Фармакофорные расширения этих трехмерных методов также доступны бесплатно в виде веб-серверов. [13] [14]
На основе структуры [ править ]
Виртуальный скрининг на основе структуры включает стыковку кандидатов-лигандов с белком-мишенью с последующим применением оценочной функции для оценки вероятности связывания лиганда с белком с высокой аффинностью. [15] [16] [17] Веб-серверы, ориентированные на перспективный виртуальный просмотр, доступны всем. [18] [19]
Гибридные методы [ править ]
Гибридные методы, основанные на сходстве структур и лигандов, также были разработаны для преодоления ограничений традиционных подходов VLS. Эти методологии используют основанную на эволюции информацию о связывании лигандов для предсказания связывающих малых молекул [20] [21] и могут использовать как глобальное структурное сходство, так и подобие карманов. [20] Подход, основанный на глобальном структурном подобии, использует как экспериментальную структуру, так и предсказанную модель белка, чтобы найти структурное сходство с белками в библиотеке голотемплат PDB. После обнаружения значительного структурного сходства, показатель коэффициента Танимото на основе двумерных отпечатков пальцев применяется для скрининга малых молекул, которые похожи на лиганды, извлеченные из выбранных шаблонов holo PDB. [22] [23] Предсказания этого метода были экспериментально оценены и показывают хорошее обогащение в идентификации активных малых молекул.
Указанный выше метод зависит от общего структурного сходства и не позволяет априори выбрать конкретный лиганд-связывающий сайт в интересующем белке. Кроме того, поскольку методы основаны на оценке двухмерного сходства лигандов, они не способны распознавать стереохимическое сходство небольших молекул, которые существенно отличаются, но демонстрируют сходство геометрической формы. Для решения этих проблем был разработан и экспериментально оценен новый подход, ориентированный на карманы, PoLi, способный воздействовать на специфические связывающие карманы в голопротеиновых матрицах .
Вычислительная инфраструктура [ править ]
Вычисление парных взаимодействий между атомами, которое является предпосылкой для работы многих программ виртуального скрининга, имеет вычислительную сложность, где N - количество атомов в системе. Из-за квадратичного масштабирования по отношению к количеству атомов вычислительная инфраструктура может варьироваться от портативного компьютера для метода на основе лиганда до мэйнфрейма для метода на основе структуры.
На основе лиганда [ править ]
Методы на основе лигандов обычно требуют доли секунды для одной операции сравнения структур. Одного процессора достаточно, чтобы выполнить большой просмотр за несколько часов. Однако можно провести несколько сравнений параллельно, чтобы ускорить обработку большой базы данных соединений.
На основе структуры [ править ]
Размер задачи требует параллельной вычислительной инфраструктуры , такой как кластер систем Linux , с запущенным процессором очереди пакетной обработки для обработки работы, например Sun Grid Engine или Torque PBS.
Требуются средства обработки ввода из больших составных библиотек. Для этого требуется форма составной базы данных, которая может запрашиваться параллельным кластером, доставляя соединения параллельно различным вычислительным узлам. Коммерческие механизмы баз данных могут быть слишком громоздкими, и лучшим выбором может быть высокоскоростной механизм индексирования, такой как Berkeley DB . Кроме того, может быть неэффективным запускать одно сравнение для каждого задания, потому что время разгона узлов кластера может легко превысить объем полезной работы. Чтобы обойти это, необходимо обрабатывать пакеты соединений в каждом задании кластера, объединяя результаты в своего рода файл журнала. Вторичный процесс для анализа файлов журналов и извлечения кандидатов с высокими показателями может быть запущен после того, как весь эксперимент будет проведен.
Точность [ править ]
Целью виртуального скрининга является идентификация молекул новой химической структуры, которые связываются с интересующей макромолекулярной мишенью . Таким образом, успех виртуального экрана определяется с точки зрения поиска новых интересных каркасов, а не общего количества совпадений. Поэтому к интерпретациям точности виртуального скрининга следует относиться с осторожностью. Ясно, что низкие показатели попадания интересных каркасов предпочтительнее высоких показателей уже известных каркасов.
Большинство тестов виртуальных скрининговых исследований в литературе ретроспективны. В этих исследованиях эффективность метода VS измеряется его способностью извлекать небольшой набор ранее известных молекул, обладающих сродством к интересующей мишени (активные молекулы или просто активные компоненты), из библиотеки, содержащей гораздо более высокую долю предполагаемых неактивных или приманки. Напротив, в перспективных приложениях виртуального скрининга полученные совпадения подвергаются экспериментальному подтверждению (например, измерениям IC 50 ). Существует консенсус в отношении того, что ретроспективные эталоны не являются хорошими предикторами предполагаемой эффективности, и, следовательно, только проспективные исследования представляют собой убедительное доказательство пригодности метода для конкретной цели. [24] [25] [26][27] [28]
Приложение к открытию лекарств [ править ]
Виртуальный скрининг - очень полезное приложение, когда дело доходит до идентификации молекул-ударов как основы медицинской химии. По мере того как подход виртуального скрининга становится все более важным и существенным методом в индустрии медицинской химии, этот подход быстро расширяется. [29]
Методы на основе лигандов [ править ]
Не зная структуры, пытаюсь предсказать, как лиганды будут связываться с рецептором. С использованием фармакофорных особенностей каждый лиганд идентифицируется как донор, так и акцепторы. Приравниваемые элементы накладываются друг на друга, однако маловероятно, что существует единственное правильное решение. [1]
Модели фармакофоров [ править ]
Этот метод используется при объединении результатов поиска с использованием разных эталонных соединений, одинаковых дескрипторов и коэффициентов, но разных активных соединений. Этот метод полезен, потому что он более эффективен, чем использование одной эталонной структуры вместе с наиболее точной производительностью, когда дело касается различных активных объектов. [1]
Фармакофор - это совокупность стерических и электронных свойств, которые необходимы для оптимального супрамолекулярного взаимодействия или взаимодействий с биологической структурой-мишенью, чтобы вызвать ее биологический ответ. Выберите представителя как набор активных, большинство методов будут искать похожие привязки. Желательно иметь несколько жестких молекул, и лиганды должны быть разнообразными, другими словами, обеспечить наличие различных свойств, которые не проявляются во время фазы связывания. [1]
Структура [ править ]
Постройте составную прогнозную модель на основе известных активных и известных неактивных знаний. QSAR (количественно-структурная взаимосвязь деятельности), которая ограничена небольшим однородным набором данных. SAR (отношение структуры и активности), где данные обрабатываются качественно и могут использоваться со структурными классами и более чем одним режимом привязки. Модели отдают предпочтение соединениям для обнаружения потенциальных клиентов. [1]
Машинное обучение [ править ]
Чтобы использовать машинное обучение для этой модели виртуального скрининга, необходим обучающий набор с известными активными и известными неактивными соединениями. Также существует модель деятельности, которая затем вычисляется посредством субструктурного анализа, рекурсивного разбиения, опорных векторных машин , k-ближайших соседей и нейронных сетей . Последний шаг - определение вероятности того, что соединение является активным, а затем ранжирование каждого соединения на основе его вероятности быть активным. [1]
Субструктурный анализ в машинном обучении [ править ]
Первая модель машинного обучения, используемая для больших наборов данных, - это анализ субструктуры, который был создан в 1973 году. Каждая субструктура фрагмента вносит непрерывный вклад в действие определенного типа. [1] Субструктура - это метод, который преодолевает трудности, связанные с огромной размерностью, когда дело доходит до анализа структур при разработке лекарств. Эффективный анализ каркаса используется для конструкций, которые имеют сходство с многоуровневым зданием или башней. Геометрия используется для нумерации граничных швов данной конструкции в начале и ближе к кульминации. При разработке метода специальной статической конденсации и подпрограмм замен этот метод оказался более продуктивным, чем предыдущие модели анализа субструктур. [30]
Рекурсивное разбиение [ править ]
Рекурсивное разделение - это метод, который создает дерево решений с использованием качественных данных. Понимание того, как правила разбивают классы с небольшой ошибкой неправильной классификации при повторении каждого шага до тех пор, пока не будет найдено разумных разделений. Однако рекурсивное разбиение может иметь плохую предсказательную способность, потенциально создавая точные модели с той же скоростью. [1]
Структурные методы стыковки известных белковых лигандов [ править ]
Лиганд может связываться с активным сайтом в белке, используя алгоритм поиска стыковки и функцию подсчета очков, чтобы идентифицировать наиболее вероятную причину для отдельного лиганда при назначении порядка приоритета. [1] [31]
См. Также [ править ]
- Грид-вычисления
- Скрининг с высокой пропускной способностью
- Док (молекулярный)
- Функции подсчета очков
- База данных ZINC
Ссылки [ править ]
- ^ Б с д е е г ч я J Гиллет В (2013). «Виртуальный скрининг на основе лигандов и структур» (PDF) . Университет Шеффилда.
- ^ Rester U (июль 2008). «От виртуальности к реальности - виртуальный скрининг при обнаружении и оптимизации потенциальных клиентов: перспективы медицинской химии». Текущее мнение в области открытия и разработки лекарств . 11 (4): 559–68. PMID 18600572 .
- ^ Rollinger JM, Stuppner Н, Лангер Т (2008). «Виртуальный скрининг для открытия биологически активных натуральных продуктов». Природные соединения в качестве лекарственных средств Том I . Прогресс в исследованиях лекарств. Fortschritte der Arzneimittelforschung. Progrès des Recherches Pharmaceutiques . Прогресс в исследованиях лекарств. 65 . С. 211, 213–49. DOI : 10.1007 / 978-3-7643-8117-2_6 . ISBN 978-3-7643-8098-4. PMC 7124045 . PMID 18084917 .
- ^ Walters WP, Stahl MT, Murcko MA (1998). «Виртуальный просмотр - обзор». Drug Discov. Сегодня . 3 (4): 160–178. DOI : 10.1016 / S1359-6446 (97) 01163-X .
- ^ Bohacek RS, McMartin C, Гуида WC (1996). «Искусство и практика структурного дизайна лекарств: перспектива молекулярного моделирования». Med. Res. Ред . 16 (1): 3–50. DOI : 10.1002 / (SICI) 1098-1128 (199601) 16: 1 <3 :: AID-MED1> 3.0.CO; 2-6 . PMID 8788213 .
- ↑ McGregor MJ, Luo Z, Jiang X (11 июня 2007 г.). «Глава 3: Виртуальный скрининг при открытии лекарств». В Хуан Z (ред.). Исследование открытия наркотиков. Новые рубежи в постгеномную эру . Wiley-VCH: Вайнхайм, Германия. С. 63–88. ISBN 978-0-471-67200-5.
- ^ McInnes C (октябрь 2007). «Стратегии виртуального скрининга в открытии лекарств». Текущее мнение в химической биологии . 11 (5): 494–502. DOI : 10.1016 / j.cbpa.2007.08.033 . PMID 17936059 .
- Перейти ↑ Sun H (2008). «Виртуальный скрининг на основе фармакофоров». Современная лекарственная химия . 15 (10): 1018–24. DOI : 10.2174 / 092986708784049630 . PMID 18393859 .
- ^ Виллет P, Барнард JM, Downs GM (1998). «Поиск химического сходства». Журнал химической информации и компьютерных наук . 38 (6): 983–996. CiteSeerX 10.1.1.453.1788 . DOI : 10.1021 / ci9800211 .
- ^ Rush TS, Грант JA, Mosyak L, Николс A (март 2005). «Основанный на форме 3-мерный метод перескока каркаса и его применение к бактериальному межбелковому взаимодействию». Журнал медицинской химии . 48 (5): 1489–95. CiteSeerX 10.1.1.455.4728 . DOI : 10.1021 / jm040163o . PMID 15743191 .
- ^ Ballester PJ, Westwood I, Laurieri N, Sim E, Richards WG (февраль 2010). «Перспективный виртуальный скрининг со сверхбыстрым распознаванием формы: идентификация новых ингибиторов ариламин-N-ацетилтрансфераз» . Журнал Королевского общества, Интерфейс . 7 (43): 335–42. DOI : 10,1098 / rsif.2009.0170 . PMC 2842611 . PMID 19586957 .
- Перейти ↑ Kumar A, Zhang KY (2018). «Достижения в разработке методов подобия форм и их применение в открытии лекарств» . Границы химии . 6 : 315. Bibcode : 2018FrCh .... 6..315K . DOI : 10.3389 / fchem.2018.00315 . PMC 6068280 . PMID 30090808 .
- ↑ Li H, Leung KS, Wong MH, Ballester PJ (июль 2016 г.). «USR-VS: веб-сервер для крупномасштабного перспективного виртуального просмотра с использованием сверхбыстрых методов распознавания форм» . Исследования нуклеиновых кислот . 44 (W1): W436–41. DOI : 10.1093 / NAR / gkw320 . PMC 4987897 . PMID 27106057 .
- ^ Sperandio O, Petitjean M, Tuffery P (июль 2009). «wwLigCSRre: сервер на основе трехмерных лигандов для идентификации и оптимизации попаданий» . Исследования нуклеиновых кислот . 37 (выпуск веб-сервера): W504–9. DOI : 10.1093 / NAR / gkp324 . PMC 2703967 . PMID 19429687 .
- ^ Kroemer RT (август 2007). «Дизайн лекарств на основе структуры: стыковка и оценка». Современная наука о белках и пептидах . 8 (4): 312–28. CiteSeerX 10.1.1.225.959 . DOI : 10.2174 / 138920307781369382 . PMID 17696866 .
- ^ Cavasotto CN, Орри AJ (2007). «Стыковка лигандов и виртуальный скрининг на основе структуры в открытии лекарств». Актуальные темы медицинской химии . 7 (10): 1006–14. DOI : 10.2174 / 156802607780906753 . PMID 17508934 .
- ^ Kooistra AJ, Vischer ВЧ, МакНота-Флорес D, Leurs R, де Esch И.Я., де - Граафа C (2016). «Функциональный виртуальный скрининг лигандов GPCR с использованием комбинированного метода оценки» . Научные отчеты . 6 : 28288. Bibcode : 2016NatSR ... 628288K . DOI : 10.1038 / srep28288 . PMC 4919634 . PMID 27339552 .
- ^ Ирвин JJ, Shoichet BK, Mysinger MM, Huang N, Colizzi F, Wassam P, Cao Y (сентябрь 2009). «Автоматическая стыковка экранов: технико-экономическое обоснование» . Журнал медицинской химии . 52 (18): 5712–20. DOI : 10.1021 / jm9006966 . PMC 2745826 . PMID 19719084 .
- ↑ Li H, Leung KS, Ballester PJ, Wong MH (2014-01-24). "istar: веб-платформа для крупномасштабной стыковки белок-лиганд" . PLOS ONE . 9 (1): e85678. Bibcode : 2014PLoSO ... 985678L . DOI : 10.1371 / journal.pone.0085678 . PMC 3901662 . PMID 24475049 .
- ^ а б Чжоу Х., Сколник Дж. (январь 2013 г.). «FINDSITE (гребешок): подход к скринингу виртуальных лигандов в протеомном масштабе на основе потоков / структуры» . Журнал химической информации и моделирования . 53 (1): 230–40. DOI : 10.1021 / ci300510n . PMC 3557555 . PMID 23240691 .
- ^ Roy A, Skolnick J (февраль 2015). «LIGSIFT: инструмент с открытым исходным кодом для структурного выравнивания лигандов и виртуального скрининга» . Биоинформатика . 31 (4): 539–44. DOI : 10.1093 / биоинформатики / btu692 . PMC 4325547 . PMID 25336501 .
- ^ Gaulton А, Беллис LJ, Бент А.П., Камеры J, Дэвис М, Херсите А, Свет Y, Макглинчите S, D Michalovich, Al-Lazikani В, Оверингтоне JP (январь 2012). «ChEMBL: крупномасштабная база данных по биологической активности для открытия лекарств» . Исследования нуклеиновых кислот . 40 (выпуск базы данных): D1100–7. DOI : 10.1093 / NAR / gkr777 . PMC 3245175 . PMID 21948594 .
- ↑ Wishart DS, Knox C, Guo AC, Shrivastava S, Hassanali M, Stothard P, Chang Z, Woolsey J (январь 2006 г.). «DrugBank: исчерпывающий ресурс для открытия и исследования лекарств in silico» . Исследования нуклеиновых кислот . 34 (выпуск базы данных): D668–72. DOI : 10.1093 / NAR / gkj067 . PMC 1347430 . PMID 16381955 .
- Перейти ↑ Wallach I, Heifets A (2018). «Большинство критериев классификации на основе лигандов поощряют запоминание, а не обобщение». Журнал химической информации и моделирования . 58 (5): 916–932. arXiv : 1706.06619 . DOI : 10.1021 / acs.jcim.7b00403 . PMID 29698607 .
- ^ Ирвин JJ (2008). «Тесты сообщества для виртуального просмотра» . Журнал компьютерного молекулярного дизайна . 22 (3–4): 193–9. Bibcode : 2008JCAMD..22..193I . DOI : 10.1007 / s10822-008-9189-4 . PMID 18273555 . S2CID 26260725 .
- ^ Хорошо AC, Oprea TI (2008). «Оптимизация методов CAMD. 3. Виртуальный скрининг обогащающих исследований: помощь или препятствие в выборе инструмента?» . Журнал компьютерного молекулярного дизайна . 22 (3–4): 169–78. Bibcode : 2008JCAMD..22..169G . DOI : 10.1007 / s10822-007-9167-2 . PMID 18188508 . S2CID 7738182 .
- ^ Шнайдер G (апрель 2010 г.). «Виртуальный просмотр: бесконечная лестница?» . Обзоры природы. Открытие наркотиков . 9 (4): 273–6. DOI : 10.1038 / nrd3139 . PMID 20357802 . S2CID 205477076 .
- ^ Ballester PJ (январь 2011). «Сверхбыстрое распознавание формы: метод и применение». Медицинская химия будущего . 3 (1): 65–78. DOI : 10.4155 / fmc.10.280 . PMID 21428826 .
- ^ Lavecchia A, Di Giovanni C (2013). «Стратегии виртуального скрининга в открытии лекарств: критический обзор». Современная лекарственная химия . 20 (23): 2839–60. DOI : 10.2174 / 09298673113209990001 . PMID 23651302 .
- ^ Gurujee CS, Дешпанд VL (февраль 1978). «Улучшенный метод анализа каркаса». Компьютеры и конструкции . 8 (1): 147–152. DOI : 10.1016 / 0045-7949 (78) 90171-2 .
- ^ Прадипкиран, Джангампалли Ади; Редди, П. Хемачандра (март 2019 г.). «Структурный дизайн и молекулярные исследования докинга для фосфорилированных ингибиторов тау-белка при болезни Альцгеймера» . Ячейки . 8 (3): 260. DOI : 10,3390 / cells8030260 . PMC 6468864 . PMID 30893872 .
Дальнейшее чтение [ править ]
- Melagraki G, Afantitis A, Sarimveis H, Koutentis PA, Markopoulos J, Igglessi-Markopoulou O (май 2007 г.). «Оптимизация антагонистов рецептора MCH1 биарилпиперидина и 4-амино-2-биарилмочевины с использованием моделирования QSAR, методов классификации и виртуального скрининга» . Журнал компьютерного молекулярного дизайна . 21 (5): 251–67. Bibcode : 2007JCAMD..21..251M . DOI : 10.1007 / s10822-007-9112-4 . PMID 17377847 . S2CID 19563229 .
- Афантитис А, Мелаграки Дж., Саримвейс Х., Котентис П.А., Маркопулос Дж., Игглесси-Маркопулу О. (февраль 2006 г.). «Исследование влияния заместителя 1- (3,3-дифенилпропил) -пиперидинилфенилацетамидов на аффинность связывания CCR5 с использованием QSAR и методов виртуального скрининга». Журнал компьютерного молекулярного дизайна . 20 (2): 83–95. Bibcode : 2006JCAMD..20 ... 83A . CiteSeerX 10.1.1.716.8148 . DOI : 10.1007 / s10822-006-9038-2 . PMID 16783600 . S2CID 21523436 .
- Eckert H, Bajorath J (март 2007 г.). «Анализ молекулярного сходства в виртуальном скрининге: основы, ограничения и новые подходы». Открытие наркотиков сегодня . 12 (5–6): 225–33. DOI : 10.1016 / j.drudis.2007.01.011 . PMID 17331887 .
- Виллетт П. (декабрь 2006 г.). «Виртуальный скрининг на основе сходства с использованием 2D-отпечатков пальцев» (PDF) . Открытие наркотиков сегодня (Представленная рукопись). 11 (23–24): 1046–53. DOI : 10.1016 / j.drudis.2006.10.005 . PMID 17129822 .
- Фара, округ Колумбия, Опреа Т.И., Просниц Э.Р., Болога К.Г., Эдвардс Б.С., Скляр Л.А. (2006). «Интеграция виртуального и физического просмотра» . Открытие лекарств сегодня: технологии . 3 (4): 377–385. DOI : 10.1016 / j.ddtec.2006.11.003 . PMC 7105924 .
- Muegge I, Oloffa S (2006). «Успехи в виртуальном просмотре» . Открытие лекарств сегодня: технологии . 3 (4): 405–411. DOI : 10.1016 / j.ddtec.2006.12.002 . PMC 7105922 .
- Шнайдер Г (апрель 2010 г.). «Виртуальный просмотр: бесконечная лестница?» . Обзоры природы. Открытие наркотиков . 9 (4): 273–6. DOI : 10.1038 / nrd3139 . PMID 20357802 . S2CID 205477076 .
Внешние ссылки [ править ]
- VLS3D - список из более чем 2000 баз данных, онлайн и автономных инструментов in silico
