Фармакофор представляет собой абстрактное описание молекулярных функций, которые необходимы для молекулярного распознавания в виде лиганда с биологической макромолекулой . IUPAC определяет фармакофор как «совокупность стерических и электронных свойств, необходимых для обеспечения оптимальных супрамолекулярных взаимодействий с конкретной биологической мишенью и для запуска (или блокирования) ее биологической реакции». [1] Фармакофорная модель объясняет, как различные по структуре лиганды могут связываться с общим рецепторным участком. Кроме того, модели фармакофоров могут использоваться для идентификации посредством дизайна de novo или виртуального скрининга. новые лиганды, которые будут связываться с одним и тем же рецептором.
Особенности [ править ]
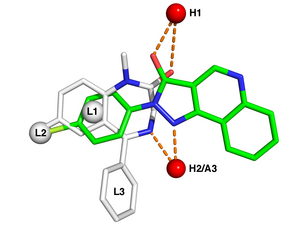
Типичные характеристики фармакофоров включают гидрофобные центроиды, ароматические кольца, акцепторы или доноры водородных связей , катионы и анионы . Эти фармакофорные точки могут быть расположены на самом лиганде или могут быть проекционными точками, предположительно расположенными в рецепторе.
Характеристики должны соответствовать различным химическим группам со схожими свойствами, чтобы идентифицировать новые лиганды. Взаимодействия лиганд-рецептор обычно являются «полярно-положительными», «полярно-отрицательными» или «гидрофобными». Четко определенная фармакофорная модель включает как гидрофобные объемы, так и векторы водородных связей.
Разработка модели [ править ]
Процесс разработки модели фармакофоров обычно включает следующие этапы:
- Выберите обучающий набор лигандов - выберите структурно разнообразный набор молекул, который будет использоваться для разработки модели фармакофоров. Поскольку фармакофорная модель должна иметь возможность различать молекулы с биологической активностью и без нее, набор молекул должен включать как активные, так и неактивные соединения.
- Конформационный анализ - Создайте набор низкоэнергетических конформаций, которые, вероятно, будут содержать биоактивную конформацию для каждой из выбранных молекул.
- Молекулярное наложение - наложение ("соответствие") всех комбинаций низкоэнергетических конформаций молекул. Могут быть подобраны аналогичные ( биоизостерические ) функциональные группы, общие для всех молекул в наборе ( например , фенильные кольца или группы карбоновых кислот). Набор конформаций (одна конформация от каждой активной молекулы), который дает наилучшее соответствие, считается активной конформацией.
- Абстракция - преобразуйте наложенные друг на друга молекулы в абстрактное представление. Например, наложенные друг на друга фенильные кольца можно более концептуально назвать фармакофорным элементом «ароматического кольца». Точно так же гидроксильные группы могут быть обозначены как « донор / акцептор водородной связи » фармакофорный элемент.
- Подтверждение . Фармакофорная модель - это гипотеза, объясняющая наблюдаемую биологическую активность набора молекул, которые связываются с общей биологической мишенью . Модель действительна только постольку, поскольку она способна учесть различия в биологической активности ряда молекул.
По мере того как биологическая активность новых молекул становится доступной, модель фармакофоров может быть обновлена для ее дальнейшего уточнения.
Приложения [ править ]
В современной вычислительной химии фармакофоры используются для определения основных характеристик одной или нескольких молекул с одинаковой биологической активностью . Затем можно выполнить поиск в базе данных различных химических соединений на предмет наличия большего количества молекул, которые имеют одинаковые характеристики и расположены в одной и той же относительной ориентации. Фармакофоры также используются в качестве отправной точки для разработки моделей 3D-QSAR . Такие инструменты и связанная с ними концепция «привилегированных структур», которые «определяются как молекулярные каркасы, которые способны предоставлять полезные лиганды для более чем одного типа рецепторов или ферментов-мишеней путем разумных структурных модификаций» [3], помогают в открытии лекарств . [4]
История [ править ]
Исторически фармакофоры были созданы Лемонтом Киром , который впервые упомянул эту концепцию в 1967 году [5] и использовал этот термин в публикации в 1971 году [6].
Разработка концепции часто ошибочно приписывается Паулю Эрлиху . Однако ни в предполагаемом источнике [7], ни в каких-либо других его работах не упоминается термин «фармакофор» и не используется это понятие. [8]
См. Также [ править ]
- Хеминформатика
- Молекулярная добыча
- Фармацевтическая компания
- QSAR
- in silico
Ссылки [ править ]
- ^ Вермут CG, Ganellin CR, Линдберг P, Mitscher LA (1998). «Глоссарий терминов, используемых в медицинской химии (Рекомендации IUPAC 1998 г.)» . Чистая и прикладная химия . 70 (5): 1129–1143. DOI : 10,1351 / pac199870051129 .
- ^ Мэдсен U, Brauner-Osborne Н, Greenwood JR, Джохэнсен Т.Н., Крогсгаард-Ларсен Р, Т Лильефорс, Нильсен М, Frølund В (2005). «Лиганды рецепторов ГАМК и глутамата и их терапевтический потенциал при расстройствах ЦНС». В Гад СК (ред.). Справочник по открытию лекарств . Хобокен, Нью-Джерси: Wiley-Interscience / J. Вайли. С. 797–907. ISBN 0-471-21384-5.
- ^ Дуарте, CD; и другие. (2007), "Привилегированные структуры: полезная концепция для рациональной разработки новых кандидатов свинец наркотиков", мини - Rev Med Chem , 7 (11): 1108-1119, DOI : 10,2174 / 138955707782331722 , PMID 18045214 .
- ^ Jangampalli Adi, Pradeepkiran (февраль 2019). «Модели на основе фармакофора для терапевтических препаратов против фосфорилированного тау при болезни Альцгеймера» . Открытие наркотиков сегодня . 24 (2): 616–623. DOI : 10.1016 / j.drudis.2018.11.005 . PMC 6397090 . PMID 30453058 .
- Перейти ↑ Kier LB (сентябрь 1967). «Расчет молекулярных орбиталей предпочтительных конформаций ацетилхолина, мускарина и мускарона». Мол. Pharmacol . 3 (5): 487–94. PMID 6052710 .
- Перейти ↑ Kier LB (1971). Теория молекулярных орбиталей в исследованиях лекарственных средств . Бостон: Academic Press. С. 164–169. ISBN 0-12-406550-3.
- ^ Эрлих P (1909). "Über den jetzigen Stand der Chemotherapie" . Бер. Dtsch. Chem. Ges . 42 : 17–47. DOI : 10.1002 / cber.19090420105 .
- ^ JH ван Дри (2007). «Монти Кир и происхождение концепции фармакофоров» (PDF) . Интернет-электронный журнал молекулярного дизайна . 6 : 271–279. CS1 maint: uses authors parameter (link)
Дальнейшее чтение [ править ]
- Гюнер О.Ф., изд. (1999). Восприятие, разработка и использование фармакофоров при разработке лекарств . ЛаХолла, Калифорния: Международная университетская линия. ISBN 0-9636817-6-1.
- Лангер Т., Хоффманн Р.Д. (2006). Фармакофоры и поиск фармакофоров . Вайнхайм: ВИЛИ-ВЧ. ISBN 3-527-31250-1.
Внешние ссылки [ править ]
Следующие пакеты компьютерного программного обеспечения позволяют пользователю моделировать фармакофор, используя различные методы вычислительной химии:
- Discovery Studio
- LigandScout
- Фаза
- МО - открытие фармакофоров
- ICM-Химик
- ZINCharmer
- Фармит
