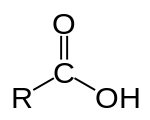
Карбоновой кислоты представляет собой органическую кислоту , которая содержит карбоксильную группу , (С (= O) OH) [1] , присоединенный к R-группе. Общая формула карбоновой кислоты - R – COOH , где R относится к алкильной , алкенильной , арильной или другой группе. Карбоновые кислоты широко распространены. Важные примеры включают аминокислоты и жирные кислоты . Депротонирование карбоновой кислоты дает анион карбоксилата .
Примеры и номенклатура [ править ]
Карбоновые кислоты обычно идентифицируются по своим тривиальным названиям . У них часто есть суффикс- кислота .Имена, рекомендованные ИЮПАК, также существуют; в этой системе у карбоновых кислот есть суффикс -ойная кислота . [2] Например, масляная кислота (C 3 H 7 CO 2 H) является бутановой кислотой в соответствии с рекомендациями IUPAC. Для номенклатуры сложных молекул, содержащих карбоновую кислоту, карбоксил можно считать положением одного из исходных цепей, даже если есть другие заместители , такие как 3-хлорпропановая кислота . Альтернативно, он может быть назван заместителем «карбокси» или «карбоновой кислоты» в другой исходной структуре, такой как 2-карбоксифуран .
Карбоксилат-анион (R – COO - или RCO 2 - ) карбоновой кислоты обычно называют суффиксом -ат в соответствии с общей структурой -иновой кислоты и -ата для сопряженной кислоты и ее сопряженного основания, соответственно. Например, конъюгат основания уксусной кислоты - это ацетат .
Угольная кислота , которая присутствует в бикарбонатных буферных системах в природе, обычно не классифицируется как одна из карбоновых кислот, несмотря на то, что она имеет фрагмент , похожий на группу COOH.
Атомы углерода | Распространенное имя | Название ИЮПАК | Химическая формула | Обычное расположение или использование |
|---|---|---|---|---|
| 1 | Муравьиная кислота | Метановая кислота | HCOOH | Укусы насекомых |
| 2 | Уксусная кислота | Этановая кислота | CH 3 COOH | Уксус |
| 3 | Пропионовая кислота | Пропановая кислота | CH 3 CH 2 COOH | Консервант для хранения зерна, запаха тела , молока, масла, сыра |
| 4 | Масляная кислота | Бутановая кислота | CH 3 (CH 2 ) 2 COOH | Сливочное масло |
| 5 | Валериановая кислота | Пентановая кислота | CH 3 (CH 2 ) 3 COOH | Валериана растение |
| 6 | Капроновая кислота | Гексановая кислота | CH 3 (CH 2 ) 4 COOH | Козий жир |
| 7 | Энантовая кислота | Гептановая кислота | CH 3 (CH 2 ) 5 COOH | Аромат |
| 8 | Каприловая кислота | Октановая кислота | CH 3 (CH 2 ) 6 COOH | Кокосы |
| 9 | Пеларгоновая кислота | Нонановая кислота | СН 3 (СН 2 ) 7 COOH | Пеларгония растение |
| 10 | Каприновая кислота | Декановая кислота | CH 3 (CH 2 ) 8 COOH | Кокосовое и пальмоядровое масло |
| 11 | Ундециловая кислота | Ундекановая кислота | CH 3 (CH 2 ) 9 COOH | Противогрибковое средство |
| 12 | Лауриновая кислота | Додекановая кислота | CH 3 (CH 2 ) 10 COOH | Кокосовое масло и мыло для мытья рук |
| 13 | Тридециловая кислота | Тридекановая кислота | CH 3 (CH 2 ) 11 COOH | Метаболит растения |
| 14 | Миристиновая кислота | Тетрадекановая кислота | CH 3 (CH 2 ) 12 COOH | Мускатный орех |
| 15 | Пентадециловая кислота | Пентадекановая кислота | CH 3 (CH 2 ) 13 COOH | Молочный жир |
| 16 | Пальмитиновая кислота | Гексадекановая кислота | CH 3 (CH 2 ) 14 COOH | пальмовое масло |
| 17 | Маргариновая кислота | Гептадекановая кислота | CH 3 (CH 2 ) 15 COOH | Феромон у разных животных |
| 18 | Стеариновая кислота | Октадекановая кислота | CH 3 (CH 2 ) 16 COOH | Шоколад , воск, мыло и масла |
| 19 | Нонадециловая кислота | Нонадекановая кислота | CH 3 (CH 2 ) 17 COOH | Жиры, растительные масла, феромоны |
| 20 | Арахидовая кислота | Икозановая кислота | CH 3 (CH 2 ) 18 COOH | Арахисовое масло |
| Составной класс | Члены |
|---|---|
| ненасыщенные монокарбоновые кислоты | акриловая кислота (2-пропеновая кислота) - CH 2 = CHCOOH, используется в синтезе полимеров |
| Жирные кислоты | средне- и длинноцепочечные насыщенные и ненасыщенные монокарбоновые кислоты с четным числом атомов углерода, примеры: докозагексаеновая кислота и эйкозапентаеновая кислота (пищевые добавки) |
| Аминокислоты | строительные блоки белков |
| Кетокислоты | кислоты биохимического значения, содержащие кетонную группу, примеры: ацетоуксусная кислота и пировиноградная кислота. |
| Ароматические карбоновые кислоты | содержащие по крайней мере одно ароматическое кольцо, примеры: бензойная кислота - натриевая соль бензойной кислоты используется в качестве пищевого консерванта, салициловая кислота - бета-гидрокси-тип, встречающийся во многих продуктах по уходу за кожей, фенилалкановые кислоты - класс соединений, в которых фенильная группа присоединена к карбоновой кислоте |
| Дикарбоновые кислоты | содержащие две карбоксильные группы, примеры: адипиновая кислота, мономер, используемый для производства нейлона, и альдаровая кислота - семейство сахарных кислот. |
| Трикарбоновые кислоты | содержащие три карбоксильные группы, примеры: лимонная кислота - содержится в цитрусовых и изоазимонная кислота. |
| Альфа-гидроксикислоты | содержащие гидроксигруппу, примеры: глицериновая кислота , гликолевая кислота и молочная кислота (2-гидроксипропановая кислота) - содержится в кислом молоке, винная кислота - содержится в вине |
| Дивиниловые эфиры жирных кислот | содержащий дважды ненасыщенную углеродную цепь, присоединенную через эфирную связь к жирной кислоте, обнаруженной в некоторых растениях |
Физические свойства [ править ]
Растворимость [ править ]
Карбоновые кислоты полярны . Поскольку они одновременно являются акцепторами водородных связей (карбонил –C = O) и донорами водородных связей (гидроксил –OH), они также участвуют в образовании водородных связей . Вместе гидроксильная и карбонильная группы образуют функциональную группу карбоксил. Карбоновые кислоты обычно существуют в виде димеров в неполярных средах из-за их тенденции к «самоассоциации». Более мелкие карбоновые кислоты (от 1 до 5 атомов углерода) растворимы в воде, тогда как более крупные карбоновые кислоты имеют ограниченную растворимость из-за возрастающей гидрофобной природы алкильной цепи. Эти кислоты с более длинной цепью обычно растворимы в менее полярных растворителях, таких как простые эфиры и спирты. [3] Водный гидроксид натрия и карбоновые кислоты, даже гидрофобные, реагируют с образованием водорастворимых солей натрия. Например,энатовая кислота имеет низкую растворимость в воде (0,2 г / л), но ее натриевая соль хорошо растворяется в воде.
Точки кипения [ править ]
Карбоновые кислоты, как правило, имеют более высокие температуры кипения, чем вода, из-за их большей площади поверхности и их тенденции образовывать стабилизированные димеры за счет водородных связей . Для того, чтобы произошло кипение, либо димерные связи должны быть разорваны, либо вся структура димеров должна быть испарена, что значительно увеличивает требования к энтальпии испарения .
Кислотность [ править ]
Карбоновые кислоты относятся к кислотам Бренстеда – Лоури, потому что они являются донорами протонов (H + ). Это наиболее распространенный тип органических кислот .
Карбоновые кислоты обычно являются слабыми кислотами , что означает, что они только частично диссоциируют на катионы H 3 O + и анионы RCOO - в нейтральном водном растворе. Например, при комнатной температуре в 1- молярном растворе уксусной кислоты диссоциирует только 0,4% кислоты. Электронно-заместители, например, -CF 3 группы , дают более сильные кислоты (рКа муравьиной кислоты составляет 3,75 , тогда как трифторуксусная кислота, с трифторметильным заместителем , имеет рК а , 0,23). Электронодонорные заместители дают более слабые кислоты (pK a муравьиной кислоты составляет 3,75, тогда как у уксусной кислоты с метильным заместителем pK a составляет 4,76).
| Карбоновая кислота [4] | p K a |
|---|---|
| Уксусная кислота (CH 3 CO 2 H) | 4,76 |
| Бензойная кислота (C 6 H 5 CO 2 H) | 4.2 |
| Муравьиная кислота (HCOOH) | 3,75 |
| Хлоруксусная кислота (CH 2 ClCO 2 H) | 2,86 |
| Дихлоруксусная кислота (CHCl 2 CO 2 H) | 1,29 |
| Щавелевая кислота (HO 2 CCO 2 H) (первая диссоциация) | 1,27 |
| Щавелевая кислота (HO 2 CCO 2 - ) (вторая диссоциация) | 4,14 |
| Трихлоруксусная кислота (CCl 3 CO 2 H) | 0,65 |
| Трифторуксусная кислота (CF 3 CO 2 H) | 0,23 |
Депротонирование карбоновых кислот дает карбоксилат-анионы; они стабилизированы резонансом , потому что отрицательный заряд делокализован по двум атомам кислорода, увеличивая стабильность аниона. Каждая из углерод-кислородных связей в карбоксилат-анионе имеет характер частичной двойной связи. Частичный положительный заряд карбонильного углерода также ослабляется отрицательными зарядами -1 / 2 на 2 атомах кислорода.
Запах [ править ]
Карбоновые кислоты часто имеют сильный кисловатый запах. Сложные эфиры карбоновых кислот имеют приятный запах, и многие из них используются в парфюмерии .
Характеристика [ править ]
Карбоновые кислоты легко идентифицируются как таковые с помощью инфракрасной спектроскопии . Они демонстрируют резкую полосу, связанную с колебанием колебательной связи C – O ( ν C = O ) между 1680 и 1725 см -1 . Характерная полоса ν O – H проявляется в виде широкого пика в области от 2500 до 3000 см –1 . [3] По данным спектрометрии 1 H ЯМР , гидроксильный водород появляется в области 10–13 ppm, хотя часто он либо расширен, либо не наблюдается из-за обмена со следами воды.
Возникновение и применение [ править ]
Многие карбоновые кислоты производятся в промышленных масштабах в больших масштабах. Они также часто встречаются в природе. Сложные эфиры жирных кислот являются основными компонентами липидов, а полиамиды аминокарбоновых кислот являются основными компонентами белков .
Карбоновые кислоты используются в производстве полимеров, фармацевтических препаратов, растворителей и пищевых добавок. Промышленно важные карбоновые кислоты включают уксусную кислоту (компонент уксуса, предшественник растворителей и покрытий), акриловую и метакриловую кислоты (предшественники полимеров, адгезивов), адипиновую кислоту (полимеры), лимонную кислоту (ароматизатор и консервант в продуктах питания и напитках), этилендиаминтетрауксусная кислота (хелатирующий агент), жирные кислоты (покрытия), малеиновая кислота (полимеры), пропионовая кислота (пищевой консервант), терефталевая кислота (полимеры). Важными карбоксилатными солями являются мыла.
Синтез [ править ]
Промышленные маршруты [ править ]
В целом, промышленные пути получения карбоновых кислот отличаются от тех, которые используются в меньших масштабах, поскольку они требуют специального оборудования.
- Карбонилирование спиртов на примере процесса Cativa производства уксусной кислоты. Муравьиная кислота получается другим путем карбонилирования, также исходя из метанола.
- Окисление альдегидов воздухом с использованием кобальтовых и марганцевых катализаторов. Требуемые альдегиды легко получить из алкенов гидроформилированием .
- Окисление углеводородов воздухом. Для простых алканов этот метод недорогой, но недостаточно селективный, чтобы быть полезным. Аллильные и бензильные соединения подвергаются более избирательному окислению. Алкильные группы бензольного кольца окисляются до карбоновой кислоты независимо от длины ее цепи. Бензойная кислота из толуола , терефталевой кислоты из пара - ксилол , и фталевой кислоты с орто - ксилол являются иллюстративными конверсиями крупномасштабных. Акриловая кислота образуется из пропена . [5]
- Окисление этена с использованием катализатора кремневольфрамовой кислоты .
- Катализируемое основанием дегидрирование спиртов.
- Карбонилирование сочетается с добавлением воды. Этот метод эффективен и универсален для алкенов, которые образуют вторичные и третичные карбокатионы , например изобутилен в пивалиновую кислоту . В реакции Коха добавление воды и окиси углерода к алкенам катализируется сильными кислотами. Гидрокарбоксилирование включает одновременное добавление воды и CO . Такие реакции иногда называют « химией Реппа ».
- HCCH + CO + H 2 O → CH 2 = CHCO 2 H
- Гидролиз триглицеридов, полученных из растительных или животных масел. Эти методы синтеза некоторых длинноцепочечных карбоновых кислот относятся к мыловарению .
- Ферментация этанола. Этот метод используется при производстве уксуса .
- Реакция Кольбе-Шмитта открывает путь к салициловой кислоте , предшественнику аспирина .
Лабораторные методы [ править ]
В препаративных методах мелкомасштабных реакций для исследований или производства тонких химикатов часто используются дорогостоящие расходные реагенты.
- Окисление первичных спиртов или альдегидов сильными окислителями, такими как дихромат калия , реактив Джонса , перманганат калия или хлорит натрия . Этот метод больше подходит для лабораторных условий, чем для промышленного использования воздуха, который «зеленее», поскольку дает меньше неорганических побочных продуктов, таких как оксиды хрома или марганца. [ необходима цитата ]
- Окислительное расщепление олефинов путем озонолиза , перманганата калия или дихромата калия .
- Гидролиз нитрилов , сложных эфиров или амидов , обычно с кислотным или основным катализом.
- Карбонизация реактива Гриньяра и литийорганических реагентов:
- RLi + CO 2 → RCO 2 Li
- RCO 2 Li + HCl → RCO 2 H + LiCl
- Галогенирование с последующим гидролизом метилкетонов в галоформной реакции.
- Катализируемое основанием расщепление неэнолизируемых кетонов, особенно арилкетонов: [6]
- RC (O) Ar + H 2 O → RCO 2 H + ArH
Менее распространенные реакции [ править ]
Многие реакции производят карбоновые кислоты, но используются только в определенных случаях или представляют в основном академический интерес.
- Диспропорционирование альдегида в реакции Канниццаро
- Перегруппировка дикетонов в перегруппировке бензиловой кислоты с образованием бензойных кислот - это реакция фон Рихтера из нитробензолов и реакция Кольбе-Шмитта из фенолов .
Реакции [ править ]
Наиболее широко применяемые реакции превращают карбоновые кислоты в сложные эфиры, амиды, карбоксилатные соли, хлорангидриды и спирты. Карбоновые кислоты реагируют с основаниями с образованием карбоксилатных солей, в которых водород гидроксильной (–ОН) группы замещен катионом металла . Например, уксусная кислота, содержащаяся в уксусе, реагирует с бикарбонатом натрия (пищевой содой) с образованием ацетата натрия, диоксида углерода и воды:
- CH 3 COOH + NaHCO 3 → CH 3 COO - Na + + CO 2 + H 2 O
Карбоновые кислоты также реагируют со спиртами с образованием сложных эфиров . Этот процесс широко используется, например, при производстве полиэфиров . Аналогичным образом карбоновые кислоты превращаются в амиды , но это превращение обычно не происходит при прямой реакции карбоновой кислоты и амина. Вместо этого сложные эфиры являются типичными предшественниками амидов. Превращение аминокислот в пептиды - важный биохимический процесс, для которого требуется АТФ .
Гидроксильная группа карбоновых кислот может быть заменена атомом хлора с использованием тионилхлорида с получением ацилхлоридов . В природе карбоновые кислоты превращаются в тиоэфиры .
Сокращение [ править ]
Как и сложные эфиры , большая часть карбоновой кислоты может быть восстановлена до спиртов путем гидрирования или использования гидридных или алкил-переносящих агентов (поскольку они будут депротонировать кислоты вместо этого [ требуется дополнительное объяснение ] без переноса), таких как литийалюминийгидрид или реагенты Гриньяра ( литийорганические соединения).
Хлорид N , N- диметил (хлорметилен) аммония (ClHC = N + (CH 3 ) 2 Cl - ) является очень хемоселективным агентом для восстановления карбоновой кислоты. Он избирательно активирует карбоновую кислоту с образованием соли карбоксиметиленаммония, которая может быть восстановлена мягким восстановителем, таким как трис ( трет- бутокси) алюмогидрид лития, с получением альдегида в однореакторной процедуре. Известно, что эта процедура допускает наличие реактивных карбонильных функциональных групп, таких как кетон, а также умеренно реакционноспособных сложноэфирных, олефиновых, нитрильных и галогенидных фрагментов. [7]
Специализированные реакции [ править ]
- Как и все карбонильные соединения, протоны на α-углероде лабильны из-за кето-енольной таутомеризации . Таким образом, α-углерод легко галогенируется при галогенировании Хелла – Волхарда – Зелинского .
- Реакция Шмидта превращает карбоновые кислоты в амины .
- Карбоновые кислоты декарбоксилируются в реакции Хунсдикера .
- Реакция Дакина-Веста превращает аминокислоту в соответствующий аминокетон.
- При деградации Барбье-Виланда карбоновая кислота в алифатической цепи, имеющей простой метиленовый мостик в альфа-положении, может иметь цепь, укороченную на один атом углерода. Обратной процедурой является синтез Арндта-Эйстерта , где кислота превращается в ацилгалогенид, который затем реагирует с диазометаном с образованием одного дополнительного метилена в алифатической цепи.
- Многие кислоты подвергаются окислительному декарбоксилированию . Ферменты , катализирующие эти реакции, известны как карбоксилазы ( EC 6.4.1) и декарбоксилазы (EC 4.1.1).
- Карбоновые кислоты восстанавливаются до альдегидов через сложный эфир и DIBAL , через хлорангидрид при восстановлении Розенмунда и через тиоэфир при восстановлении Фукуямы .
- При декарбоксилировании кетонов карбоновые кислоты превращаются в кетоны.
- Литийорганические реагенты (> 2 экв.) Реагируют с карбоновыми кислотами с образованием 1,1-диолата дилития, стабильного тетраэдрического промежуточного соединения, которое при кислотной обработке разлагается с образованием кетона.
- Электролиз Кольбы является электролитической, decarboxylative реакции димеризации. Он избавляется от карбоксильных групп двух молекул кислоты и соединяет оставшиеся фрагменты вместе.
Карбоксильный радикал [ править ]
Карбоксильный радикал • COOH существует недолго. [8] кислоты константа диссоциации из • СООН была измерена с помощью электронного парамагнитного резонанса спектроскопии. [9] Карбоксильная группа имеет тенденцию к димеризации с образованием щавелевой кислоты .
См. Также [ править ]
| Викискладе есть медиафайлы по теме карбоновых кислот . |
| В Wikiquote есть цитаты, связанные с: Карбоновая кислота. |
- Кислотный ангидрид
- Хлорид кислоты
- Амид
- Аминокислота
- Сложный эфир
- Список карбоновых кислот
- Дикарбоновая кислота
- Полигидроксикарбоновая кислота (PHC).
- Псевдокислота
- Тиокарбокси
Ссылки [ править ]
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « карбоновые кислоты ». DOI : 10,1351 / goldbook.C00852
- ^ Рекомендации 1979 . Органическая химия Номенклатура ИЮПАК. Правила C-4 карбоновые кислоты и их производные.
- ^ a b Моррисон, RT; Бойд, RN (1992). Органическая химия (6-е изд.). ISBN 0-13-643669-2.
- ^ Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). CRC Press . С. 5–94–5–98. ISBN 978-1439855119.
- ^ Riemenschneider, Вильгельм (2002). «Карбоновые кислоты алифатические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a05_235 . ISBN 3527306730..
- ↑ Перри С. Ривз (1977). «Карбоксилирование ароматических соединений: ферроценкарбоновая кислота». Орг. Synth . 56 : 28. DOI : 10,15227 / orgsyn.056.0028 .
- ^ Фудзисава, Тамоцу; Сато, Тошио. «Восстановление карбоновых кислот до альдегидов: 6-Ооксидеканаль» . Органический синтез . 66 : 121. DOI : 10,15227 / orgsyn.066.0121 .; Сборник , 8 , с. 498
- ^ Миллиган, Делавэр; Jacox, ME (1971). «Инфракрасный спектр и структура промежуточных продуктов в реакции ОН с СО». Журнал химической физики . 54 (3): 927–942. Bibcode : 1971JChPh..54..927M . DOI : 10.1063 / 1.1675022 .
- ^ Значение p K a = -0,2 ± 0,1. Jeevarajan, AS; Кармайкл, I .; Фессенден, Р.В. (1990). "Измерение ESR p K a карбоксильного радикала и Ab Initio расчет константы сверхтонкого углерода-13". Журнал физической химии . 94 (4): 1372–1376. DOI : 10.1021 / j100367a033 .
Внешние ссылки [ править ]
| Поищите карбоксил в Викисловаре, бесплатном словаре. |
- Карбоновые кислоты pH и титрование - бесплатное ПО для расчетов, анализа данных, моделирования и построения диаграмм распределения
- PHC.