Преобразование гена - это процесс, при котором одна последовательность ДНК заменяет гомологичную последовательность , так что последовательности становятся идентичными после события преобразования. Преобразование гена может быть либо аллельным , что означает, что один аллель одного и того же гена заменяет другой аллель, либо эктопическим , что означает, что одна паралогичная последовательность ДНК преобразует другую.
Конверсия аллельного гена [ править ]
Конверсия аллельного гена происходит во время мейоза, когда гомологичная рекомбинация между гетерозиготными сайтами приводит к несоответствию в спаривании оснований. Это несоответствие затем распознается и исправляется клеточным механизмом, вызывая преобразование одного из аллелей в другой. Это может вызвать неменделирующую сегрегацию аллелей в половых клетках. [1]
Конверсия неаллельного / эктопического гена [ править ]
Рекомбинация происходит не только во время мейоза, но и как механизм репарации двухцепочечных разрывов (DSB), вызванных повреждением ДНК. Эти DSB обычно восстанавливаются с использованием сестринской хроматиды разорванного дуплекса, а не гомологичной хромосомы, поэтому они не приводят к аллельной конверсии. Рекомбинация также происходит между гомологичными последовательностями, присутствующими в разных геномных локусах (паралогическими последовательностями), которые возникли в результате предыдущих дупликаций генов. Предполагается, что конверсия генов, происходящая между паралогическими последовательностями ( эктопическая конверсия генов ), ответственна за согласованную эволюцию семейств генов. [1] [2] [3]
Механизм [ править ]
Преобразование одного аллеля в другой часто происходит из-за репарации несоответствия оснований во время гомологичной рекомбинации : если одна из четырех хроматид во время мейоза соединяется с другой хроматидой, что может происходить из-за гомологии последовательностей , может произойти перенос цепи ДНК с последующей репарацией несовпадения. Это может изменить последовательность одной из хромосом, чтобы она стала идентичной другой.
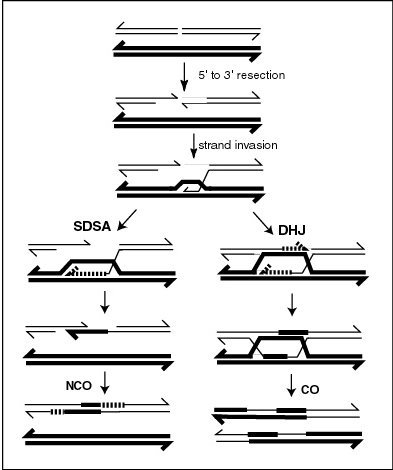
Мейотическая рекомбинация инициируется путем образования двухцепочечного разрыва (DSB). Затем 5'-концы разрыва разрушаются, оставляя длинные 3'-выступы из нескольких сотен нуклеотидов. Один из этих 3'-сегментов одноцепочечной ДНК затем вторгается в гомологичную последовательность на гомологичной хромосоме, образуя промежуточный продукт, который может быть восстановлен различными путями, приводя либо к кроссоверам (CO), либо к непересекающимся (NCO). На различных этапах процесса рекомбинации образуется гетеродуплексная ДНК (двухцепочечная ДНК, состоящая из одиночных цепей каждой из двух гомологичных хромосом, которые могут быть или не быть полностью комплементарными). Когда в гетеродуплексной ДНК возникают несоответствия, последовательность одной цепи будет восстановлена, чтобы связать другую цепь с идеальной комплементарностью, что приведет к преобразованию одной последовательности в другую.Этот процесс восстановления может происходить по одному из двух альтернативных путей, как показано на рисунке. Одним путем структура, названная двойнымФормируется соединение Холлидея (DHJ), приводящее к обмену цепями ДНК. По другому пути, называемому зависимым от синтеза отжигом (SDSA), происходит обмен информацией, но не физический. Конверсия гена будет происходить во время SDSA, если две молекулы ДНК являются гетерозиготными в месте рекомбинационной репарации. Преобразование гена также может происходить во время рекомбинационной репарации с участием DHJ, и это преобразование гена может быть связано с физической рекомбинацией дуплексов ДНК на двух сторонах DHJ.
Предвзятое или непредвзятое преобразование гена [ править ]
Предвзятое преобразование гена (BGC) происходит, когда один аллель имеет более высокую вероятность быть донором, чем другой в событии преобразования гена. Например, когда возникает несоответствие T: G, его более или менее вероятно исправят в пару C: G, чем в пару T: A. Это увеличивает вероятность передачи этого аллеля следующему поколению. Беспристрастная конверсия гена означает, что обе возможности возникают с равной вероятностью.
Конверсия генов с учетом GC [ править ]
Конверсия генов с учетом GC (gBGC) - это процесс, при котором содержание GC в ДНК увеличивается из-за конверсии генов во время рекомбинации. [2] Доказательства наличия gBGC существуют для дрожжей и людей, и недавно эта теория была проверена на других эукариотических линиях. [4] В проанализированных последовательностях ДНК человека было обнаружено, что скорость кроссовера положительно коррелирует с содержанием GC. [2] В области pseudoautosomal (PAR) из Х и Y хромосом у людей, которые , как известно, имеют высокий уровень рекомбинации также имеют высокое содержание GC. [1] Некоторые гены млекопитающих, претерпевающие согласованную эволюцию (например, рибосомные опероны, тРНК и гены гистонов), очень богаты GC. [1]Было показано, что содержание GC выше в паралогичных гистоновых генах человека и мыши, которые являются членами больших подсемейств (предположительно претерпевающих согласованную эволюцию), чем в паралогичных гистоновых генах с относительно уникальными последовательностями. [5] Есть также свидетельства смещения GC в процессе исправления несоответствия. [1] Считается, что это может быть адаптацией к высокой скорости дезаминирования метилцитозина, которая может приводить к переходам C → T.
BGC гена Fxy у Mus musculus [ править ]
Ген Fxy или Mid1 у некоторых млекопитающих, тесно связанных с домашними мышами (люди, крысы и другие виды Mus), расположен в сцепленной с полом области Х-хромосомы. Однако у Mus musculus он недавно транслоцировался так, что 3'-конец гена перекрывается с районом PAR X-хромосомы, который, как известно, является горячей точкой рекомбинации. Эта часть гена испытала резкое увеличение содержания GC и скорости замены в положении 3-го кодона, а также в интронах, но 5'-область гена, которая связана с Х-хромосомой, этого не произошло. Поскольку этот эффект присутствует только в области гена, в которой наблюдается повышенная скорость рекомбинации, он должен быть вызван смещенной конверсией гена, а не давлением отбора. [2]
Влияние конверсии генов, обусловленной GC, на геномные структуры человека [ править ]
Содержание GC широко варьируется в геноме человека (40–80%), но, по-видимому, есть большие участки генома, где содержание GC в среднем выше или ниже, чем в других регионах. [1] Эти области, хотя и не всегда имеют четкие границы, известны как изохоры. Одним из возможных объяснений присутствия GC-богатых изохор является то, что они эволюционировали из-за GC-смещенной конверсии генов в регионах с высокими уровнями рекомбинации.
Эволюционное значение [ править ]
Адаптивная функция рекомбинации [ править ]
Исследования конверсии генов способствовали нашему пониманию адаптивной функции мейотической рекомбинации. Обычный паттерн сегрегации пары аллелей (Aa) среди 4 продуктов мейоза - 2A: 2a. Обнаружение нечастых событий генной конверсии (например, моделей сегрегации 3: 1 или 1: 3 во время отдельных мейозов) дает представление об альтернативных путях рекомбинации, ведущих либо к кроссоверным, либо к некроссоверным хромосомам. Считается, что события генной конверсии возникают там, где аллели «А» и «а» оказываются рядом с точным местом события молекулярной рекомбинации. Таким образом, можно измерить частоту, с которой события конверсии гена связаны с кроссовером или непересечением хромосомных областей, смежных с событием непосредственного преобразования, но вне его.Были проведены многочисленные исследования конверсии генов у различных грибов (которые особенно подходят для таких исследований), и результаты этих исследований были рассмотрены Уайтхаусом.[6] Из этого обзора ясно, что большинство событий конверсии генов не связаны с обменом внешних маркеров. Таким образом, большинство событий конверсии генов у нескольких изученных грибов связано с отсутствием кроссовера внешних маркеров. События конверсии генов без кроссовера в основном производятся с помощью отжига зависимых цепей от синтеза (SDSA). [7] Этот процесс включает ограниченный информационный обмен, но не физический обмен ДНК между двумя участвующими гомологичными хромосомами в месте события конверсии, и при этом возникает небольшая генетическая вариация. Таким образом, объяснения адаптивной функции мейотической рекомбинации, которые фокусируются исключительно на адаптивных преимуществах создания новых генетических вариаций или физического обмена, кажутся неадекватными для объяснения большинства событий рекомбинации во время мейоза. Однако большинство событий мейотической рекомбинации можно объяснить предположением, что они являются адаптацией для восстановления повреждений ДНК, которые должны передаваться гаметам. [8]
Особый интерес с точки зрения того, что рекомбинация является адаптацией к репарации ДНК, представляют исследования на дрожжах, показывающие, что конверсия генов в митотических клетках увеличивается под действием УФ [9] [10] и ионизирующего излучения [11].
Генетические болезни человека [ править ]
В дискуссиях о генетических заболеваниях человека хорошо известным механизмом мутации является опосредованная псевдогеном конверсия генов, которая вводит патогенные мутации в функциональные гены. Напротив, возможно, что псевдогены могут служить шаблонами. В ходе эволюции гены функционального источника, которые потенциально могут быть полезными, были получены из множества копий их единого исходного гена. Изменения, спланированные псевдогеном, в конечном итоге могут стать фиксированными, если они не будут оказывать вредного воздействия. [12] Таким образом, фактически, псевдогены могут действовать как источники вариантов последовательностей, которые могут быть перенесены в функциональные гены в новых комбинациях, и на них можно воздействовать путем отбора .Лектин 11 ( SIGLEC 11), человеческий иммуноглобулин, который связывается с сиаловой кислотой, можно рассматривать как пример такого события преобразования гена, которое сыграло значительную роль в эволюции. При сравнении гомологичных генов человеческого SIGLEC11 и его псевдогена у шимпанзе , бонобо, гориллы и орангутана выяснилось , что произошла генная конверсия последовательности 5 'вышележащих областей и экзонов, которые кодируют домен узнавания сиаловой кислоты, примерно 2 кбп от близко фланкирующий псевдоген hSIGLECP16 (Hayakawa et al., 2005). Три свидетельства об этом событии вместе предполагают, что это адаптивное изменение, которое очень важно с эволюционной точки зрения для рода. Homo . Это включает в себя то, что это преобразование гена произошло только в человеческой линии, кора головного мозга приобрела важную экспрессию SIGLEC11, особенно в человеческой линии, и проявление изменения связывания субстрата в человеческой линии по сравнению с его аналогом у шимпанзе. Конечно, частота вклада этого опосредованного псевдогеном механизма конверсии генов в функциональные и адаптивные изменения в эволюции человека все еще неизвестна, и пока она почти не исследована. [13] Несмотря на это, введение положительно селективных генетических изменений с помощью такого механизма может быть предложено для рассмотрения на примере SIGLEC11. Иногда из-за столкновения сменных элементову некоторых членов семейства генов это вызывает вариацию между ними и, наконец, может также снизить скорость преобразования генов из-за отсутствия сходства последовательностей, что приводит к дивергентной эволюции .
Геномный анализ [ править ]
Из различных анализов генома был сделан вывод, что двухцепочечные разрывы (DSB) могут быть восстановлены посредством гомологичной рекомбинации , по крайней мере, двумя разными, но связанными путями. [12] В случае основного пути будут использоваться гомологичные последовательности по обе стороны от DSB, что похоже на модель консервативной репарации DSB [14], которая была первоначально предложена для мейотической рекомбинации у дрожжей. [15] где второстепенный путь ограничен только одной стороной DSB, как постулируется неконсервативной моделью односторонней инвазии. [16]Однако в обоих случаях последовательность партнеров рекомбинации будет абсолютно консервативной. Благодаря своей высокой степени гомологии, новые копии гена, которые возникли после дупликации гена, естественно имеют тенденцию к неравному кроссоверу или однонаправленным событиям конверсии гена. В последнем процессе существуют акцепторная и донорная последовательности, и акцепторная последовательность будет заменена последовательностью, скопированной с донора, в то время как последовательность донора останется неизменной. [13]
Эффективная гомология между взаимодействующими последовательностями делает событие конверсии гена успешным. Кроме того, частота конверсии гена обратно пропорциональна расстоянию между взаимодействующими последовательностями в цис [17] [12], а скорость преобразования гена обычно прямо пропорциональна длине непрерывного тракта последовательности в предполагаемой преобразованной области. Похоже, что конверсионные тракты, сопровождающие кроссовер, длиннее (средняя длина = ~ 460 п.н.), чем конверсионные тракты без кроссовера (средняя длина = 55–290 п.н.). [18]В исследованиях генов глобулинов человека давно подтверждено, что событие конверсии гена или события миграции ветвей могут либо стимулироваться, либо ингибироваться специфическими мотивами, которые существуют вблизи последовательности ДНК (Papadakis and Patrinos, 1999). [12] Другой основной классификацией событий конверсии генов являются интерлокусные (также называемые неаллельными) и межараллельные преобразования генов. События цис- или транс-неаллельной или интерлокусной конверсии гена происходят между копиями неаллельного гена, находящимися на сестринских хроматидах или гомологичных хромосомах, а в случае межаллельных событий конверсии гена происходят между аллелями, находящимися на гомологичных хромосомах (адаптировано из Chen et al. (2007). [13] [12]Если сравнить события межлокусной конверсии гена, часто будет обнаружено, что они демонстрируют предвзятую направленность. Иногда, например, в случае генов глобина человека (Papadakis and Patrinos, 1999), [12] направление преобразования гена коррелирует с относительными уровнями экспрессии генов, которые участвуют в событии, при этом ген экспрессируется на более высоком уровне, называемом «главный» ген, преобразовав его с более низкой экспрессией, называется «рабским» геном. Первоначально сформулированное в контексте эволюции правило «гена хозяина / подчиненного» следует объяснять с осторожностью. Фактически, увеличение транскрипции гена демонстрирует не только увеличение вероятности его использования в качестве донора, но также и в качестве акцептора. [12] [19]
Эффект [ править ]
Обычно организм, унаследовавший разные копии гена от каждого из своих родителей, называется гетерозиготным. Обычно это представлено как генотип: Aa (т.е. одна копия варианта ( аллеля ) «A» и одна копия аллеля «a»). Когда гетерозигота создает гаметы посредством мейоза , аллели обычно дублируются и в конечном итоге в соотношении 2: 2 образуются 4 клетки, которые являются прямыми продуктами мейоза. Однако при конверсии гена наблюдается соотношение, отличное от ожидаемого 2A: 2a, в котором A и a являются двумя аллелями. Примеры: 3A: 1a и 1A: 3a. Другими словами, может быть, например, в три раза больше аллелей A, чем аллелей, экспрессируемых в дочерних клетках, как в случае 3A: 1a.
Медицинское значение [ править ]
Конверсия гена, приводящая к мутации гена CYP21A2 , является распространенной генетической причиной врожденной гиперплазии надпочечников . Конверсия соматических генов - один из механизмов, который может привести к семейной ретинобластоме , врожденному раку сетчатки , и предполагается, что конверсия генов может играть роль в развитии болезни Хантингтона .
Ссылки [ править ]
- ^ a b c d e f Галтье Н., Пигано Г., Муширу Д., Дюре Л. (октябрь 2001 г.). «Эволюция GC-содержания в геномах млекопитающих: гипотеза предвзятого преобразования генов» . Генетика . 159 (2): 907–11. PMC 1461818 . PMID 11693127 .
- ^ а б в г Дюре Л., Гальтье Н. (2009). «Предвзятая конверсия генов и эволюция геномных ландшафтов млекопитающих». Анну Рев Геном Хум Генет . 10 : 285–311. DOI : 10.1146 / annurev-genom-082908-150001 . PMID 19630562 .
- ^ Харпак, Арбель; Лань, Сюнь; Гао, Цзыюэ; Причард, Джонатан К. (28 ноября 2017 г.). «Частая неаллельная конверсия генов в человеческой линии и ее влияние на дивергенцию дубликатов генов» . Труды Национальной академии наук . 114 (48): 12779–12784. DOI : 10.1073 / pnas.1708151114 . ISSN 0027-8424 . PMC 5715747 . PMID 29138319 .
- ^ Pessia Е, Попа А, Муссе S, Резвой С, Duret л, Марэ Г.А. (2012). «Доказательства широко распространенной конверсии генов с ошибкой GC у эукариот» . Genome Biol Evol . 4 (7): 675–82. DOI : 10.1093 / GbE / evs052 . PMC 5635611 . PMID 22628461 .
- ^ Galtier N (февраль 2003). «Преобразование генов движет эволюцией содержания GC в гистонах млекопитающих». Тенденции Genet . 19 (2): 65–8. DOI : 10.1016 / s0168-9525 (02) 00002-1 . PMID 12547511 .
- ^ Уайтхаус, HLK (1982). Генетическая рекомбинация: понимание механизмов . Вайли. п. 321 и таблица 38. ISBN 978-0471102052.
- ^ McMahill MS, Sham CW, епископ DK (ноябрь 2007). «Синтез-зависимый отжиг нитей в мейозе» . PLoS Biol . 5 (11): e299. DOI : 10.1371 / journal.pbio.0050299 . PMC 2062477 . PMID 17988174 .
- ^ Бернштейн, Харрис; Бернштейн, Кэрол; Мичод, Ричард Э. (2011). «19. Мейоз как эволюционная адаптация к репарации ДНК». В Круман, Инна (ред.). Ремонт ДНК . 2011: InTech. DOI : 10.5772 / 25117 . ISBN 978-953-307-697-3.CS1 maint: location ( ссылка )
- Перейти ↑ Ito T, Kobayashi K (октябрь 1975 г.). «Исследования по индукции конверсии митотических генов ультрафиолетовым излучением. II. Спектры действия». Мутат. Res . 30 (1): 43–54. DOI : 10.1016 / 0027-5107 (75) 90251-1 . PMID 1101053 .
- ^ Хэннэн М.А., Калкинс Дж, Лассвелл WL (1980). «Рекомбинагенные и мутагенные эффекты солнечного света (УФ-В) на Saccharomyces cerevisiae ». Мол. Genet Genet . 177 (4): 577–80. DOI : 10.1007 / bf00272666 . PMID 6991864 .
- ^ Raju MR, Gnanapurani M, Stackler B и др. (Сентябрь 1971 г.). «Индукция гетероаллельных реверсий и летальность у Saccharomyces cerevisiae при воздействии излучения различной ЛПЭ (лучи 60 Со, тяжелые ионы и - мезоны) в атмосфере воздуха и азота». Radiat. Res . 47 (3): 635–43. DOI : 10.2307 / 3573356 . JSTOR 3573356 . PMID 5119583 .
- ^ Б с д е е г Ch, Jain-Min (2001). Конверсия генов в эволюции и болезни . Вайли. ISBN 9780470015902.
- ^ a b c Чен, Цзянь-Минь; Купер, Дэвид Н .; Чужанова, Надя; Ферек, Клод; Патринос, Джордж П. (2007). «Конверсия генов: механизмы, эволюция и болезни человека». Природа Обзоры Генетики . 8 (10): 762–775. DOI : 10.1038 / nrg2193 . ISSN 1471-0056 . PMID 17846636 .
- ^ Шостак JW, Орр-Weaver TL, Ротштейн RJ, Stahl FW (1983). «Модель репарации двухцепочечного разрыва для рекомбинации». Cell . 33 (1): 25–35. DOI : 10.1016 / 0092-8674 (83) 90331-8 . PMID 6380756 .
- ↑ Ota T, Nei M (январь 1995 г.). «Эволюция псевдогенов иммуноглобулина VH у кур» . Мол. Биол. Evol . 12 (1): 94–102. DOI : 10.1093 / oxfordjournals.molbev.a040194 . PMID 7877500 .
- ^ Belmaaza A, Chartrand P (май 1994). «Односторонние события инвазии в гомологичной рекомбинации при двухцепочечных разрывах». Мутат. Res . 314 (3): 199–208. DOI : 10.1016 / 0921-8777 (94) 90065-5 . PMID 7513053 .
- ^ Шилдкраут, Е. (2005). «Частота конверсии и делеции генов во время репарации двухцепочечных разрывов в клетках человека контролируется расстоянием между прямыми повторами» . Исследования нуклеиновых кислот . 33 (5): 1574–1580. DOI : 10.1093 / NAR / gki295 . ISSN 1362-4962 . PMC 1065255 . PMID 15767282 .
- ^ Джеффрис AJ, май CA (февраль 2009). «Интенсивная и сильно локализованная активность генной конверсии в горячих точках мейотического кроссовера человека» . Генетика природы . 36 (2): 151–156. DOI : 10.1038 / ng1287 . PMID 14704667 .
- ^ Schildkraut, E .; Миллер, Калифорния; Николофф, JA (2006). «Транскрипция донора увеличивает его использование во время индуцированной двухцепочечным разрывом генной конверсии в клетках человека» . Молекулярная и клеточная биология . 26 (8): 3098–3105. DOI : 10.1128 / MCB.26.8.3098-3105.2006 . ISSN 0270-7306 . PMC 1446947 . PMID 16581784 .
Внешние ссылки [ править ]
- Gene + преобразование в предметных заголовках медицинской тематики Национальной медицинской библиотеки США (MeSH)
- изображения: http://www.web-books.com/MoBio/Free/Ch8D4.htm и http://www.web-books.com/MoBio/Free/Ch8D2.htm