Дезоксирибонуклеиновой кислоты ( / д я ɒ к с ɪ ˌ г aɪ б oʊ щ ¯u ˌ к л я ɪ к , - ˌ к л eɪ - / ( слушать )![]() ; [1] ДНК ) представляет собой молекулу , состоит из двух полинуклеотидных цепей, обвиваются вокруг друг друга, образуя двойную спираль, несущую генетические инструкции для развития, функционирования, роста иразмножение всех известных организмов и многих вирусов . ДНК и рибонуклеиновая кислота (РНК) являются нуклеиновыми кислотами . Наряду с белками , липидами и сложными углеводами ( полисахаридами ) нуклеиновые кислоты являются одним из четырех основных типов макромолекул , которые необходимы для всех известных форм жизни .
; [1] ДНК ) представляет собой молекулу , состоит из двух полинуклеотидных цепей, обвиваются вокруг друг друга, образуя двойную спираль, несущую генетические инструкции для развития, функционирования, роста иразмножение всех известных организмов и многих вирусов . ДНК и рибонуклеиновая кислота (РНК) являются нуклеиновыми кислотами . Наряду с белками , липидами и сложными углеводами ( полисахаридами ) нуклеиновые кислоты являются одним из четырех основных типов макромолекул , которые необходимы для всех известных форм жизни .
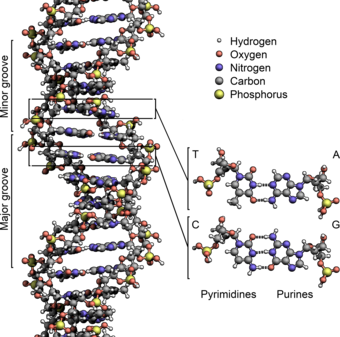
Две цепи ДНК известны как полинуклеотиды, поскольку они состоят из более простых мономерных единиц, называемых нуклеотидами . [2] [3] Каждый нуклеотид состоит из одного из четырех азотсодержащих азотистых оснований ( цитозин [C], гуанин [G], аденин [A] или тимин [T]), сахара, называемого дезоксирибозой , и фосфатной группы . Нуклеотиды соединены друг с другом в цепь ковалентными связями.(известная как фосфо-диэфирная связь) между сахаром одного нуклеотида и фосфатом следующего, в результате чего получается чередующийся сахарно-фосфатный остов . Азотистые основания двух отдельных полинуклеотидных цепей связаны вместе в соответствии с правилами спаривания оснований (A с T и C с G) водородными связями для образования двухцепочечной ДНК. Дополнительные азотистые основания делятся на две группы: пиримидины и пурины . В ДНК пиримидины - это тимин и цитозин; пурины - это аденин и гуанин.
Обе нити двухцепочечной ДНК хранят одинаковую биологическую информацию . Эта информация воспроизводится, когда две нити разделяются. Большая часть ДНК (более 98% для человека) не кодирует , что означает, что эти участки не служат образцами для белковых последовательностей . Две цепи ДНК идут в противоположных направлениях друг к другу и, таким образом, антипараллельны . К каждому сахару присоединен один из четырех типов азотистых оснований (неформально, оснований ). Именно последовательность этих четырех азотистых оснований вдоль скелета кодирует генетическую информацию. Нити РНК создаются с использованием нитей ДНК в качестве матрицы в процессе, называемомтранскрипция , при которой основания ДНК заменяются соответствующими основаниями, за исключением случая тимина (T), для которого РНК заменяет урацил (U). [4] В соответствии с генетическим кодом эти цепи РНК определяют последовательность аминокислот в белках в процессе, называемом трансляцией .
Внутри эукариотических клеток ДНК организована в длинные структуры, называемые хромосомами . Перед типичным делением клетки эти хромосомы дублируются в процессе репликации ДНК , обеспечивая полный набор хромосом для каждой дочерней клетки. Эукариотические организмы ( животные , растения , грибы и простейшие ) хранят большую часть своей ДНК в ядре клетки в виде ядерной ДНК , а некоторые - в митохондриях в виде митохондриальной ДНК или в хлоропластах в виде хлоропластной ДНК . [5]Напротив, прокариоты ( бактерии и археи ) хранят свою ДНК только в цитоплазме , в кольцевых хромосомах . В хромосомах эукариот белки хроматина , такие как гистоны , уплотняют и организуют ДНК. Эти уплотняющие структуры направляют взаимодействия между ДНК и другими белками, помогая контролировать, какие части ДНК транскрибируются.
Характеристики
ДНК - это длинный полимер, состоящий из повторяющихся звеньев, называемых нуклеотидами , каждая из которых обычно обозначается одной буквой: A, T, C или G. [6] [7] Структура ДНК динамична по всей длине, будучи способны скручиваться в узкие петли и другие формы. [8] У всех видов он состоит из двух спиральных цепей, связанных друг с другом водородными связями . Обе цепи намотаны вокруг одной оси и имеют одинаковый шаг в 34 ангстрем (Å) (3,4 нанометра ). Пара цепочек имеет радиус 10 ангстрем (1,0 нанометр). [9]Согласно другому исследованию, при измерении в другом растворе длина цепи ДНК составляла от 22 до 26 ангстрем (от 2,2 до 2,6 нанометров), а длина одной нуклеотидной единицы - 3,3 Å (0,33 нм). [10] Хотя каждый отдельный нуклеотид очень мал, полимер ДНК может быть очень большим и содержать сотни миллионов нуклеотидов, например, в хромосоме 1 . Хромосома 1 - самая большая хромосома человека с приблизительно 220 миллионами пар оснований , и ее длина составила бы 85 мм в случае выпрямления. [11]
ДНК обычно существует не как одна нить, а как пара нитей, которые крепко скреплены вместе. [9] [12] Эти две длинные нити наматываются друг на друга в форме двойной спирали . Нуклеотид содержит как сегмент основной цепи молекулы (который удерживает цепь вместе), так и азотистое основание (которое взаимодействует с другой цепью ДНК в спирали). Основание, связанное с сахаром, называется нуклеозидом , а основание, связанное с сахаром и одной или несколькими фосфатными группами, называется нуклеотидом . Биополимер , содержащий несколько связанных нуклеотидов (как в ДНК) называется полинуклеотид .[13]
Основа нити ДНК состоит из чередующихся фосфатных и сахарных групп. [14] Сахар в ДНК - 2-дезоксирибоза , пентозный ( пятиуглеродный ) сахар. Сахара соединены вместе фосфатными группами, которые образуют фосфодиэфирные связи между третьим и пятым атомами углерода соседних сахарных колец. Они известны как 3'-концевые (три основных конца) и 5'-концевые (пять простых концов) атомы углерода, причем основной символ используется для отличия этих атомов углерода от атомов основания, с которым дезоксирибоза образует гликозидную связь.. Следовательно, любая цепь ДНК обычно имеет один конец, на котором есть фосфатная группа, присоединенная к 5'-углеродному углероду рибозы (5'-фосфорил), и другой конец, на котором есть свободная гидроксильная группа, присоединенная к 3'-углеродному атому рибоза (3 'гидроксил). Ориентация 3 'и 5' атомов углерода вдоль сахарофосфатного остова придает направленность (иногда называемую полярностью) каждой цепи ДНК. В двойной спирали нуклеиновой кислоты направление нуклеотидов в одной цепи противоположно их направлению в другой цепи: цепи антипараллельны.. Говорят, что асимметричные концы нитей ДНК имеют направленность пяти основных концов (5 ') и трех основных концов (3'), причем 5 'конец имеет концевую фосфатную группу, а 3' конец - концевую гидроксильную группу. Одно из основных различий между ДНК и РНК - это сахар, при этом 2-дезоксирибоза в ДНК заменяется альтернативным пентозным сахаром рибозой в РНК. [12]
Двойная спираль ДНК стабилизируется главным образом двумя силами: водородными связями между нуклеотидами и взаимодействиями стэкинга оснований между ароматическими азотистыми основаниями. [16] Четыре основания, обнаруженные в ДНК, - это аденин (A), цитозин (C), гуанин (G) и тимин (T). Эти четыре основания присоединены к сахарному фосфату с образованием полного нуклеотида, как показано для аденозинмонофосфата . Аденин соединяется с тимином, а гуанин - с цитозином, образуя пары оснований AT и GC . [17] [18]
Классификация нуклеооснований
Нуклеотидные основания подразделяются на два типа: пурины , A и G, которые представляют собой конденсированные пяти- и шестичленные гетероциклические соединения , и пиримидины , шестичленные кольца C и T. [12] Пятое пиримидиновое азотистое основание, урацил ( U), обычно занимает место тимина в РНК и отличается от тимина отсутствием метильной группы в его кольце. Помимо РНК и ДНК, многие искусственные аналоги нуклеиновых кислот были созданы для изучения свойств нуклеиновых кислот или для использования в биотехнологии. [19]
Неканонические основы
Модифицированные основания встречаются в ДНК. Первый из них был признан 5-метилцитозин , который был найден в геноме из микобактерий туберкулеза в 1925 г. [20] Причина присутствия этих неканонических оснований в бактериальных вирусов ( бактериофагов ), чтобы избежать ферменты рестрикции присутствуют в бактерий. Эта ферментная система действует, по крайней мере, частично как молекулярная иммунная система, защищающая бактерии от заражения вирусами. [21] Модификации оснований цитозина и аденина, наиболее распространенных и модифицированных оснований ДНК, играют жизненно важную роль в эпигенетическом контроле экспрессии генов у растений и животных. [22]
Список неканонических оснований, обнаруженных в ДНК
Известно, что в ДНК встречается ряд неканонических оснований. [23] Большинство из них являются модификациями канонических оснований плюс урацил.
- Модифицированный аденозин
- N6-карбамоил-метиладенин
- N6-метиаденин
- Модифицированный гуанин
- 7-деазагуанин
- 7-метилгуанин
- Модифицированный цитозин
- N4-метилцитозин
- 5-карбоксилцитозин
- 5-формилцитозин
- 5-гликозилгидроксиметилцитозин
- 5-гидроксицитозин
- 5-метилцитозин
- Модифицированный тимидин
- α-глутамитимидин
- α-Putrescinylthymine
- Урацил и модификации
- База J
- Урацил
- 5-дигидроксипентаурацил
- 5-гидроксиметилдезоксиурацил
- Другие
- Дезоксиархеозин
- 2,6-диаминопурин
Канавки
Двойные спиральные нити образуют основу ДНК. Другая двойная спираль может быть обнаружена в промежутках или канавках между прядями. Эти пустоты примыкают к парам оснований и могут обеспечивать сайт связывания . Поскольку пряди не расположены симметрично относительно друг друга, канавки имеют неодинаковый размер. Одна канавка, большая канавка, имеет ширину 22 ангстрем (Å), а другая, малая канавка, имеет ширину 12 Å. [24] Ширина большой канавки означает, что края оснований более доступны в большой канавке, чем в малой канавке. В результате белки, такие как факторы транскрипции, которые могут связываться с конкретными последовательностями в двухцепочечной ДНК, обычно контактируют со сторонами оснований, выставленных в большой бороздке.[25] Эта ситуация варьируется в зависимости от необычных конформаций ДНК внутри клетки (см. Ниже) , но большие и второстепенные бороздки всегда называются так, чтобы отражать различия в размерах, которые будут видны, если ДНК скручивается обратно в обычную B-форму.
Базовая пара
В двойной спирали ДНК каждый тип азотистых оснований на одной цепи связывается только с одним типом азотистых оснований на другой цепи. Это называется дополнительным спариванием оснований . Пурины образуют водородные связи с пиримидинами, причем аденин связывается только с тимином по двум водородным связям, а цитозин связывается только с гуанином по трем водородным связям. Такое расположение двух нуклеотидов, связывающихся вместе по двойной спирали, называется парой оснований Уотсона-Крика. ДНК с высоким содержанием GC более стабильна, чем ДНК с низким содержанием GC. Пара оснований Хугстина - редкий вариант спаривания оснований. [26] Поскольку водородные связи не являются ковалентными, их можно относительно легко сломать и снова соединить. Таким образом, две нити ДНК в двойной спирали могут быть разорваны, как застежка-молния, под действием механической силы или высокой температуры . [27] В результате такой комплементарности пар оснований вся информация в двухцепочечной последовательности спирали ДНК дублируется на каждой цепи, что жизненно важно для репликации ДНК. Это обратимое и специфическое взаимодействие между комплементарными парами оснований имеет решающее значение для всех функций ДНК в организмах. [7]
оцДНК против дцДНК
Как отмечалось выше, большинство молекул ДНК на самом деле представляют собой две полимерные нити, спирально связанные нековалентными связями; эта двухцепочечная ( дцДНК ) структура поддерживается в основном за счет взаимодействия стэкинга внутрицепочечных оснований, которые являются наиболее сильными для стеков G, C. Две цепи могут разделиться - процесс, известный как плавление - с образованием двух молекул одноцепочечной ДНК ( оцДНК ). Плавление происходит при высокой температуре, низком уровне соли и высоком pH (низкий pH также плавит ДНК, но поскольку ДНК нестабильна из-за кислотной депуринизации, низкий pH используется редко).
Стабильность формы дцДНК зависит не только от содержания GC (% пар оснований G, C), но также от последовательности (поскольку укладка зависит от последовательности), а также длины (более длинные молекулы более стабильны). Стабильность можно измерить разными способами; распространенным способом является «температура плавления», которая представляет собой температуру, при которой 50% молекул ds превращаются в молекулы ss; температура плавления зависит от ионной силы и концентрации ДНК. В результате как процент пар оснований GC, так и общая длина двойной спирали ДНК определяют силу ассоциации между двумя цепями ДНК. Длинные спирали ДНК с высоким содержанием GC имеют более сильно взаимодействующие цепи, тогда как короткие спирали с высоким содержанием AT имеют более слабые взаимодействующие цепи. [28]В биологии части двойной спирали ДНК, которые должны легко разделяться, такие как коробка TATAAT Pribnow в некоторых промоторах , как правило, имеют высокое содержание AT, что облегчает разделение цепей. [29]
В лаборатории силу этого взаимодействия можно измерить, определив температуру, необходимую для разрыва половины водородных связей, их температуру плавления (также называемую значением T m ). Когда все пары оснований в двойной спирали ДНК плавятся, цепи разделяются и существуют в растворе как две полностью независимые молекулы. Эти одноцепочечные молекулы ДНК не имеют единой общей формы, но некоторые конформации более стабильны, чем другие. [30]
Смысл и антисмысл
Последовательность ДНК называется «смысловой», если она такая же, как у копии информационной РНК, которая транслируется в белок. [31] Последовательность на противоположной цепи называется «антисмысловой» последовательностью. Как смысловые, так и антисмысловые последовательности могут существовать в разных частях одной и той же цепи ДНК (т.е. обе цепи могут содержать как смысловые, так и антисмысловые последовательности). Как у прокариот, так и у эукариот продуцируются антисмысловые последовательности РНК, но функции этих РНК не совсем ясны. [32] Одно из предположений состоит в том, что антисмысловые РНК участвуют в регуляции экспрессии генов посредством спаривания оснований РНК-РНК. [33]
Несколько последовательностей ДНК в прокариотах и эукариотах и больше в плазмидах и вирусах стирают различие между смысловыми и антисмысловыми цепями из-за перекрывающихся генов . [34] В этих случаях некоторые последовательности ДНК выполняют двойную функцию, кодируя один белок при считывании вдоль одной цепи и второй белок при считывании в противоположном направлении вдоль другой цепи. У бактерий это перекрытие может быть вовлечено в регуляцию транскрипции генов [35], в то время как у вирусов перекрывающиеся гены увеличивают объем информации, которая может быть закодирована в небольшом вирусном геноме. [36]
Суперспирализация
ДНК можно скрутить, как веревку, в процессе, называемом суперспирализацией ДНК . Когда ДНК находится в «расслабленном» состоянии, нить обычно окружает ось двойной спирали каждые 10,4 пары оснований, но если ДНК скручена, нити становятся более плотными или более свободными. [37] Если ДНК скручена в направлении спирали, это положительная суперспирализация, и основания удерживаются вместе более плотно. Если они скручены в противоположном направлении, это отрицательная сверхспирализация, и основания легче распадаются. В природе большая часть ДНК имеет небольшую отрицательную суперспирализацию, которая создается ферментами, называемыми топоизомеразами . [38]Эти ферменты также необходимы для снятия напряжения скручивания, возникающего в цепях ДНК во время таких процессов, как транскрипция и репликация ДНК . [39]
Альтернативные структуры ДНК
ДНК существует во многих возможных конформациях, которые включают формы A-ДНК , B-ДНК и Z-ДНК , хотя только B-ДНК и Z-ДНК наблюдались непосредственно в функциональных организмах. [14] Конформация, которую принимает ДНК, зависит от уровня гидратации, последовательности ДНК, количества и направления суперспирализации, химических модификаций оснований, типа и концентрации ионов металлов , а также присутствия полиаминов в растворе. [40]
В первых опубликованных отчетах о рентгенограммах A-ДНК, а также о B-ДНК использовались анализы, основанные на преобразованиях Паттерсона, которые предоставили лишь ограниченный объем структурной информации для ориентированных волокон ДНК. [41] [42] Альтернативный анализ был предложен Wilkins et al. в 1953 г. для картин дифракции рассеяния рентгеновских лучей B-ДНК in vivo высокогидратированных волокон ДНК в терминах квадратов функций Бесселя . [43] В том же журнале Джеймс Уотсон и Фрэнсис Крик представили свое молекулярное моделирование.анализ дифрактограмм ДНК, чтобы предположить, что структура была двойной спиралью. [9]
Хотя форма B-ДНК наиболее распространена в условиях, встречающихся в клетках, [44] это не четко определенная конформация, а семейство родственных конформаций ДНК [45], которые возникают при высоких уровнях гидратации, присутствующих в клетках. Соответствующие им картины дифракции рентгеновских лучей и рассеяния характерны для молекулярных паракристаллов со значительной степенью беспорядка. [46] [47]
По сравнению с B-ДНК форма A-ДНК представляет собой более широкую правую спираль с мелкой широкой малой бороздкой и более узкой и глубокой большой бороздкой. Форма A встречается в нефизиологических условиях в частично дегидратированных образцах ДНК, тогда как в клетке она может образовываться в гибридных парах ДНК и цепей РНК, а также в комплексах фермент-ДНК. [48] [49] Сегменты ДНК, основания которых были химически модифицированы путем метилирования, могут претерпеть более сильные изменения в конформации и принять Z-форму . Здесь нити вращаются вокруг оси спирали по левой спирали, противоположной более распространенной форме B. [50]Эти необычные структуры могут распознаваться специфическими белками, связывающими Z-ДНК, и могут участвовать в регуляции транскрипции. [51] Исследование 2020 года пришло к выводу, что ДНК стала правосторонней из-за ионизации космическими лучами . [52]
Альтернативная химия ДНК
В течение многих лет экзобиологи предполагали существование теневой биосферы , постулируемой микробной биосферы Земли, в которой используются совершенно иные биохимические и молекулярные процессы, чем в известной в настоящее время жизни. Одним из предложений было существование форм жизни, которые используют мышьяк вместо фосфора в ДНК . В 2010 году был объявлен отчет о возможности наличия у бактерии GFAJ-1 [53] [54], хотя результаты исследования были оспорены, [54] [55], и данные свидетельствуют о том, что бактерия активно предотвращает включение мышьяка в основную цепь ДНК. и другие биомолекулы. [56]
Квадруплексные конструкции
На концах линейных хромосом находятся специализированные участки ДНК, называемые теломерами . Основная функция этих областей - позволить клетке реплицировать концы хромосом с помощью фермента теломеразы , поскольку ферменты, которые обычно реплицируют ДНК, не могут копировать крайние 3'-концы хромосом. [57] Эти специализированные хромосомные крышки также помогают защитить концы ДНК и не позволяют системам репарации ДНК в клетке рассматривать их как повреждения, которые необходимо исправить. [58] В клетках человека теломеры обычно представляют собой отрезки одноцепочечной ДНК, содержащие несколько тысяч повторов простой последовательности TTAGGG. [59]
Эти богатые гуанином последовательности могут стабилизировать концы хромосом, образуя структуры из наборов из четырех оснований, а не обычные пары оснований, обнаруживаемые в других молекулах ДНК. Здесь четыре гуаниновых основания, известные как гуаниновая тетрада , образуют плоскую пластину. Эти плоские блоки с четырьмя базами затем складываются друг на друга, образуя стабильную структуру G-квадруплекса . [61] Эти структуры стабилизируются водородными связями между краями оснований и хелатированием иона металла в центре каждого четырехосновного элемента. [62] Также могут быть сформированы другие структуры, с центральным набором из четырех оснований, исходящих либо из одной нити, сложенной вокруг оснований, либо из нескольких различных параллельных нитей, каждая из которых вносит одну основу в центральную структуру.
В дополнение к этим сложенным друг другу структурам теломеры также образуют большие петлевые структуры, называемые петлями теломер или Т-петлями. Здесь одноцепочечная ДНК закручивается в длинный круг, стабилизированный белками, связывающими теломеры. [63] В самом конце Т-петли одноцепочечная теломерная ДНК удерживается на участке двухцепочечной ДНК теломерной цепью, нарушая двухспиральную ДНК и спаривание оснований с одной из двух цепей. Эта трехцепочечная структура называется петлей смещения или D-петлей . [61]
| Одно отделение | Несколько веток |
Разветвленная ДНК
В ДНК изнашивание происходит, когда на конце комплементарной двойной цепи ДНК существуют некомплементарные области. Однако разветвленная ДНК может возникать, если вводится третья цепь ДНК, и она содержит соседние области, способные гибридизоваться с потрепанными областями ранее существовавшей двойной цепи. Хотя простейший пример разветвленной ДНК включает только три цепи ДНК, также возможны комплексы, включающие дополнительные цепи и несколько ответвлений. [64] Разветвленную ДНК можно использовать в нанотехнологиях для построения геометрических фигур, см. Раздел об использовании в технологии ниже.
Искусственные основы
Было синтезировано несколько искусственных азотистых оснований, которые успешно включены в аналог ДНК из восьми оснований, названный ДНК Хатимоджи . Названные S, B, P и Z, эти искусственные основания способны связываться друг с другом предсказуемым образом (S – B и P – Z), поддерживать структуру двойной спирали ДНК и транскрибироваться в РНК. Их существование можно рассматривать как указание на то, что нет ничего особенного в четырех естественных нуклеиновых основаниях, которые возникли на Земле. [65] [66] С другой стороны, ДНК тесно связана с РНК.который не только действует как транскрипт ДНК, но также выполняет многие задачи в клетках как молекулярные машины. Для этого его нужно сложить в конструкцию. Было показано , что позволит создать все возможные структуры по крайней мере , четыре основания , необходимые для соответствующей РНК , [67] в то время как большее количество также возможно , но это было бы против естественного принципа наименьших усилий .
Химические модификации и измененная упаковка ДНК
| цитозин | 5-метилцитозин | тимин |
Базовые модификации и упаковка ДНК
На экспрессию генов влияет то, как ДНК упакована в хромосомы в структуру, называемую хроматином . Базовые модификации могут быть вовлечены в упаковке, с областями , которые имеют низкий или экспрессию гена , как правило , не содержащую высокие уровни метилирования из цитозина оснований. Упаковка ДНК и ее влияние на экспрессию генов также может происходить путем ковалентных модификаций ядра гистонового белка, вокруг которого ДНК обернута в структуре хроматина, или путем ремоделирования, осуществляемого комплексами ремоделирования хроматина (см. Ремоделирование хроматина ). Кроме того, существует перекрестное взаимодействие между метилированием ДНК и модификацией гистонов, поэтому они могут согласованно влиять на экспрессию хроматина и генов.[68]
Например, метилирование цитозина дает 5-метилцитозин , который важен для X-инактивации хромосом. [69] Средний уровень метилирования варьируется между организмами - червь Caenorhabditis elegans не имеет метилирования цитозина, в то время как позвоночные имеют более высокие уровни, причем до 1% их ДНК содержит 5-метилцитозин. [70] Несмотря на важность 5-метилцитозина, он может дезаминировать, оставляя тиминовое основание, поэтому метилированные цитозины особенно подвержены мутациям . [71] Другие модификации оснований включают метилирование аденина в бактериях, присутствие 5-гидроксиметилцитозина.в головном мозге , [72] и гликозилирование урацила , чтобы произвести «J-основание» в кинетопластиды . [73] [74]
Повреждать
ДНК может быть повреждена многими видами мутагенов , которые изменяют последовательность ДНК . Мутагены включают окислители , алкилирующие агенты, а также высокоэнергетическое электромагнитное излучение, такое как ультрафиолетовый свет и рентгеновские лучи . Тип повреждения ДНК зависит от типа мутагена. Например, ультрафиолетовый свет может повредить ДНК, образуя димеры тимина , которые являются поперечными связями между пиримидиновыми основаниями. [76] С другой стороны, окислители, такие как свободные радикалы или перекись водородавызывают множественные формы повреждений, включая модификации оснований, особенно гуанозина, и двухцепочечные разрывы. [77] Типичная клетка человека содержит около 150 000 оснований, поврежденных окислением. [78] Из этих окислительных повреждений наиболее опасными являются двухцепочечные разрывы, так как они трудно поддаются восстановлению и могут вызывать точечные мутации , вставки , делеции в последовательности ДНК и хромосомные транслокации . [79] Эти мутации могут вызывать рак . Из-за ограничений, присущих механизмам восстановления ДНК, если бы люди жили достаточно долго, у всех в конечном итоге разовьется рак. [80] [81]Повреждения ДНК, которые происходят в природе , из-за нормальных клеточных процессов, которые производят активные формы кислорода, гидролитической активности клеточной воды и т. Д., Также часто происходят. Хотя большая часть этих повреждений восстанавливается, в любой клетке могут оставаться некоторые повреждения ДНК, несмотря на действие процессов восстановления. Эти оставшиеся повреждения ДНК накапливаются с возрастом в постмитотических тканях млекопитающих. Это накопление, по-видимому, является важной первопричиной старения. [82] [83] [84]
Многие мутагены помещаются в пространство между двумя соседними парами оснований, это называется интеркаляцией . Большинство интеркаляторов представляют собой ароматические и плоские молекулы; примеры включают бромид этидия , акридины , дауномицин и доксорубицин . Чтобы интеркалятор поместился между парами оснований, основания должны разделяться, искажая цепи ДНК за счет раскручивания двойной спирали. Это подавляет как транскрипцию, так и репликацию ДНК, вызывая токсичность и мутации. [85] В результате интеркаляторы ДНК могут быть канцерогенами , а в случае талидомида - тератогеном . [86] Другие, такие как бензо [а ] эпоксид пирендиола и афлатоксин образуют аддукты ДНК, которые вызывают ошибки в репликации. [87] Тем не менее, из-за их способности подавлять транскрипцию и репликацию ДНК, другие подобные токсины также используются в химиотерапии для подавления быстрорастущих раковых клеток. [88]
Биологические функции
ДНК обычно встречается в виде линейных хромосом у эукариот и кольцевых хромосом у прокариот . Набор хромосом в клетке составляет ее геном ; геном человека имеет около 3 миллиардов пар оснований ДНК скомпонованы в 46 хромосом. [89] Информация, переносимая ДНК, хранится в последовательности частей ДНК, называемых генами . Передача инфекциигенетической информации в генах достигается за счет комплементарного спаривания оснований. Например, при транскрипции, когда клетка использует информацию в гене, последовательность ДНК копируется в комплементарную последовательность РНК за счет притяжения между ДНК и правильными нуклеотидами РНК. Обычно эта копия РНК затем используется для создания соответствующей белковой последовательности в процессе, называемом трансляцией , который зависит от того же взаимодействия между нуклеотидами РНК. Альтернативно клетка может просто копировать свою генетическую информацию в процессе, называемом репликацией ДНК . Подробности этих функций описаны в других статьях; здесь основное внимание уделяется взаимодействиям между ДНК и другими молекулами, которые обеспечивают функцию генома.
Гены и геномы
Геномная ДНК плотно и упорядоченно упаковывается в процессе, называемом конденсацией ДНК , чтобы соответствовать небольшим доступным объемам клетки. У эукариот ДНК расположена в ядре клетки , а небольшие количества - в митохондриях и хлоропластах . У прокариот ДНК содержится в теле неправильной формы в цитоплазме, называемом нуклеоидом . [90] Генетическая информация в геноме хранится в генах, и полный набор этой информации в организме называется его генотипом . Ген - это единица наследственности и участок ДНК, который влияет на определенные характеристики организма. Гены содержатоткрытая рамка считывания, которая может быть транскрибирована, и регуляторные последовательности, такие как промоторы и энхансеры , которые контролируют транскрипцию открытой рамки считывания.
У многих видов белок кодирует лишь небольшая часть общей последовательности генома . Например, только около 1,5% генома человека состоит из экзонов , кодирующих белок , при этом более 50% ДНК человека состоит из некодирующих повторяющихся последовательностей . [91] Причины наличия такого большого количества некодирующей ДНК в геномах эукариот и необычайные различия в размере генома или C-значении между видами представляют собой давнюю загадку, известную как « загадка C-ценности ». [92] Однако некоторые последовательности ДНК, которые не кодируют белок, могут кодировать функциональную некодирующую РНК.молекулы, которые участвуют в регуляции экспрессии генов . [93]
Некоторые некодирующие последовательности ДНК играют структурную роль в хромосомах. Теломеры и центромеры обычно содержат небольшое количество генов, но они важны для функции и стабильности хромосом. [58] [95] Распространенной формой некодирующей ДНК у людей являются псевдогены , которые представляют собой копии генов, которые были отключены в результате мутации. [96] Эти последовательности обычно представляют собой просто молекулярные окаменелости , хотя иногда они могут служить сырым генетическим материалом для создания новых генов в процессе их дупликации и дивергенции . [97]
Транскрипция и перевод
Ген - это последовательность ДНК, которая содержит генетическую информацию и может влиять на фенотип организма. Внутри гена последовательность оснований вдоль цепи ДНК определяет последовательность информационной РНК , которая затем определяет одну или несколько белковых последовательностей. Взаимосвязь между нуклеотидными последовательностями генов и аминокислотными последовательностями белков определяется правилами трансляции , известными под общим названием генетический код . Генетический код состоит из трехбуквенных «слов», называемых кодонами, образованных из последовательности из трех нуклеотидов (например, ACT, CAG, TTT).
При транскрипции кодоны гена копируются в информационную РНК с помощью РНК-полимеразы . Эта копия РНК затем декодируется рибосомой, которая считывает последовательность РНК путем спаривания оснований информационной РНК для переноса РНК , которая несет аминокислоты. Поскольку существует 4 основания в комбинации 3-буквенных, существует 64 возможных кодонов (4 3 комбинаций). Они кодируют двадцать стандартных аминокислот , давая большинству аминокислот более одного возможного кодона. Есть также три «стоповых» или «бессмысленных» кодона, обозначающих конец кодирующей области; это кодоны TAA, TGA и TAG.
Репликация
Деление клеток необходимо для роста организма, но когда клетка делится, она должна реплицировать ДНК в своем геноме, чтобы две дочерние клетки имели ту же генетическую информацию, что и их родительские. Двухцепочечная структура ДНК обеспечивает простой механизм репликации ДНК . Здесь две нити разделяются, а затем комплементарная последовательность ДНК каждой нити воссоздается ферментом, называемым ДНК-полимеразой . Этот фермент создает комплементарную цепь, находя правильное основание посредством комплементарного спаривания оснований и прикрепляя его к исходной цепи. Поскольку ДНК-полимеразы могут удлинять цепь ДНК только в направлении от 5 'до 3', для копирования антипараллельных цепей двойной спирали используются различные механизмы.[98] Таким образом, основание на старой цепи определяет, какое основание появляется на новой цепи, и в итоге клетка получает идеальную копию своей ДНК.
Внеклеточные нуклеиновые кислоты
Голая внеклеточная ДНК (еДНК), большая часть которой высвобождается в результате гибели клеток, почти повсеместна в окружающей среде. Его концентрация в почве может достигать 2 мкг / л, а в естественной водной среде может достигать 88 мкг / л. [99] Для еДНК были предложены различные возможные функции: она может участвовать в горизонтальном переносе генов ; [100] он может обеспечивать питательными веществами; [101] и может действовать как буфер для набора или титрования ионов или антибиотиков. [102] Внеклеточная ДНК действует как функциональный компонент внеклеточного матрикса в биопленках нескольких видов бактерий. Он может действовать как фактор распознавания, регулирующий прикрепление и распространение определенных типов клеток в биопленке;[103] это может способствовать образованию биопленки; [104], и это может способствовать физической прочности биопленки и устойчивости к биологическому стрессу. [105]
Внеклеточная ДНК плода обнаруживается в крови матери, и ее можно секвенировать, чтобы получить большой объем информации о развивающемся плоде. [106]
Под названием экологической ДНК эДНК стала широко использоваться в естественных науках в качестве инструмента исследования экологии , мониторинга перемещений и присутствия видов в воде, воздухе или на суше, а также оценки биоразнообразия местности. [107] [108]
Взаимодействие с белками
Все функции ДНК зависят от взаимодействия с белками. Эти белковые взаимодействия могут быть неспецифическими, или белок может специфически связываться с одной последовательностью ДНК. Ферменты также могут связываться с ДНК, и из них особенно важны полимеразы, которые копируют последовательность оснований ДНК при транскрипции и репликации ДНК.
ДНК-связывающие белки
Структурные белки, связывающие ДНК, являются хорошо изученными примерами неспецифических ДНК-белковых взаимодействий. Внутри хромосом ДНК находится в комплексах со структурными белками. Эти белки организуют ДНК в компактную структуру, называемую хроматином . У эукариот эта структура включает связывание ДНК с комплексом небольших основных белков, называемых гистонами , тогда как у прокариот задействовано несколько типов белков. [109] [110] Гистоны образуют дискообразный комплекс, называемый нуклеосомой , который содержит два полных витка двухцепочечной ДНК, обернутой вокруг ее поверхности. Эти неспецифические взаимодействия образуются через основные остатки в гистонах, образуя ионные связи.к кислой сахарно-фосфатной основе ДНК и, таким образом, в значительной степени не зависят от последовательности оснований. [111] Химические модификации этих основных аминокислотных остатков включают метилирование , фосфорилирование и ацетилирование . [112] Эти химические изменения изменяют силу взаимодействия между ДНК и гистонами, делая ДНК более или менее доступной для факторов транскрипции и изменяя скорость транскрипции. [113] Другие неспецифические ДНК-связывающие белки в хроматине включают белки группы с высокой подвижностью, которые связываются с изогнутой или искаженной ДНК. [114]Эти белки важны для изгиба массивов нуклеосом и их упорядочения в более крупные структуры, составляющие хромосомы. [115]
Отдельной группой ДНК-связывающих белков являются ДНК-связывающие белки, которые специфически связывают одноцепочечную ДНК. У людей репликационный белок А является наиболее изученным членом этого семейства и используется в процессах, в которых двойная спираль разделяется, включая репликацию ДНК, рекомбинацию и репарацию ДНК. [116] Эти связывающие белки, по-видимому, стабилизируют одноцепочечную ДНК и защищают ее от образования петель или разрушения под действием нуклеаз .
Напротив, другие белки эволюционировали, чтобы связываться с определенными последовательностями ДНК. Наиболее интенсивно из них изучаются различные факторы транскрипции , которые представляют собой белки, регулирующие транскрипцию. Каждый фактор транскрипции связывается с одним конкретным набором последовательностей ДНК и активирует или ингибирует транскрипцию генов, которые имеют эти последовательности, близкие к их промоторам. Факторы транскрипции делают это двумя способами. Во-первых, они могут связываться с РНК-полимеразой, ответственной за транскрипцию, либо напрямую, либо через другие белки-медиаторы; это определяет местонахождение полимеразы на промоторе и позволяет ей начать транскрипцию. [118] Кроме того, факторы транскрипции могут связывать ферменты.которые модифицируют гистоны на промоторе. Это изменяет доступность матрицы ДНК для полимеразы. [119]
Поскольку эти ДНК-мишени могут встречаться по всему геному организма, изменения активности одного типа фактора транскрипции могут влиять на тысячи генов. [120] Следовательно, эти белки часто являются мишенями процессов передачи сигналов, которые контролируют реакции на изменения окружающей среды или клеточную дифференцировку и развитие. Специфичность взаимодействия этих факторов транскрипции с ДНК обусловлена множественными контактами белков с краями оснований ДНК, что позволяет им «читать» последовательность ДНК. Большинство взаимодействий с основанием происходит в большой бороздке, где основания наиболее доступны. [25]
ДНК-модифицирующие ферменты
Нуклеазы и лигазы
Нуклеазы являются ферменты , которые вырезать нити ДНК путем катализировать гидролиз из фосфодиэфирных связей . Нуклеазы, гидролизующие нуклеотиды на концах цепей ДНК, называются экзонуклеазами , а эндонуклеазы разрезаются внутри цепей. Наиболее часто используемые нуклеазы в молекулярной биологии - это эндонуклеазы рестрикции , которые разрезают ДНК по определенным последовательностям. Например, фермент EcoRV, показанный слева, распознает последовательность из 6 оснований 5'-GATATC-3 'и делает разрез на горизонтальной линии. В природе эти ферменты защищают бактерии от фагов.инфекция путем переваривания ДНК фага, когда она попадает в бактериальную клетку, действуя как часть системы рестрикционной модификации . [122] В технологии эти специфичные для последовательности нуклеазы используются при молекулярном клонировании и снятии отпечатков пальцев ДНК .
Ферменты, называемые ДНК-лигазами, могут присоединяться к разрезанным или разорванным цепям ДНК. [123] Лигазы особенно важны в репликации отстающей нити ДНК, поскольку они объединяют короткие сегменты ДНК, образующиеся в репликационной вилке, в полную копию ДНК-матрицы. Они также используются при репарации ДНК и генетической рекомбинации . [123]
Топоизомеразы и геликазы
Топоизомеразы - это ферменты, обладающие как нуклеазной, так и лигазной активностью. Эти белки изменяют степень суперспирализации ДНК. Некоторые из этих ферментов работают, разрезая спираль ДНК и позволяя одной секции вращаться, тем самым снижая уровень ее суперспирализации; фермент затем запечатывает разрыв ДНК. [38] Другие типы этих ферментов способны разрезать одну спираль ДНК, а затем пропускать вторую цепь ДНК через этот разрыв, прежде чем воссоединиться со спиралью. [124] Топоизомеразы необходимы для многих процессов с участием ДНК, таких как репликация ДНК и транскрипция. [39]
Геликазы - это белки, которые представляют собой тип молекулярного мотора . Они используют химическую энергию нуклеозидтрифосфатов , преимущественно аденозинтрифосфата (АТФ), для разрыва водородных связей между основаниями и раскручивания двойной спирали ДНК на одиночные нити. [125] Эти ферменты необходимы для большинства процессов, где ферментам необходим доступ к основаниям ДНК.
Полимеразы
Полимеразы - это ферменты, которые синтезируют полинуклеотидные цепи из нуклеозидтрифосфатов . Последовательность их продуктов создается на основе существующих полинуклеотидных цепей, которые называются шаблонами . Эти ферменты функционируют, многократно добавляя нуклеотид к 3'- гидроксильной группе в конце растущей полинуклеотидной цепи. Как следствие, все полимеразы действуют в направлении от 5 'до 3'. [126] В активном центре этих ферментов входящие пары оснований нуклеозидтрифосфата в матрицу: это позволяет полимеразам точно синтезировать комплементарную цепь своей матрицы. Полимеразы классифицируются по типу используемого шаблона.
При репликации ДНК ДНК-зависимые ДНК-полимеразы создают копии полинуклеотидных цепей ДНК. Для сохранения биологической информации важно, чтобы последовательность оснований в каждой копии была точно комплементарной последовательности оснований в цепи матрицы. Многие ДНК-полимеразы обладают корректирующей активностью. Здесь полимераза распознает случайные ошибки в реакции синтеза из-за отсутствия спаривания оснований между несовпадающими нуклеотидами. Если обнаруживается несоответствие, активируется 3'-5'- экзонуклеазная активность и неправильное основание удаляется. [127] У большинства организмов ДНК-полимеразы функционируют в виде большого комплекса, называемого реплисомой, который содержит множество дополнительных субъединиц, таких какЗажим ДНК или геликазы . [128]
РНК-зависимые ДНК-полимеразы представляют собой специализированный класс полимераз, которые копируют последовательность цепи РНК в ДНК. Они включают обратную транскриптазу , вирусный фермент, участвующий в инфицировании клеток ретровирусами , и теломеразу , которая необходима для репликации теломер. [57] [129] Например, обратная транскриптаза ВИЧ - это фермент для репликации вируса СПИДа. [129] Теломераза - необычная полимераза, потому что она содержит собственную матрицу РНК как часть своей структуры. Он синтезирует теломерына концах хромосом. Теломеры предотвращают слияние концов соседних хромосом и защищают концы хромосом от повреждений. [58]
Транскрипция осуществляется ДНК-зависимой РНК-полимеразой, которая копирует последовательность цепи ДНК в РНК. Чтобы начать транскрибирование гена, РНК-полимераза связывается с последовательностью ДНК, называемой промотором, и разделяет цепи ДНК. Затем он копирует последовательность гена в транскрипт информационной РНК, пока не достигнет области ДНК, называемой терминатором , где она останавливается и отделяется от ДНК. Как и в случае ДНК-зависимых ДНК-полимераз человека, РНК-полимераза II , фермент, транскрибирующий большинство генов в геноме человека, действует как часть большого белкового комплекса с множеством регуляторных и вспомогательных субъединиц. [130]
Генетическая рекомбинация
Спираль ДНК обычно не взаимодействует с другими сегментами ДНК, а в клетках человека разные хромосомы даже занимают отдельные области в ядре, называемые « территориями хромосом ». [132] Это физическое разделение различных хромосом важно для способности ДНК функционировать как стабильное хранилище информации, поскольку один из немногих случаев взаимодействия хромосом - это хромосомный кроссовер, который происходит во время полового размножения , когда происходит генетическая рекомбинация . Хромосомный кроссовер - это когда две спирали ДНК разрываются, меняют местами участок и затем снова соединяются.
Рекомбинация позволяет хромосомам обмениваться генетической информацией и производить новые комбинации генов, что увеличивает эффективность естественного отбора и может иметь важное значение для быстрой эволюции новых белков. [133] Генетическая рекомбинация также может участвовать в репарации ДНК, особенно в ответе клетки на двухцепочечные разрывы. [134]
Наиболее распространенной формой хромосомного кроссовера является гомологичная рекомбинация , при которой две участвующие хромосомы имеют очень похожие последовательности. Негомологичная рекомбинация может повредить клетки, так как она может вызвать хромосомные транслокации и генетические аномалии. Реакция рекомбинации катализируется ферментами, известными как рекомбиназы , такими как RAD51 . [135] Первым этапом рекомбинации является двухцепочечный разрыв, вызванный либо эндонуклеазой, либо повреждением ДНК. [136] Затем серия шагов, частично катализируемых рекомбиназой, приводит к соединению двух спиралей по крайней мере одним соединением Холлидея., в котором сегмент одной нити в каждой спирали отжигается с комплементарной цепью в другой спирали. Соединение Холлидея - это тетраэдрическая структура соединения, которую можно перемещать вдоль пары хромосом, заменяя одну нить на другую. Затем реакцию рекомбинации останавливают расщеплением соединения и повторным лигированием высвободившейся ДНК. [137] Во время рекомбинации ДНК меняют только цепи одинаковой полярности. Существует два типа расщепления: расщепление восток-запад и расщепление север-юг. Расщепление север-юг разрезает обе нити ДНК, тогда как расщепление восток-запад сохраняет одну нить ДНК нетронутой. Образование соединения Холлидея во время рекомбинации делает возможным генетическое разнообразие, обмен генами на хромосомах и экспрессию вирусных геномов дикого типа.
Эволюция
ДНК содержит генетическую информацию, которая позволяет всем формам жизни функционировать, расти и воспроизводиться. Однако неясно, как долго за 4 миллиарда лет истории жизни ДНК выполняла эту функцию, поскольку было высказано предположение, что самые ранние формы жизни могли использовать РНК в качестве своего генетического материала. [138] [139] РНК могла выступать в качестве центральной части раннего клеточного метаболизма, поскольку она может как передавать генетическую информацию, так и осуществлять катализ в составе рибозимов . [140] Этот древний мир РНК, где нуклеиновые кислоты использовались как для катализа, так и для генетики, возможно, повлияли на эволюциюсовременного генетического кода на основе четырех нуклеотидных оснований. Это могло бы произойти, поскольку количество различных оснований в таком организме представляет собой компромисс между небольшим количеством оснований, увеличивающим точность репликации, и большим количеством оснований, повышающих каталитическую эффективность рибозимов. [141] Однако нет прямых доказательств существования древних генетических систем, поскольку восстановление ДНК из большинства окаменелостей невозможно, потому что ДНК выживает в окружающей среде менее одного миллиона лет и медленно распадается на короткие фрагменты в растворе. [142] Заявления о более древней ДНК были сделаны, в первую очередь сообщение об изоляции жизнеспособной бактерии из кристалла соли 250 миллионов лет, [143] но эти утверждения являются спорными. [144] [145]
Строительные блоки ДНК ( аденин , гуанин и родственные органические молекулы ) могли быть сформированы внеземными цивилизациями в космическом пространстве . [146] [147] [148] Комплекс ДНК и РНК органические соединения из жизни , в том числе урацила , цитозина и тимина , также были сформированы в лаборатории в условиях , имитирующих те , что в космическом пространстве , с использованием исходных химических веществ, такие как пиримидин , найдено в метеоритах . Пиримидин, как полициклические ароматические углеводороды(ПАУ), наиболее богатое углеродом химическое вещество во Вселенной , возможно, образовалось в красных гигантах или в межзвездных облаках космической пыли и газа. [149]
В феврале 2021 года ученые впервые сообщили о секвенировании ДНК останков животных , в данном случае мамонта, возрастом более миллиона лет, - самой старой ДНК, секвенированной на сегодняшний день. [150] [151]
Использование в технологии
Генная инженерия
Были разработаны методы очистки ДНК от организмов, такие как экстракция фенол-хлороформ , и манипуляции с ней в лаборатории, такие как рестрикционные расщепления и полимеразная цепная реакция . Современная биология и биохимия интенсивно используют эти методы в технологии рекомбинантных ДНК. Рекомбинантная ДНК - это последовательность ДНК, созданная человеком, которая была собрана из других последовательностей ДНК. Они могут быть трансформированы в организмы в форме плазмид или в соответствующем формате с использованием вирусного вектора . [152] генетически модифицированныеорганизмы , полученные может быть использовано для получения продуктов , таких как рекомбинантные белки , используемых в медицинских исследованиях , [153] или быть выращены в сельском хозяйстве . [154] [155]
ДНК-профилирование
Судебно-медицинские эксперты могут использовать ДНК крови , спермы , кожи , слюны или волос, обнаруженных на месте преступления, чтобы идентифицировать совпадающую ДНК человека, например преступника. [156] Этот процесс формально называется профилированием ДНК , также называемым дактилоскопией ДНК . При профилировании ДНК между людьми сравнивается длина различных участков повторяющейся ДНК, таких как короткие тандемные повторы и минисателлиты . Этот метод обычно является чрезвычайно надежным методом выявления совпадающей ДНК. [157]Однако идентификация может быть затруднена, если место происшествия заражено ДНК нескольких человек. [158] ДНК , профилирование был разработан в 1984 году британский генетик сэр Алек Джеффрис , [159] и впервые использована в криминалистике обличить Питчфорк в 1988 убийствах Эндерби случае. [160]
Развитие судебной медицины и возможность теперь получать генетическое соответствие на мельчайших образцах крови, кожи, слюны или волос привели к пересмотру многих случаев. Теперь могут быть обнаружены доказательства, которые были невозможны с научной точки зрения во время первоначального исследования. В сочетании с отменой закона о двойной ответственности в некоторых местах это может позволить возобновить дела, если предыдущие судебные процессы не смогли предоставить достаточных доказательств, чтобы убедить присяжных. Людей, обвиняемых в серьезных преступлениях, могут попросить предоставить образец ДНК для сопоставления. Наиболее очевидная защита от совпадений ДНК, полученных судебно-медицинскими методами, - это утверждение о перекрестном заражении улик. Это привело к тщательно продуманным и строгим процедурам рассмотрения новых случаев серьезных преступлений.
ДНК-профилирование также успешно используется для точной идентификации жертв массовых несчастных случаев [161], тел или частей тел в серьезных авариях, а также отдельных жертв в массовых военных захоронениях путем сопоставления с членами семьи.
ДНК-профилирование также используется в ДНК-тестировании отцовства, чтобы определить, является ли кто-либо биологическим родителем или бабушкой или дедушкой ребенка с вероятностью отцовства обычно 99,99%, когда предполагаемый родитель биологически связан с ребенком. Обычные методы секвенирования ДНК применяются после рождения ребенка, но есть новые методы проверки отцовства, когда мать еще беременна. [162]
Ферменты ДНК или каталитическая ДНК
Дезоксирибозимы , также называемые ДНКзимами или каталитической ДНК, были впервые обнаружены в 1994 году. [163] Они в основном представляют собой одноцепочечные последовательности ДНК, выделенные из большого пула случайных последовательностей ДНК с помощью комбинаторного подхода, называемого отбором in vitro или систематической эволюцией лигандов путем экспоненциального обогащения. (SELEX). ДНКзимы катализируют различные химические реакции, включая расщепление РНК-ДНК, лигирование РНК-ДНК, фосфорилирование-дефосфорилирование аминокислот, образование углерод-углеродных связей и т. Д. ДНКзимы могут увеличивать каталитическую скорость химических реакций до 100000000000 раз по сравнению с некаталитической реакцией. [164]Наиболее широко изученный класс ДНКзимов - это типы, расщепляющие РНК, которые использовались для обнаружения различных ионов металлов и создания терапевтических агентов. Сообщалось о нескольких металлоспецифичных ДНКзимах, включая ДНКзим GR-5 (специфический для свинца), [163] ДНКзим CA1-3 (медьспецифический), [165] ДНКзим 39E (специфичный для уранила) и ДНКзим NaA43 ( натрий-специфический). [166] ДНКзим NaA43, который, как сообщается, более чем в 10 000 раз селективен к натрию по сравнению с ионами других металлов, был использован для создания сенсора натрия в клетках в реальном времени.
Биоинформатика
Биоинформатика включает в себя разработку методов хранения, сбора данных , поиска и обработки биологических данных, включая данные о последовательностях нуклеиновых кислот ДНК . Это привело к широко применяемым достижениям в области информатики , особенно алгоритмов поиска строк , машинного обучения и теории баз данных . [167] Для поиска конкретных последовательностей нуклеотидов были разработаны алгоритмы поиска строк или сопоставления, которые находят вхождение последовательности букв внутри более крупной последовательности букв. [168] Последовательность ДНК может быть выровнена с другими последовательностями ДНК для идентификациигомологичные последовательности и найдите конкретные мутации, которые делают их отличными. Эти методы, особенно множественное выравнивание последовательностей , используются для изучения филогенетических отношений и функции белков. [169] Наборы данных, представляющие ценность последовательностей ДНК целого генома, например, полученные в рамках Human Genome Project , трудно использовать без аннотаций, которые определяют расположение генов и регуляторных элементов на каждой хромосоме. Области последовательности ДНК, которые имеют характерные паттерны, связанные с генами, кодирующими белки или РНК, могут быть идентифицированы с помощью алгоритмов поиска генов , которые позволяют исследователям предсказывать наличие определенныхгенные продукты и их возможные функции в организме еще до того, как они были выделены экспериментально. [170] Также можно сравнивать целые геномы, что может пролить свет на эволюционную историю конкретного организма и позволить исследовать сложные эволюционные события.
ДНК-нанотехнологии
Нанотехнология ДНК использует уникальные свойства молекулярного распознавания ДНК и других нуклеиновых кислот для создания самособирающихся разветвленных комплексов ДНК с полезными свойствами. [171] Таким образом, ДНК используется как структурный материал, а не как носитель биологической информации. Это привело к созданию двумерных периодических решеток (как из плиток, так и с использованием метода ДНК-оригами ) и трехмерных структур в форме многогранников . [172] Наномеханические устройства и алгоритмическая самосборка также были продемонстрированы, [173] и эти структуры ДНК были использованы для создания шаблона расположения других молекул, таких какнаночастицы золота и белки стрептавидина . [174]
История и антропология
Поскольку ДНК собирает мутации с течением времени, которые затем передаются по наследству, она содержит историческую информацию, и, сравнивая последовательности ДНК, генетики могут сделать выводы об эволюционной истории организмов, их филогенезе . [175] Эта область филогенетики - мощный инструмент эволюционной биологии . Если сравнить последовательности ДНК внутри вида, популяционные генетики могут узнать историю конкретных популяций. Это может быть использовано в различных исследованиях, от экологической генетики до антропологии .
Хранение информации
ДНК как устройство хранения информации имеет огромный потенциал, поскольку она имеет гораздо более высокую плотность хранения по сравнению с электронными устройствами. Однако высокая стоимость, чрезвычайно медленное время чтения и записи ( задержка памяти ) и недостаточная надежность препятствовали его практическому использованию. [176] [177]
История
ДНК была впервые выделена швейцарским врачом Фридрихом Мишером, который в 1869 году обнаружил микроскопическое вещество в гноях выброшенных хирургических повязок. Поскольку он находился в ядрах клеток, он назвал его «нуклеином». [178] [179] В 1878 году Альбрехт Коссель выделил небелковый компонент «нуклеина», нуклеиновой кислоты, а позже выделил пять его основных азотистых оснований . [180] [181]
В 1909 году Фебус Левен идентифицировал основание, сахар и фосфатно-нуклеотидную единицу РНК (затем названную «нуклеиновой кислотой дрожжей»). [182] [183] [184] В 1929 году Левен идентифицировал сахар дезоксирибозы в «нуклеиновой кислоте тимуса» (ДНК). [185] Левен предположил, что ДНК состоит из цепочки из четырех нуклеотидных единиц, связанных друг с другом через фосфатные группы («тетрануклеотидная гипотеза»). Левен думал, что цепь короткая, а основания повторяются в фиксированном порядке. В 1927 году Николай Кольцов предположил, что унаследованные черты будут унаследованы через «гигантскую наследственную молекулу», состоящую из «двух зеркальных цепей, которые будут воспроизводиться полуконсервативным образом, используя каждую цепочку в качестве шаблона».[186] [187]В 1928 году Фредерик Гриффит в своем эксперименте обнаружил, что черты «гладкой» формы пневмококка могут быть переданы «грубой» форме тех же бактерий путем смешивания убитых «гладких» бактерий с живой «грубой» формой. [188] [189] Эта система дала первое четкое предположение о том, что ДНК несет генетическую информацию.
В 1933 году, изучая яйца девственных морских ежей , Жан Брахе предположил, что ДНК находится в ядре клетки, а РНК присутствует исключительно в цитоплазме . В то время считалось, что «нуклеиновая кислота дрожжей» (РНК) встречается только в растениях, а «нуклеиновая кислота тимуса» (ДНК) - только у животных. Последний считался тетрамером с функцией буферизации клеточного pH. [190] [191]
В 1937 году Уильям Эстбери создал первые дифракционные рентгеновские лучи, которые показали, что ДНК имеет правильную структуру. [192]
В 1943 году Освальд Эйвери вместе с коллегами Колином МакЛаудом и Маклином Маккарти идентифицировали ДНК как трансформирующий принцип , поддерживая предположение Гриффита ( эксперимент Эйвери-Маклауда-Маккарти ). [193] В конце 1951 года, Фрэнсис Крик начал работать с Джеймсом Уотсоном в Кавендишской лаборатории в Кембриджском университете . Роль ДНК в наследственности была подтверждена в 1952 году, когда Альфред Херши и Марта Чейз в эксперименте Херши-Чейза показали, что ДНК - этогенетический материал из энтеробактерий фага Т2 . [194]
В мае 1952 года Раймонд Гослинг , аспирант, работавший под руководством Розалинды Франклин , сделал рентгеновское изображение, обозначенное как « Фото 51 », [195] при высоких уровнях гидратации ДНК. Эта фотография была предоставлена Уотсону и Крику Морисом Уилкинсом и имела решающее значение для получения правильной структуры ДНК. Франклин сказал Крику и Ватсону, что костяк должен быть снаружи. До этого у Линуса Полинга, Уотсона и Крика были ошибочные модели с цепями внутри и основанием, направленными наружу. Ее определение космической группы кристаллов ДНК показало Крику, что две цепи ДНК антипараллельны.. [196]
В феврале 1953 года Линус Полинг и Роберт Кори предложили модель нуклеиновых кислот, содержащую три переплетенные цепи, с фосфатами около оси и основаниями снаружи. [197] Уотсон и Крик завершили свою модель, которая теперь принята как первая правильная модель двойной спирали ДНК . 28 февраля 1953 года Крик прервал обеденный перерыв для посетителей в пабе Eagle в Кембридже, чтобы объявить, что они с Ватсоном «открыли секрет жизни». [198]
В выпуске журнала Nature от 25 апреля 1953 г. была опубликована серия из пяти статей, в которых приводилась структура ДНК Ватсона и Крика с двойной спиралью и подтверждающие ее доказательства. [199] О структуре сообщалось в письме, озаглавленном « МОЛЕКУЛЯРНАЯ СТРУКТУРА ЯДЕРНЫХ КИСЛОТ. Структура для нуклеиновой кислоты дезоксирибозы », в котором они сказали: «Наше внимание не ускользнуло от нашего внимания, что определенная пара, которую мы постулировали, сразу предполагает возможный механизм копирования. для генетического материала ". [9] Затем следует письмо Франклина и Гослинга, которое было первой публикацией их собственных данных дифракции рентгеновских лучей и их оригинального метода анализа. [42] [200]Затем последовало письмо Уилкинса и двух его коллег, в котором содержался анализ структуры рентгеновских лучей B-ДНК in vivo и поддерживалось присутствие in vivo структуры Уотсона и Крика. [43]
В 1962 году, после смерти Франклина, Уотсон, Крик и Уилкинс совместно получили Нобелевскую премию по физиологии и медицине . [201] Нобелевские премии присуждаются только живым лауреатам. Продолжаются споры о том, кому следует признать открытие. [202]
В своей влиятельной презентации в 1957 году Крик изложил центральную догму молекулярной биологии , которая предсказала взаимосвязь между ДНК, РНК и белками, и сформулировал «гипотезу адаптера». [203] Окончательное подтверждение механизма репликации, подразумеваемого двойной спиральной структурой, за которой в 1958 году последовал эксперимент Мезельсона-Шталя . [204] Дальнейшая работа Крика и его сотрудников показала, что генетический код основан на неперекрывающихся триплетах оснований, называемых кодонами , что позволило Хар Гобинд Хорана , Роберту У. Холли и Маршаллу Уоррену Ниренбергу расшифровать генетический код. [205]Эти открытия представляют собой рождение молекулярной биологии . [206]
Смотрите также
- Аутосома - любая хромосома, кроме половой.
- Сравнение программного обеспечения для моделирования нуклеиновых кислот
- Кристаллография - научное исследование кристаллической структуры
- ДНК-кодированная химическая библиотека
- Микрочип ДНК
- Генетическое заболевание - проблема со здоровьем, вызванная одной или несколькими аномалиями в геноме.
- Генетическая генеалогия - использование ДНК-тестирования в сочетании с традиционными генеалогическими методами для установления родства между людьми и поиска предков.
- Гаплотип - группа генов от одного родителя
- Мейоз - Тип деления клеток у организмов, размножающихся половым путем, используемых для производства гамет.
- Обозначение нуклеиновых кислот - универсальное обозначение с использованием латинских букв A, C, G и T для обозначения четырех нуклеотидов ДНК.
- Последовательность нуклеиновой кислоты - последовательность нуклеотидов в нуклеиновой кислоте
- Пангенезис - бывшая теория, согласно которой наследование основывалось на частицах из всех частей тела.
- Фосфорамидит
- Рибосомная ДНК
- Саузерн-блот
- Методы рассеяния рентгеновских лучей
- Ксено нуклеиновая кислота
Рекомендации
- ^ «дезоксирибонуклеиновая кислота» . Словарь Мерриама-Вебстера .
- Перейти ↑ Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P (2014). Молекулярная биология клетки (6-е изд.). Гирлянда. п. Глава 4: ДНК, хромосомы и геномы. ISBN 978-0-8153-4432-2. Архивировано 14 июля 2014 года.
- ^ Перселл А. «ДНК» . Основы биологии . Архивировано 5 января 2017 года.
- ^ "Урацил" . Genome.gov . Проверено 21 ноября 2019 .
- Перейти ↑ Russell P (2001). iGenetics . Нью-Йорк: Бенджамин Каммингс. ISBN 0-8053-4553-1.
- ^ Saenger Вт (1984). Принципы строения нуклеиновых кислот . Нью-Йорк: Springer-Verlag. ISBN 0-387-90762-9.
- ^ a b Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Питер В. (2002). Молекулярная биология клетки (Четвертое изд.). Нью-Йорк и Лондон: Наука о гирляндах. ISBN 0-8153-3218-1. OCLC 145080076 . Архивировано 1 ноября 2016 года.
- ^ Иробалиева RN, Фогг JM, Catanese DJ, Catanese DJ, Sutthibutpong T, Chen M, Barker AK, Ludtke SJ, Harris SA, Schmid MF, Chiu W, Zechiedrich L (октябрь 2015 г.). «Структурное разнообразие суперспиральной ДНК» . Nature Communications . 6 : 8440. Bibcode : 2015NatCo ... 6.8440I . DOI : 10.1038 / ncomms9440 . ISSN 2041-1723 . PMC 4608029 . PMID 26455586 .
- ^ a b c d Уотсон Дж. Д., Крик Ф. Х. (апрель 1953 г.). «Молекулярная структура нуклеиновых кислот; структура нуклеиновой кислоты дезоксирибозы» (PDF) . Природа . 171 (4356): 737–38. Bibcode : 1953Natur.171..737W . DOI : 10.1038 / 171737a0 . ISSN 0028-0836 . PMID 13054692 . S2CID 4253007 . Архивировано 4 февраля 2007 года (PDF) .
- ^ Манделькерна M, Элиас JG, Eden D, Crothers DM (октябрь 1981). «Размеры ДНК в растворе». Журнал молекулярной биологии . 152 (1): 153–61. DOI : 10.1016 / 0022-2836 (81) 90099-1 . ISSN 0022-2836 . PMID 7338906 .
- ^ Грегори С.Г., Барлоу К.Ф., Маклей К.Э., Каул Р., Сварбрек Д., Данхэм А. и др. (Май 2006 г.). «Последовательность ДНК и биологическая аннотация хромосомы 1 человека» . Природа . 441 (7091): 315–21. Bibcode : 2006Natur.441..315G . DOI : 10,1038 / природа04727 . PMID 16710414 .
- ^ а б в Берг Дж, Тимочко Дж, Страйер Л (2002). Биохимия . WH Freeman and Company. ISBN 0-7167-4955-6.
- ^ Комиссия IUPAC-IUB по биохимической номенклатуре (CBN) (декабрь 1970). «Аббревиатуры и символы нуклеиновых кислот, полинуклеотидов и их составляющих. Рекомендации 1970» . Биохимический журнал . 120 (3): 449–54. DOI : 10.1042 / bj1200449 . ISSN 0306-3283 . PMC 1179624 . PMID 5499957 . Архивировано из оригинала 5 февраля 2007 года.
- ^ a b Ghosh A, Bansal M (апрель 2003 г.). «Глоссарий структур ДНК от А до Я». Acta Crystallographica Раздел D . 59 (Pt 4): 620–26. DOI : 10.1107 / S0907444903003251 . ISSN 0907-4449 . PMID 12657780 .
- ^ Создано из PDB 1D65
- ^ Яковчук P, E Protozanova, Франк-Каменецкий MD (2006). «Вклады укладки оснований и спаривания оснований в термостабильность двойной спирали ДНК» . Исследования нуклеиновых кислот . 34 (2): 564–74. DOI : 10.1093 / NAR / gkj454 . ISSN 0305-1048 . PMC 1360284 . PMID 16449200 .
- ^ Тропп BE (2012). Молекулярная биология (4-е изд.). Садбери, Массачусетс: Обучение Джонс и Барлетт. ISBN 978-0-7637-8663-2.
- ^ Карр S (1953). «Структура ДНК Ватсона-Крика» . Мемориальный университет Ньюфаундленда. Архивировано 19 июля 2016 года . Дата обращения 13 июля 2016 .
- Перейти ↑ Verma S, Eckstein F (1998). «Модифицированные олигонуклеотиды: синтез и стратегия для пользователей» . Ежегодный обзор биохимии . 67 : 99–134. DOI : 10.1146 / annurev.biochem.67.1.99 . ISSN 0066-4154 . PMID 9759484 .
- ^ Джонсон TB, Coghill RD (1925). «Пиримидины. CIII. Открытие 5-метилцитозина в туберкулиновой кислоте, нуклеиновой кислоте туберкулезной палочки». Журнал Американского химического общества . 47 : 2838–44. DOI : 10.1021 / ja01688a030 . ISSN 0002-7863 .
- ^ Weigele P, Raleigh EA (октябрь 2016). «Биосинтез и функция модифицированных оснований у бактерий и их вирусов» . Химические обзоры . 116 (20): 12655–12687. DOI : 10.1021 / acs.chemrev.6b00114 . ISSN 0009-2665 . PMID 27319741 .
- ^ Кумар S, Chinnusamy В, Мохапатра Т (2018). «Эпигенетика модифицированных оснований ДНК: 5-метилцитозин и не только» . Границы генетики . 9 : 640. DOI : 10,3389 / fgene.2018.00640 . ISSN 1664-8021 . PMC 6305559 . PMID 30619465 .
- ↑ Carell T, Kurz MQ, Müller M, Rossa M, Spada F (апрель 2018 г.). «Неканонические основы в геноме: регулирующий информационный слой в ДНК». Angewandte Chemie . 57 (16): 4296–4312. DOI : 10.1002 / anie.201708228 . PMID 28941008 .
- ↑ Wing R, Drew H, Takano T, Broka C, Tanaka S, Itakura K, Dickerson RE (октябрь 1980 г.). «Анализ кристаллической структуры полного витка B-ДНК». Природа . 287 (5784): 755–58. Bibcode : 1980Natur.287..755W . DOI : 10.1038 / 287755a0 . PMID 7432492 . S2CID 4315465 .
- ↑ a b Pabo CO, Sauer RT (1984). «Узнавание белка-ДНК». Ежегодный обзор биохимии . 53 : 293–321. DOI : 10.1146 / annurev.bi.53.070184.001453 . PMID 6236744 .
- ^ Николова Э.Н., Чжоу Х., Готтардо Флорида, Алви Х.С., Кимси И.Дж., Аль-Хашими Х.М. (2013). "Исторический счет пар оснований Хугстина в дуплексной ДНК" . Биополимеры . 99 (12): 955–68. DOI : 10.1002 / bip.22334 . PMC 3844552 . PMID 23818176 .
- ^ Клэюзн-Шауманн Н, М Риф, Тольксдорф С, Gaub ОН (апрель 2000 г.). «Механическая стабильность одиночных молекул ДНК» . Биофизический журнал . 78 (4): 1997–2007. Bibcode : 2000BpJ .... 78.1997C . DOI : 10.1016 / S0006-3495 (00) 76747-6 . PMC 1300792 . PMID 10733978 .
- ^ Chalikian TV, Фёлькер J, Слива GE, Breslauer KJ (июль 1999). «Более унифицированная картина термодинамики плавления дуплекса нуклеиновой кислоты: характеристика калориметрическими и волюметрическими методами» . Труды Национальной академии наук Соединенных Штатов Америки . 96 (14): 7853–58. Bibcode : 1999PNAS ... 96.7853C . DOI : 10.1073 / pnas.96.14.7853 . PMC 22151 . PMID 10393911 .
- ^ deHaseth PL, Helmann JD (июнь 1995 г.). «Образование открытого комплекса РНК-полимеразой Escherichia coli: механизм полимеразно-индуцированного разделения цепей двойной спиральной ДНК». Молекулярная микробиология . 16 (5): 817–24. DOI : 10.1111 / j.1365-2958.1995.tb02309.x . PMID 7476180 . S2CID 24479358 .
- ^ Исакссон J, Ачарья S, Бармен Дж, Cheruku Р, Chattopadhyaya J (декабрь 2004 г.). «Одноцепочечные богатые аденином ДНК и РНК сохраняют структурные характеристики своих соответствующих двухцепочечных конформаций и демонстрируют направленные различия в структуре укладки» (PDF) . Биохимия . 43 (51): 15996–6010. DOI : 10.1021 / bi048221v . PMID 15609994 . Архивировано 10 июня 2007 года (PDF) .
- ↑ Обозначение двух цепей ДНК. Архивировано 24 апреля 2008 г. в информационном бюллетене Wayback Machine JCBN / NC-IUB 1989 г. Проверено 7 мая 2008 г.
- ^ Hüttenhofer A, Schattner P, Poláček N (май 2005). «Некодирующие РНК: надежда или шумиха?». Тенденции в генетике . 21 (5): 289–97. DOI : 10.1016 / j.tig.2005.03.007 . PMID 15851066 .
- ^ Манро SH (ноябрь 2004). «Разнообразие антисмысловой регуляции у эукариот: множественные механизмы, новые паттерны». Журнал клеточной биохимии . 93 (4): 664–71. DOI : 10.1002 / jcb.20252 . PMID 15389973 . S2CID 23748148 .
- ^ Makalowska I, Lin CF, Makalowski W (февраль 2005). «Перекрывающиеся гены в геномах позвоночных». Вычислительная биология и химия . 29 (1): 1–12. DOI : 10.1016 / j.compbiolchem.2004.12.006 . PMID 15680581 .
- ^ Джонсон З.И., Чишолй SW (ноябрь 2004). «Свойства перекрывающихся генов сохраняются в микробных геномах» . Геномные исследования . 14 (11): 2268–72. DOI : 10.1101 / gr.2433104 . PMC 525685 . PMID 15520290 .
- Перейти ↑ Lamb RA, Horvath CM (август 1991). «Разнообразие стратегий кодирования вирусов гриппа» . Тенденции в генетике . 7 (8): 261–66. DOI : 10.1016 / 0168-9525 (91) 90326-L . PMC 7173306 . PMID 1771674 .
- ^ Benham CJ, Мильке SP (2005). «Механика ДНК» (PDF) . Ежегодный обзор биомедицинской инженерии . 7 : 21–53. DOI : 10.1146 / annurev.bioeng.6.062403.132016 . PMID 16004565 . S2CID 1427671 .
- ^ а б Шампу JJ (2001). «Топоизомеразы ДНК: структура, функция и механизм» (PDF) . Ежегодный обзор биохимии . 70 : 369–413. DOI : 10.1146 / annurev.biochem.70.1.369 . PMID 11395412 . S2CID 18144189 .
- ^ a b Wang JC (июнь 2002 г.). «Клеточные роли топоизомераз ДНК: молекулярная перспектива». Обзоры природы Молекулярная клеточная биология . 3 (6): 430–40. DOI : 10.1038 / nrm831 . PMID 12042765 . S2CID 205496065 .
- ^ Басу HS, Феюрштайн BG, Zarling Д.А., Шефер RH, Мартон LJ (октябрь 1988). «Распознавание детерминант Z-РНК и Z-ДНК полиаминами в растворе: экспериментальные и теоретические исследования». Журнал биомолекулярной структуры и динамики . 6 (2): 299–309. DOI : 10.1080 / 07391102.1988.10507714 . PMID 2482766 .
- ^ Franklin RE, Гослинг RG (6 марта 1953). "Структура тимонуклеатных волокон натрия I. Влияние содержания воды" (PDF) . Acta Crystallogr . 6 (8–9): 673–77. DOI : 10.1107 / S0365110X53001939 . Архивировано (PDF) из оригинала 9 января 2016 года.
Франклин Р. Е., Гослинг Р. Г. (1953). «Структура волокон тимонуклеата натрия. II. Цилиндрически симметричная функция Паттерсона» (PDF) . Acta Crystallogr . 6 (8–9): 678–85. DOI : 10.1107 / S0365110X53001940 . - ^ a b Франклин RE, Гослинг RG (апрель 1953 г.). «Молекулярная конфигурация в тимонуклеате натрия» (PDF) . Природа . 171 (4356): 740–41. Bibcode : 1953Natur.171..740F . DOI : 10.1038 / 171740a0 . PMID 13054694 . S2CID 4268222 . Архивировано 3 января 2011 года (PDF) .
- ^ a b Wilkins MH, Stokes AR, Wilson HR (апрель 1953 г.). «Молекулярная структура дезоксипентозных нуклеиновых кислот» (PDF) . Природа . 171 (4356): 738–40. Bibcode : 1953Natur.171..738W . DOI : 10.1038 / 171738a0 . PMID 13054693 . S2CID 4280080 . Архивировано 13 мая 2011 года (PDF) .
- Перейти ↑ Leslie AG, Arnott S, Chandrasekaran R, Ratliff RL (октябрь 1980 г.). «Полиморфизм двойных спиралей ДНК». Журнал молекулярной биологии . 143 (1): 49–72. DOI : 10.1016 / 0022-2836 (80) 90124-2 . PMID 7441761 .
- ^ Baianu IC (1980). «Структурный порядок и частичный беспорядок в биологических системах» . Бык. Математика. Биол . 42 (4): 137–41. DOI : 10.1007 / BF02462372 . S2CID 189888972 .
- ^ Hosemann R, Багчи Р. Н. (1962). Прямой анализ дифракции на веществе . Амстердам - Нью-Йорк: Издательство Северной Голландии.
- ^ Baianu IC (1978). «Рассеяние рентгеновских лучей частично неупорядоченными мембранными системами» (PDF) . Acta Crystallogr . 34 (5): 751–53. Bibcode : 1978AcCrA..34..751B . DOI : 10.1107 / S0567739478001540 .
- ^ Wahl MC, Сундаралинги M (1997). «Кристаллические структуры дуплексов А-ДНК». Биополимеры . 44 (1): 45–63. DOI : 10.1002 / (SICI) 1097-0282 (1997) 44: 1 <45 :: AID-BIP4> 3.0.CO; 2- # . PMID 9097733 .
- ^ Lu XJ, Shakked Z, Olson WK (июль 2000). «Конформационные мотивы А-формы в лиганд-связанных структурах ДНК». Журнал молекулярной биологии . 300 (4): 819–40. DOI : 10.1006 / jmbi.2000.3690 . PMID 10891271 .
- ↑ Rothenburg S, Koch-Nolte F, Haag F (декабрь 2001 г.). «Метилирование ДНК и образование Z-ДНК как медиаторы количественных различий в экспрессии аллелей». Иммунологические обзоры . 184 : 286–98. DOI : 10.1034 / j.1600-065x.2001.1840125.x . PMID 12086319 . S2CID 20589136 .
- Перейти ↑ Oh DB, Kim YG, Rich A (декабрь 2002 г.). «Z-ДНК-связывающие белки могут действовать как мощные эффекторы экспрессии генов in vivo» . Труды Национальной академии наук Соединенных Штатов Америки . 99 (26): 16666–71. Bibcode : 2002PNAS ... 9916666O . DOI : 10.1073 / pnas.262672699 . PMC 139201 . PMID 12486233 .
- ↑ Globus N, Blandford RD (20 мая 2020 г.). «Хиральная загадка жизни». Письма в астрофизический журнал . 895 (1): L11. arXiv : 2002.12138 . Bibcode : 2020ApJ ... 895L..11G . DOI : 10.3847 / 2041-8213 / ab8dc6 . S2CID 211532577 .
- ↑ Палмер Дж (2 декабря 2010 г.). «Любящие мышьяк бактерии могут помочь в охоте за инопланетной жизнью» . BBC News . Архивировано 3 декабря 2010 года . Проверено 2 декабря 2010 года .
- ^ a b Bortman H (2 декабря 2010 г.). «Бактерии, поедающие мышьяк, открывают новые возможности для инопланетной жизни» . Space.com . Архивировано 4 декабря 2010 года . Проверено 2 декабря 2010 года .
- ↑ Кацнельсон A (2 декабря 2010 г.). «Микроб, поедающий мышьяк, может изменить химию жизни» . Новости природы . DOI : 10.1038 / news.2010.645 . Архивировано 12 февраля 2012 года.
- ^ Кресся D (3 октября 2012). « Бактерия « Arsenic-life »все-таки предпочитает фосфор». Новости природы . DOI : 10.1038 / nature.2012.11520 . S2CID 87341731 .
- ↑ a b Greider CW, Blackburn EH (декабрь 1985 г.). «Идентификация специфической активности терминальной трансферазы теломер в экстрактах Tetrahymena» . Cell . 43 (2 Пет 1): 405–13. DOI : 10.1016 / 0092-8674 (85) 90170-9 . PMID 3907856 .
- ^ a b c Наджент К.И., Лундблад V (апрель 1998 г.). «Обратная транскриптаза теломеразы: компоненты и регуляция» . Гены и развитие . 12 (8): 1073–85. DOI : 10,1101 / gad.12.8.1073 . PMID 9553037 .
- ^ Райт WE, Tesmer В.М., Хаффман KE, Levene SD, Shay JW (ноябрь 1997). «Нормальные человеческие хромосомы имеют длинные теломерные выступы, богатые G, на одном конце» . Гены и развитие . 11 (21): 2801–09. DOI : 10,1101 / gad.11.21.2801 . PMC 316649 . PMID 9353250 .
- ^ Создано из архивации 17 октября 2016 г. на Wayback Machine.
- ^ a b Бердж С., Паркинсон Г. Н., Хейзел П., Тодд А. К., Нейдл С. (2006). «Квадруплексная ДНК: последовательность, топология и структура» . Исследования нуклеиновых кислот . 34 (19): 5402–15. DOI : 10.1093 / NAR / gkl655 . PMC 1636468 . PMID 17012276 .
- Перейти ↑ Parkinson GN, Lee MP, Neidle S (июнь 2002 г.). «Кристаллическая структура параллельных квадруплексов теломерной ДНК человека». Природа . 417 (6891): 876–80. Bibcode : 2002Natur.417..876P . DOI : 10.1038 / nature755 . PMID 12050675 . S2CID 4422211 .
- ^ Гриффит JD, Комю л, Розенфельд S, Stansel Р. М., Bianchi А, Мосс Н, де Ланге T (май 1999 г.). «Теломеры млекопитающих заканчиваются большой дуплексной петлей». Cell . 97 (4): 503–14. CiteSeerX 10.1.1.335.2649 . DOI : 10.1016 / S0092-8674 (00) 80760-6 . PMID 10338214 . S2CID 721901 .
- ^ Симэн NC (ноябрь 2005). «ДНК позволяет контролировать структуру материи в наномасштабе» . Ежеквартальные обзоры биофизики . 38 (4): 363–71. DOI : 10.1017 / S0033583505004087 . PMC 3478329 . PMID 16515737 .
- ↑ Warren M (21 февраля 2019 г.). «Четыре новых буквы ДНК - двойной алфавит жизни» . Природа . 566 (7745): 436. Bibcode : 2019Natur.566..436W . DOI : 10.1038 / d41586-019-00650-8 . PMID 30809059 .
- ^ Хошика С., Леал Н.А., Ким М.Дж., Ким М.С., Каралкар Н.Б., Ким Г.Дж. и др. (22 февраля 2019 г.). «ДНК и РНК Хатимодзи: генетическая система с восемью строительными блоками (платный доступ)» . Наука . 363 (6429): 884–887. Bibcode : 2019Sci ... 363..884H . DOI : 10.1126 / science.aat0971 . PMC 6413494 . PMID 30792304 .
- ↑ Burghardt B, Hartmann AK (февраль 2007 г.). «Дизайн вторичной структуры РНК» . Physical Review E . 75 (2): 021920. arXiv : Physics / 0609135 . Bibcode : 2007PhRvE..75b1920B . DOI : 10.1103 / PhysRevE.75.021920 . PMID 17358380 . S2CID 17574854 .
- ^ Ху Q, Розенфельд MG (2012). «Эпигенетическая регуляция эмбриональных стволовых клеток человека» . Границы генетики . 3 : 238. DOI : 10,3389 / fgene.2012.00238 . PMC 3488762 . PMID 23133442 .
- ^ Клозе RJ, Bird AP (февраль 2006). «Метилирование геномной ДНК: метка и ее медиаторы». Направления биохимических наук . 31 (2): 89–97. DOI : 10.1016 / j.tibs.2005.12.008 . PMID 16403636 .
- ↑ Bird A (январь 2002 г.). «Паттерны метилирования ДНК и эпигенетическая память» . Гены и развитие . 16 (1): 6–21. DOI : 10,1101 / gad.947102 . PMID 11782440 .
- Перейти ↑ Walsh CP, Xu GL (2006). «Метилирование цитозина и репарация ДНК». Актуальные темы микробиологии и иммунологии . 301 : 283–315. DOI : 10.1007 / 3-540-31390-7_11 . ISBN 3-540-29114-8. PMID 16570853 .
- ^ Kriaucionis S, Хайнц N (май 2009). «Основание ядерной ДНК 5-гидроксиметилцитозин присутствует в нейронах Пуркинье и в мозге» . Наука . 324 (5929): 929–30. Bibcode : 2009Sci ... 324..929K . DOI : 10.1126 / science.1169786 . PMC 3263819 . PMID 19372393 .
- ^ Ratel D, Ravanat JL, Berger F, Wion D (март 2006). «N6-метиладенин: другое метилированное основание ДНК» . BioEssays . 28 (3): 309–15. DOI : 10.1002 / bies.20342 . PMC 2754416 . PMID 16479578 .
- ^ Gommers-Ampt JH, Ван Leeuwen F, де Бир AL, Vliegenthart JF, Dizdaroglu M, Kowalak JA, Крейн PF, Borst P (декабрь 1993). «Бета-D-глюкозил-гидроксиметилурацил: новое модифицированное основание, присутствующее в ДНК паразитических простейших T. brucei». Cell . 75 (6): 1129–36. DOI : 10.1016 / 0092-8674 (93) 90322-H . hdl : 1874/5219 . PMID 8261512 . S2CID 24801094 .
- ^ Создано из PDB 1JDG
- ^ Douki Т, Рейно-Angelin А, кадеты Дж, шалфей Е (август 2003 г.). «Фотопродукты бипиримидина, а не окислительные повреждения, являются основным типом повреждений ДНК, участвующих в генотоксическом эффекте солнечного УФА-излучения». Биохимия . 42 (30): 9221–26. DOI : 10.1021 / bi034593c . PMID 12885257 .
- ^ Кадет Дж, Delatour Т, Т Douki, Gasparutto D, Пуже ДП, ДЛ Ravanat, Sauvaigo S (март 1999 г.). «Гидроксильные радикалы и повреждение оснований ДНК». Мутационные исследования . 424 (1–2): 9–21. DOI : 10.1016 / S0027-5107 (99) 00004-4 . PMID 10064846 .
- ↑ Бекман КБ, Эймс Б.Н. (август 1997 г.). «Окислительный распад ДНК» . Журнал биологической химии . 272 (32): 19633–36. DOI : 10.1074 / jbc.272.32.19633 . PMID 9289489 .
- ^ Valerie K, Povirk LF (сентябрь 2003). «Регуляция и механизмы репарации двухцепочечных разрывов млекопитающих» . Онкоген . 22 (37): 5792–812. DOI : 10.1038 / sj.onc.1206679 . PMID 12947387 .
- ^ Джонсон G (28 декабря 2010 г.). «Выявление доисторических опухолей и дебаты» . Нью-Йорк Таймс . Архивировано 24 июня 2017 года.
Если бы мы прожили достаточно долго, рано или поздно все мы заболели бы раком.
- ^ Альбертс Б., Джонсон А., Льюис Дж. И др. (2002). «Предотвратимые причины рака» . Молекулярная биология клетки (4-е изд.). Нью-Йорк: Наука Гарланд. ISBN 0-8153-4072-9. Архивировано из оригинала 2 января 2016 года.
Независимо от обстоятельств следует ожидать некоторую неснижаемую фоновую заболеваемость раком: мутаций нельзя полностью избежать, потому что они являются неизбежным следствием фундаментальных ограничений точности репликации ДНК, как обсуждалось в Глава 5. Если человек может жить достаточно долго, неизбежно, что хотя бы одна из его или ее клеток в конечном итоге накопит набор мутаций, достаточный для развития рака.
- ^ Бернштейн Н, Payne СМ, Бернштейн С, Garewal Н, Дворжак К (2008). «Рак и старение как последствия неремонтированного повреждения ДНК» . В Kimura H, Suzuki A (ред.). Новое исследование повреждений ДНК . Нью-Йорк: Nova Science Publishers. С. 1–47. ISBN 978-1-60456-581-2. Архивировано 25 октября 2014 года.
- ^ Hoeijmakers JH (октябрь 2009). «Повреждение ДНК, старение и рак». Медицинский журнал Новой Англии . 361 (15): 1475–85. DOI : 10.1056 / NEJMra0804615 . PMID 19812404 .
- Перейти ↑ Freitas AA, de Magalhães JP (2011). «Обзор и оценка теории старения повреждения ДНК». Мутационные исследования . 728 (1–2): 12–22. DOI : 10.1016 / j.mrrev.2011.05.001 . PMID 21600302 .
- Перейти ↑ Ferguson LR, Denny WA (сентябрь 1991 г.). «Генетическая токсикология акридинов». Мутационные исследования . 258 (2): 123–60. DOI : 10.1016 / 0165-1110 (91) 90006-H . PMID 1881402 .
- Перейти ↑ Stephens TD, Bunde CJ, Fillmore BJ (июнь 2000 г.). «Механизм действия в тератогенезе талидомида». Биохимическая фармакология . 59 (12): 1489–99. DOI : 10.1016 / S0006-2952 (99) 00388-3 . PMID 10799645 .
- ^ Джеффри AM (1985). «Модификация ДНК химическими канцерогенами». Фармакология и терапия . 28 (2): 237–72. DOI : 10.1016 / 0163-7258 (85) 90013-0 . PMID 3936066 .
- ^ Braña МФ, Кий М, Gradillas А, де Паскуаль-Тереза Б, Рамос А (ноябрь 2001 года). «Интеркаляторы как противоопухолевые препараты». Текущий фармацевтический дизайн . 7 (17): 1745–80. DOI : 10,2174 / 1381612013397113 . PMID 11562309 .
- ^ Вентер JC, Адамс MD, Майерс EW, Ли PW, Mural RJ, Sutton GG и др. (Февраль 2001 г.). «Последовательность генома человека» . Наука . 291 (5507): 1304–51. Bibcode : 2001Sci ... 291.1304V . DOI : 10.1126 / science.1058040 . PMID 11181995 .
- ^ Thanbichler M, Ван SC, Шапиро L (октябрь 2005). «Бактериальный нуклеоид: высокоорганизованная и динамичная структура» . Журнал клеточной биохимии . 96 (3): 506–21. DOI : 10.1002 / jcb.20519 . PMID 15988757 .
- ^ Вольфсбергская Т.Г., McEntyre J, Шулер GD (февраль 2001). «Путеводитель по проекту генома человека» . Природа . 409 (6822): 824–26. Bibcode : 2001Natur.409..824W . DOI : 10.1038 / 35057000 . PMID 11236998 .
- ↑ Грегори TR (январь 2005 г.). «Загадка ценности С у растений и животных: обзор параллелей и призыв к партнерству» . Летопись ботаники . 95 (1): 133–46. DOI : 10.1093 / Aob / mci009 . PMC 4246714 . PMID 15596463 .
- ^ Birney Е, Stamatoyannopoulos JA , Датта А, Гиго R, Gingeras TR, Маргулис ЕН, и др. (Июнь 2007 г.). «Идентификация и анализ функциональных элементов в 1% генома человека в рамках пилотного проекта ENCODE» . Природа . 447 (7146): 799–816. Bibcode : 2007Natur.447..799B . DOI : 10,1038 / природа05874 . PMC 2212820 . PMID 17571346 .
- ^ Создано из PDB 1MSW. Архивировано 6 января 2008 г. на Wayback Machine.
- ^ Pidoux AL, Allshire RC (март 2005). «Роль гетерохроматина в функции центромеры» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 360 (1455): 569–79. DOI : 10.1098 / rstb.2004.1611 . PMC 1569473 . PMID 15905142 .
- ↑ Harrison PM, Hegyi H, Balasubramanian S, Luscombe NM, Bertone P, Echols N, Johnson T, Gerstein M (февраль 2002 г.). «Молекулярные окаменелости в геноме человека: идентификация и анализ псевдогенов в хромосомах 21 и 22» . Геномные исследования . 12 (2): 272–80. DOI : 10.1101 / gr.207102 . PMC 155275 . PMID 11827946 .
- Перейти ↑ Harrison PM, Gerstein M (май 2002 г.). «Изучение геномов через эоны: семейства белков, псевдогены и эволюция протеома». Журнал молекулярной биологии . 318 (5): 1155–74. DOI : 10.1016 / S0022-2836 (02) 00109-2 . PMID 12083509 .
- ^ ALBA M (2001). «Репликативные ДНК-полимеразы» . Геномная биология . 2 (1): ОБЗОРЫ 3002. DOI : 10.1186 / GB-2001-2-1-reviews3002 . PMC 150442 . PMID 11178285 .
- Перейти ↑ Tani K, Nasu M (2010). «Роль внеклеточной ДНК в бактериальных экосистемах». В Кикучи Ю., Рыкова Е.Ю. (ред.). Внеклеточные нуклеиновые кислоты . Springer. стр. 25 -38. ISBN 978-3-642-12616-1.
- ^ Власова В.В., Лактионов П.П., Рыкова Е.Ю. (июль 2007). «Внеклеточные нуклеиновые кислоты». BioEssays . 29 (7): 654–67. DOI : 10.1002 / bies.20604 . PMID 17563084 . S2CID 32463239 .
- ^ Финкель SE, Kolter R (ноябрь 2001). «ДНК как питательное вещество: новая роль гомологов генов компетентности бактерий» . Журнал бактериологии . 183 (21): 6288–93. DOI : 10.1128 / JB.183.21.6288-6293.2001 . PMC 100116 . PMID 11591672 .
- ^ Mulcahy H, Charron-Mazenod L, Lewenza S (ноябрь 2008 г.). «Внеклеточная ДНК хелатирует катионы и индуцирует устойчивость к антибиотикам в биопленках Pseudomonas aeruginosa» . PLOS Патогены . 4 (11): e1000213. DOI : 10.1371 / journal.ppat.1000213 . PMC 2581603 . PMID 19023416 .
- ^ Берн C, Kysela DT, Brun YV (август 2010). «Бактериальная внеклеточная ДНК препятствует оседанию подвижных клеток-потомков внутри биопленки» . Молекулярная микробиология . 77 (4): 815–29. DOI : 10.1111 / j.1365-2958.2010.07267.x . PMC 2962764 . PMID 20598083 .
- ^ Whitchurch CB, Tolker-Nielsen T, Ragas PC, Маттик JS (февраль 2002). «Внеклеточная ДНК, необходимая для образования бактериальной биопленки». Наука . 295 (5559): 1487. DOI : 10.1126 / science.295.5559.1487 . PMID 11859186 .
- ↑ Ху В, Ли Л., Шарма С., Ван Дж, Макхарди Я, Люкс Р, Ян З, Хе Х, Гимзевски Дж., Ли Й, Ши В. (2012). «ДНК создает и укрепляет внеклеточный матрикс в биопленках Myxococcus xanthus, взаимодействуя с экзополисахаридами» . PLOS ONE . 7 (12): e51905. Bibcode : 2012PLoSO ... 751905H . DOI : 10.1371 / journal.pone.0051905 . PMC 3530553 . PMID 23300576 .
- ↑ Hui L, Bianchi DW (февраль 2013 г.). «Последние достижения в пренатальном исследовании генома человеческого плода» . Тенденции в генетике . 29 (2): 84–91. DOI : 10.1016 / j.tig.2012.10.013 . PMC 4378900 . PMID 23158400 .
- ^ Foote AD, Thomsen PF, Sveegaard S, Wahlberg M, Kielgast J, Kyhn LA и др. (2012). «Изучение возможности использования ДНК окружающей среды (eDNA) для генетического мониторинга морских млекопитающих» . PLOS ONE . 7 (8): e41781. Bibcode : 2012PLoSO ... 741781F . DOI : 10.1371 / journal.pone.0041781 . PMC 3430683 . PMID 22952587 .
- ^ "Исследователи обнаруживают наземных животных, используя ДНК в близлежащих водоемах" .
- ↑ Sandman K, Pereira SL, Reeve JN (декабрь 1998 г.). «Разнообразие прокариотических хромосомных белков и происхождение нуклеосом». Клеточные и молекулярные науки о жизни . 54 (12): 1350–64. DOI : 10.1007 / s000180050259 . PMID 9893710 . S2CID 21101836 .
- ↑ Dame RT (май 2005 г.). «Роль нуклеоид-ассоциированных белков в организации и уплотнении бактериального хроматина» . Молекулярная микробиология . 56 (4): 858–70. DOI : 10.1111 / j.1365-2958.2005.04598.x . PMID 15853876 . S2CID 26965112 .
- ↑ Luger K, Mäder AW, Richmond RK, Sargent DF, Richmond TJ (сентябрь 1997 г.). «Кристаллическая структура ядерной частицы нуклеосомы при разрешении 2,8 A». Природа . 389 (6648): 251–60. Bibcode : 1997Natur.389..251L . DOI : 10.1038 / 38444 . PMID 9305837 . S2CID 4328827 .
- ^ Jenuwein T, Allis CD (август 2001). «Перевод гистонового кода» (PDF) . Наука . 293 (5532): 1074–80. DOI : 10.1126 / science.1063127 . PMID 11498575 . S2CID 1883924 . Архивировано 8 августа 2017 года (PDF) .
- Перейти ↑ Ito T (2003). «Сборка и ремоделирование нуклеосом». Актуальные темы микробиологии и иммунологии . 274 : 1–22. DOI : 10.1007 / 978-3-642-55747-7_1 . ISBN 978-3-540-44208-0. PMID 12596902 .
- ↑ Thomas JO (август 2001). «HMG1 и 2: архитектурные ДНК-связывающие белки». Сделки Биохимического Общества . 29 (Pt 4): 395–401. DOI : 10.1042 / BST0290395 . PMID 11497996 .
- ^ Grosschedl Р, К Гис, Пейджел J (март 1994). «Белки домена HMG: архитектурные элементы сборки нуклеопротеиновых структур». Тенденции в генетике . 10 (3): 94–100. DOI : 10.1016 / 0168-9525 (94) 90232-1 . PMID 8178371 .
- ^ Iftode С, Даниэлы Y, Боровиц JA (1999). «Репликационный белок А (RPA): эукариотический SSB». Критические обзоры в биохимии и молекулярной биологии . 34 (3): 141–80. DOI : 10.1080 / 10409239991209255 . PMID 10473346 .
- ^ Созданный из PDB 1LMB архивации 6 января 2008 года в Wayback Machine
- ^ Myers LC, Корнберг RD (2000). «Медиатор регуляции транскрипции». Ежегодный обзор биохимии . 69 : 729–49. DOI : 10.1146 / annurev.biochem.69.1.729 . PMID 10966474 .
- ^ Spiegelman Б.М., Heinrich R (октябрь 2004). «Биологический контроль с помощью регулируемых транскрипционных коактиваторов» . Cell . 119 (2): 157–67. DOI : 10.1016 / j.cell.2004.09.037 . PMID 15479634 .
- ^ Li Z, Ван калькара S, Qu C, Cavenee WK, Zhang MQ, Ren B (июль 2003). «Глобальная регуляторная роль транскрипции c-Myc в клетках лимфомы Беркитта» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (14): 8164–69. Bibcode : 2003PNAS..100.8164L . DOI : 10.1073 / pnas.1332764100 . PMC 166200 . PMID 12808131 .
- ^ Созданный из PDB 1RVA архивации 6 января 2008 года в Wayback Machine
- ^ Bickle TA, Крюгер DH (июнь 1993). «Биология рестрикции ДНК» . Микробиологические обзоры . 57 (2): 434–50. DOI : 10.1128 / MMBR.57.2.434-450.1993 . PMC 372918 . PMID 8336674 .
- ^ a b Доэрти AJ, Suh SW (ноябрь 2000 г.). «Структурная и механистическая консервация в ДНК-лигазах» . Исследования нуклеиновых кислот . 28 (21): 4051–58. DOI : 10.1093 / NAR / 28.21.4051 . PMC 113121 . PMID 11058099 .
- ^ Шоффлер AJ, Berger JM (декабрь 2005). «Последние достижения в понимании взаимосвязи структура-функция в механизме топоизомеразы типа II». Сделки Биохимического Общества . 33 (Pt 6): 1465–70. DOI : 10.1042 / BST20051465 . PMID 16246147 .
- ^ Tuteja N, Tuteja К (май 2004). «Распутывание ДНК-геликаз. Мотив, структура, механизм и функция» (PDF) . Европейский журнал биохимии . 271 (10): 1849–63. DOI : 10.1111 / j.1432-1033.2004.04094.x . PMID 15128295 .
- ↑ Joyce CM, Steitz TA (ноябрь 1995 г.). «Полимеразные структуры и функции: вариации на тему?» . Журнал бактериологии . 177 (22): 6321–29. DOI : 10.1128 / jb.177.22.6321-6329.1995 . PMC 177480 . PMID 7592405 .
- ^ Hubscher U, G Maga, Spadari S (2002). «ДНК-полимеразы эукариот» (PDF) . Ежегодный обзор биохимии . 71 : 133–63. DOI : 10.1146 / annurev.biochem.71.090501.150041 . PMID 12045093 . S2CID 26171993 .
- Перейти ↑ Johnson A, O'Donnell M (2005). «Репликазы клеточной ДНК: компоненты и динамика на вилке репликации». Ежегодный обзор биохимии . 74 : 283–315. DOI : 10.1146 / annurev.biochem.73.011303.073859 . PMID 15952889 .
- ^ a b Tarrago-Litvak L, Andréola ML, Nevinsky GA, Sarih-Cottin L, Litvak S (май 1994 г.). «Обратная транскриптаза ВИЧ-1: от энзимологии к терапевтическому вмешательству» . Журнал FASEB . 8 (8): 497–503. DOI : 10.1096 / fasebj.8.8.7514143 . PMID 7514143 . S2CID 39614573 .
- Перейти ↑ Martinez E (декабрь 2002 г.). «Мультибелковые комплексы в транскрипции эукариотических генов». Молекулярная биология растений . 50 (6): 925–47. DOI : 10,1023 / A: 1021258713850 . PMID 12516863 . S2CID 24946189 .
- ^ Созданный из PDB 1M6G архивации 10 января 2010 года на Wayback Machine
- ^ Кремер T, Кремер C (апрель 2001). «Хромосомные территории, ядерная архитектура и регуляция генов в клетках млекопитающих». Природа Обзоры Генетики . 2 (4): 292–301. DOI : 10.1038 / 35066075 . PMID 11283701 . S2CID 8547149 .
- Перейти ↑ Pál C, Papp B, Lercher MJ (май 2006 г.). «Комплексный взгляд на эволюцию белка». Природа Обзоры Генетики . 7 (5): 337–48. DOI : 10.1038 / nrg1838 . PMID 16619049 . S2CID 23225873 .
- ^ O'Driscoll M, Jeggo PA (январь 2006). «Роль восстановления двухцепочечных разрывов - выводы из генетики человека». Природа Обзоры Генетики . 7 (1): 45–54. DOI : 10.1038 / nrg1746 . PMID 16369571 . S2CID 7779574 .
- ^ Vispé S, M Defais (октябрь 1997). «Белок Rad51 млекопитающих: гомолог RecA с плейотропными функциями». Биохимия . 79 (9–10): 587–92. DOI : 10.1016 / S0300-9084 (97) 82007-X . PMID 9466696 .
- ^ Neale MJ, Кини S (июль 2006). «Уточнение механики обмена нити ДНК в мейотической рекомбинации» . Природа . 442 (7099): 153–58. Bibcode : 2006Natur.442..153N . DOI : 10,1038 / природа04885 . PMC 5607947 . PMID 16838012 .
- ^ Дикман MJ, Ingleston С.М., Седельникова SE, Рафферти JB, Lloyd RG, Grasby JA, Хорнби DP (ноябрь 2002). «Резолвазома RuvABC» . Европейский журнал биохимии . 269 (22): 5492–501. DOI : 10.1046 / j.1432-1033.2002.03250.x . PMID 12423347 . S2CID 39505263 .
- Перейти ↑ Joyce GF (июль 2002 г.). «Древность эволюции на основе РНК». Природа . 418 (6894): 214–21. Bibcode : 2002Natur.418..214J . DOI : 10.1038 / 418214a . PMID 12110897 . S2CID 4331004 .
- ^ Оргел LE (2004). «Пребиотическая химия и происхождение мира РНК». Критические обзоры в биохимии и молекулярной биологии . 39 (2): 99–123. CiteSeerX 10.1.1.537.7679 . DOI : 10.1080 / 10409230490460765 . PMID 15217990 .
- ^ Давенпорт RJ (май 2001). «Рибозимы. Копирование в мире РНК». Наука . 292 (5520): 1278a – 1278. DOI : 10.1126 / science.292.5520.1278a . PMID 11360970 . S2CID 85976762 .
- ^ Szathmáry E (апрель 1992). «Каков оптимальный размер генетического алфавита?» . Труды Национальной академии наук Соединенных Штатов Америки . 89 (7): 2614–18. Bibcode : 1992PNAS ... 89.2614S . DOI : 10.1073 / pnas.89.7.2614 . PMC 48712 . PMID 1372984 .
- ↑ Lindahl T (апрель 1993 г.). «Неустойчивость и распад первичной структуры ДНК». Природа . 362 (6422): 709–15. Bibcode : 1993Natur.362..709L . DOI : 10.1038 / 362709a0 . PMID 8469282 . S2CID 4283694 .
- ^ Vreeland RH, Розенцвейг WD, Пауэрс DW (октябрь 2000). «Выделение галотолерантной бактерии возрастом 250 миллионов лет из первичного кристалла соли». Природа . 407 (6806): 897–900. Bibcode : 2000Natur.407..897V . DOI : 10.1038 / 35038060 . PMID 11057666 . S2CID 9879073 .
- ^ Hebsgaard MB, Phillips MJ, Виллерслев E (май 2005). «Геологически древняя ДНК: факт или артефакт?». Тенденции в микробиологии . 13 (5): 212–20. DOI : 10.1016 / j.tim.2005.03.010 . PMID 15866038 .
- ^ Никель DC, Learn GH, дождь МВт, Mullins СО, Миттлер JE (январь 2002). «Удивительно современная ДНК для« бактерии »возрастом 250 миллионов лет. Журнал молекулярной эволюции . 54 (1): 134–37. Bibcode : 2002JMolE..54..134N . DOI : 10.1007 / s00239-001-0025-х . PMID 11734907 . S2CID 24740859 .
- Перейти ↑ Callahan MP, Smith KE, Cleaves HJ, Ruzicka J, Stern JC, Glavin DP, House CH, Dworkin JP (август 2011). «Углеродистые метеориты содержат широкий спектр внеземных азотистых оснований» . Труды Национальной академии наук Соединенных Штатов Америки . 108 (34): 13995–98. Bibcode : 2011PNAS..10813995C . DOI : 10.1073 / pnas.1106493108 . PMC 3161613 . PMID 21836052 .
- ^ Steigerwald J (8 августа 2011). «Исследователи НАСА: строительные блоки ДНК могут быть созданы в космосе» . НАСА . Архивировано 23 июня 2015 года . Проверено 10 августа 2011 года .
- ^ ScienceDaily Staff (9 августа 2011 г.). «Строительные блоки ДНК могут быть созданы в космосе, - свидетельствуют данные НАСА» . ScienceDaily . Архивировано 5 сентября 2011 года . Проверено 9 августа 2011 года .
- ^ Marlaire R (3 марта 2015). «НАСА Эймс воспроизводит строительные блоки жизни в лаборатории» . НАСА . Архивировано 5 марта 2015 года . Дата обращения 5 марта 2015 .
- ↑ Хант, Кэти (17 февраля 2021 г.). «Самая старая ДНК в мире, полученная от мамонта, жившего более миллиона лет назад» . Новости CNN . Проверено 17 февраля 2021 года .
- ↑ Callaway, Ewen (17 февраля 2021 г.). «Геном мамонта, которому миллион лет, бьет рекорды по старейшей древней ДНК - сохранившиеся в вечной мерзлоте зубы возрастом до 1,6 миллиона лет позволяют идентифицировать новый вид мамонта в Сибири» . Природа . DOI : 10.1038 / d41586-021-00436-х . Проверено 17 февраля 2021 года .
- Перейти ↑ Goff SP, Berg P (декабрь 1976 г.). «Создание гибридных вирусов, содержащих сегменты ДНК фага SV40 и лямбда, и их размножение в культивируемых клетках обезьян». Cell . 9 (4 PT 2): 695–705. DOI : 10.1016 / 0092-8674 (76) 90133-1 . PMID 189942 . S2CID 41788896 .
- ^ Houdebine LM (2007). «Модели трансгенных животных в биомедицинских исследованиях». Обзоры и протоколы обнаружения и проверки целей . Методы молекулярной биологии. 360 . С. 163–202. DOI : 10.1385 / 1-59745-165-7: 163 . ISBN 978-1-59745-165-9. PMID 17172731 .
- ^ Даниеля H, Dhingra A (апрель 2002). «Мультигенная инженерия: рассвет новой захватывающей эры в биотехнологии» . Текущее мнение в области биотехнологии . 13 (2): 136–41. DOI : 10.1016 / S0958-1669 (02) 00297-5 . PMC 3481857 . PMID 11950565 .
- ↑ Job D (ноябрь 2002 г.). «Биотехнология растений в сельском хозяйстве». Биохимия . 84 (11): 1105–10. DOI : 10.1016 / S0300-9084 (02) 00013-5 . PMID 12595138 .
- ↑ Curtis C, Hereward J (29 августа 2017 г.). «От места преступления до зала суда: путешествие образца ДНК» . Разговор . Архивировано 22 октября 2017 года . Проверено 22 октября 2017 года .
- ↑ Collins A, Morton NE (июнь 1994 г.). «Отношения правдоподобия для идентификации ДНК» . Труды Национальной академии наук Соединенных Штатов Америки . 91 (13): 6007–11. Bibcode : 1994PNAS ... 91.6007C . DOI : 10.1073 / pnas.91.13.6007 . PMC 44126 . PMID 8016106 .
- ^ Weir BS, Triggs CM, Старлинг L, Стоуэлл Л.И., Уолш К., Buckleton J (март 1997). «Интерпретация смесей ДНК» (PDF) . Журнал судебной медицины . 42 (2): 213–22. DOI : 10,1520 / JFS14100J . PMID 9068179 . S2CID 14511630 .
- ^ Джеффреис AJ, Уилсон В, Тхеин SL (1985). «Индивидуальные« отпечатки пальцев »ДНК человека». Природа . 316 (6023): 76–79. Bibcode : 1985Natur.316 ... 76J . DOI : 10.1038 / 316076a0 . PMID 2989708 . S2CID 4229883 .
- ↑ Колин Вилы - первое обвинение в убийстве на основании доказательств ДНК также очищает главного подозреваемого. Служба криминалистики, доступ 23 декабря 2006 г.
- ^ «Идентификация ДНК в инцидентах со смертельным исходом» . Национальный институт юстиции. Сентябрь 2006 Архивировано из оригинала 12 ноября 2006 года.
- ^ «Анализы крови на отцовство, которые работают на ранних сроках беременности» New York Times 20 июня 2012 г. Архивировано 24 июня 2017 г. в Wayback Machine
- ^ a b Breaker RR, Джойс Г.Ф. (декабрь 1994 г.). «Фермент ДНК, расщепляющий РНК». Химия и биология . 1 (4): 223–29. DOI : 10.1016 / 1074-5521 (94) 90014-0 . PMID 9383394 .
- ^ Chandra M, Сачдева A, Silverman SK (октябрь 2009). «ДНК-катализируемый гидролиз ДНК, специфичный для последовательности» . Природа Химическая биология . 5 (10): 718–20. DOI : 10.1038 / nchembio.201 . PMC 2746877 . PMID 19684594 .
- ^ Карми N, Шульц Л.А., Breaker RR (декабрь 1996). «Селекция саморасщепляющихся ДНК in vitro» . Химия и биология . 3 (12): 1039–46. DOI : 10.1016 / S1074-5521 (96) 90170-2 . PMID 9000012 .
- ^ Torabi SF, В Р, Макги CE, Чен л, Хуанг К, Чжэн N, Ченг - J, Л Y (май 2015 г.). «Выбор in vitro натрий-специфического ДНКзима и его применение во внутриклеточном зондировании» . Труды Национальной академии наук Соединенных Штатов Америки . 112 (19): 5903–08. Bibcode : 2015PNAS..112.5903T . DOI : 10.1073 / pnas.1420361112 . PMC 4434688 . PMID 25918425 .
- ^ Балди Р , Brunak S (2001). Биоинформатика: подход машинного обучения . MIT Press. ISBN 978-0-262-02506-5. OCLC 45951728 .
- ^ Gusfield D (15 января 1997). Алгоритмы на строках, деревьях и последовательностях: информатика и вычислительная биология . Издательство Кембриджского университета . ISBN 978-0-521-58519-4.
- ^ Сджоландер K (январь 2004). «Филогеномный вывод молекулярной функции белков: достижения и проблемы». Биоинформатика . 20 (2): 170–79. CiteSeerX 10.1.1.412.943 . DOI : 10.1093 / биоинформатики / bth021 . PMID 14734307 .
- ↑ Mount DM (2004). Биоинформатика: анализ последовательности и генома (2-е изд.). Колд-Спринг-Харбор, Нью-Йорк: Лаборатория Колд-Спринг-Харбор. ISBN 0-87969-712-1. OCLC 55106399 .
- ^ Rothemund PW (март 2006). «Складывание ДНК для создания наноразмерных форм и узоров» (PDF) . Природа . 440 (7082): 297–302. Bibcode : 2006Natur.440..297R . DOI : 10,1038 / природа04586 . PMID 16541064 . S2CID 4316391 .
- ^ Андерсен ES, Донг М., Нильсен М.М., Ян К., Субрамани Р., Мамдух В., Голас М.М., Сандер Б., Старк Х, Оливейра К.Л., Педерсен Дж. С., Биркедал В., Бесенбахер Ф, Готельф К. В., Кьемс Дж. (Май 2009 г.). «Самостоятельная сборка наноразмерной коробки ДНК с управляемой крышкой». Природа . 459 (7243): 73–76. Bibcode : 2009Natur.459 ... 73А . DOI : 10,1038 / природа07971 . hdl : 11858 / 00-001M-0000-0010-9362-B . PMID 19424153 . S2CID 4430815 .
- ^ Ishitsuka Y, Ha T (май 2009). «ДНК-нанотехнология: наномашина оживает». Природа Нанотехнологии . 4 (5): 281–82. Bibcode : 2009NatNa ... 4..281I . DOI : 10.1038 / nnano.2009.101 . PMID 19421208 .
- ^ Aldaye FA, Palmer AL, Sleiman HF (сентябрь 2008). «Сборка материалов с использованием ДНК в качестве руководства». Наука . 321 (5897): 1795–99. Bibcode : 2008Sci ... 321.1795A . DOI : 10.1126 / science.1154533 . PMID 18818351 . S2CID 2755388 .
- Перейти ↑ Wray GA (2002). «Знакомство с ветвями древа жизни с помощью ДНК» . Геномная биология . 3 (1): ОБЗОРЫ0001. DOI : 10.1186 / GB-2001-3-1-reviews0001 . PMC 150454 . PMID 11806830 .
- ↑ Panda D, Molla KA, Baig MJ, Swain A, Behera D, Dash M (май 2018). «ДНК как устройство для хранения цифровой информации: надежда или шумиха?» . 3 Biotech . 8 (5): 239. DOI : 10.1007 / s13205-018-1246-7 . PMC 5935598 . PMID 29744271 .
- ^ Акрам F, Хак IU, Али H, Laghari AT (октябрь 2018). «Тенденции хранения цифровых данных в ДНК: обзор». Отчеты по молекулярной биологии . 45 (5): 1479–1490. DOI : 10.1007 / s11033-018-4280-у . PMID 30073589 . S2CID 51905843 .
- ^ Мишер F (1871). "Ueber die chemische Zusammensetzung der Eiterzellen" [О химическом составе гнойных клеток]. Medicinisch-chemische Untersuchungen (на немецком языке). 4 : 441–60.
Ich habe mich daher später mit meinen Versuchen an die ganzen Kerne gehalten, die Trennung der Körper, die ich einstweilen ohne weiteres Präjudiz als lösliches und unlösliches Nuclein bezeichnen will, einem günstigelassend Material üinem günstigend Materials. (Поэтому в своих экспериментах я впоследствии ограничился целым ядром, оставив более благоприятному материалу разделение веществ, которое в настоящее время, без дальнейших предубеждений, я буду обозначать как растворимый и нерастворимый ядерный материал («нуклеин»).
- ^ Dahm R (январь 2008). «Открытие ДНК: Фридрих Мишер и первые годы исследований нуклеиновых кислот». Генетика человека . 122 (6): 565–81. DOI : 10.1007 / s00439-007-0433-0 . PMID 17901982 . S2CID 915930 .
- ^ См .:
- Коссель А (1879). "Ueber Nucleïn der Hefe" [О нуклеине в дрожжах]. Zeitschrift für Physiologische Chemie (на немецком языке). 3 : 284–91.
- Коссель А (1880 г.). "Ueber Nucleïn der Hefe II" [О нуклеине в дрожжах, Часть 2]. Zeitschrift für Physiologische Chemie (на немецком языке). 4 : 290–95.
- Коссель А (1881). "Ueber die Verbreitung des Hypoxanthins im Thier- und Pflanzenreich" [О распределении гипоксантинов в царстве животных и растений]. Zeitschrift für Physiologische Chemie (на немецком языке). 5 : 267–71.
- Коссель А (1881). Trübne KJ (ред.). Untersuchungen über die Nucleine und ihre Spaltungsprodukte [ Исследования нуклеина и продуктов его расщепления ] (на немецком языке). Страсбург, Германия. п. 19.
- Коссель А. (1882 г.). «Убер Ксантин и Гипоксантин» [О ксантине и гипоксантине]. Zeitschrift für Physiologische Chemie . 6 : 422–31.
- Альбрект Коссель (1883 г.) «Zur Chemie des Zellkerns». Архивировано 17 ноября 2017 г. в Wayback Machine (О химии клеточного ядра), Zeitschrift für Physiologische Chemie , 7 : 7–22.
- Коссель А. (1886 г.). "Weitere Beiträge zur Chemie des Zellkerns" [Дальнейшие разработки в области химии ядра клетки]. Zeitschrift für Physiologische Chemie (на немецком языке). 10 : 248–64.
На стр. 264, Коссель прозорливо заметил: Der Erforschung der Quantitativen Verhältnisse der vier stickstoffreichen Basen, der Abhängigkeit ihrer Menge von den Physicologischen Zuständen der Zelle, verspricht wichtige Aufschlüsse Physiology über die-element. (Изучение количественных соотношений четырех азотистых оснований [и] зависимости их количества от физиологического состояния клетки - обещает важное понимание фундаментальных физиолого-химических процессов.)
- Перейти ↑ Jones ME (сентябрь 1953 г.). "Альбрехт Коссель, биографический очерк" . Йельский журнал биологии и медицины . 26 (1): 80–97. PMC 2599350 . PMID 13103145 .
- ^ Levene PA, Jacobs WA (1909). «Über Inosinsäure». Berichte der Deutschen Chemischen Gesellschaft (на немецком языке). 42 : 1198–203. DOI : 10.1002 / cber.190904201196 .
- ^ Levene PA, Jacobs WA (1909). "Uber die Hefe-Nucleinsäure" . Berichte der Deutschen Chemischen Gesellschaft (на немецком языке). 42 (2): 2474–78. DOI : 10.1002 / cber.190904202148 .
- ^ Levene Р (1919). «Строение нуклеиновой кислоты дрожжей» . J Biol Chem . 40 (2): 415–24. DOI : 10.1016 / S0021-9258 (18) 87254-4 .
- ^ Cohen JS, Португалия FH (1974). «Поиски химической структуры ДНК» (PDF) . Коннектикут Медицина . 38 (10): 551–52, 554–57. PMID 4609088 .
- ^ Кольцов предположил, что генетическая информация клетки закодирована в длинной цепи аминокислот. Видеть:
- Кольцов, Н. К. (12 декабря 1927 г.). Физико-химические основы морфологии [ Физико-химические основы морфологии ] (Речь). 3-е Всесоюзное совещание зоологов, анатомов и гистологов. Ленинград, СССР
- Отпечатано на: Кольцов, Н. К. (1928). "Физико-химические основы морфологии" [Физико-химические основы морфологии]. Успехи экспериментальной биологии (Достижения в области экспериментальной биологии) серии B (на русском языке ). 7 (1):?.
- Перепечатано на немецком языке как: Кольцов Н.К. (1928). "Physikalisch-chemische Grundlagen der Morphologie" [Физико-химические основы морфологии]. Biologisches Zentralblatt (на немецком языке). 48 (6): 345–69.
- В 1934 году Кольцов утверждал, что белки, содержащие генетическую информацию клетки, воспроизводятся. См .: Кольцов Н. (октябрь 1934 г.). «Строение хромосом в слюнных железах дрозофилы». Наука . 80 (2075): 312–13. Bibcode : 1934Sci .... 80..312K . DOI : 10.1126 / science.80.2075.312 . PMID 17769043 .
Со страницы 313: «Я думаю, что размер хромосом в слюнных железах [дрозофилы] определяется путем умножения
генонем.
. Этим термином я обозначаю осевую нить хромосомы, в которой генетики определяют линейную комбинацию генов; … В нормальной хромосоме обычно есть только одна генонема; перед клеточным делением эта генонема разделилась на две цепи ».
- ^ Сойфер В.Н. (сентябрь 2001). «Последствия политической диктатуры для российской науки». Природа Обзоры Генетики . 2 (9): 723–29. DOI : 10.1038 / 35088598 . PMID 11533721 . S2CID 46277758 .
- ↑ Griffith F (январь 1928 г.). «Значение типов пневмококков» . Журнал гигиены . 27 (2): 113–59. DOI : 10.1017 / S0022172400031879 . PMC 2167760 . PMID 20474956 .
- Перейти ↑ Lorenz MG, Wackernagel W (сентябрь 1994 г.). «Бактериальный перенос генов путем естественной генетической трансформации в окружающей среде» . Микробиологические обзоры . 58 (3): 563–602. DOI : 10.1128 / MMBR.58.3.563-602.1994 . PMC 372978 . PMID 7968924 .
- ^ Браш J (1933). "Исследования по синтезу тимонуклеарного кулона по развитию де л'оэф д'Орсен". Archives de Biologie (на итальянском языке). 44 : 519–76.
- ^ Burian R (1994). "Цитохимическая эмбриология Жана Браше: связь с обновлением биологии во Франции?" (PDF) . В Debru C, Gayon J, Picard JF (ред.). Les Sciences Biologiques et Medicales во Франции 1920–1950 . Cahiers pour I'histoire de la recherche. 2 . Париж: Издания CNRS. С. 207–20.
- ^ См .:
- Эстбери В. Т., Белл Ф. О. (1938). «Некоторые недавние разработки в области рентгеновского исследования белков и родственных структур» (PDF) . Симпозиумы Колд-Спринг-Харбор по количественной биологии . 6 : 109–21. DOI : 10.1101 / sqb.1938.006.01.013 . Архивировано из оригинального (PDF) 14 июля 2014 года.
- Эстбери В. Т. (1947). «Рентгенологические исследования нуклеиновых кислот» . Симпозиумы Общества экспериментальной биологии (1): 66–76. PMID 20257017 . Архивировано из оригинала 5 июля 2014 года.
- ^ Avery OT, Маклеод CM, МакКарти M (февраль 1944). "Исследования химической природы вещества, индуцирующего трансформацию пневмококков: индукция трансформации фракцией дезоксирибонуклеиновой кислоты, выделенной из пневмококка типа III" . Журнал экспериментальной медицины . 79 (2): 137–58. DOI : 10,1084 / jem.79.2.137 . PMC 2135445 . PMID 19871359 .
- ↑ Hershey AD, Chase M (май 1952 г.). «Независимые функции вирусного белка и нуклеиновой кислоты в росте бактериофага» . Журнал общей физиологии . 36 (1): 39–56. DOI : 10,1085 / jgp.36.1.39 . PMC 2147348 . PMID 12981234 .
- ↑ Рентгеновский снимок B-ДНК справа от связанного изображения. Архивировано 25 мая 2012 года в Archive.today.
- ^ Шварц J (2008). В погоне за геном: от Дарвина до ДНК . Кембридж, Массачусетс: Издательство Гарвардского университета.
- Перейти ↑ Pauling L, Corey RB (февраль 1953 г.). «Предлагаемая структура нуклеиновых кислот» . Труды Национальной академии наук Соединенных Штатов Америки . 39 (2): 84–97. Полномочный код : 1953PNAS ... 39 ... 84P . DOI : 10.1073 / pnas.39.2.84 . PMC 1063734 . PMID 16578429 .
- Перейти ↑ Regis E (2009). Что такое жизнь ?: исследование природы жизни в эпоху синтетической биологии . Оксфорд: Издательство Оксфордского университета . п. 52. ISBN 978-0-19-538341-6.
- ^ «Двойная спираль ДНК: 50 лет» . Архивы природы . Архивировано из оригинала 5 апреля 2015 года.
- ^ "Оригинальное изображение дифракции рентгеновских лучей" . Государственная библиотека Орегона. Архивировано 30 января 2009 года . Проверено 6 февраля 2011 года .
- ^ "Нобелевская премия по физиологии и медицине 1962" . Nobelprize.org .
- ↑ Maddox B (январь 2003 г.). «Двойная спираль и« обиженная героиня » » (PDF) . Природа . 421 (6921): 407–08. Bibcode : 2003Natur.421..407M . DOI : 10,1038 / природа01399 . PMID 12540909 . S2CID 4428347 . Архивировано 17 октября 2016 года (PDF) .
- ^ Крик Ф (1955). Примечание для RNA Tie Club (PDF) (Речь). Кембридж, Англия. Архивировано из оригинального (PDF) 1 октября 2008 года.
- ^ Мезельсон M, Stahl FW (июль 1958). «Репликация ДНК в Escherichia Coli» . Труды Национальной академии наук Соединенных Штатов Америки . 44 (7): 671–82. Полномочный код : 1958PNAS ... 44..671M . DOI : 10.1073 / pnas.44.7.671 . PMC 528642 . PMID 16590258 .
- ^ "Нобелевская премия по физиологии и медицине 1968" . Nobelprize.org .
- ↑ Pray L (2008). «Открытие структуры и функции ДНК: Уотсон и Крик». Природное образование . 1 (1): 100.
дальнейшее чтение
- Берри А, Уотсон Дж (2003). ДНК: секрет жизни . Нью-Йорк: Альфред А. Кнопф. ISBN 0-375-41546-7.
- Калладин ЧР, Дрю Х.Р., Луизи Б.Ф., Трэверс А.А. (2003). Понимание ДНК: молекула и как она работает . Амстердам: Elsevier Academic Press. ISBN 0-12-155089-3.
- Карина Д., Клейтон Дж (2003). 50 лет ДНК . Бейзингстоук: Пэлгрейв Макмиллан. ISBN 1-4039-1479-6.
- Джадсон Х.Ф. (1979). Восьмой день творения: создатели революции в биологии (2-е изд.). Лабораторный пресс Колд-Спринг-Харбор. ISBN 0-671-22540-5.
- Olby RC (1994). Путь к двойной спирали: открытие ДНК . Нью-Йорк: Dover Publications. ISBN 0-486-68117-3., впервые опубликовано в октябре 1974 г. Макмилланом, с предисловием Фрэнсиса Крика; полный учебник ДНК, пересмотренный в 1994 году с 9-страничным постскриптумом
- Миклас Д (2003). Наука о ДНК: первый курс . Колд Спринг Харбор Пресс. ISBN 978-0-87969-636-8.
- Ридли М (2006). Фрэнсис Крик: первооткрыватель генетического кода . Ашленд, Огайо: Выдающиеся жизни, книги Атласа. ISBN 0-06-082333-X.
- Olby RC (2009). Фрэнсис Крик: биография . Плейнвью, Нью-Йорк: Лаборатория издательства Колд-Спринг-Харбор. ISBN 978-0-87969-798-3.
- Розенфельд I (2010). ДНК: графическое руководство по молекуле, которая потрясла мир . Издательство Колумбийского университета. ISBN 978-0-231-14271-7.
- Шульц М., Cannon Z (2009). Материал жизни: графическое руководство по генетике и ДНК . Хилл и Ван. ISBN 978-0-8090-8947-5.
- Стент Г.С. , Уотсон Дж. (1980). Двойная спираль: личный отчет об открытии структуры ДНК . Нью-Йорк: Нортон. ISBN 0-393-95075-1.
- Уотсон Дж (2004). ДНК: секрет жизни . Случайный дом. ISBN 978-0-09-945184-6.
- Уилкинс М (2003). Третий человек двойной спирали - автобиография Мориса Уилкинса . Кембридж, Англия: University Press. ISBN 0-19-860665-6.
внешняя ссылка
| Библиотечные ресурсы о ДНК |
|
| В Wikiquote есть цитаты, связанные с: ДНК |
| В Викиверситете есть ресурсы для изучения ДНК |
| Викискладе есть медиафайлы, связанные с ДНК . |
- ДНК в Керли
- Прогнозирование сайта связывания ДНК на белке
- ДНК - игра двойной спирали С официального сайта Нобелевской премии
- ДНК под электронным микроскопом
- Учебный центр Dolan DNA
- Двойная спираль: 50 лет ДНК , природы
- Протеопедическая ДНК
- Proteopedia Forms_of_DNA
- ENCODE Thread Explorer Домашняя страница ENCODE. Природа
- Double Helix 1953–2003 Национальный центр биотехнологического образования
- Модули Генетической Образование для учителей - ДНК от начала Учебного пособия
- Молекула PDB ДНК месяца
- Ключ к химии наследственности был найден в The New York Times в июне 1953 года. Первое освещение в американской газете открытия структуры ДНК.
- Олби Р. (январь 2003 г.). «Тихий дебют двойной спирали» . Природа . 421 (6921): 402–05. Bibcode : 2003Natur.421..402O . DOI : 10,1038 / природа01397 . PMID 12540907 .
- ДНК с самого начала Еще один сайт Центра изучения ДНК, посвященный ДНК, генам и наследственности от Менделя до проекта генома человека.
- Реестр личных документов Фрэнсиса Крика за 1938–2007 гг., Библиотека специальных коллекций Мандевилля, Калифорнийский университет, Сан-Диего
- Семистраничное рукописное письмо, которое Крик отправил своему 12-летнему сыну Майклу в 1953 году с описанием структуры ДНК. Смотрите, как медаль Крика уходит с молотка , Nature, 5 апреля 2013 г.
