 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК фосфат железа (2+) лития (1: 1: 1) | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.124.705 |
| Номер ЕС |
|
PubChem CID | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| FeLiO 4п | |
| Молярная масса | 157,757 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
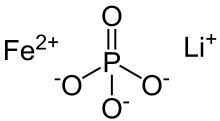
Литий-фосфат железа ( LFP ) представляет собой неорганическое соединение с формулой LiFePO.
4. Это твердое вещество серого, красно-серого, коричневого или черного цвета, не растворимое в воде. Материал привлек к себе внимание в качестве компонента лития фосфата железа батарей , [1] типа литий-ионного аккумулятора . Этот химический состав аккумуляторов предназначен для использования в электроинструментах , электромобилях и установках солнечной энергии. [2] Он также используется в учебных ноутбуках OLPC XO .
В большинстве литиевых батарей (Li-ion), используемых в продуктах 3C (компьютеры, связь, бытовая электроника), используются катоды из других соединений лития, таких как оксид лития-кобальта ( LiCoO
2), оксид лития-марганца ( LiMn
2О
4) и оксида лития-никеля ( LiNiO
2). Эти аноды , как правило , изготовлены из графита .
Фосфат лития-железа существует в природе в форме минерала трифилита , но этот материал не имеет достаточной чистоты для использования в батареях.
LiMPO
4[ редактировать ]
С общей химической формулой LiMPO
4, соединения в LiFePO
4семья принимает оливиновую структуру. M включает не только Fe, но также Co, Mn и Ti. [3] Как первый коммерческий LiMPO
4был C / LiFePO
4, вся группа ЛиМПО
4неофициально называется «фосфат лития-железа» или « LiFePO.
4». Однако в качестве катодного материала батареи можно использовать более одной фазы типа оливина. Соединения оливина, такие как A
уMPO
4, Ли
1-хMFePO
4, и LiFePO
4-яМ имеют такую же кристаллическую структуру, что и LiMPO.
4и может заменить катод. Все могут называться «LFP».
Марганец, фосфат, железо и литий также образуют структуру оливина . Эта структура является полезным элементом катода литиевых аккумуляторных батарей. [4] Это связано со структурой оливина, создаваемой при соединении лития с марганцем, железом и фосфатом (как описано выше). Оливиновые структуры литиевых аккумуляторных батарей имеют большое значение, поскольку они доступны по цене, стабильны и могут безопасно храниться в качестве энергии. [5]
История и производство [ править ]
Арумугам Мантирам и Джон Б. Гуденаф первыми определили полианионный класс катодных материалов для литий-ионных батарей . [6] [7] [8] LiFePO
4затем был идентифицирован как катодный материал, принадлежащий к классу полианионов, для использования в батареях в 1996 году Padhi et al. [9] [10] Обратимое извлечение лития из LiFePO
4и введение лития в FePO
4был продемонстрирован. Дифракция нейтронов подтвердила, что LFP смог обеспечить безопасность большого входного / выходного тока литиевых батарей. [11]
Материал может быть получен путем нагревания различных солей железа и лития с фосфатами или фосфорной кислотой . Было описано множество связанных путей, включая те, которые используют гидротермальный синтез . [12]
Физические и химические свойства [ править ]
В LiFePO
4, литий имеет заряд +1, железо +2 заряда, уравновешивая заряд -3 для фосфата. После удаления Li материал превращается в трехвалентную форму FePO 4 . [13]
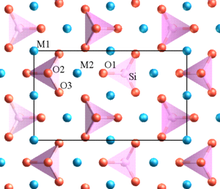
Атом железа и 6 атомов кислорода образуют октаэдрическую координационную сферу , описываемую как FeO.
6, с ионом Fe в центре. Фосфатные группы, ПО
4, являются четырехгранными. Трехмерный каркас образован FeO
6октаэдры, имеющие общие углы O. Ионы лития располагаются в октаэдрических каналах зигзагообразно. В кристаллографии считается, что эта структура принадлежит пространственной группе P mnb орторомбической кристаллической системы. Постоянные решетки : a = 6,008 Å, b = 10,334 Å и c = 4,693 Å. Объем элементарной ячейки 291,4 Å 3 .
В отличие от двух традиционных катодных материалов - LiMnO
4и LiCoO
2, ионы лития LiMPO
4мигрируют в одномерном свободном объеме решетки. Во время заряда / разряда ионы лития извлекаются одновременно с окислением Fe:
Извлечение лития из LiFePO
4производит FePO
4с аналогичной структурой. FePO
4принимает пространственную группу P mnb с объемом элементарной ячейки 272,4 3 , что лишь немного меньше, чем у его литированного предшественника. Экстракция ионов лития уменьшает объем решетки, как в случае с оксидами лития. LiMPO
4Угловой общий FeO
6октаэдры разделены атомами кислорода ПО
43- тетраэдры и не может образовывать непрерывный FeO
6 сеть, снижающая проводимость.
Почти плотно упакованный гексагональный массив оксидных центров обеспечивает относительно небольшой свободный объем для миграции ионов Li + внутри. По этой причине ионная проводимость Li + относительно низкая при температуре окружающей среды. Подробности литиирования FePO 4 и делитирования LiFePO 4 были изучены. Вовлечены две фазы литиированного материала. [13] [14]
Приложения [ править ]
Аккумуляторы LFP имеют рабочее напряжение 3,3 В, плотность заряда 170 мАч / г, высокую плотность мощности , длительный срок службы и стабильность при высоких температурах.
Основные коммерческие преимущества LFP заключаются в том, что он не создает проблем безопасности, таких как перегрев и взрыв, а также имеет длительный срок службы, высокую удельную мощность и более широкий диапазон рабочих температур. Электростанции и автомобили используют LFP. [15] [16]
BAE объявила, что в их гибридном автобусе HybriDrive Orion 7 используются аккумуляторные батареи LFP мощностью около 180 кВт. AES разработала аккумуляторные системы на несколько триллионов ватт, которые могут обеспечивать дополнительные услуги электросети, включая резервную мощность и регулировку частоты. В Китае активно действуют BAK и Tianjin Lishen.
Сравнение [ править ]
Хотя емкость LFP на 25% меньше, чем у других литиевых батарей из-за рабочего напряжения (3,2 В против 3,7 для катодной химии на основе Co), она на 70% больше, чем никель-водородные батареи .
Основное различие между батареями LFP и другими типами литий-ионных батарей заключается в том, что батареи LFP не содержат кобальта (что снимает этические вопросы относительно источников материалов) и имеют плоскую кривую разряда.
Батареи LFP имеют недостатки, в том числе более высокую стоимость из-за более низкой плотности энергии. Плотность энергии значительно ниже, чем у LiCoO.
2(хотя и выше, чем у никель-металлогидридной батареи ).
Аккумуляторы на основе оксида лития-кобальта более склонны к тепловому выходу из строя при перезарядке, а кобальт является дорогим и не широко доступным. Другие химические вещества, такие как NMC Ni Mn Co, вытеснили химические ячейки LiCo в большинстве приложений. Первоначальное соотношение Ni, Mn и Co было сегодня 3: 3: 3, ячейки изготавливаются с соотношением 8: 1: 1, в результате чего содержание Co резко снижено.
Интеллектуальная собственность [ править ]
Основные патенты на соединения LFP принадлежат четырем организациям. Техасский университет в Остине за открытие материала. Hydro-Québec , Université de Montréal и Французский национальный центр научных исследований (CNRS) за углеродное покрытие, которое увеличивает его проводимость и фактически делает LFP пригодным для промышленных разработок. [17] Эти патенты лежат в основе зрелых технологий массового производства. Самая большая производственная мощность - до 250 тонн в месяц. Ключевая особенность Ли
1-хMFePO
4 от A123 - это нано-LFP, который изменяет его физические свойства и добавляет в анод благородные металлы, а также использует специальный графит в качестве катода.
Основная особенность LiMPO
4от Phostech - это повышенная емкость и проводимость за счет соответствующего углеродного покрытия. Особенность LiFePO
4• zM от Aleees: высокая емкость и низкий импеданс, достигнутые благодаря стабильному контролю ферритов и роста кристаллов. Этот улучшенный контроль реализуется путем приложения сильных механических усилий перемешивания к прекурсорам в состояниях высокого перенасыщения, что вызывает кристаллизацию оксидов металлов и LFP.
В патентных исках в США в 2005 и 2006 годах Техасский университет в Остине | Техасский университет в Остине и Гидро-Квебек заявил, что LiFePO
4поскольку катод нарушает их патенты, US 5910382 и US 6514640 . Формула изобретения включает уникальную кристаллическую структуру и химическую формулу материала катода батареи.
7 апреля 2006 г. A123 подала иск о признании недействительности патентов UT. A123 отдельно подала в Ведомство США по патентам и товарным знакам (USPTO) две процедуры повторной экспертизы ex parte , в которых они стремились признать патенты недействительными на основании предшествующего уровня техники.
В параллельном судебном разбирательстве UT подала в суд на Valence Technology, Inc. («Валенсия») - компанию, которая занимается коммерциализацией продукции LFP, в которой якобы нарушены права.
ВПТЗ США выдало Свидетельство о повторной экспертизе для патента '382 15 апреля 2008 г. и для патента' 640 12 мая 2009 г., которым были изменены формулы этих патентов. Это позволило продолжить рассмотрение текущих исков о нарушении патентных прав, поданных Hydro-Quebec против Valence и A123. После слушания по Маркману 27 апреля 2011 г. Западный окружной суд Техаса постановил, что иски по повторно рассмотренным патентам имеют более узкую сферу действия, чем первоначально предоставленное.
9 декабря 2008 г. Европейское патентное ведомство отозвало патент доктора Гуденаф под номером 0904607. Это решение в основном снизило патентный риск использования LFP в европейских автомобильных приложениях. Считается, что решение основано на отсутствии новизны. [18]
Первым крупным мировым соглашением стал судебный процесс между NTT и Техасским университетом в Остине (Юта). В октябре 2008 года [19] NTT объявили, что урегулируют дело в Верховном гражданском суде Японии на 30 миллионов долларов. В рамках соглашения UT согласился с тем, что NTT не крадила информацию и что NTT поделится своими патентами LFP с UT. Патент NTT также на оливиновый LFP с общей химической формулой A
уMPO
4(A для щелочного металла и M для комбинации Co и Fe), в настоящее время используется компанией BYD . Хотя химически материалы почти такие же, с точки зрения патентов, A
уMPO
4NTT отличается от материалов, покрытых UT. А
уMPO
4имеет большую емкость, чем LiMPO
4. В основе дела лежало то, что инженер NTT Окада Сигето, который работал в лабораториях UT, разрабатывая материал, был обвинен в краже интеллектуальной собственности UT .
По состоянию на 2020 год организация под названием LifePO + C утверждает, что владеет ключевым IP-адресом и предлагает лицензии. Это консорциум между Johnson Matthey, CNRS, Монреальским университетом и Hydro Quebec.
Исследование [ править ]
Плотность мощности [ править ]
LFP имеет два недостатка: низкая проводимость и низкая константа диффузии лития, оба из которых ограничивают скорость заряда / разряда. Добавление проводящих частиц в делитированный FePO
4повышает его электронную проводимость. Например, добавление в LiMPO проводящих частиц с хорошей диффузионной способностью, таких как графит и углерод [20]
4порошки значительно улучшают проводимость между частицами, повышают эффективность LiMPO
4и увеличивает обратимую мощность до 95% от теоретических значений. LiMPO
4показывает хорошие характеристики при езде на велосипеде даже при токе заряда / разряда до 5C. [21]
Стабильность [ править ]
Покрытие LFP неорганическими оксидами может сделать структуру LFP более стабильной и повысить проводимость. Традиционный LiCoO
2с оксидным покрытием показывает улучшенные циклические характеристики. Это покрытие также препятствует растворению Co и замедляет распад LiCoO.
2вместимость. Аналогично LiMPO
4с неорганическим покрытием, таким как ZnO [22] и ZrO2, [23] имеет более длительный срок службы, большую емкость и лучшие характеристики при быстром разряде. Добавление проводящего углерода увеличивает эффективность. Мицуи Зосен и Алиис сообщили, что добавление проводящих металлических частиц, таких как медь и серебро, повысило эффективность. [24] ЛиМПО
4 с 1 мас.% металлических добавок имеет обратимую емкость до 140 мАч / г и лучшую эффективность при высоком токе разряда.
Замена металла [ править ]
Замена железа или лития в LiMPO другими металлами
4может также повысить эффективность. Замена цинка на железо увеличивает кристалличность LiMPO.
4потому что цинк и железо имеют одинаковые ионные радиусы. [25] Циклическая вольтамперометрия подтверждает, что LiFe
1-хM
ИксPO
4после замещения металлов имеет более высокую обратимость внедрения и извлечения иона лития. Во время экстракции лития Fe (II) окисляется до Fe (III), и объем решетки сокращается. Уменьшение объема изменяет пути возврата лития.
Процессы синтеза [ править ]
Массовое производство со стабильным и высоким качеством по-прежнему сталкивается с множеством проблем.
Подобно оксидам лития, LiMPO
4могут быть синтезированы различными методами, включая: твердофазный синтез , эмульсионную сушку, золь-гель процесс , соосаждение раствора, парофазное осаждение , электрохимический синтез, облучение электронным пучком , микроволновый процесс [ неопределенно ] , гидротермальный синтез, ультразвуковой пиролиз и пиролиз распылением .
В процессе сушки эмульсии эмульгатор сначала смешивается с керосином. Далее к этой смеси добавляют растворы солей лития и солей железа. Этот процесс производит наноуглеродные частицы. [26] Гидротермальный синтез производит LiMPO.
4с хорошей кристалличностью. Электропроводящий углерод получают путем добавления в раствор полиэтиленгликоля с последующей термической обработкой. [27] При осаждении из паровой фазы образуется тонкая пленка LiMPO.
4. [28] В пламенном пиролизе распылением FePO 4 смешивают с карбонатом лития и глюкозой и заряжают электролитами . Затем смесь впрыскивают внутрь пламени и фильтруют, чтобы собрать синтезированный LiFePO.
4. [29]
См. Также [ править ]
- Литий-железо-фосфатный аккумулятор
- Системы A123
- Технология Валентности
Ссылки [ править ]
- ^ Парк, хорошо; Чо, Й .; Lee, S .; Ю, Х.-К .; Песня, Х.-К .; Чо, Дж., «Кто будет водить электромобили, оливин или шпинель?», Energy Environ. Sci. 2011 г., том 4, страницы 1621-1633. DOI : 10.1039 / c0ee00559b
- ^ Одзава, Райан. «Запуск нового хранилища энергии, чтобы отключить дома Гавайев от сети» . Блог Гавайев . Проверено 9 июля 2015 . CS1 maint: обескураженный параметр ( ссылка )
- ^ Федотов, Станислав С .; Лучинин, Никита Д .; Аксёнов Дмитрий А .; Морозов, Анатолий В .; Рязанцев, Сергей В .; Габоарди, Маттиа; Plaisier, Jasper R .; Стивенсон, Кейт Дж .; Абакумов Артем М .; Антипов, Евгений В. (2020-03-20). «Положительный электрод калий-ионной батареи на основе титана с чрезвычайно высоким окислительно-восстановительным потенциалом» . Nature Communications . 11 (1): 1484. Bibcode : 2020NatCo..11.1484F . DOI : 10.1038 / s41467-020-15244-6 . ISSN 2041-1723 . PMC 7083823 . PMID 32198379 .
LiTiPO4F
- ^ Ким, Jongsoon. «Термическая стабильность бинарных оливиновых катодов Fe-Mn для литиевых аккумуляторных батарей» . Королевское химическое общество . Дата обращения 19 октября 2012 . CS1 maint: обескураженный параметр ( ссылка )
- ^ Wang, J .; Сан, X., "Olivine Lifepo4: Остающиеся проблемы для будущего хранения энергии", Energy Environ. Sci. 2015 г., том 8, страницы 1110-1138. DOI : 10.1039 / C4EE04016C
- ^ Маскелье, Кристиан; Крогеннек, Лоуренс (2013). «Полианионные (фосфаты, силикаты, сульфаты) каркасы в качестве электродных материалов для аккумуляторных Li (или Na) батарей». Химические обзоры . 113 (8): 6552–6591. DOI : 10.1021 / cr3001862 . PMID 23742145 .
- ^ Manthiram, A .; Гуденаф, Дж. Б. (1989). «Введение лития в каркасы Fe 2 (SO 4 ) 3 ». Журнал источников энергии . 26 (3–4): 403–408. Bibcode : 1989JPS .... 26..403M . DOI : 10.1016 / 0378-7753 (89) 80153-3 .
- ^ Manthiram, A .; Гуденаф, Дж. Б. (1987). «Введение лития в каркасы Fe 2 (MO 4 ) 3 : Сравнение M = W с M = Mo». Журнал химии твердого тела . 71 (2): 349–360. Bibcode : 1987JSSCh..71..349M . DOI : 10.1016 / 0022-4596 (87) 90242-8 .
- ^ " LiFePO
4: Новый катодный материал для аккумуляторных батарей », AK Padhi, KS Nanjundaswamy, JB G динаф, Тезисы собраний электрохимического общества, 96-1 , май 1996 г., стр. 73 - ^ «Фосфооливины как материалы положительных электродов для перезаряжаемых литиевых батарей» AK Padhi, KS Nanjundaswamy и JB G динаф, J. Electrochem. Soc., Том 144, выпуск 4, стр. 1188-1194 (апрель 1997 г.)
- ^ Материалы природы, 2008, 7, 707-711.
- ^ Югович, Драган; Ускокович, Драган (15 мая 2009 г.). «Обзор последних разработок в процедурах синтеза порошков фосфата лития-железа» . Журнал источников энергии . 190 (2): 538–544. Bibcode : 2009JPS ... 190..538J . DOI : 10.1016 / j.jpowsour.2009.01.074 . ISSN 0378-7753 . Проверено 21 ноября 2017 . CS1 maint: обескураженный параметр ( ссылка )
- ^ a b Любовь, Кори Т .; Коровина, Анна; Патридж, Кристофер Дж .; Свидер-Лион; Карен Э .; Twigg, Mark E .; Рамакер, Дэвид Э. (2013). «Обзор механизмов фазового перехода LiFePO 4 и новые наблюдения рентгеновской спектроскопии поглощения». Журнал Электрохимического общества . 160 (5): A3153 – A3161. DOI : 10.1149 / 2.023305jes .
- ^ Малик, Р .; Abdellahi, A .; Седер, Г., "Критический обзор механизмов введения Li вэлектродыLiFePO 4 ", J. Electrochem. Soc. 2013 г., том 160, стр. A3179-A3197. DOI : 10.1149 / 2.029305jes
- ^ Литий-ионные аккумуляторные батареи на основе катодных материалов со структурой оливина (LiFePO4) - Кумар и др. , 15 ноября 2015 г., получено 1 апреля 2020 г.
- ^ https://offgridham.com/2016/03/about-lifepo4-batteries/
- ^ http://www.clariant.com.br/C12576850036A6E9/8650B24BC3A7BAF3C12579C2003552DA/$FILE/20120314_BASF_enters_into_a_sublicense_agreement_with_LiFePO4C_Licensing_AG.pdf
- ^ "ЕПВ аннулирует европейский патент Техасского университета на фосфаты металлического лития; благо для валентности" .
- ^ "NTT улаживает судебный процесс по патентам на литий-ионные батареи" .
- ^ Деб, Анируддха; Бергманн, Уве; Кэрнс, Элтон Дж .; Крамер, Стивен П. (июнь 2004 г.). "Структурные исследования электродов LiFePO 4 методом рентгеновской абсорбционной спектроскопии Fe". Журнал физической химии B . 108 (22): 7046–7051. DOI : 10.1021 / jp036361t .
- ^ Haas, O .; Deb, A .; Кэрнс, EJ; Вокаун, А. (2005). «Синхротронное рентгеновское исследование поглощения LiFePO [sub 4] электродов». Журнал Электрохимического общества . 152 (1): A191. DOI : 10.1149 / 1.1833316 .
- ^ Квон, Санг Джун; Ким, Чхоль Ву; Чон, Ун Тэ; Ли, Кён Суб (октябрь 2004 г.). «Синтез и электрохимические свойства оливина LiFePO4 как катодного материала, полученного методом механического легирования». Журнал источников энергии . 137 (1): 93–99. Bibcode : 2004JPS ... 137 ... 93K . DOI : 10.1016 / j.jpowsour.2004.05.048 .
- ^ Dominko, R .; Беле, М .; Габершек, М .; Ремскар, М .; Hanzel, D .; Goupil, JM; Пейовник, С .; Ямник, Дж. (Февраль 2006 г.). «Пористые оливиновые композиты, синтезированные золь-гель методом». Журнал источников энергии . 153 (2): 274–280. Bibcode : 2006JPS ... 153..274D . DOI : 10.1016 / j.jpowsour.2005.05.033 .
- ^ Леон, В .; Висенте, К. Перес; Тирадо, JL; Biensan, Ph .; Тессье, К. (2008). «Оптимизированная химическая стабильность и электрохимические характеристики композиционных материалов LiFePO [sub 4], полученных с помощью покрытия ZnO». Журнал Электрохимического общества . 155 (3): A211 – A216. DOI : 10.1149 / 1.2828039 .
- ^ Лю, H .; Ван, GX; Wexler, D .; Wang, JZ; Лю, Гонконг (январь 2008 г.). «Электрохимические характеристики катодного материала LiFePO4, покрытого нанослоем ZrO2». Электрохимические коммуникации . 10 (1): 165–169. DOI : 10.1016 / j.elecom.2007.11.016 .
- ^ Croce, F .; D 'Epifanio, A .; Hassoun, J .; Deptula, A .; Olczac, T .; Скросати, Б. (2002). «Новая концепция синтеза улучшенного катода литиевой батареи LiFePO [sub 4]». Электрохимические и твердотельные письма . 5 (3): A47 – A50. DOI : 10.1149 / 1.1449302 .
- ^ Ni, JF; Чжоу, HH; Чен, Джей Ти; Чжан, XX (август 2005 г.). «LiFePO4, легированный ионами, полученный методом соосаждения». Материалы Письма . 59 (18): 2361–2365. DOI : 10.1016 / j.matlet.2005.02.080 .
- ↑ Чо, Тэ-Хён; Чунг, Хун-Тхэк (июнь 2004 г.). «Синтез LiFePO4 оливинового типа методом сушки в эмульсии». Журнал источников энергии . 133 (2): 272–276. Bibcode : 2004JPS ... 133..272C . DOI : 10.1016 / j.jpowsour.2004.02.015 .
- ^ Хамид, NA; Wennig, S .; Hardt, S .; Heinzel, A .; Schulz, C .; Виггерс, Х. (октябрь 2012 г.). «Катоды большой емкости для литий-ионных аккумуляторов из наноструктурированного LiFePO4, синтезированного с помощью очень гибкого и масштабируемого пиролиза с распылением пламени». Журнал источников энергии . 216 : 76–83. Bibcode : 2012JPS ... 216 ... 76H . DOI : 10.1016 / j.jpowsour.2012.05.047 .
