| Вирус эшерихии ΦX174 | |
|---|---|
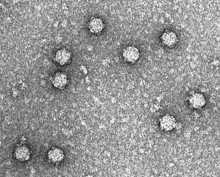 | |
| Электронная микрофотография фага ΦX174 | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Царство : | Моноднавирия |
| Королевство: | Sangervirae |
| Тип: | Phixviricota |
| Учебный класс: | Malgrandaviricetes |
| Заказ: | Petitvirales |
| Семья: | Микровирусы |
| Род: | Синшеймервирус |
| Разновидность: | Вирус эшерихии ΦX174 |
Фи Х 174 (или ΦX174 ) бактериофаг представляет собой одноцепочечную ДНК ( оцДНК вирус) , который заражает кишечной палочки , а также первая ДНК на основе генома , чтобы быть секвенированы. Эта работа была завершена Фредом Сэнгером и его командой в 1977 году. [1] В 1962 году Уолтер Фирс и Роберт Зиншеймер уже продемонстрировали физическую ковалентно замкнутую кольцевость ДНК ΦX174. [2] Лауреат Нобелевской премии Артур Корнберг использовал ΦX174 в качестве модели, чтобы сначала доказать, что ДНК, синтезированная в пробирке очищенными ферментами, может производить все свойства природного вируса, открывая эрусинтетическая биология . [3] [4] В 1972–1974 годах Джерард Гурвиц , Сью Викнер и Рид Викнер с сотрудниками определили гены, необходимые для производства ферментов, катализирующих превращение одноцепочечной формы вируса в двухцепочечную репликативную форму. [5] В 2003 году группа Крейга Вентера сообщила , что геном ΦX174 был первым, полностью собранным in vitro из синтезированных олигонуклеотидов. [6] Частица вируса ΦX174 также была успешно собрана in vitro . [7] В 2012 году было показано, насколько высокоперекрывающийся геном может быть полностью декомпрессирован и при этом оставаться функциональным. [8]
Геном [ править ]
Этот бактериофаг имеет [+] смысловой кольцевой одноцепочечный геном ДНК из 5 386 нуклеотидов . [9] GC-содержание генома составляет 44%, и 95% нуклеотидов принадлежат кодирующим генам. Из-за сбалансированной базовой структуры генома она используется в качестве контрольной ДНК для секвенсоров Illumina.
Гены [ править ]
ΦX174 кодирует 11 генов, названных последовательными буквами алфавита в том порядке, в котором они были обнаружены, за исключением A *, который является альтернативным стартовым кодоном в больших генах A. Только гены A * и K считаются несущественными, хотя есть некоторые сомнения относительно A *, потому что его стартовый кодон может быть изменен на ATT, но не на любую другую последовательность. [10] В настоящее время известно, что ATT все еще способен продуцировать белок [11] в E. coli, и поэтому этот ген не может быть второстепенным.
Фаг ΦX174 использовался, чтобы попытаться установить отсутствие неоткрытой генетической информации с помощью подхода «доказательства путем синтеза». [12]
Транскриптом [ править ]
В 2020 году был сгенерирован транскриптом ΦX174. [13] Примечательными особенностями транскриптома ΦX174 является серия до четырех относительно слабых промоторов, последовательно включенных до четырех Rho-независимых (внутренних) терминаторов и одного Rho-зависимого терминатора.
Белки [ править ]
ΦX174 кодирует 11 белков .
| Протеин | Копии | Функция [14] |
|---|---|---|
| А | - | Разрывает ДНК РФ, чтобы инициировать репликацию по катящемуся кругу ; лигирует концы линейной ДНК фага с образованием одноцепочечной кольцевой ДНК |
| А * | - | Подавляет репликацию ДНК клетки-хозяина; блокирует суперинфицирующий фаг; не важно |
| B | 60 в прокапсиде | Белок внутреннего каркаса, участвующий в сборке прокапсида |
| C | - | Упаковка ДНК |
| D | 240 в прокапсиде | Внешний каркасный белок, участвующий в сборке прокапсида |
| E | - | Клетка - хозяин лизис |
| F | 60 в вирионе | Основной белок капсида |
| грамм | 60 в вирионе | Основной протеин шипа |
| ЧАС | 12 в вирионе | Пилотный белок ДНК (или второстепенный спайковый белок) |
| J | 60 в вирионе | Связывается с новой одноцепочечной ДНК фага; сопровождает ДНК фага в прокапсид |
| K | - | Оптимизирует размер пакета; не важно |
Протеом [ править ]
Недавно сообщалось об идентификации всех белков ΦX174 с помощью масс-спектрометрии. [15]
Цикл заражения [ править ]
Заражение начинается, когда G-белок связывается с липополисахаридами на поверхности бактериальной клетки-хозяина. Белок H (или белок-пилот ДНК) направляет вирусный геном через бактериальную мембрану бактерий E.coli [16], скорее всего, через предсказанную спираль N-концевого трансмембранного домена . [17] Однако стало очевидно, что белок H является многофункциональным белком. [18] Это единственный вирусный капсидный белок ΦX174, у которого отсутствует кристаллическая структура по нескольким причинам. Он имеет низкое содержание ароматических веществ и высокое содержание глицина.содержание, что делает структуру белка очень гибкой и, кроме того, отдельные атомы водорода (группа R для глицинов) трудно обнаружить в кристаллографии белка. Кроме того, белок H индуцирует лизис бактериального хозяина в высоких концентрациях, поскольку предсказанная N-концевая трансмембранная спираль легко протыкает стенки бактериальной стенки. Согласно биоинформатике , этот белок содержит четыре предсказанных домена спиральной спирали, которые имеют значительную гомологию с известными факторами транскрипции. Кроме того, было определено, что белок H de novo необходим для оптимального синтеза других вирусных белков. [19] Мутации в белке H, которые предотвращают включение вируса, можно преодолеть, если доставить избыточное количество белка B, внутреннего каркасного белка.
ДНК выбрасывается через гидрофильный канал в 5-кратной вершине. [20] Понятно, что белок H находится в этой области, но экспериментальные данные не подтвердили его точное местоположение. Попав внутрь бактерии-хозяина, репликация генома [+] оцДНК происходит через промежуточный продукт отрицательной смысловой ДНК . Это происходит по мере того, как суперспирали фагового генома и вторичная структура, образованная такой суперспирализацией, привлекают примосомы.белковый комплекс. Он перемещается один раз по геному и синтезирует [-] оцДНК из положительного исходного генома. [+] Геномы оцДНК для упаковки в вирусы создаются по механизму катящегося круга. Это механизм, с помощью которого двухцепочечный суперспиральный геном разрывается на положительной цепи кодируемым вирусом A-белком, также привлекая бактериальную ДНК-полимеразу (DNAP) к месту расщепления. DNAP использует отрицательную цепь в качестве матрицы для создания положительной смысловой ДНК. По мере того, как он перемещается по геному, он вытесняет внешнюю цепь уже синтезированной ДНК, которая немедленно покрывается белками SSBP . Белок A расщепляет полный геном каждый раз, когда он распознает исходную последовательность.
Поскольку белок D является наиболее распространенным транскриптом гена, он является наиболее распространенным белком в вирусном прокапсиде. Точно так же транскрипты генов для F, J и G более многочисленны, чем для H, поскольку стехиометрия для этих структурных белков составляет 5: 5: 5: 1. Примосомы представляют собой белковые комплексы, которые прикрепляют / связывают фермент геликазу на матрице. Примосомы дают праймеры РНК для синтеза ДНК цепям.
Филогенетика и разнообразие [ править ]
ΦX174 тесно связан с другими микровирусами , особенно с фагом NC (например, NC1, NC7, NC11, NC16, NC37, NC5, NC41, NC56, NC51 и т. Д.) И более отдаленно связан с G4-подобными фагами и даже более отдаленно связан с ними. к α3-подобному фагу. Rokyta et al. 2006 год представил филогенетическое древо их взаимоотношений. [21]
Использует [ редактировать ]
Экспериментальная эволюция [ править ]
ΦX174 использовался в качестве модельного организма во многих эволюционных экспериментах. [22]
Биотехнология [ править ]
ΦX174 регулярно используется в качестве положительного контроля при секвенировании ДНК из-за его относительно небольшого размера генома по сравнению с другими организмами, его относительно сбалансированного содержания нуклеотидов - около 23% G, 22% C, 24% A и 31% T, т. Е. 45% G + C и 55% A + T, см. Номер доступа NC_001422.1 [9] для его последовательности длиной 5386 нуклеотидов. Приборы для секвенирования Illumina используют ΦX174 в качестве положительного контроля [23], а один цикл секвенирования Illumina может покрыть геном ΦX174 несколько миллионов раз, что делает этот геном, вероятно, наиболее сильно секвенированным геномом в истории. [ необходима цитата ]
ΦX174 также используется для проверки устойчивости средств индивидуальной защиты к вирусам, передающимся с кровью. [24]
ΦX174 также был модифицирован для включения пептидного дисплея (фагового дисплея) из G-белка вирусного капсида. [25]
Синтетическая биология [ править ]
Геном ΦX174 был первым фагом, который был клонирован в дрожжах [26], который представляет собой удобный сухой док для модификаций генома. [27] ΦX174 был также первым геномом, который был полностью декомпрессирован с удалением всех перекрытий генов. Эффект этих изменений привел к значительному снижению привязанности к хозяину, нарушению регуляции экспрессии белков и чувствительности к температуре. [28]
См. Также [ править ]
- Бактериофаг MS2
Ссылки [ править ]
- ^ Sanger F, Air GM, Barrell BG, Brown NL, Coulson AR, Fiddes CA и др. (Февраль 1977 г.). «Нуклеотидная последовательность ДНК бактериофага phi X174». Природа . 265 (5596): 687–95. Bibcode : 1977Natur.265..687S . DOI : 10.1038 / 265687a0 . PMID 870828 . S2CID 4206886 .
- ^ Фирс W, Sinsheimer RL (октябрь 1962 г.). «Структура ДНК бактериофага phi-X174. III. Ультрацентробежные доказательства кольцевой структуры». Журнал молекулярной биологии . 5 (4): 424–34. DOI : 10.1016 / S0022-2836 (62) 80031-X . PMID 13945085 .
- ^ Национальная библиотека медицинских профилей в науке. Документы Артура Корнберга. «Создание жизни в пробирке», 1959-1970 гг. ссылка [необходим неосновной источник ]
- ^ Goulian M, Корнберг A, Sinsheimer RL (декабрь 1967). «Ферментативный синтез ДНК, XXIV. Синтез ДНК инфекционного фага phi-X174» . Труды Национальной академии наук Соединенных Штатов Америки . 58 (6): 2321–8. Bibcode : 1967PNAS ... 58.2321G . DOI : 10.1073 / pnas.58.6.2321 . JSTOR 58720 . PMC 223838 . PMID 4873588 .
- ^ Wickner S, Гурвиц J (октябрь 1974). «Превращение вирусной ДНК phiX174 в двухцепочечную форму очищенными белками Escherichia coli» . Труды Национальной академии наук Соединенных Штатов Америки . 71 (10): 4120–4. DOI : 10.1073 / pnas.71.10.4120 . PMC 434340 . PMID 4610569 .
- ^ Smith HO, Hutchison CA, Pfannkoch C, Вентер JC (декабрь 2003). «Создание синтетического генома путем сборки всего генома: бактериофаг phiX174 из синтетических олигонуклеотидов» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (26): 15440–5. Bibcode : 2003PNAS..10015440S . DOI : 10.1073 / pnas.2237126100 . JSTOR 3149024 . PMC 307586 . PMID 14657399 .
- ^ Cherwa JE, Organtini LJ, Эшли RE, Hafenstein SL, Фейн BA (сентябрь 2011). «В VITRO ASSEMBLY прокапсида øX174 из олигомеров внешних каркасных белков и промежуточных продуктов ранней пентамерной сборки». Журнал молекулярной биологии . 412 (3): 387–96. DOI : 10.1016 / j.jmb.2011.07.070 . PMID 21840317 .
- ^ Jaschke PR, Либерман Е., Родригес J, Sierra A, D Endy (декабрь 2012). «Полностью декомпрессированный геном синтетического бактериофага øX174, собранный и заархивированный в дрожжах» . Вирусология . 434 (2): 278–84. DOI : 10.1016 / j.virol.2012.09.020 . PMID 23079106 .
- ^ a b c Enterobacteria phage phiX174 sensu lato , полный геном. «Полный геном: номер NC_001422» , Национальный центр биотехнологической информации . Проверено 30 января, 2016.
- ^ Баас PD, Liewerink H, ван Teeffelen HA, ван Mansfeld AD, ван Boom JH, Янс HS (июнь 1987). «Изменение стартового кодона ATG белка A бактериофага phi X174 на кодон ATT дает жизнеспособный фаг, указывающий на то, что белок A не является существенным для воспроизводства phi X174» . Письма FEBS . 218 (1): 119–25. DOI : 10.1016 / 0014-5793 (87) 81030-х . PMID 2954853 . S2CID 24174007 .
- ^ Хект А, Глазго Дж, Jaschke PR, Bawazer Л.А., Мансон М.С., Кокрэн JR, и др. (Апрель 2017 г.). «Измерения инициации трансляции со всех 64 кодонов в E. coli» . Исследования нуклеиновых кислот . 45 (7): 3615–3626. DOI : 10.1093 / NAR / gkx070 . PMC 5397182 . PMID 28334756 .
- ^ Jaschke PR, Dotson GA, Hung KS, Лю Д., Энди Д. (ноябрь 2019 г.). «Окончательная демонстрация путем синтеза полноты аннотации генома» . Труды Национальной академии наук Соединенных Штатов Америки . 116 (48): 24206–24213. DOI : 10.1073 / pnas.1905990116 . PMC 6883844 . PMID 31719208 .
- ^ Logel DY, Jaschke PR (август 2020). «Карта транскрипции бактериофага ϕX174 с высоким разрешением». Вирусология . 547 : 47–56. DOI : 10.1016 / j.virol.2020.05.008 . PMID 32560904 .
- ↑ Fane BA, Brentlinger KL, Burch AD, Chen M, Hafenstein S, Moore E, Novak CR, Uchiyama A (2006). «ɸX174 et al., Microviridae ». В календаре R (ред.). Бактериофаги (2-е изд.). Нью-Йорк: Oxford Univ. Нажмите. п. 130. ISBN 978-0195148503.
- ↑ Райт Б.В., Руан Дж., Член Моллоя, Яшке ПР (ноябрь 2020 г.). «Модуляризация генома показывает, что топология перекрывающихся генов необходима для эффективного размножения вирусов». Синтетическая биология ACS . 9 (11): 3079–3090. DOI : 10.1021 / acssynbio.0c00323 . PMID 33044064 .
- ^ Jazwinski С.М., Линдберг А.А., Корнберг A (июль 1975). «Липополисахаридный рецептор бактериофагов phiX174 и S13». Вирусология . 66 (1): 268–82. DOI : 10.1016 / 0042-6822 (75) 90197-X . PMID 1094681 .
- ^ Тушнади GE, Симон I (сентябрь 2001). «Сервер прогнозирования трансмембранной топологии HMMTOP» . Биоинформатика . 17 (9): 849–50. DOI : 10.1093 / биоинформатики / 17.9.849 . PMID 11590105 .
- ^ Cherwa JE, Young LN, Фейн BA (март 2011). «Разделение функций многофункционального белка: выделение мутанта экспериментального белка ДНК, который влияет на морфогенез частиц». Вирусология . 411 (1): 9–14. DOI : 10.1016 / j.virol.2010.12.026 . PMID 21227478 .
- ^ Ruboyianes М. В., Чен М, Дубрава MS, Cherwa JE, Фейн BA (октябрь 2009). «Экспрессия пилотных белков ДНК с N-концевой делецией ингибирует ранние стадии репликации phiX174» . Журнал вирусологии . 83 (19): 9952–6. DOI : 10,1128 / JVI.01077-09 . PMC 2748053 . PMID 19640994 .
- ^ McKenna R, Xia D, Willingmann P, Ilag LL, Krishnaswamy S, Rossmann MG и др. (Январь 1992 г.). «Атомная структура одноцепочечной ДНК бактериофага phi X174 и ее функциональные последствия» . Природа . 355 (6356): 137–43. Bibcode : 1992Natur.355..137M . DOI : 10.1038 / 355137a0 . PMC 4167681 . PMID 1370343 .
- ^ Rokyta DR, Burch CL, Caudle SB, Wichman HA (февраль 2006). «Горизонтальный перенос генов и эволюция геномов микровирид-колифагов» . Журнал бактериологии . 188 (3): 1134–42. DOI : 10.1128 / JB.188.3.1134-1142.2006 . PMC 1347346 . PMID 16428417 .
- ^ Wichman HA, Brown CJ (август 2010). «Экспериментальная эволюция вирусов: Microviridae как модельная система» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 365 (1552): 2495–501. DOI : 10,1098 / rstb.2010.0053 . PMC 2935103 . PMID 20643739 .
- ^ «Использование PhiX Control для циклов секвенирования HiSeq®» . Иллюмина. Архивировано из оригинала 9 января 2019 года . Проверено 8 января 2019 .
- ^ "PPE-Info - Стандартные детали" . wwwn.cdc.gov . Проверено 8 февраля 2019 .
- ^ Кристакос KJ, Chapman JA, Фейн BA, Campos SK (январь 2016). «PhiXing-it, отображение чужеродных пептидов на бактериофаге ΦX174» . Вирусология . 488 : 242–8. DOI : 10.1016 / j.virol.2015.11.021 . PMC 6191337 . PMID 26655242 .
- ^ Jaschke PR, Либерман Е., Родригес J, Sierra A, D Endy (декабрь 2012). «Полностью декомпрессированный геном синтетического бактериофага øX174, собранный и заархивированный в дрожжах» . Вирусология . 434 (2): 278–84. DOI : 10.1016 / j.virol.2012.09.020 . PMID 23079106 .
- ^ Ando H, Lemire S, Пирес DP, Лу ТК (сентябрь 2015). «Разработка модульных вирусных матриксов для целевого редактирования бактериальной популяции» . Клеточные системы . 1 (3): 187–196. DOI : 10.1016 / j.cels.2015.08.013 . PMC 4785837 . PMID 26973885 .
- ↑ Райт Б.В., Руан Дж., Член Моллоя, Яшке ПР (ноябрь 2020 г.). «Модуляризация генома показывает, что топология перекрывающихся генов необходима для эффективного размножения вирусов». Синтетическая биология ACS . 9 (11): 3079–3090. DOI : 10.1021 / acssynbio.0c00323 . PMID 33044064 .
Внешние ссылки [ править ]
- Гудселл Д. (февраль 2000 г.). «Бактериофаг phiX174» . Молекула месяца . RCSB-PDB.

