
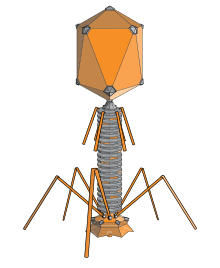
Бактериофага ( / б æ к т ɪər я oʊ е eɪ dʒ / ), также известный как неформально фага ( / е eɪ dʒ / ), представляет собой вирус , который заражает и реплицируется в пределах бактерий и архей . Этот термин произошел от слова «бактерии» и греческого слова φαγεῖν ( фагин ), что означает «пожирать». Бактериофаги состоят из белков , которые инкапсулируют с ДНК или РНК геном и может иметь простую или сложную структуру. Их геномы могут кодировать всего четыре гена (например, MS2 ) и сотни генов . Фаги размножаются внутри бактерии после инъекции их генома в ее цитоплазму .
Бактериофаги - одни из самых распространенных и разнообразных организмов в биосфере . [1] Бактериофаги - это повсеместно распространенные вирусы, которые встречаются везде, где существуют бактерии. По оценкам, на планете более 10 31 бактериофагов, больше, чем у всех других организмов на Земле, включая бактерии, вместе взятые. [2] Вирусы являются наиболее распространенным биологическим объектом в толще воды мирового океана, и второй по величине составляющей биомассы после прокариота , [3] , где до 9x10 8 вирион на миллилитр были найдены в микробных матах на поверхности, [4] и до 70% морских бактериймогут быть инфицированы фагами. [5]
Фаги использовались с конца 20 века в качестве альтернативы антибиотикам в бывшем Советском Союзе и Центральной Европе, а также во Франции. [6] [7] Они рассматриваются как возможная терапия против штаммов многих бактерий с множественной лекарственной устойчивостью (см. Фаговая терапия ). [8] С другой стороны, было показано , что фаги Inoviridae усложняют биопленки, участвующие в пневмонии и муковисцидозе, и защищают бактерии от лекарств, предназначенных для искоренения болезни, тем самым способствуя устойчивой инфекции. [9]
Классификация [ править ]
Бактериофаги широко распространены в биосфере, имеют разные геномы и образ жизни. Фаги классифицируются Международным комитетом по таксономии вирусов (ICTV) в соответствии с морфологией и нуклеиновой кислотой.
| Заказ | Семья | Морфология | Нуклеиновая кислота | Примеры |
|---|---|---|---|---|
| Белфривиралес | Turriviridae | Обернутый, изометрический | Линейная дцДНК | |
| Caudovirales | Ackermannviridae | Без оболочки , сократительный хвост | Линейная дцДНК | |
| Myoviridae | Безобутальный сократительный хвост | Линейная дцДНК | T4 , Mu , P1 , P2 | |
| Siphoviridae | Хвост без оболочки, не сокращающийся (длинный) | Линейная дцДНК | λ , Т5 , HK97 , N15 | |
| Podoviridae | Хвост без оболочки, не сокращающийся (короткий) | Линейная дцДНК | T7 , T3 , Φ29 , P22 | |
| Halopanivirales | Sphaerolipoviridae | Обернутый, изометрический | Линейная дцДНК | |
| Haloruvirales | Pleolipoviridae | Обволакивающий, плеоморфный | Круговая оцДНК, круговая дцДНК или линейная дцДНК | |
| Kalamavirales | Tectiviridae | Без оболочки, изометрическая | Линейная дцДНК | |
| Левивиралес | Левивириды | Без оболочки, изометрическая | Линейная оцРНК | MS2 , Qβ |
| Ligamenvirales | Lipothrixviridae | Обволакивающий, стержневидный | Линейная дцДНК | Нитчатый вирус Acidianus 1 |
| Rudiviridae | Без оболочки, стержневидный | Линейная дцДНК | Палочковидный вирус Sulfolobus islandicus 1 | |
| Миндивиралес | Cystoviridae | Обволакивающий, сферический | Сегментированная дцРНК | Φ6 |
| Petitvirales | Микровирусы | Без оболочки, изометрическая | Круговая оцДНК | ΦX174 |
| Tubulavirales | Inoviridae | Без оболочки, нитчатый | Круговая оцДНК | M13 |
| Винавиралес | Corticoviridae | Без оболочки, изометрическая | Круговая дцДНК | PM2 |
| Не назначен | Ampullaviridae | Обернутый, в форме бутылки | Линейная дцДНК | |
| Bicaudaviridae | Без оболочки, в форме лимона | Круговая дцДНК | ||
| Clavaviridae | Без оболочки, стержневидный | Круговая дцДНК | ||
| Finnlakeviridae | дцДНК | FLiP [10] | ||
| Fuselloviridae | Без оболочки, в форме лимона | Круговая дцДНК | ||
| Globuloviridae | Обернутый, изометрический | Линейная дцДНК | ||
| Guttaviridae | Без оболочки, яйцевидной формы | Круговая дцДНК | ||
| Plasmaviridae | Обволакивающий, плеоморфный | Круговая дцДНК | ||
| Portogloboviridae | Обернутый, изометрический | Круговая дцДНК | ||
| Спиравиры | Без развертки, стержневидный | Круговая оцДНК | ||
| Tristromaviridae | Обволакивающий, стержневидный | Линейная дцДНК |
Было высказано предположение, что представители Picobirnaviridae заражают бактерии, но не млекопитающих. [11]
Другое предложенное семейство - Autolykiviridae (дцДНК). [12]
История [ править ]
В 1896 году Эрнест Ханбери Ханкин сообщил, что что-то в водах рек Ганг и Ямуна в Индии обладает выраженным антибактериальным действием против холеры и может проходить через очень тонкий фарфоровый фильтр. [13] В 1915 году британский бактериолог Фредерик Творт , суперинтендант Лондонского института Брауна, обнаружил небольшой агент, заражавший и убивающий бактерии. Он считал, что агент должен быть одним из следующих:
- стадия жизненного цикла бактерий
- фермент , произведенный сами, или бактерий
- вирус, который вырос и уничтожил бактерии [14]
Исследования Творта были прерваны началом Первой мировой войны , а также нехваткой финансирования и открытиями антибиотиков.
Независимо, франко-канадский микробиолог Феликс д'Эрелль , работающий в Институте Пастера в Париже , объявил 3 сентября 1917 года, что он открыл «невидимый, антагонистический микроб дизентерийной палочки». Для д'Эреля не возникало сомнений в природе его открытия: «В мгновение ока я понял: причиной моих чистых пятен на самом деле был невидимый микроб… вирус, паразитирующий на бактериях». [15] Д'Эрелль назвал вирус бактериофагом, поедающим бактерии (от греческого « фагин», означающего «пожирать»). Он также записал драматический рассказ о человеке, страдающем дизентерией, которому бактериофаги вернули хорошее здоровье.[16] Именно Д'Эрелль провел большое количество исследований бактериофагов и представил концепцию фаговой терапии . [17]
Более чем полвека спустя, в 1969 году, Макс Дельбрюк , Альфред Херши и Сальвадор Лурия были удостоены Нобелевской премии по физиологии и медицине за открытие репликации вирусов и их генетической структуры. [18] [ актуально? ]
Использует [ редактировать ]
Фаговая терапия [ править ]
Было обнаружено, что фаги являются антибактериальными агентами и использовались в бывшей советской республике Грузия (впервые здесь был применен Георгий Элиава с помощью соавтора бактериофагов Феликса д'Эрелля ) в течение 1920-х и 1930-х годов для лечения бактериальных инфекций. Они имели широкое применение, в том числе и для лечения солдат Красной Армии . Однако на Западе от них отказались для широкого использования по нескольким причинам:
- Были открыты и широко распространены антибиотики. Их было легче изготовить, хранить и выписывать.
- Были проведены медицинские испытания фагов, но из-за недостатка понимания возникли вопросы о достоверности этих испытаний. [19]
- Публикация исследований в Советском Союзе проводилась в основном на русском или грузинском языках и в течение многих лет не отслеживалась на международном уровне.
Использование фагов продолжалось после окончания холодной войны в России, [20] Грузии и других странах Центральной и Восточной Европы. О первом регулируемом рандомизированном двойном слепом клиническом исследовании было сообщено в журнале Journal of Wound Care в июне 2009 г., в котором оценивалась безопасность и эффективность коктейля с бактериофагами для лечения инфицированных венозных язв голени у людей. [21] FDA одобрило исследование как клиническое испытание фазы I. Результаты исследования продемонстрировали безопасность терапевтического применения бактериофагов, но не показали эффективности. Авторы объяснили, что использование определенных химических веществ, входящих в стандартную процедуру ухода за ранами (например, лактоферрина)или серебро) могли повлиять на жизнеспособность бактериофага. [21] Вскоре после этого в августе 2009 года в журнале Clinical Otolaryngology было опубликовано другое контролируемое клиническое испытание в Западной Европе (лечение ушных инфекций, вызванных Pseudomonas aeruginosa ) . [22] В исследовании делается вывод о том, что препараты бактериофагов безопасны и эффективны для лечения хронических инфекций уха у людей. Кроме того, были проведены многочисленные экспериментальные клинические испытания на животных и другие экспериментальные клинические испытания, оценивающие эффективность бактериофагов при различных заболеваниях, таких как инфицированные ожоги и раны, а также инфекции легких, связанные с кистозным фиброзом. [22]
Тем временем исследователи бактериофагов разрабатывают модифицированные вирусы для преодоления устойчивости к антибиотикам и конструируют гены фагов, ответственные за кодирование ферментов, разрушающих матрикс биопленки, структурные белки фага и ферменты, ответственные за лизис клеточной стенки бактерий. [4] [5] [6] Были получены результаты, показывающие, что небольшие по размеру и короткохвостые фаги Т4 могут быть полезны при обнаружении кишечной палочки в организме человека. [23]
Терапевтическая эффективность коктейля фагов оценивалась на модели мышей с носовой инфекцией, вызванной множественной лекарственной устойчивостью (МЛУ) A. baumannii . Мыши, получавшие коктейль с фагами, показали в 2,3 раза более высокую выживаемость, чем мыши, не получавшие лечения, через семь дней после заражения. [24] В 2017 году пациенту с поджелудочной железой, пораженной МЛУ A. baumannii, было назначено несколько антибиотиков, несмотря на то, что его здоровье продолжало ухудшаться в течение четырех месяцев. Без эффективных антибиотиков пациент был подвергнут фаговой терапии с использованием фагового коктейля, содержащего девять различных фагов, эффективность которых против МЛУ A. baumannii была продемонстрирована.. После этого лечения нисходящая клиническая траектория пациента изменилась и выздоровела. [25]
Д'Эрелль «быстро узнал, что бактериофаги встречаются везде, где процветают бактерии: в сточных водах, в реках, собирающих сточные воды из труб, и в стуле выздоравливающих пациентов». [26] Это включает реки, которые традиционно считались исцеляющими, включая реку Ганг в Индии . [27]
Другое [ править ]
Пищевая промышленность - С 2006 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и Министерство сельского хозяйства США (USDA) одобрили несколько продуктов с бактериофагами. LMP-102 (Intralytix) был одобрен для обработки готовых к употреблению (RTE) птицы и мясных продуктов. В том же году FDA одобрило LISTEX (разработанный и произведенный Micreos ) с использованием бактериофагов на сыре для уничтожения бактерий Listeria monocytogenes , чтобы придать им статус, общепризнанный как безопасный (GRAS). [28] В июле 2007 года один и тот же бактериофаг был одобрен для использования во всех пищевых продуктах. [29]В 2011 году Министерство сельского хозяйства США подтвердило, что LISTEX является средством для обработки чистой этикетки и включено в USDA. [30] Исследования в области безопасности пищевых продуктов продолжаются, чтобы выяснить, являются ли литические фаги жизнеспособным вариантом для борьбы с другими патогенами пищевого происхождения в различных пищевых продуктах.
Молочная промышленность - Бактериофаги, присутствующие в окружающей среде, могут вызывать сбои ферментации сырных заквасок. Чтобы избежать этого, можно использовать заквасочные культуры со смешанными штаммами и режимы ротации культур. [31]
Диагностика - В 2011 году FDA одобрило первый продукт на основе бактериофагов для использования в диагностике in vitro. [32] Тест на посев крови KeyPath MRSA / MSSA использует смесь бактериофагов для обнаружения Staphylococcus aureus в положительных культурах крови и определения устойчивости или чувствительности к метициллину . Тест возвращает результаты примерно через пять часов, по сравнению с двумя-тремя днями для стандартных методов идентификации микробов и определения чувствительности. Это был первый ускоренный тест на чувствительность к антибиотикам, одобренный FDA. [33]
Противодействие биологическому оружию и токсинам - правительственные учреждения на Западе в течение нескольких лет обращались к Грузии и бывшему Советскому Союзу за помощью в использовании фагов для борьбы с биологическим оружием и токсинами, такими как сибирская язва и ботулизм . [34]Разработки продолжаются среди исследовательских групп в США. Другие применения включают распыление в садоводстве для защиты растений и овощных продуктов от гниения и распространения бактериальных заболеваний. Другие области применения бактериофагов - это биоциды для поверхностей из окружающей среды, например, в больницах, и в качестве профилактического лечения катетеров и медицинских устройств перед их использованием в клинических условиях. В настоящее время существует технология нанесения фагов на сухие поверхности, например, на униформу, занавески или даже хирургические швы. Клинические испытания, опубликованные в « Клинической отоларингологии» [22], показывают успех в ветеринарном лечении домашних собак с отитом .
Метод обнаружения и идентификации бактерий SEPTIC использует ионную эмиссию и ее динамику во время фаговой инфекции и обеспечивает высокую специфичность и скорость обнаружения. [35]
Фаговый дисплей - это другое использование фагов с участием библиотеки фагов с вариабельным пептидом, связанным с поверхностным белком. Каждый фаговый геном кодирует вариант белка, отображаемый на его поверхности (отсюда и название), обеспечивая связь между вариантом пептида и его кодирующим геном. Варианты фагов из библиотеки могут быть выбраны по их аффинности связывания с иммобилизованной молекулой (например, токсином ботулизма) для ее нейтрализации. Связанные отобранные фаги могут быть размножены путем повторного заражения чувствительного бактериального штамма, что позволяет им извлекать закодированные в них пептиды для дальнейшего изучения. [36]
Открытие противомикробных лекарств. Фаговые белки часто обладают антимикробной активностью и могут служить в качестве основы для пептидомиметиков , то есть лекарств, имитирующих пептиды. [37] В технологии фаг -лиганд фаговые белки используются для различных целей, таких как связывание бактерий и бактериальных компонентов (например, эндотоксин ) и лизис бактерий. [38]
Фундаментальные исследования. Бактериофаги - важные модельные организмы для изучения принципов эволюции и экологии . [39]
Репликация [ править ]
Бактериофаги могут иметь литический или лизогенный цикл . С помощью литических фагов, таких как фаг Т4 , бактериальные клетки вскрываются (лизируются) и разрушаются после немедленной репликации вириона. Как только клетка разрушается, потомство фага может найти новых хозяев для заражения. Литические фаги больше подходят для фаговой терапии . Некоторые литические фаги подвергаются феномену, известному как ингибирование лизиса, когда законченное фаговое потомство не будет немедленно лизироваться из клетки, если внеклеточные концентрации фага высоки. Этот механизм не идентичен механизму покоя умеренного фага и обычно носит временный характер.
Напротив, лизогенный цикл не приводит к немедленному лизису клетки-хозяина. Фаги, способные подвергаться лизогении, известны как фаги умеренного климата . Их вирусный геном будет интегрироваться с ДНК хозяина и реплицироваться вместе с ним относительно безвредно или даже может стать плазмидой . Вирус остается бездействующим до тех пор, пока условия хозяина не ухудшатся, возможно, из-за истощения питательных веществ, а затем эндогенные фаги (известные как профаги) становятся активными. В этот момент они запускают репродуктивный цикл, что приводит к лизису клетки-хозяина. Поскольку лизогенный цикл позволяет клетке-хозяину продолжать выживать и воспроизводиться, вирус реплицируется во всех потомках клетки. Пример бактериофага известного следовать лизогенную цикла и литический цикл является фага лямбда из E.coli. [40]
Иногда профаги могут приносить пользу бактериям-хозяевам, пока они находятся в спящем состоянии, добавляя новые функции к бактериальному геному , что называется лизогенным преобразованием . Примерами являются превращение безвредных штаммов Corynebacterium diphtheriae или Vibrio cholerae бактериофагами в высоковирулентные, вызывающие дифтерию или холеру соответственно. [41] [42] Были предложены стратегии борьбы с некоторыми бактериальными инфекциями путем нацеливания на эти кодирующие токсин профаги. [43]
Привязанность и проникновение [ править ]
Бактериальные клетки защищены клеточной стенкой из полисахаридов , которые являются важными факторами вирулентности, защищающими бактериальные клетки как от иммунной защиты хозяина, так и от антибиотиков . [44] Чтобы попасть в клетку-хозяина, бактериофаги связываются со специфическими рецепторами на поверхности бактерий, включая липополисахариды , тейхоевые кислоты , белки или даже жгутики.. Эта специфичность означает, что бактериофаг может инфицировать только определенные бактерии, несущие рецепторы, с которыми они могут связываться, что, в свою очередь, определяет круг хозяев фага. Ферменты, разлагающие полисахариды, такие как эндолизины, представляют собой связанные с вирионами белки, которые ферментативно разрушают внешний слой капсулы своих хозяев на начальном этапе строго запрограммированного процесса фаговой инфекции. Условия роста хозяев также влияют на способность фага прикрепляться к ним и вторгаться в них. [45] Поскольку вирионы фагов не перемещаются независимо, они должны полагаться на случайные встречи с правильными рецепторами в растворе, такими как кровь, лимфатическая циркуляция, орошение, почвенная вода и т. Д.
Миовирусные бактериофаги используют движение, подобное шприцу для подкожных инъекций, для введения своего генетического материала в клетку. После контакта с соответствующим рецептором хвостовые волокна изгибаются, чтобы приблизить базовую пластину к поверхности клетки. Это называется обратимым связыванием. После полного присоединения инициируется необратимое связывание, и хвост сокращается, возможно, с помощью АТФ , присутствующего в хвосте [5], вводя генетический материал через бактериальную мембрану. [46]Инъекция осуществляется посредством своего рода изгибающего движения в стержне, когда он идет в сторону, сокращается ближе к ячейке и толкается обратно вверх. У подовирусов отсутствует удлиненная хвостовая оболочка, как у миовируса, поэтому вместо этого они используют свои маленькие зубчатые волокна хвоста ферментативно, чтобы разрушить часть клеточной мембраны перед вставкой своего генетического материала.
Синтез белков и нуклеиновой кислоты [ править ]
Через несколько минут бактериальные рибосомы начинают транслировать вирусную мРНК в белок. Для фагов на основе РНК РНК-репликаза синтезируется на ранней стадии процесса. Белки модифицируют бактериальную РНК-полимеразу, поэтому она преимущественно транскрибирует вирусную мРНК. Нормальный синтез белков и нуклеиновых кислот в организме хозяина нарушается, и вместо этого он вынужден производить вирусные продукты. Эти продукты становятся частью новых вирионов внутри клетки, белков-помощников, которые вносят вклад в сборку новых вирионов, или белков, участвующих в лизисе клетки . В 1972 году Вальтер Фирс ( Гентский университет , Бельгия)) был первым, кто установил полную нуклеотидную последовательность гена, а в 1976 году - вирусного генома бактериофага MS2 . [47] Некоторые бактериофаги дцДНК кодируют рибосомные белки, которые, как полагают, модулируют трансляцию белков во время фаговой инфекции. [48]
Сборка вириона [ править ]
В случае фага Т4 создание новых вирусных частиц включает помощь вспомогательных белков, которые действуют каталитически во время морфогенеза фага . [49] Сначала собираются опорные плиты, а затем на них строятся хвосты. Головные капсиды, сконструированные отдельно, спонтанно собираются вместе с хвостами. Во время сборки вириона фага Т4 морфогенетические белки, кодируемые генами фага, взаимодействуют друг с другом в характерной последовательности. Поддержание соответствующего баланса в количествах каждого из этих белков, продуцируемых во время вирусной инфекции, по-видимому, имеет решающее значение для нормального морфогенеза фага Т4 . [50]ДНК эффективно упакована в головах. Весь процесс занимает около 15 минут.
Выпуск вирионов [ править ]
Фаги могут высвобождаться посредством лизиса клеток, экструзии или, в некоторых случаях, почкования. Лизис хвостатыми фагами достигается ферментом эндолизином , который атакует и разрушает пептидогликан клеточной стенки . Совершенно другой тип фага, нитчатый фаг , заставляет клетку-хозяин постоянно секретировать новые вирусные частицы. Освободившиеся вирионы описываются как свободные и, если они не являются дефектными, способны инфицировать новую бактерию. Почкование связано с определенными фагами Mycoplasma . В отличие от высвобождения вириона, фаги, проявляющие лизогенный цикл, не убивают хозяина, а, скорее, становятся долгосрочными резидентами в качестве профага .
Связь [ править ]
Исследования 2017 года показали, что бактериофаг Φ3T вырабатывает короткий вирусный белок, который сигнализирует другим бактериофагам о том, что они бездействуют, а не убивают бактерию-хозяин. Арбитриум - это название, данное этому белку открывшими его исследователями. [51] [52]
Структура генома [ править ]
Учитывая миллионы различных фагов в окружающей среде, геномы фагов бывают самых разных форм и размеров. РНК-фаг, такой как MS2, имеет самый маленький геном, всего в несколько килобаз. Однако некоторые ДНК-фаги, такие как Т4, могут иметь большие геномы с сотнями генов; размер и форма капсида варьируются вместе с размером генома. [53] Самые большие геномы бактериофагов достигают размера 735 т.п.н. [54]
Геномы бактериофагов могут быть сильно мозаичными , т.е. геном многих видов фагов, по-видимому, состоит из множества отдельных модулей. Эти модули могут быть обнаружены у других видов фагов в другом расположении. Микобактериофаги , бактериофаги с микобактериальными хозяевами, являются прекрасными примерами этого мозаицизма. У этих микобактериофагов генетический ассортимент может быть результатом повторяющихся случаев сайт-специфической рекомбинации и незаконной рекомбинации (результат приобретения фаговым геномом генетических последовательностей бактериального хозяина). [55]Эволюционные механизмы, формирующие геномы бактериальных вирусов, различаются в зависимости от семейства и зависят от типа нуклеиновой кислоты, характеристик структуры вириона, а также от режима жизненного цикла вируса. [56]
Системная биология [ править ]
Фаги часто оказывают сильное воздействие на хозяев. Как следствие, картина транскрипции инфицированной бактерии может значительно измениться. Например, заражение Pseudomonas aeruginosa умеренным фагом PaP3 изменило экспрессию 38% (2160/5633) генов хозяина. Многие из этих эффектов, вероятно, являются косвенными, поэтому задача состоит в том, чтобы определить прямые взаимодействия между бактериями и фагами. [57]
Было сделано несколько попыток составить карту белок-белковых взаимодействий между фагами и их хозяином. Например, было обнаружено, что лямбда бактериофага взаимодействует со своим хозяином, E. coli , посредством 31 взаимодействия. Однако масштабное исследование выявило 62 взаимодействия, большинство из которых были новыми. Опять же, значение многих из этих взаимодействий остается неясным, но эти исследования показывают, что, скорее всего, существует несколько ключевых взаимодействий и множество косвенных взаимодействий, роль которых остается не охарактеризованной. [58]
В окружающей среде [ править ]
Метагеномика позволила обнаруживать бактериофаги в воде, что ранее было невозможно. [59]
Кроме того, бактериофаги использовались для гидрологического отслеживания и моделирования в речных системах, особенно там, где происходит взаимодействие поверхностных и подземных вод . Использование фагов предпочтительнее более традиционных маркеров красителей, поскольку они значительно меньше абсорбируются при прохождении через грунтовые воды и их легко обнаружить при очень низких концентрациях. [60] Незагрязненная вода может содержать примерно 2 × 10 8 бактериофагов на мл. [61]
Считается, что бактериофаги вносят значительный вклад в горизонтальный перенос генов в естественной среде, главным образом посредством трансдукции , но также и посредством трансформации . [62] Метагеномические исследования также показали, что виромы из различных сред несут гены устойчивости к антибиотикам, включая те, которые могут вызывать множественную лекарственную устойчивость . [63]
Модельные бактериофаги [ править ]
Следующие бактериофаги широко изучаются:
- 186 фаг
- λ фаг
- Фаг Φ6
- Фаг Φ29
- ΦX174
- Фаг G4
- Фаг M13
- Фаг MS2 ( размер 23–28 нм ) [64]
- Фаг N4
- Фаг P1
- P2 фаг
- Фаг P4
- Фаг R17
- Фаг Т2
- Фаг Т4 ( геном 169 т.п.н. , [65] 200 нм длиной [66] )
- Фаг Т7
- Фаг Т12
См. Также [ править ]
- Вирофаги , вирусы, поражающие другие вирусы
- Бактериоядное животное
- CrAssphage
- ДНК-вирусы
- Экология фагов
- Монографии по фагам (полный список монографий, посвященных фагам и фагам, с 1921 г. по настоящее время)
- Полифаг
- РНК-вирусы
- Трансдукция
- Вириома
- CRISPR
- Фагемид
Ссылки [ править ]
- ^ a b McGrath S и van Sinderen D (редакторы). (2007). Бактериофаг: генетика и молекулярная биология (1-е изд.). Caister Academic Press. ISBN 978-1-904455-14-1.
- ^ «Новая фаговая терапия спасает пациента с бактериальной инфекцией с множественной лекарственной устойчивостью» . UC Health - Калифорнийский университет в Сан-Диего . Проверено 13 мая 2018 .
- ^ Suttle, Curtis A. (сентябрь 2005). «Вирусы в море» . Природа . 437 (7057): 356–361. DOI : 10,1038 / природа04160 . ISSN 0028-0836 .
- ^ a b Wommack, KE; Колвелл, Р.Р. (2000). «Вириопланктон: вирусы в водных экосистемах» . Обзоры микробиологии и молекулярной биологии . 64 (1): 69–114. DOI : 10.1128 / MMBR.64.1.69-114.2000 . PMC 98987 . PMID 10704475 .
- ^ a b c Прескотт, Л. (1993). Микробиология, Wm. C. Brown Publishers, ISBN 0-697-01372-3
- ^ a b BBC Horizon (1997): Вирус, который лечит - Документальный фильм об истории фаговой медицины в России и на Западе
- ↑ Borrell, Brendan (август 2012). «Научный разговор: Фаговый фактор». Scientific American . С. 80–83.
- Перейти ↑ Keen, EC (2012). «Фаговая терапия: концепция лечения» . Границы микробиологии . 3 : 238. DOI : 10,3389 / fmicb.2012.00238 . PMC 3400130 . PMID 22833738 .
- ^ Sweere, Johanna M .; Ван Беллегхем, Джонас Д .; Исхак, Хизер; Бах, Мишель С .; Попеску, Медея; Сункари, Вивекананда; Кабер, Гернот; Манашероб, Роберт; Suh, Gina A .; Цао, Сиоу; де Вриз, Кристиан Р. (2019). «Бактериофаг запускает противовирусный иммунитет и препятствует избавлению от бактериальной инфекции» . Наука . 363 (6434): eaat9691. DOI : 10.1126 / science.aat9691 . ISSN 0036-8075 .
- ^ Элина Лаанто, Сари Мянтинен, Луиджи Де Колибус, Дженни Марьякангас, Эшли Гиллум, Дэвид И. Стюарт, Янне Дж. Равантти, Юха Хьюсконен, Лотта-Риина Сундберг: вирус, обнаруженный в северном озере, связывает вирусы оцДНК и дцДНК . В: Proceedings of the National Academy of Sciences 114 (31), июль 2017 г., DOI: 10.1073 / pnas.1703834114
- ^ Кришнамурти SR, Ван Д. (2018). «Обширное сохранение прокариотических сайтов связывания рибосом в известных и новых пикобирнавирусах» . Вирусология . 516 : 108–114. DOI : 10.1016 / j.virol.2018.01.006 . PMID 29346073 .
- ↑ Кэтрин М. Кауфман, Фатима А. Хуссейн, Джой Ян, Филип Аревало, Джулия М. Браун, Уильям К. Чанг, Дэвид ВанИнсберге, Джозеф Эльшербини, Радхи С. Шарма, Майкл Б. Катлер, Либуша Келли, Мартин Ф. Польз : Основная линия вирусов дцДНК без хвоста, являющихся неизвестными убийцами морских бактерий . В: Nature Vol. 554. С. 118–122. 24 января 2018 г. doi: 10.1038 / nature25474
- ^ Ханкин, Э. Х. (1896). "Бактерицидное действие воды" Жамна и Ганж на вибрионе холеры " . Annales de l'Institut Pasteur (на французском языке). 10 : 511–23.
- ^ Twort, FW (1915). «Исследование природы ультрамикроскопических вирусов» . Ланцет . 186 (4814): 1241–43. DOI : 10.1016 / S0140-6736 (01) 20383-3 .
- ^ d'Hérelles, Феликс (1917). "Sur un microbe invisible antagoniste des bacilles dysentériques" (PDF) . Comptes Rendus de l'Académie des Sciences de Paris . 165 : 373–5. Архивировано 11 мая 2011 года (PDF) . Проверено 5 сентября 2010 года .
- ^ d'Hérelles, Феликс (1949). «Бактериофаг» (PDF) . Новости науки . 14 : 44–59 . Проверено 5 сентября 2010 года .
- Перейти ↑ Keen, EC (2012). «Феликс д'Эрель и наше микробное будущее». Будущая микробиология . 7 (12): 1337–39. DOI : 10.2217 / fmb.12.115 . PMID 23231482 .
- ^ "Нобелевская премия по физиологии и медицине 1969" . Нобелевский фонд . Проверено 28 июля 2007 года .
- ^ Каттер, Элизабет; Де Вос, Даниэль; Гвасалия, Гурам; Алавидзе, Земфира; Гогохия, Лаша; Куль, Сара; Абедон, Стивен (1 января 2010 г.). «Фаготерапия в клинической практике: лечение инфекций человека». Текущая фармацевтическая биотехнология . 11 (1): 69–86. DOI : 10.2174 / 138920110790725401 . PMID 20214609 . S2CID 31626252 .
- ^ Сергей Головин Бактериофаги: убийцы в роли спасителей // Наука и жизнь . - 2017. - № 6. - С. 26–33
- ^ а б Роудс, Д. Д.; Wolcott, RD; Кусковский, Массачусетс; Wolcott, BM; Уорд, LS; Сулаквелидзе, А (июнь 2009 г.). «Бактериофаговая терапия венозных язв ног у людей: результаты исследования безопасности фазы I». Журнал ухода за ранами . 18 (6): 237–8, 240–3. DOI : 10,12968 / jowc.2009.18.6.42801 . PMID 19661847 .
- ^ a b c Райт, А .; Хокинс, Швейцария; Änggård, EE; Харпер, Д.Р. (август 2009 г.). «Контролируемое клиническое испытание терапевтического препарата бактериофага при хроническом отите, вызванном устойчивостью к антибиотикам Pseudomonas aeruginosa ; предварительный отчет об эффективности» . Клиническая отоларингология . 34 (4): 349–357. DOI : 10.1111 / j.1749-4486.2009.01973.x . PMID 19673983 .
- ^ Tawil, Нэнси (апрель 2012). «Поверхностное плазмонное резонансное обнаружение E. coli и устойчивых к математике бактериофагов S. aureus» . PLOS Genetics . 3 (5): e78. DOI : 10.1371 / journal.pgen.0030078 . PMC 1877875 . PMID 17530925 .
- ^ Ча, Kyoungeun; О, Hynu K .; Jang, Jae Y .; Джо, Юнёль; Kim, Won K .; Ha, Geon U .; Ko, Kwan S .; Мён, Хиджун (10 апреля 2018 г.). «Характеристика двух новых бактериофагов, заражающих Acinetobacter baumannii с множественной лекарственной устойчивостью (МЛУ), и оценка их терапевтической эффективности in vivo» . Границы микробиологии . 9 : 696. DOI : 10,3389 / fmicb.2018.00696 . ISSN 1664-302X . PMC 5932359 . PMID 29755420 .
- ^ Schooley, Роберт Т .; Бисвас, Бисваджит; Гилл, Джейсон Дж .; Эрнандес-Моралес, Адриана; Ланкастер, Джейкоб; Арендодатель, Лорен; Барр, Джереми Дж .; Рид, Шэрон Л .; Ровер, Форест (октябрь 2017 г.). «Разработка и использование персонализированных лечебных коктейлей на основе бактериофагов для лечения пациента с распространенной устойчивой инфекцией Acinetobacter baumannii» . Противомикробные препараты и химиотерапия . 61 (10). DOI : 10,1128 / AAC.00954-17 . ISSN 0066-4804 . PMC 5610518 . PMID 28807909 .
- ^ Кучмент, Анна (2012), Забытое лекарство: прошлое и будущее фаговой терапии , Springer, стр. 11, ISBN 978-1-4614-0250-3
- ^ Deresinski, Стан (15 апреля 2009). «Бактериофаговая терапия: использование более мелких блох» (PDF) . Клинические инфекционные болезни . 48 (8): 1096–1101. DOI : 10,1086 / 597405 . PMID 19275495 .
- ^ США FDA / CFSAN: Ответное письмо агентства, уведомление GRAS № 000198
- ^ (US FDA / CFSAN: Ответное письмо агентства, уведомление GRAS № 000218)
- ^ Директива ФССН 7120 архивации 18 октября 2011 в Wayback Machine
- ^ Атамер, Зейнеп; Самтлебе, Мейке; Неве, Хорст; Дж. Хеллер, Кнут; Хинрихс, Йорг (16 июля 2013 г.). «Обзор: устранение бактериофагов в сыворотке и сывороточных продуктах» . Границы микробиологии . 4 : 191. DOI : 10,3389 / fmicb.2013.00191 . PMC 3712493 . PMID 23882262 .
- ^ FDA 510 (k) Предварительное уведомление о продаже
- ^ FDA одобряет первый тест, чтобы быстро диагностировать и различать MRSA и MSSA . FDA (6 мая 2011 г.)
- ↑ Вайсман, Дарья (25 мая 2007 г.) Изучение сибирской язвы в лаборатории советской эпохи - при западном финансировании . Нью-Йорк Таймс
- ^ Добози-Кинг, М .; Seo, S .; Kim, JU; Young, R .; Cheng, M .; Киш, LB (2005). «Быстрое обнаружение и идентификация бактерий: определение каскада ионов, запускаемых фагами (SEPTIC)» (PDF) . Журнал биологической физики и химии . 5 : 3–7. DOI : 10.4024 / 1050501.jbpc.05.01 .
- ^ Смит Г.П., Петренко В.А. (апрель 1997 г.). «Фаговый дисплей». Chem. Ред . 97 (2): 391–410. DOI : 10.1021 / cr960065d . PMID 11848876 .
- ^ Лю, Цзин; Дехби, Мохаммед; Моек, Грег; Архин, Фрэнсис; Бауда, Паскаль; Бержерон, Доминик; Каллехо, Марио; Ферретти, Винсент; Ха, Нхуан (февраль 2004 г.). «Открытие антимикробных препаратов с помощью геномики бактериофагов». Природа Биотехнологии . 22 (2): 185–191. DOI : 10.1038 / nbt932 . PMID 14716317 . S2CID 9905115 .
- ^ Технологическая основа Фаг-лигандная технология
- Перейти ↑ Keen, EC (2014). «Компромиссы в жизнях бактериофагов» . Бактериофаг . 4 (1): e28365. DOI : 10,4161 / bact.28365 . PMC 3942329 . PMID 24616839 .
- ↑ Мейсон, Кеннет А., Джонатан Б. Лосос, Сьюзен Р. Сингер, Питер Х. Рэйвен и Джордж Б. Джонсон. (2011). Биология , стр. 533. Макгроу-Хилл, Нью-Йорк. ISBN 978-0-07-893649-4 .
- ↑ Мокроусов I (2009). « Corynebacterium diphtheriae : разнообразие генома, популяционная структура и перспективы генотипирования». Инфекция, генетика и эволюция . 9 (1): 1–15. DOI : 10.1016 / j.meegid.2008.09.011 . PMID 19007916 .
- ^ Чарльз RC, Райан ET (октябрь 2011 г.). «Холера в 21 веке». Современное мнение об инфекционных заболеваниях . 24 (5): 472–7. DOI : 10.1097 / QCO.0b013e32834a88af . PMID 21799407 . S2CID 6907842 .
- ^ Кин, EC (декабрь 2012 г.). «Парадигмы патогенеза: нацеливание на мобильные генетические элементы болезни» . Границы клеточной и инфекционной микробиологии . 2 : 161. DOI : 10.3389 / fcimb.2012.00161 . PMC 3522046 . PMID 23248780 .
- ^ Друлис-Кава, Зузанна; Майковска-Скробек, Гражина; MacIejewska, Барбара (2015). «Бактериофаги и белки фагового происхождения - подходы к применению» . Современная лекарственная химия . 22 (14): 1757–1773. DOI : 10.2174 / 0929867322666150209152851 . PMC 4468916 . PMID 25666799 .
- ^ Габашвили, И .; Хан, С .; Hayes, S .; Сервер, П. (1997). «Полиморфизм бактериофага Т7». Журнал молекулярной биологии . 273 (3): 658–67. DOI : 10.1006 / jmbi.1997.1353 . PMID 9356254 .
- ^ Maghsoodi, A .; Chatterjee, A .; Andricioaei, I .; Перкинс, Северная Каролина (25 ноября 2019 г.). «Как работает машина инъекции фага Т4, включая энергию, силы и динамический путь» . Труды Национальной академии наук . 116 (50): 25097–25105. DOI : 10.1073 / pnas.1909298116 . ISSN 0027-8424 . PMC 6911207 . PMID 31767752 .
- ^ Fiers, W .; Contreras, R .; Duerinck, F .; Haegeman, G .; Iserentant, D .; Merregaert, J .; Мин Джоу, Вт .; Molemans, F .; Raeymaekers, A .; Van Den Berghe, A .; Volckaert, G .; Изебаерт, М. (1976). «Полная нуклеотидная последовательность РНК бактериофага MS2: первичная и вторичная структура гена репликазы». Природа . 260 (5551): 500–507. Bibcode : 1976Natur.260..500F . DOI : 10.1038 / 260500a0 . PMID 1264203 . S2CID 4289674 .
- ^ Mizuno, CM; Guyomar, C; Roux, S; Lavigne, R; Родригес-Валера, Ф; Салливан, МБ; Gillet, R; Forterre, P; Крупович, М (2019). «Многочисленные культивируемые и некультивируемые вирусы кодируют рибосомные белки» . Nature Communications . 10 (1): 752. Bibcode : 2019NatCo..10..752M . DOI : 10.1038 / s41467-019-08672-6 . PMC 6375957 . PMID 30765709 .
- ^ Snustad DP. Доминирующие взаимодействия в клетках Escherichia coli, смешанных с бактериофагом T4D дикого типа и мутантами amber, и их возможное влияние на тип функции гена-продукта: каталитическая или стехиометрическая. Вирусология. 1968 Август; 35 (4): 550-63. DOI: 10.1016 / 0042-6822 (68) 90285-7. PMID 4878023 .
- ^ Пол Э. Взаимодействие морфогенетических генов бактериофага Т4. J Mol Biol. 1970; 47 (3): 293-306. DOI: 10.1016 / 0022-2836 (70) 90303-7
- Перейти ↑ Callaway, Ewen (2017). «Вы говорите о вирусе? Фаги отправляют химические сообщения» . Природа . DOI : 10.1038 / nature.2017.21313 .
- ^ Эрез, Зоар; Стейнбергер-Леви, Ида; Шамир, Майя; Дорон, Шани; Стокар-Авихаил, Авигайль; Пелег, Йоав; Меламед, Сара; Ливитт, Азита; Савидор, Алон; Олбек, Шира; Амитаи, Гил; Сорек, Ротем (26 января 2017 г.). «Связь между вирусами определяет решения о лизисе – лизогении» . Природа . 541 (7638): 488–493. Bibcode : 2017Natur.541..488E . DOI : 10,1038 / природа21049 . ISSN 0028-0836 . PMC 5378303 . PMID 28099413 .
- ^ Черный, LW; Томас, Дж. А. (2012). Конденсированная структура генома . Успехи экспериментальной медицины и биологии. 726 . С. 469–87. DOI : 10.1007 / 978-1-4614-0980-9_21 . ISBN 978-1-4614-0979-3. PMC 3559133 . PMID 22297527 .
- ^ Аль-Шайеб, Basem; Сачдева, Рохан; Чен Линь-Син; Уорд, Фред; Мунк, Патрик; Devoto, Audra; Кастель, Синди Дж .; Olm, Matthew R .; Баума-Грегсон, Кейт; Амано, Юки; Он, Кристина (февраль 2020 г.). «Клады огромных фагов из экосистем Земли» . Природа . 578 (7795): 425–431. DOI : 10.1038 / s41586-020-2007-4 . ISSN 1476-4687 . PMC 7162821 . PMID 32051592 .
- ^ Моррис Р, Маринелли LJ, Jacobs-Сера D, Hendrix RW, Hatfull GF (март 2008 г.). «Геномная характеристика микобактериофага Giles: доказательства приобретения фагом ДНК хозяина путем незаконной рекомбинации» . Журнал бактериологии . 190 (6): 2172–82. DOI : 10.1128 / JB.01657-07 . PMC 2258872 . PMID 18178732 .
- ^ Krupovic M, Прангишвили D, Hendrix RW, Бэмфорд DH (декабрь 2011). «Геномика бактериальных и архейных вирусов: динамика в прокариотической виросфере» . Обзоры микробиологии и молекулярной биологии . 75 (4): 610–35. DOI : 10.1128 / MMBR.00011-11 . PMC 3232739 . PMID 22126996 .
- ↑ Zhao X, Chen C, Shen W, Huang G, Le S, Lu S, Li M, Zhao Y, Wang J, Rao X, Li G, Shen M, Guo K, Yang Y, Tan Y, Hu F (2016 ). «Глобальный транскриптомный анализ взаимодействий между Pseudomonas aeruginosa и бактериофагом PaP3» . Sci Rep . 6 : 19237. Bibcode : 2016NatSR ... 619237Z . DOI : 10.1038 / srep19237 . PMC 4707531 . PMID 26750429 .
- ^ Blasche S, S Wuchty, Раджагопал С.В., Uetz P (2013). «Сеть взаимодействия белков бактериофага лямбда с его хозяином, Escherichia coli» . J. Virol . 87 (23): 12745–55. DOI : 10,1128 / JVI.02495-13 . PMC 3838138 . PMID 24049175 .
- ^ Брейтбарт M , P Саламон, Andresen B, Mahaffy JM, Сегал М. Мид D, F Азам, Ровер F (октябрь 2002). «Геномный анализ некультивируемых морских вирусных сообществ» . Proc. Natl. Акад. Sci. США . 99 (22): 14250–5. Bibcode : 2002PNAS ... 9914250B . DOI : 10.1073 / pnas.202488399 . PMC 137870 . PMID 12384570 .
- ^ Мартин, К. (1988). «Применение методов отслеживания бактериофагов в юго-западной воде». Журнал «Вода и окружающая среда» . 2 (6): 638–642. DOI : 10.1111 / j.1747-6593.1988.tb01352.x .
- Перейти ↑ Bergh, O (1989). «Большое количество вирусов, обнаруженных в водной среде». Природа . 340 (6233): 467–468. Bibcode : 1989Natur.340..467B . DOI : 10.1038 / 340467a0 . PMID 2755508 . S2CID 4271861 .
- ^ Кин, Эрик С .; Блисковский, Валерий В .; Малагон, Франциско; Бейкер, Джеймс Д .; Принц, Джеффри С .; Клаус, Джеймс С .; Адхья, Sankar L .; Гройсман, Эдуардо А. (2017). "Роман" Суперпредседатель "Бактериофаги способствуют горизонтальному переносу генов путем трансформации" . mBio . 8 (1): e02115–16. DOI : 10,1128 / mBio.02115-16 . PMC 5241400 . PMID 28096488 .
- ^ Лекунберри, Итциар; Субиратс, Джессика; Borrego, Carles M .; Бальказар, Хосе Л. (2017). «Изучение вклада бактериофагов в устойчивость к антибиотикам». Загрязнение окружающей среды . 220 (Pt B): 981–984. DOI : 10.1016 / j.envpol.2016.11.059 . hdl : 10256/14115 . PMID 27890586 .
- ^ Штраус, Джеймс Х .; Зиншеймер, Роберт Л. (июль 1963 г.). «Очистка и свойства бактериофага MS2 и его рибонуклеиновой кислоты». Журнал молекулярной биологии . 7 (1): 43–54. DOI : 10.1016 / S0022-2836 (63) 80017-0 . PMID 13978804 .
- ^ Миллер, ES; Куттер, Э; Мосиг, G; Arisaka, F; Кунисава, Т; Рюгер, W (март 2003 г.). «Геном бактериофага Т4» . Обзоры микробиологии и молекулярной биологии . 67 (1): 86–156, содержание. DOI : 10.1128 / MMBR.67.1.86-156.2003 . PMC 150520 . PMID 12626685 .
- ^ Ackermann, H.-W .; Криш, HM (6 апреля 2014 г.). «Каталог бактериофагов Т4-типа». Архив вирусологии . 142 (12): 2329–2345. DOI : 10.1007 / s007050050246 . PMID 9672598 . S2CID 39369249 .
Библиография [ править ]
- Хаузер, АР (2016). «Помимо антибиотиков: новые терапевтические подходы к бактериальным инфекциям» . Клинические инфекционные болезни . 63 (1): 89–95. DOI : 10,1093 / CID / ciw200 . PMC 4901866 . PMID 27025826 .
- Strathdee, Штеффани; Паттерсон, Том (2019). Идеальный хищник . Книги Hachette . ISBN 978-0316418089.
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме бактериофагов . |
| В Wikiquote есть цитаты, связанные с: Бактериофагом |
- Хойслер, Т. (2006) «Вирусы против супербактерий», Macmillan
- Анимация бактериофага, нацеленного на бактерии E. coli
- Phage.org общая информация о бактериофагах
- бактериофаги иллюстрации и геномика
- Бактериофаги захватывают добычу
- Подкаст NPR Science Friday, «Использование фаговых вирусов для борьбы с инфекцией», апрель 2008 г.
- Анимация научно правильного бактериофага Т4, нацеленного на бактерии E. coli
- Анимация от компании Hybrid Animation Medical для бактериофага Т4, нацеленного на бактерии E. coli
- Бактериофаги: что это такое. Презентация профессора Грэма Хатфулла из Питтсбургского университета на YouTube
