| Имена | |||
|---|---|---|---|
| Название ИЮПАК Бис (η 8 -циклооктатетраенил) уран (IV) | |||
| Другие имена Циклооктатетраенид урана U (COT) 2 | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 16 H 16 U | |||
| Молярная масса | 446,33 г / моль | ||
| Внешность | зеленые кристаллы [1] | ||
| Опасности | |||
| Основные опасности | пирофорный и токсичный | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
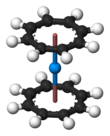
Ураноцен , U (C 8 H 8 ) 2 , представляет собой уранорганическое соединение, состоящее из атома урана, зажатого между двумя циклооктатетраенидными кольцами. Это было одно из первых синтезированных актинидорганических соединений . Это зеленое, чувствительное к воздуху твердое вещество, растворяющееся в органических растворителях. Ураноцен, член « актиноценов », группы металлоценов, включающих элементы из ряда актинидов . Это наиболее изученная система бис [8] аннулен-металл , хотя она не имеет известного практического применения. [2]
Синтез, структура и связь [ править ]
Ураноцен был впервые описан в 1968 году группой Эндрю Стрейтвизера , когда он был получен реакцией дикалия циклооктатетраенида и тетрахлорида урана в ТГФ при 0 ° C: [1]
Ураноцен очень реактивен по отношению к кислороду, пирофорен на воздухе, но устойчив к гидролизу . Считая молекулу U 4+ (C 8 H 8 2- ) 2 , η 8 - циклооктатетраенидные группы плоские, как и ожидалось для кольца, содержащего 10 π-электронов , и взаимно параллельны, образуя сэндвич, содержащий атом урана. . В твердом состоянии кольца затмеваются, что придает молекуле симметрию D 8h . В растворе кольца вращаются с низким энергетическим барьером.
С помощью фотоэлектронной спектроскопии было показано, что уран-циклооктатетраенильная связь в первую очередь обусловлена смешиванием 6d-орбиталей урана с пи- орбиталями лиганда и, следовательно, передачей электронного заряда урану с меньшим таким взаимодействием с участием урановых (5f) 2 -орбиталей. [3] Расчеты электронной теории согласуются с этим результатом [4] [5] и указывают на то, что более слабое взаимодействие 5f-орбиталей с открытой оболочкой с орбиталями лигандов определяет | M J |, величину квантового числа углового момента вдоль Ось 8-кратной симметрии основного состояния. [5]
Спектроскопические свойства [ править ]
Ураноцен парамагнитен . Его магнитная восприимчивость согласуется со значениями 3 или 4 для | M J |, при этом на соответствующий магнитный момент влияет спин-орбитальная связь . [6] Его спектр ЯМР согласуется с | M J | значение 3. [7] Расчеты электронной теории от простейших [8] до наиболее точных [9] также дают | M J | значения 3 для основного состояния и 2 для первого возбужденного состояния, соответствующие обозначениям двухгрупповой симметрии [10] E 3g и E 2g для этих состояний.
Зеленый цвет ураноцена обусловлен тремя сильными переходами в его видимом спектре . [1] [11] Помимо определения частот колебаний, спектры комбинационного рассеяния указывают на наличие низколежащего (E 2g ) возбужденного электронного состояния. [11] [12] На основании расчетов [5] видимые переходы приписываются переходам преимущественно 5f-в-6d природы, приводя к состояниям E 2u и E 3u .
Аналогичные соединения [ править ]
Аналогичные соединения формы M (C 8 H 8 ) 2 существуют для M = ( Nd , Tb , Pu , Pa , Np , Th и Yb ). Расширения включают стабильное на воздухе производное U (C 8 H 4 Ph 4 ) 2 и циклогептатриенильные соединения [U (C 7 H 7 ) 2 ] - . [2] Напротив, бис (циклооктатетраен) железо имеет совершенно другую структуру, каждая из которых имеет η 6 - и η4 -C 8 H 8 лиганды.
Ссылки [ править ]
- ^ a b c Streitwieser, A .; Мюллер-Вестерхофф, У. (1968). «Бис (циклооктатетраенил) уран (ураноцен). Новый класс сэндвич-комплексов, в которых используются атомные f-орбитали». Варенье. Chem. Soc. 90 (26): 7364–7364. DOI : 10.1021 / ja01028a044 .
- ^ а б Сейферт, Д. (2004). «Ураноцен. Первый представитель нового класса металлоорганических производных f-элементов» . Металлоорганические соединения . 23 (15): 3562–3583. DOI : 10.1021 / om0400705 .
- ^ Кларк, JP; Грин, JC (1977). "Исследование электронной структуры бис ( эта -цикло-октатетраен) -актиноидов с помощью гелиевой (I) и - (II) фотоэлектронной спектроскопии". J. Chem. Soc., Dalton Trans. (5): 505–508. DOI : 10.1039 / DT9770000505 .
- ^ Roesch, N .; Штрейтвизер, А. (1983). "Квазирелятивистское исследование рассеянных волн SCF-X альфа ураноцена, тороцена и цероцена". Варенье. Chem. Soc. 105 (25): 7237–7240. DOI : 10.1021 / ja00363a004 .
- ^ a b c Чанг, AHH; Питцер, Р.М. (1989). «Электронное строение и спектры ураноцена». Варенье. Chem. Soc. 111 (7): 2500–2507. DOI : 10.1021 / ja00189a022 .
- ^ Карракер, DG; Stone, JA; Джонс, ER; Эдельштейн, Н. (1970). «Бис (циклооктатетраенил) нептуний (IV) и бис (циклооктатетраенил) плутоний (IV)». J. Chem. Phys. 92 (16): 4841–4845. DOI : 10.1021 / ja00719a014 .
- Перейти ↑ Fischer, RD (1979). «ЯМР-спектроскопия металлоорганических соединений f-элементов: практическое применение». In Marks, TJ; Фишер, Р. Д. (ред.). Том 44 - Металлоорганика f-элементов . Серия институтов перспективных исследований НАТО: Серия C - Математические и физические науки. Дордрехт, Голландия: Рейдел. С. 337–377. ISBN 90-277-0990-4.
- ^ Hayes, RG; Эдельштейн, Н. (1972). «Расчет элементарных молекулярных орбиталей U (C 8 H 8 ) 2 и его применение к электронной структуре U (C 8 H 8 ) 2 , Np (C 8 H 8 ) 2. И Pu (C 8 H 8 ) 2» ". Варенье. Chem. Soc. 94 (25): 8688–8691. DOI : 10.1021 / ja00780a008 .
- ^ Лю, Вт .; Долг, М .; Фульде, П. (1997). «Низколежащие электронные состояния лантаноценов и актиноценов M (C 8 H 8 ) 2 (M = Nd, Tb, Yb, U)». J. Chem. Phys. 107 (9): 3584–3591. DOI : 10.1063 / 1.474698 .
- ^ Герцберг, Г. (1966). Молекулярные спектры и молекулярная структура III. Электронные спектры и электронное строение многоатомных молекул . Принстон, Нью-Джерси: Д. Ван Ностранд. п. 566.
- ^ a b Даллингер, РФ; Stein, P .; Спиро, Т.Г. (1978). "Резонансная рамановская спектроскопия ураноцена: наблюдение аномально поляризованной электронной полосы и определение уровней энергии". Варенье. Chem. Soc. 100 (25): 7865–7870. DOI : 10.1021 / ja00493a013 .
- ^ Хагер, JS; Zahardis, J .; Pagni, RM; и другие. (2004). «Раман в атмосфере азота. Рамановская спектроскопия высокого разрешения кристаллического ураноцена, торицена и ферроцена». J. Chem. Phys. 120 (6): 2708–2718. DOI : 10.1063 / 1.1637586 . PMID 15268415 .
| Викискладе есть медиафайлы по ураноцену . |
Дальнейшее чтение [ править ]
- Элементы f , Николас Кальцояннис и Питер Скотт. ISBN 0-19-850467-5
- Химия элементов , Н. Н. Гринвуд и А. Эрншоу. ISBN 0-08-022057-6
- Лантаноиды и актиниды: органоактиниды